| Учебный сайт Екатерины Швецовой | |||
| Главная | Обо мне | Семестры | Ссылки |
| 1 семестр | 2 семестр | 3 семестр | 4 семестр | 7 семестр | 8 семестр |
Остовные водородные связи белка Rhodanese (идентификатор PDB 1E0C)
Водородная связь - взаимодействие между двумя электроотрицательными атомами одной или разных молекул посредством атома водорода. Ниже рассмотрены примеры водородных связей в белке сульфуртрансферазы.
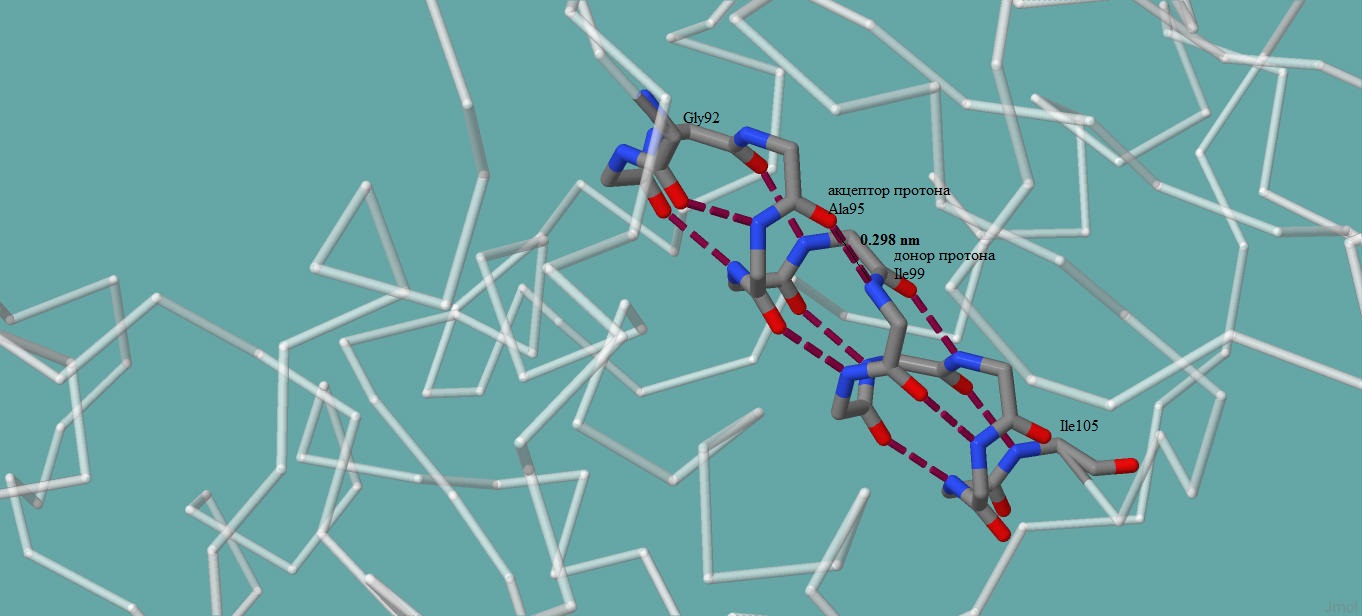
Рис. 1. Остовные водородные связи в альфа-спирали белка Rhodanese (идентификатор PDB 1E0C).
На рис. 1. изображена альфа-спираль, образованная аминокислотными остатками с 92 по 105 цепи А. Детально показана водородная связь между атомом азота изолейцина 99 (является донором протона) и атомом кислорода аланина 95 (акцептор протона). Номера остатков показывают, что между данными изолейцином и аланином, образующими водородную связь, в цепи находятся три тругих аминокислотных остатка. Длина связи составляет 2,98 А.
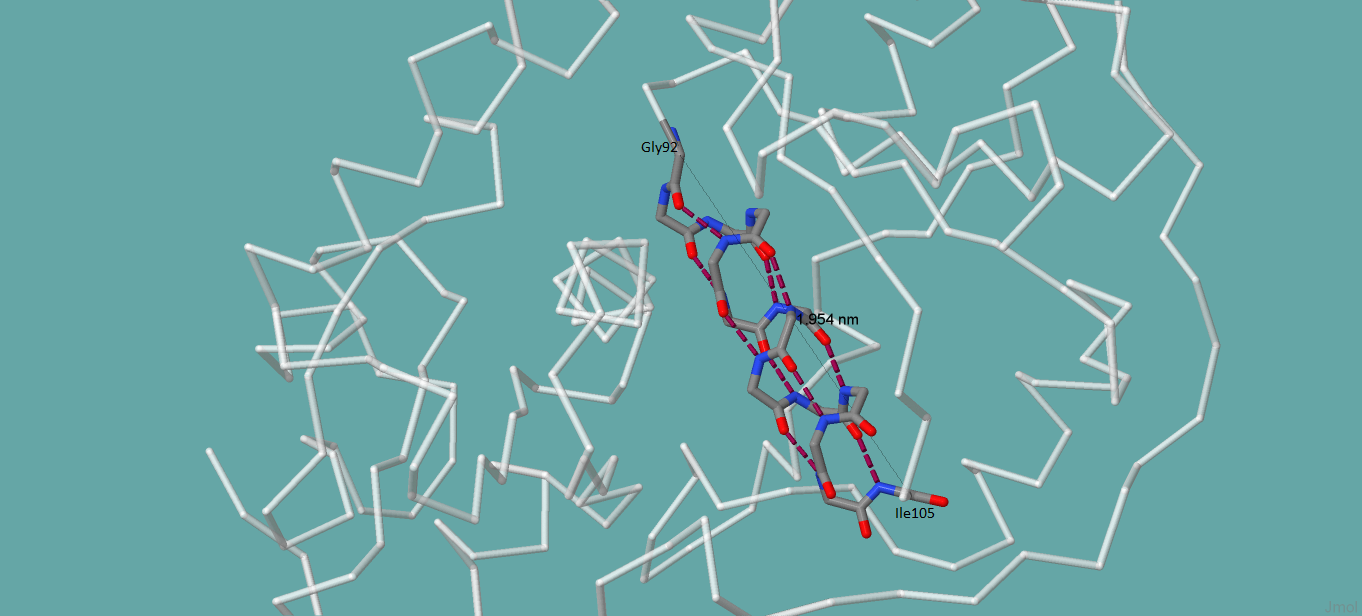
Рис. 2. Измерения в альфа-спирали.
Данная спираль содержит 13 аминокислотных остатков и 3 витка. Как показано на рис. 2., общая длина спирали составляет 19,54 А. Поэтому можно заключить, что шаг спирали составляет 6,5 А, а число аминокислотных остатков на один виток - 4,3.
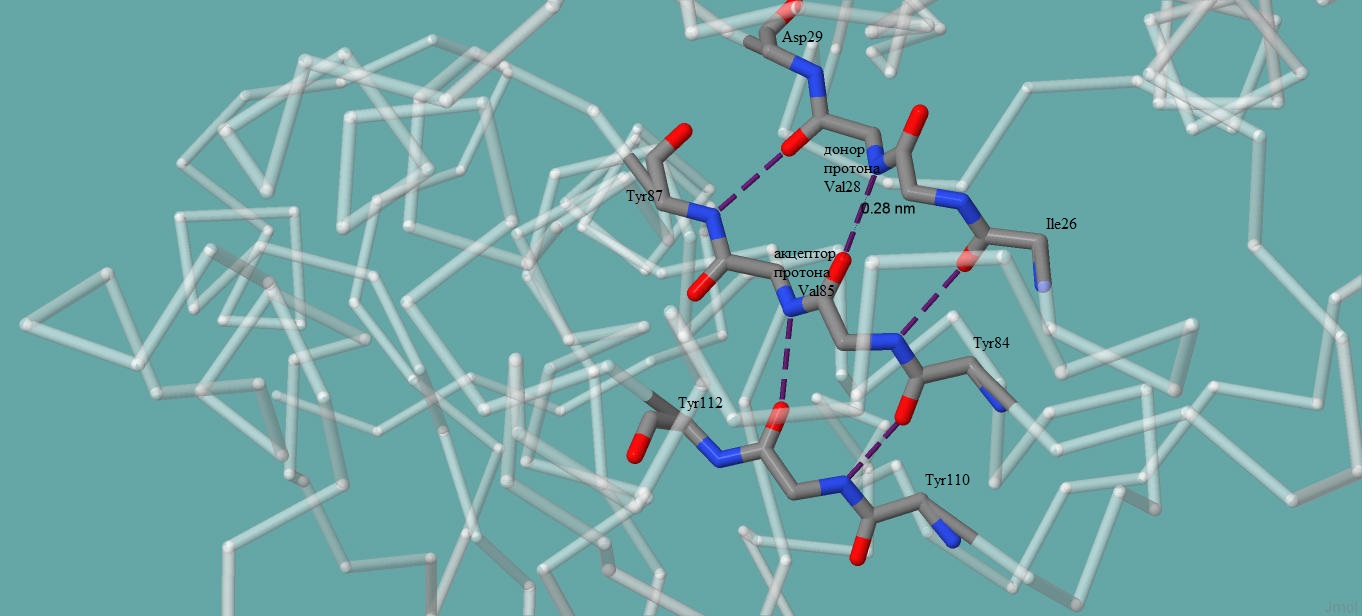
Рис. 3. Остовные водородные связи в бета-листе белка Rhodanese (идентификатор PDB 1E0C).
Рис. 3. иллюстрирует расположение водородных связей в бета-листе белка. Детально показана водородная связь между атомом азота валина 28 (является донором протона) и атомом кислорода валина 85 (акцептор протона).

Рис. 4. Направление тяжей бета-листа белка Rhodanese (идентификатор PDB 1E0C).
На рис. 4. показано направление бета-тяжей данного бета-листа. Видно, что все три тяжа параллельны.
©Shvetsova Ekaterina, FBB MSU, 2013
Дата последнего изменения: 07.12.2016