ASN100/N
находятся на разных тяжах b-листа снаружи глобулы
HIS126/N
находятся на одной петле, выдающейся из белка
100%
43,5%
В этом задании будут рассматриваться две структуры одного белка, а именно аллергена берёзовой пыльцы, полученные разными методами. Информация о структурах представлена в таблице ниже.
| ЯМР | РСА | |
|---|---|---|
| PDB ID | 1B6F | 1LLT |
| Conformers Calculated: 60 Conformers Submitted: 23 |
Resolution: 3.10 Angstrem R-Value Free: 0.301 R-Value Work: 0.274 |
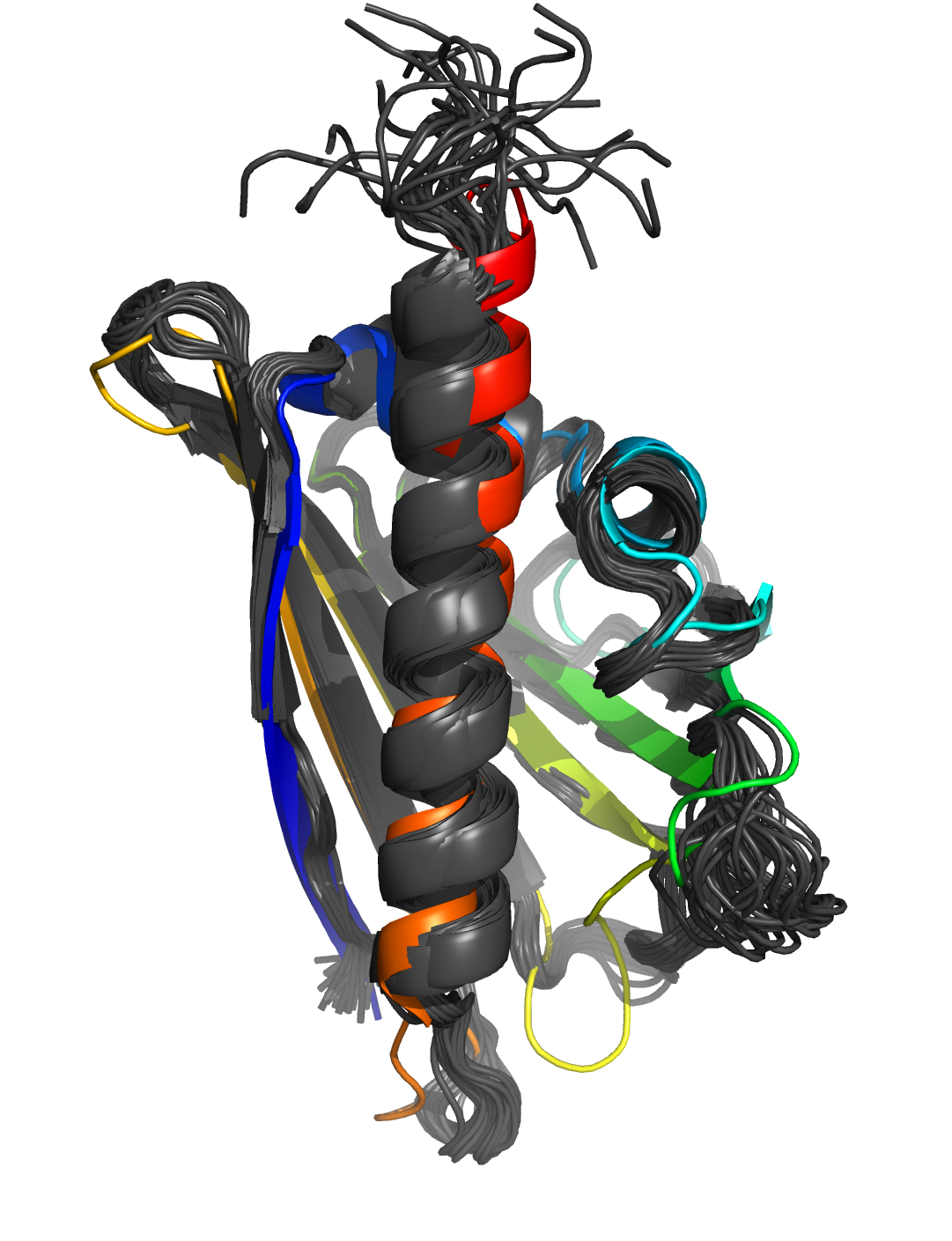
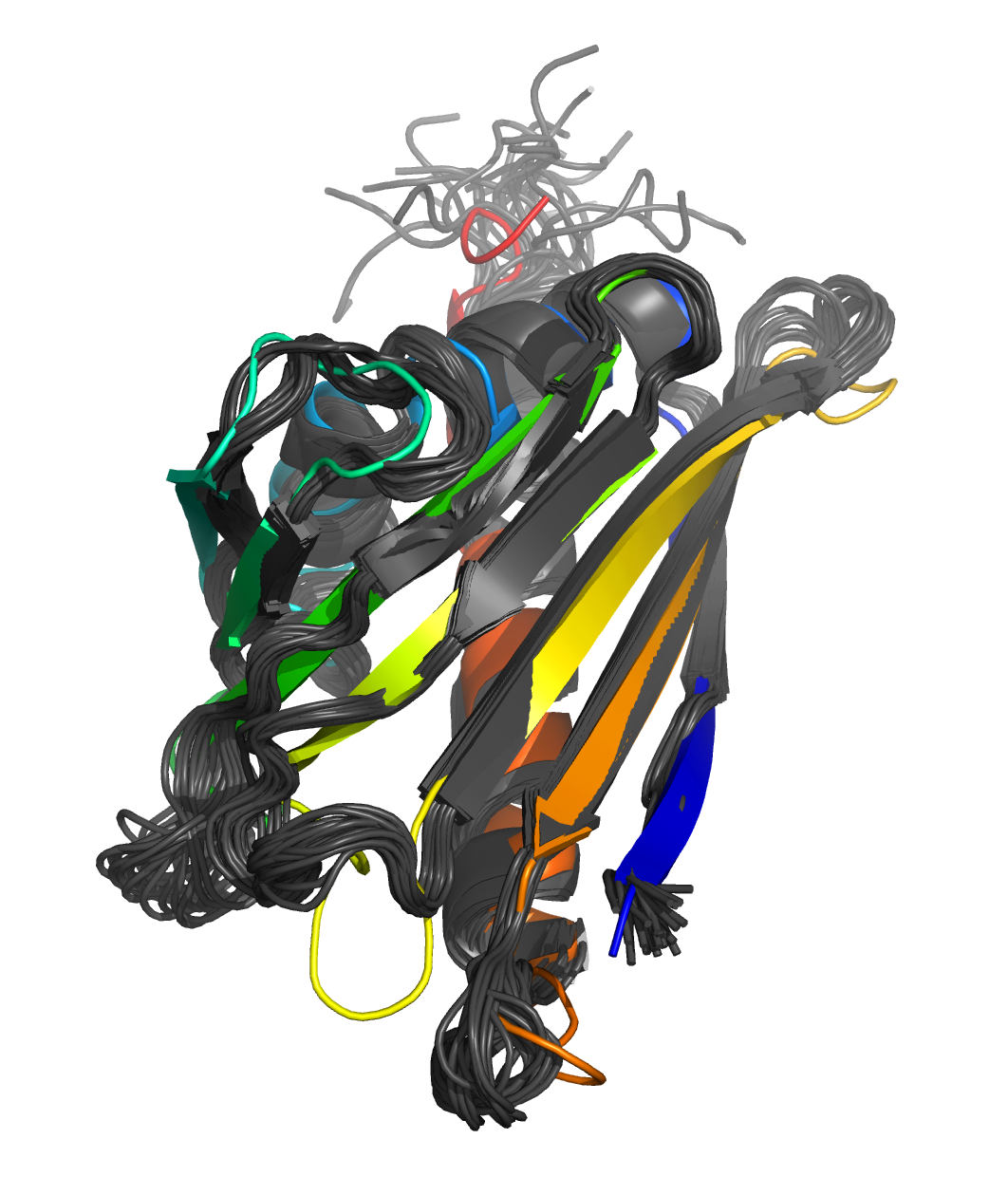
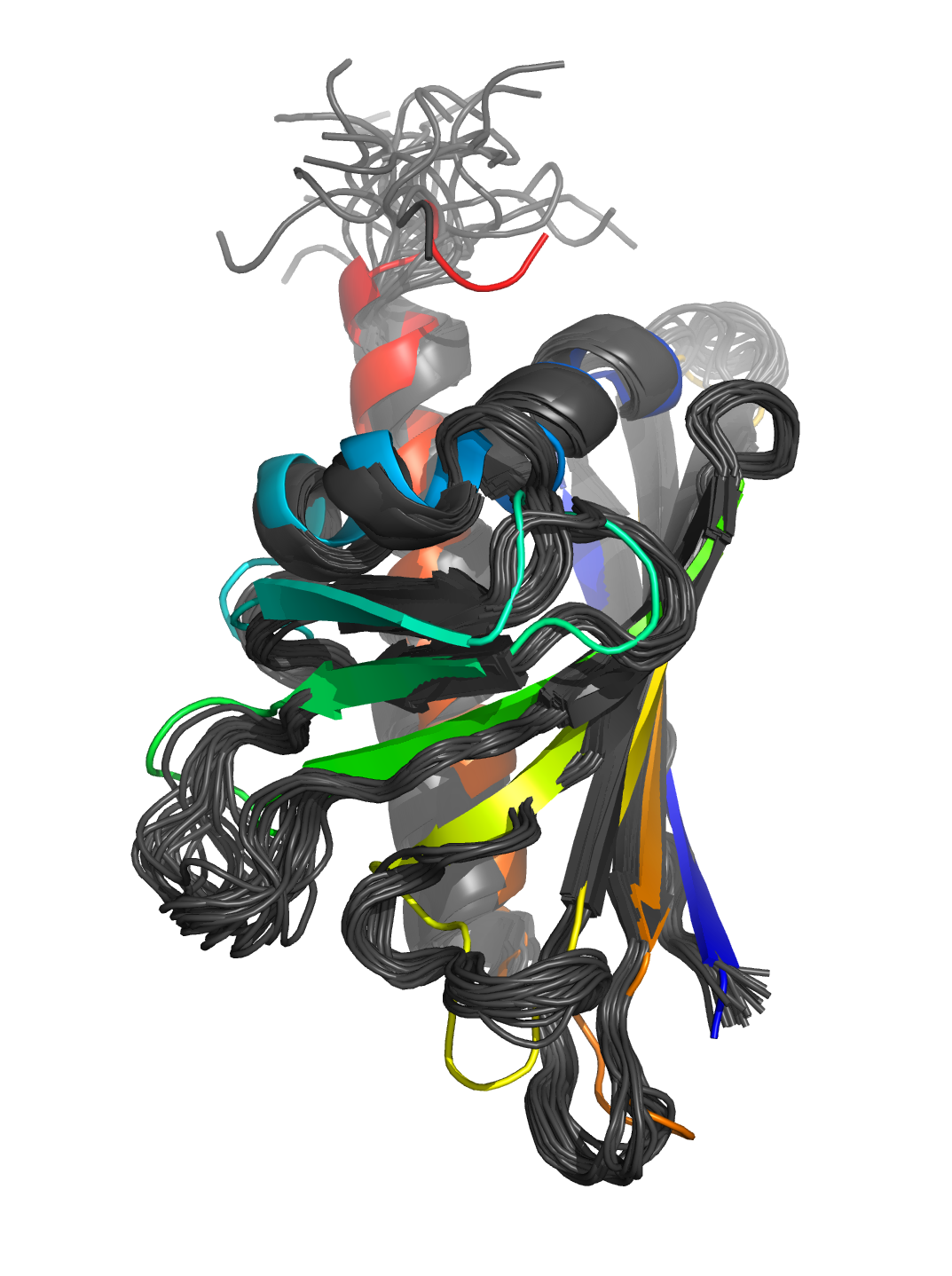
Серая - ЯМР-структура 1B6F.
Цветная - структура 1LLT, полученная методом РСА.
Наложение структур получено с помощью команды super.
Самое значимое отличие структур - длинный бета-тяж, обозначенный на рисунках зелёным: в
ЯМР-структуре 1B6F (серой) он гораздо короче, чем соответствующий тяж в РСА-структуре, и
скручен относительно последнего. Последовательности моделей совпадают. В предположительно стабильных участках
соответствующие остатки в двух можелях расположены похоже, в нестабильных участках, например, петлях между бета-тяжами,
боковые цепи остатков, ожидаемо, могут не накладываться друг на друга.
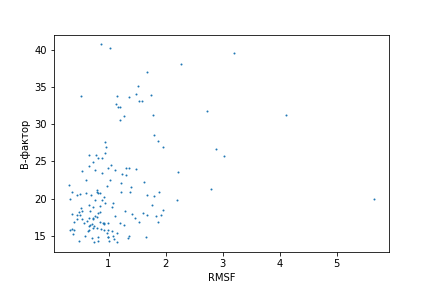
На рисунке изображен график, где каждая точка соответствует одному остатку, а её координаты x и y соответствуют среднему значению RMSF для этого остатка в ЯМР модели и среднему значению B-фактора этого остатка в РСА модели соответственно. Заметна некоторая корреляция рассматриваемых параметров: для остатков с бОльшим B-фактором, то есть имеющих менее стабильное положение, параметр RMSF в среднем больше. Можно сделать вывод о том, что подвижность атома увеличивает значение параметра RMSF для него.
В этом задании требовалось рассмотреть несколько примеров водородных связей из рассмотренных в 1-м задании моделей.
Полученная информация представлена в таблице.
В ядре белка не были найдены водородные связи, образованные боковыми цепями остатков, поэтому далее рассматриваются только две связи.
| Водородная связь: | между атомами остова в ядре белка | в петлях, выходящих на поверхность глобулы |
|---|---|---|
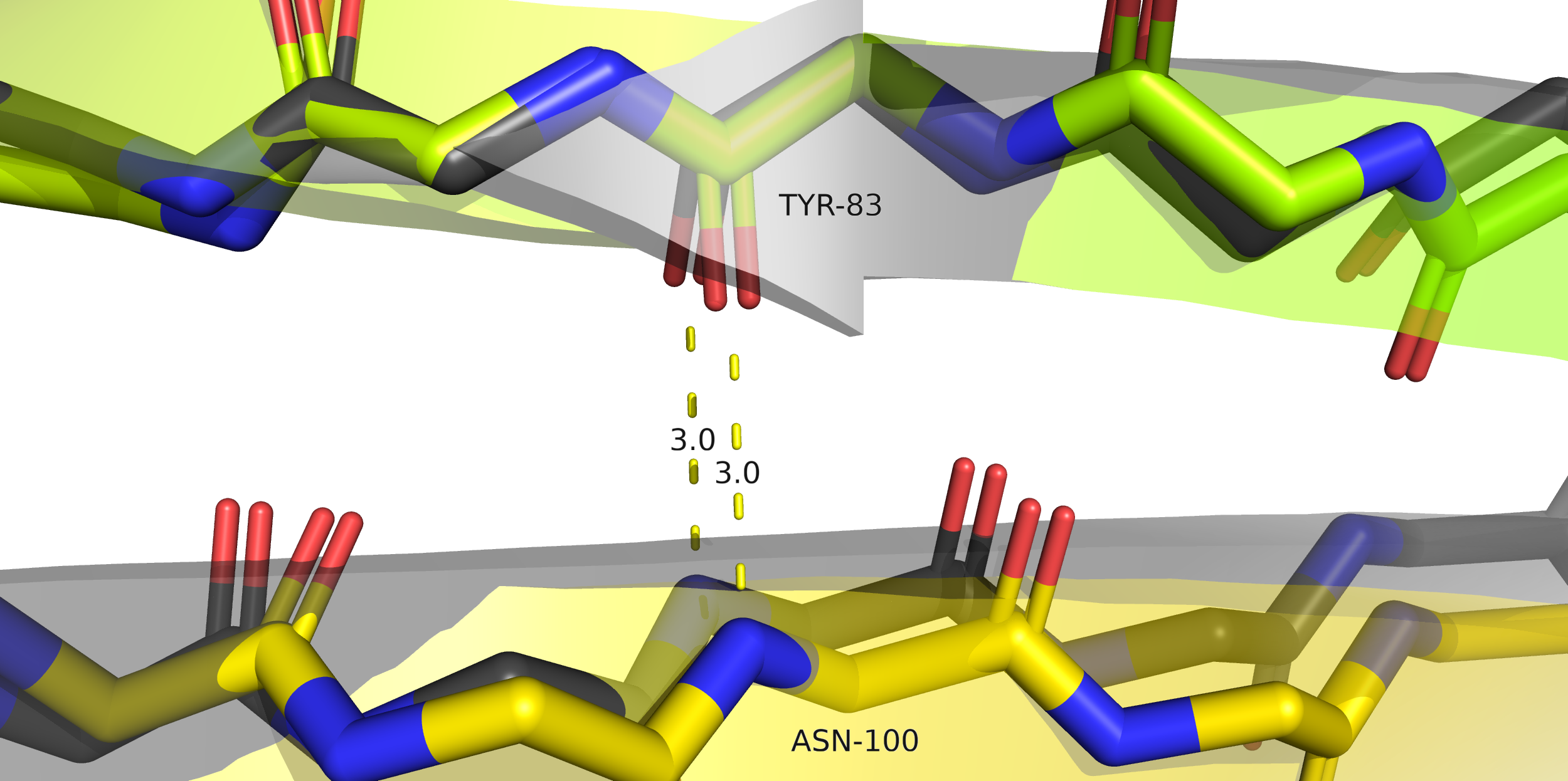
| Остатки, образующие связь | TYR83/O ASN100/N находятся на разных тяжах b-листа снаружи глобулы |
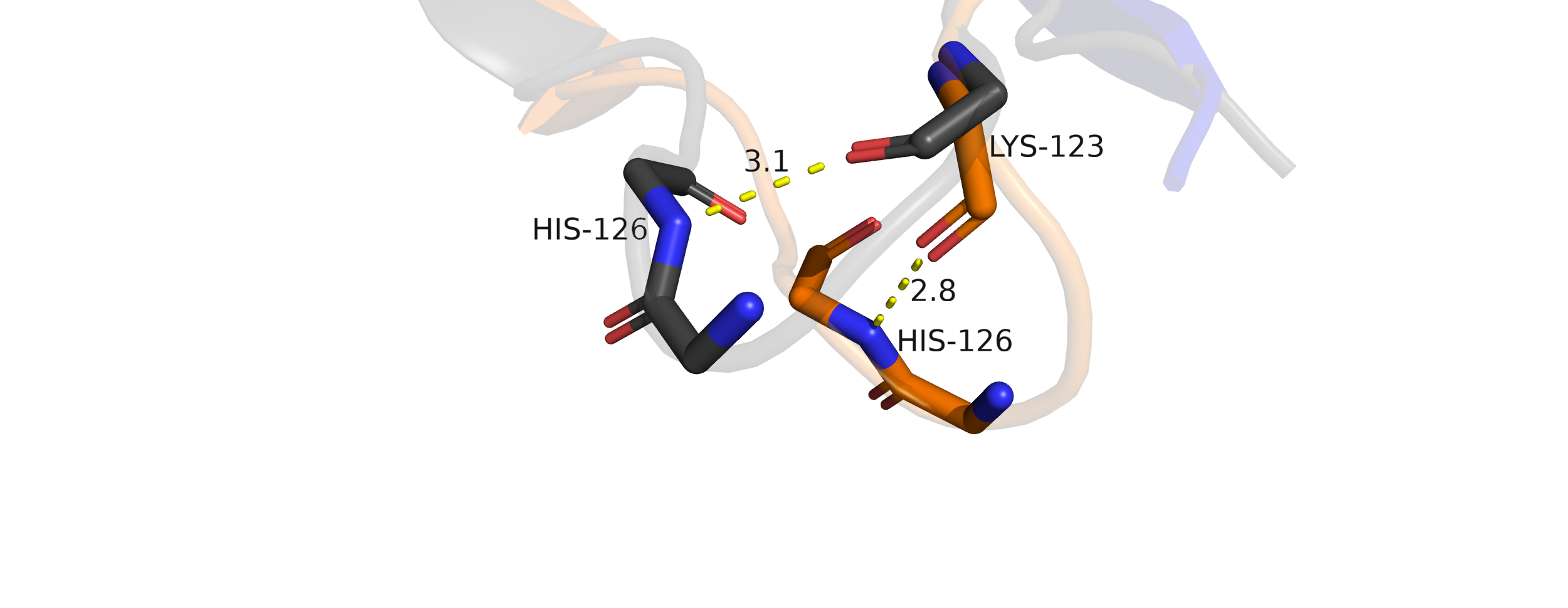
LYS123/O HIS126/N находятся на одной петле, выдающейся из белка |
| Расстояние в РСА | 3.0 | 2.8 |
| В каком числе (и проценте) моделей ЯМР есть водородная связь | 23 модели 100% |
10 моделей 43,5% |
| Min значение расстояния в ЯМР | 2.7 | 2.5 |
| Max значение расстояния в ЯМР | 3.2 | 4.1 |
| Медианное значение расстояния в ЯМР | 3.0 | 3.1 |

|

|
|
| Выводы | Связь подтверждается и в РСА, и во всех ЯМР моделях. Можно с уверенностью говорить о её существовани. | Связи нет или, возможно, она есть, но слабая, в большинстве ЯМР моделей. Это говорит о том, что, вероятно, связь не очень сильная. Кроме того, подвижность петли, в которй она расположена, может мешать её стабильности. |
© Антоненкова Юлия, 2017