Описание структуры белка с PDB ID 2GVV
СТРУКТУРА В ЦЕЛОМ
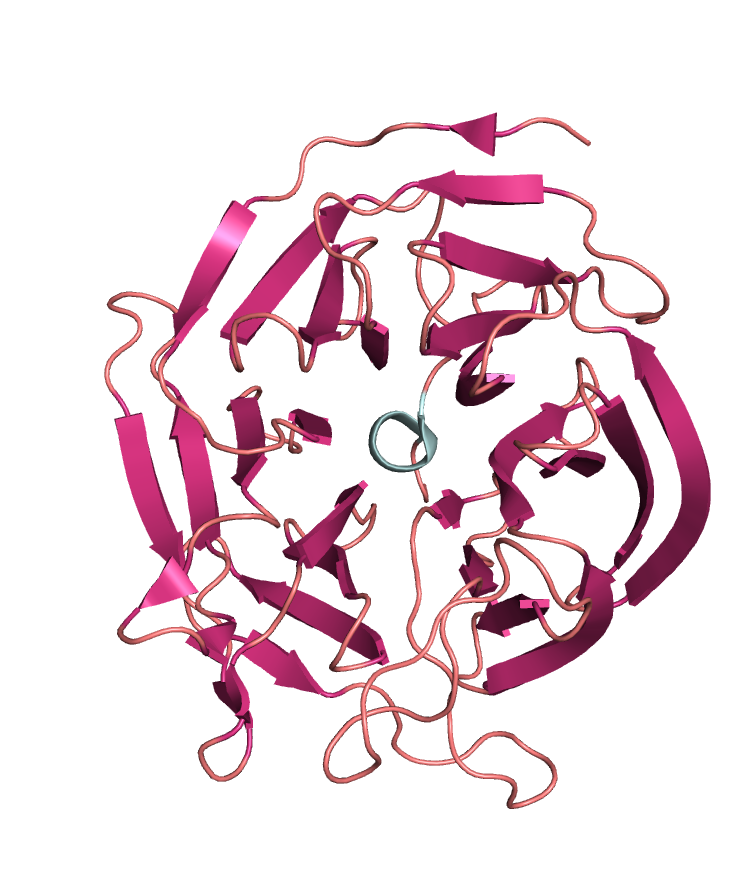
Тип макромолекулы: белок класса гидролаз (hydrolase). Название белка - диизопропилфлюорофосфатаза (diisopropyl fluorophosphatase (DFPase)). Общий вид структуры белка 2GVV показан на рис. 1.
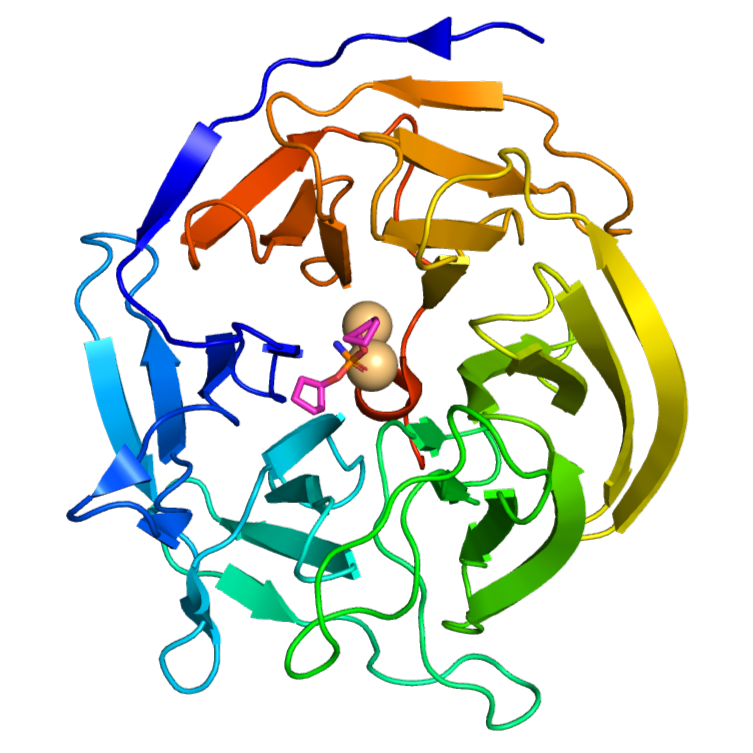
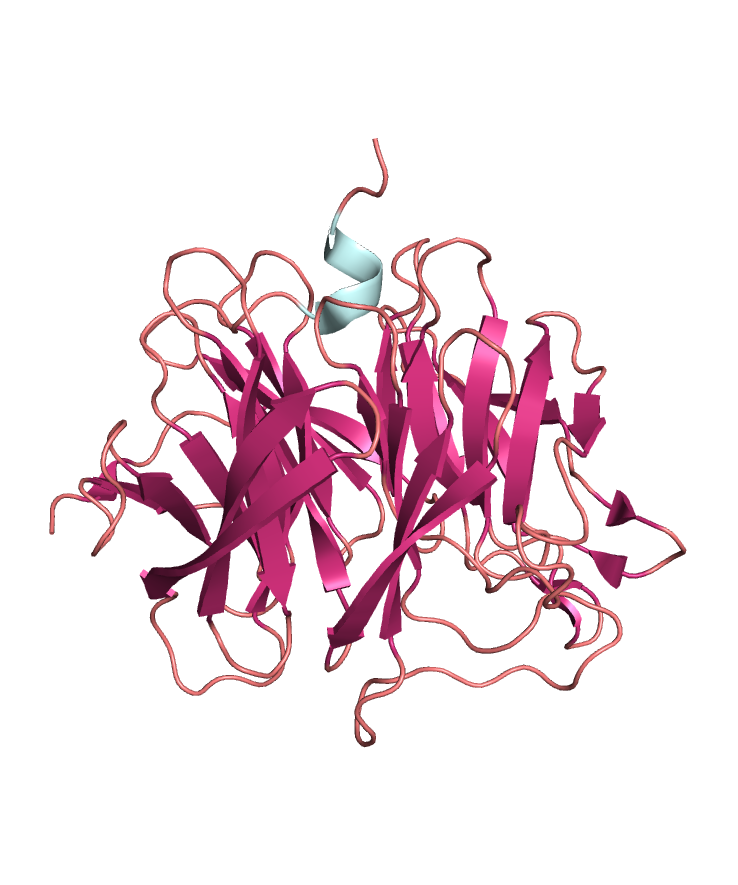
Полимерные цепи: в структуре молекулы присутствует одна полимерная цепь А, состоящая из 314 аминокислотных остатков. В биологическую единицу входит одна полимерная цепь А. Биологическая единица совпадает с асимметрической. Вид полимерной цепи А белка 2GVV показан на рис. 2.
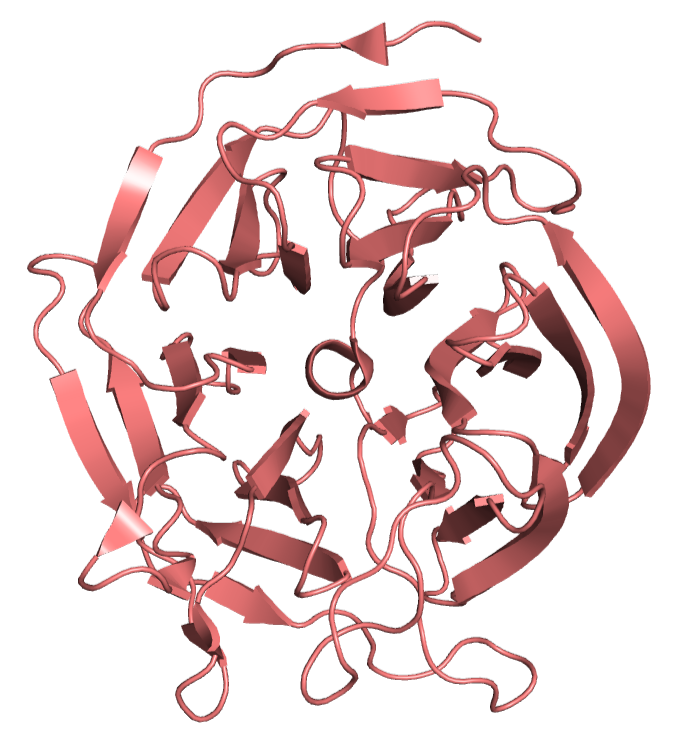
ОТДЕЛЬНЫЕ ЦЕПИ
Полимерная цепь А относится к Loligo vulgaris (Обыкновенный кальмар).
Uniprot_id: Q7SIG4.
Название: Диизопропилфлюорофосфатаза (Diisopropyl-fluorophosphatase (DFPase)). Биологическая функция и субстрат неизвестны. Однако фермент способен воздействовать на фосфорные ангидридные связи (такие как фосфор-галогенид и фосфор-цианид) в фосфорорганических соединениях (включая нервно-паралитические газы).
В последовательности нет мутаций относительно референса из Uniprot.
В составе цепи нет модифицированных аминокислотных остатков.
ВТОРИЧНАЯ СТРУКТУРА
Вторичная структура белка 2GVV в основном представлена бета-тяжами, соединёнными петлями. Также присутствует одна альфа-спираль в конце полимерной цепи А. Вторичная структура белка 2GVV показана на рис. 3, 4.
МАЛЫЕ МОЛЕКУЛЫ
1. Ион кальция (CA, CALCIUM ION).
2. Дициклопентил фосфорамидат (DI9, DICYCLOPENTYL PHOSPHORAMIDATE).
Белковое окружение лиганда DI9 показано на рис. 5.
Файлы с данными о малых молекулах из PDB: CА, DI9.
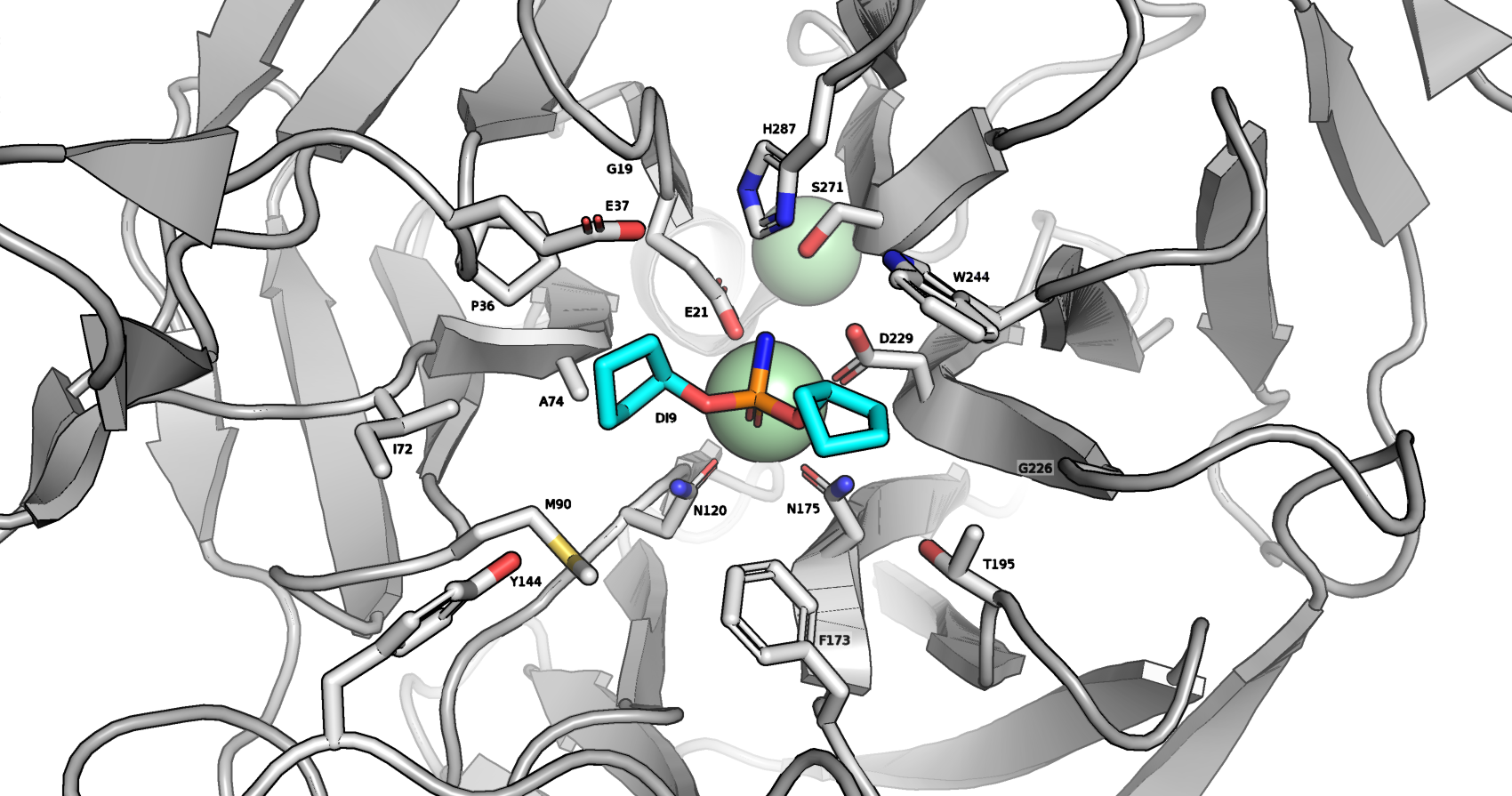
ВЗАИМОДЕСТВИЯ В БЕЛКЕ 2GVV
Водородные связи, затрагивающие атомы остова белка
На рис. 6 изображены Водородные связи, затрагивающие атомы остова белка, между аминокислотами ILE-249 и ILE-263, ARG-264 и ILE-6, ARG-262 и ILE-6.
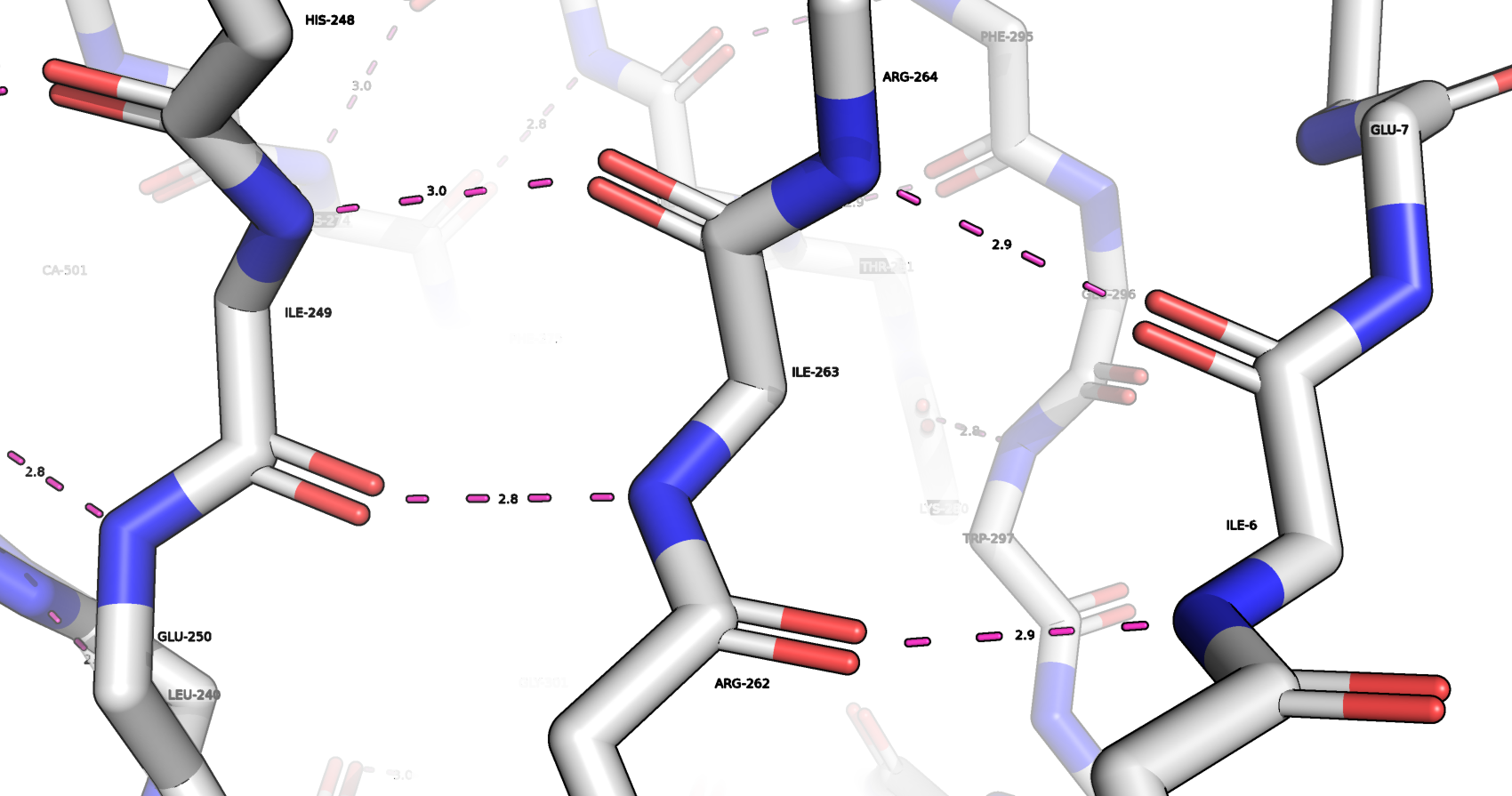
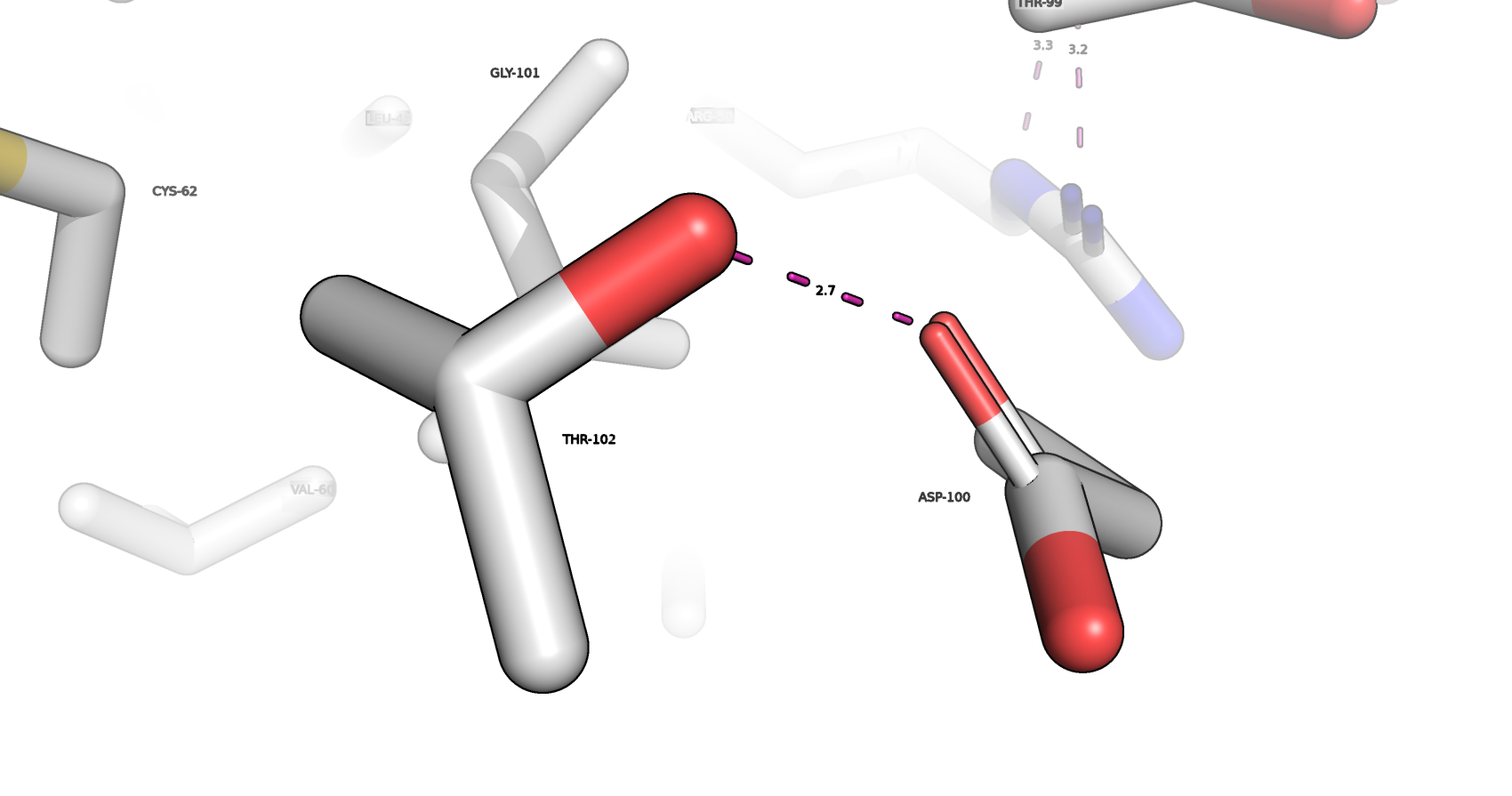
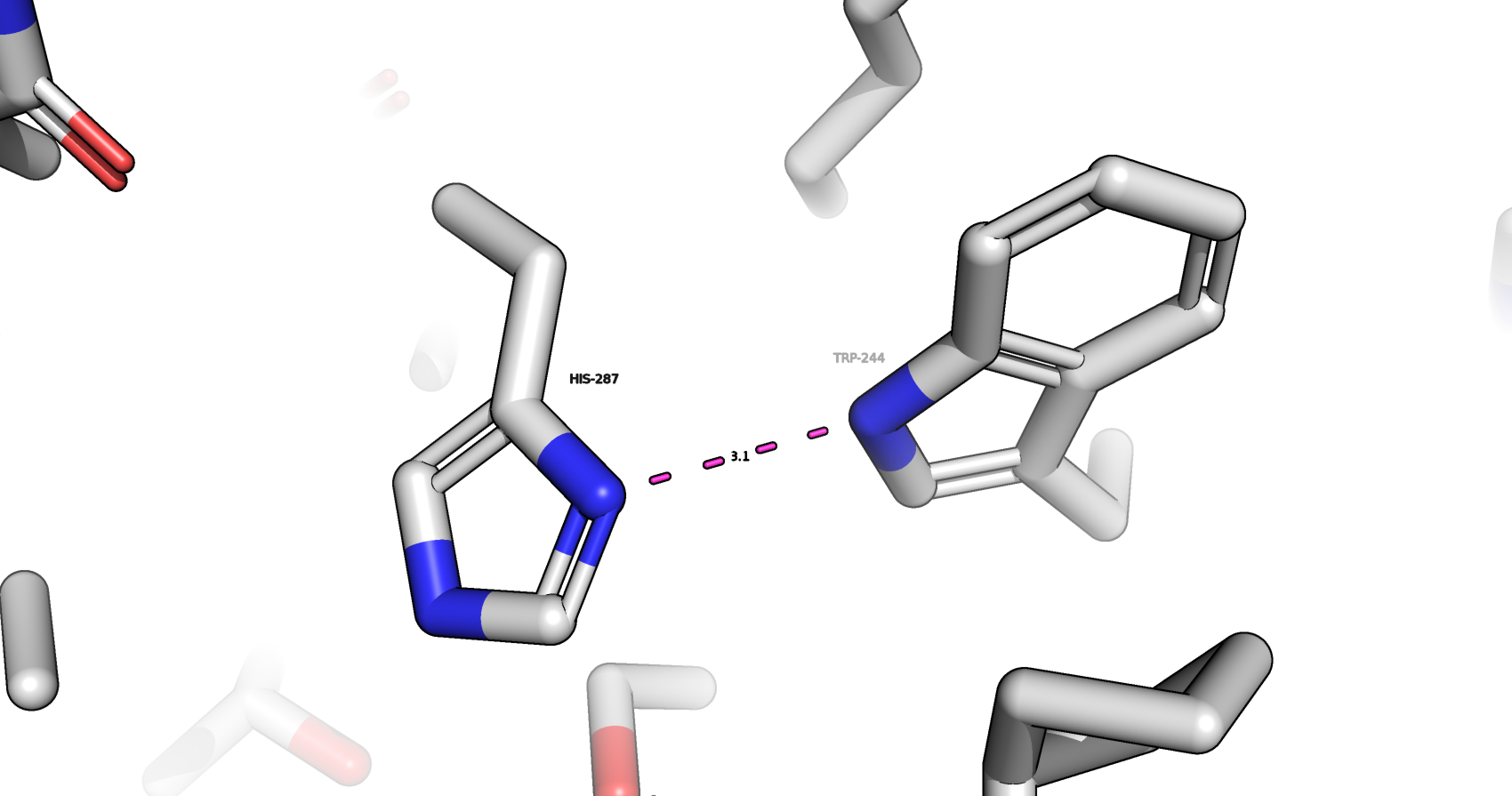
Водородные связи, затрагивающие атомы боковых радикалов аминокислот
На рис. 7, 8 изображены водородные связи между боковыми радикалами аминокислот THR-102 и ASP-100, HIS-287 TRP-244.
Солевые мостики
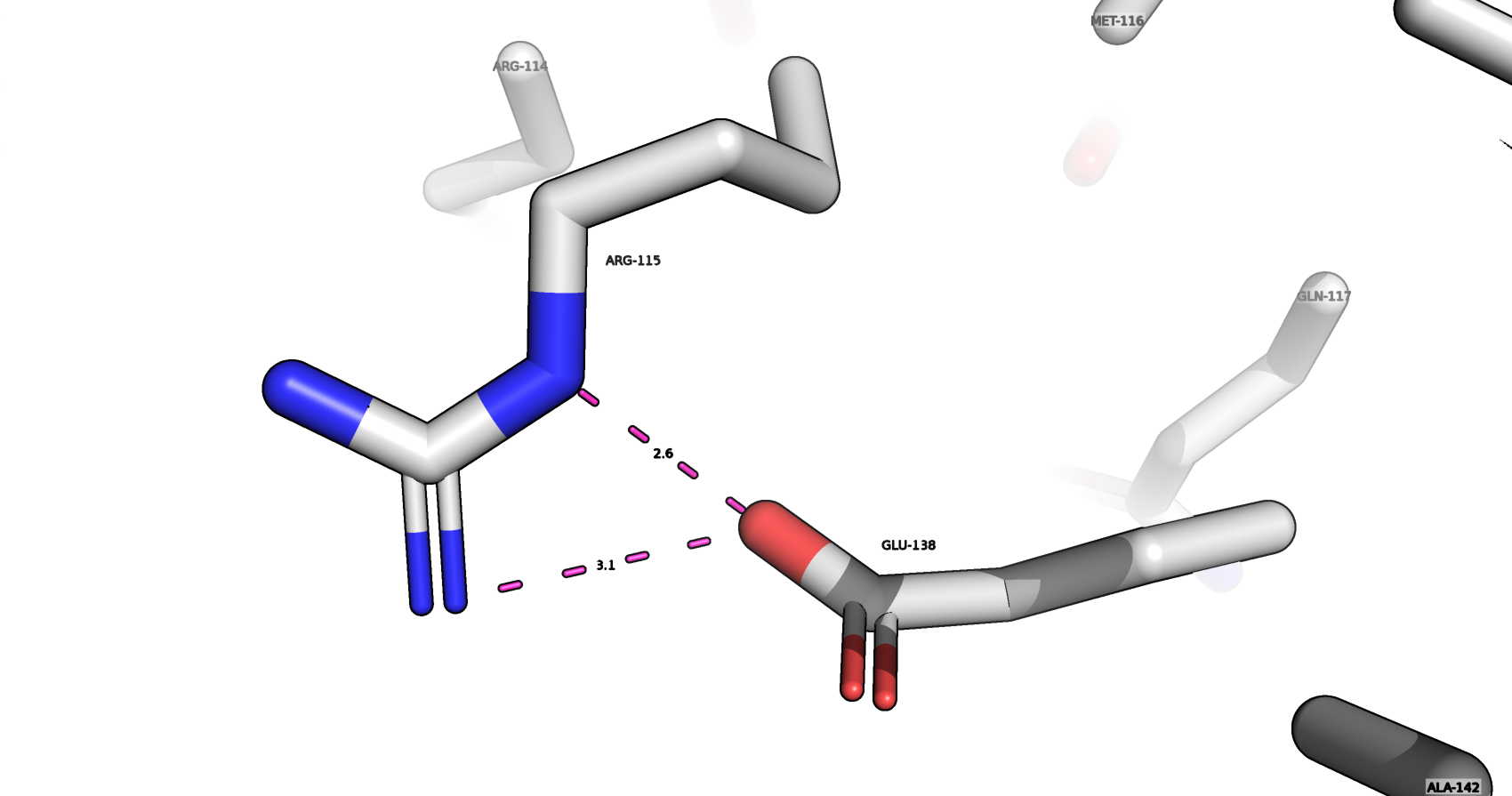
На рис. 9 изображены солевые мостики между аминокислотами ARG-115 и GLU-138.
Дисульфидные связи
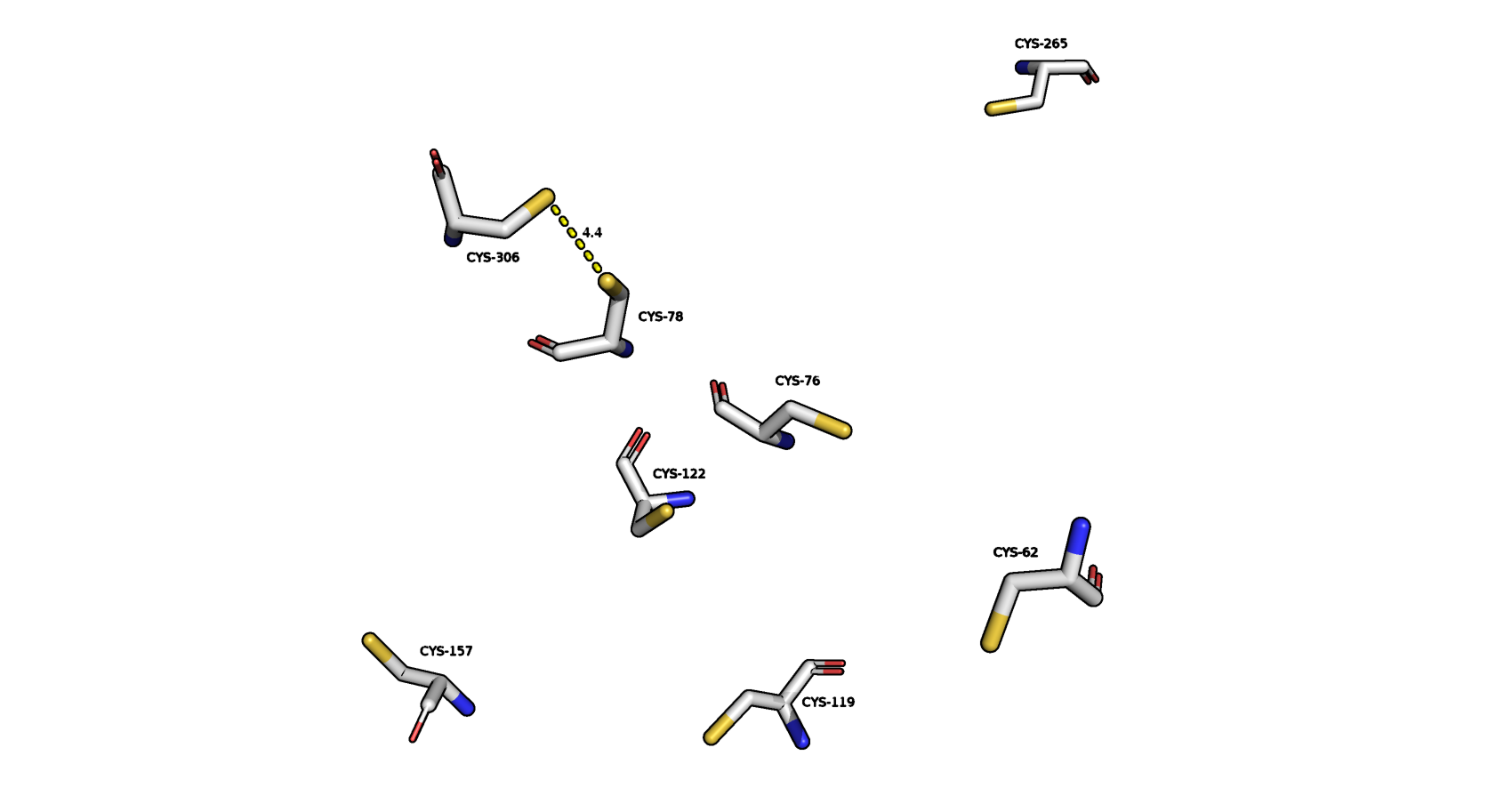
В белке 2GVV присутствуют цистеины, однако они не образуют дисульфидных связей. Наименьшее расстояние между цистеинами составляет 4.4 А (между CYS-306 и CYS-78). Все цистеины белка 2GVV изображены на рис. 10.
Стекинг-взаимодействия
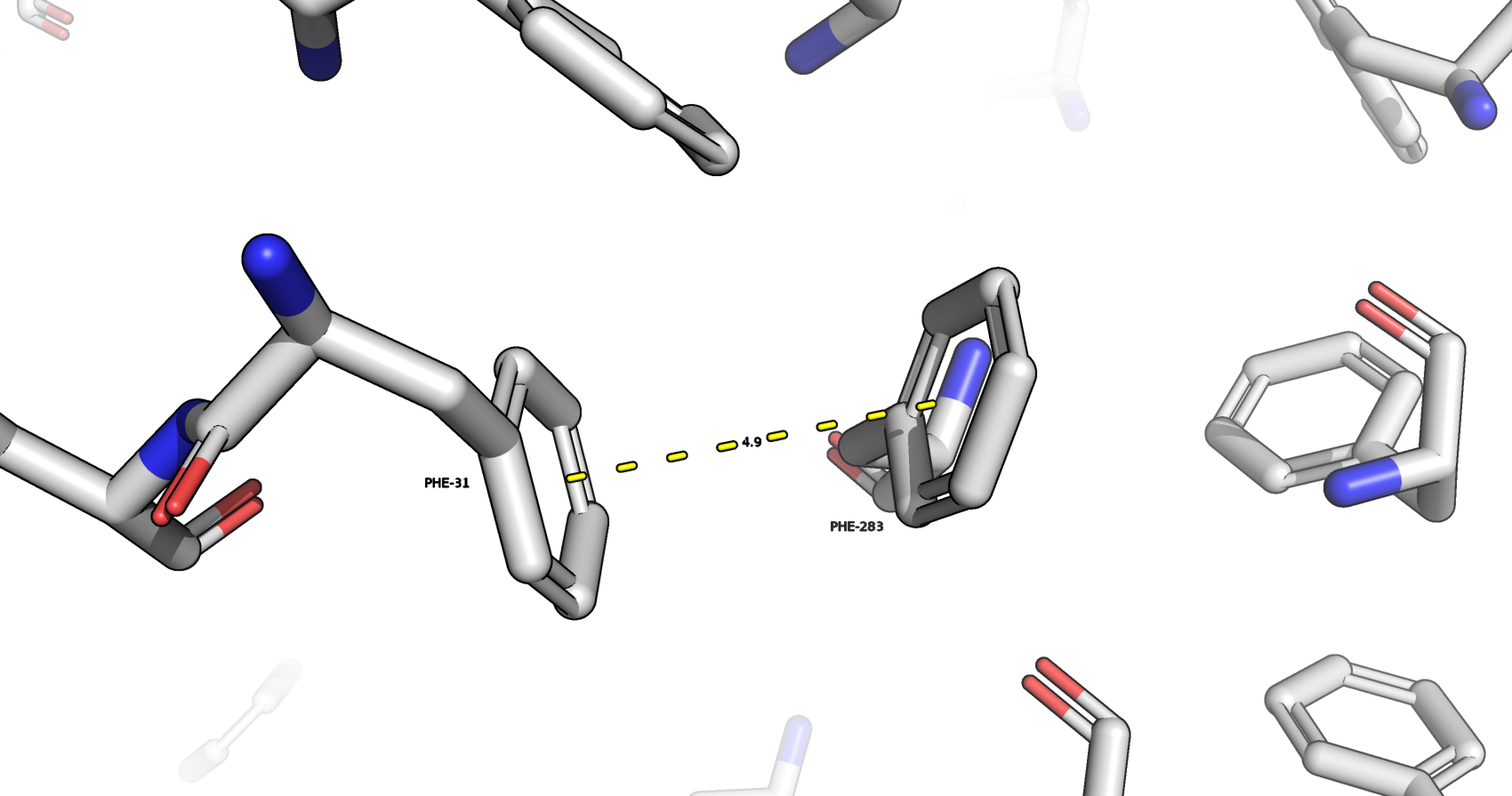
В структуре белка присутствуют ароматические кольца аминокислот триптофана, тирозина и фенилаланина. На рис. 11 показано расстояние (4.9 А) между аминокислотами PHE-31 и PHE-283. Они расположены достаточно близко для возможных стекинг-взаимодействий (допустимое расстояние 4-6 А).
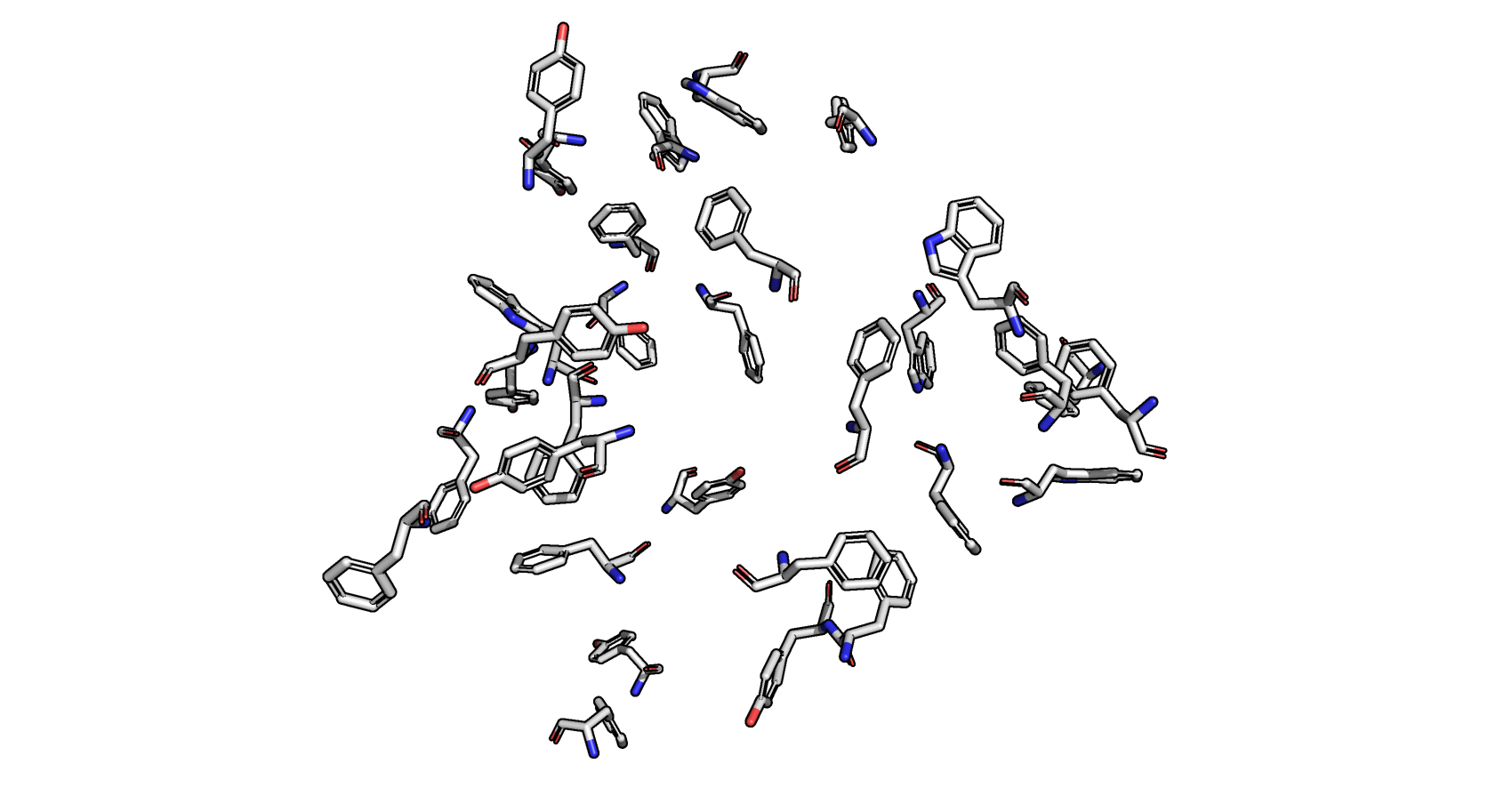
На рис. 12 изображены все ароматические кольца аминокислот триптофана, тирозина и фенилаланина, присутствующие в белке 2GVV.
СПИСОК ЛИТЕРАТУРЫ
1. Информация о белке 2GVV из базы данных PDB: PDB
2. Информация о белке Q7SIG4 из базы данных Uniprot: Uniprot