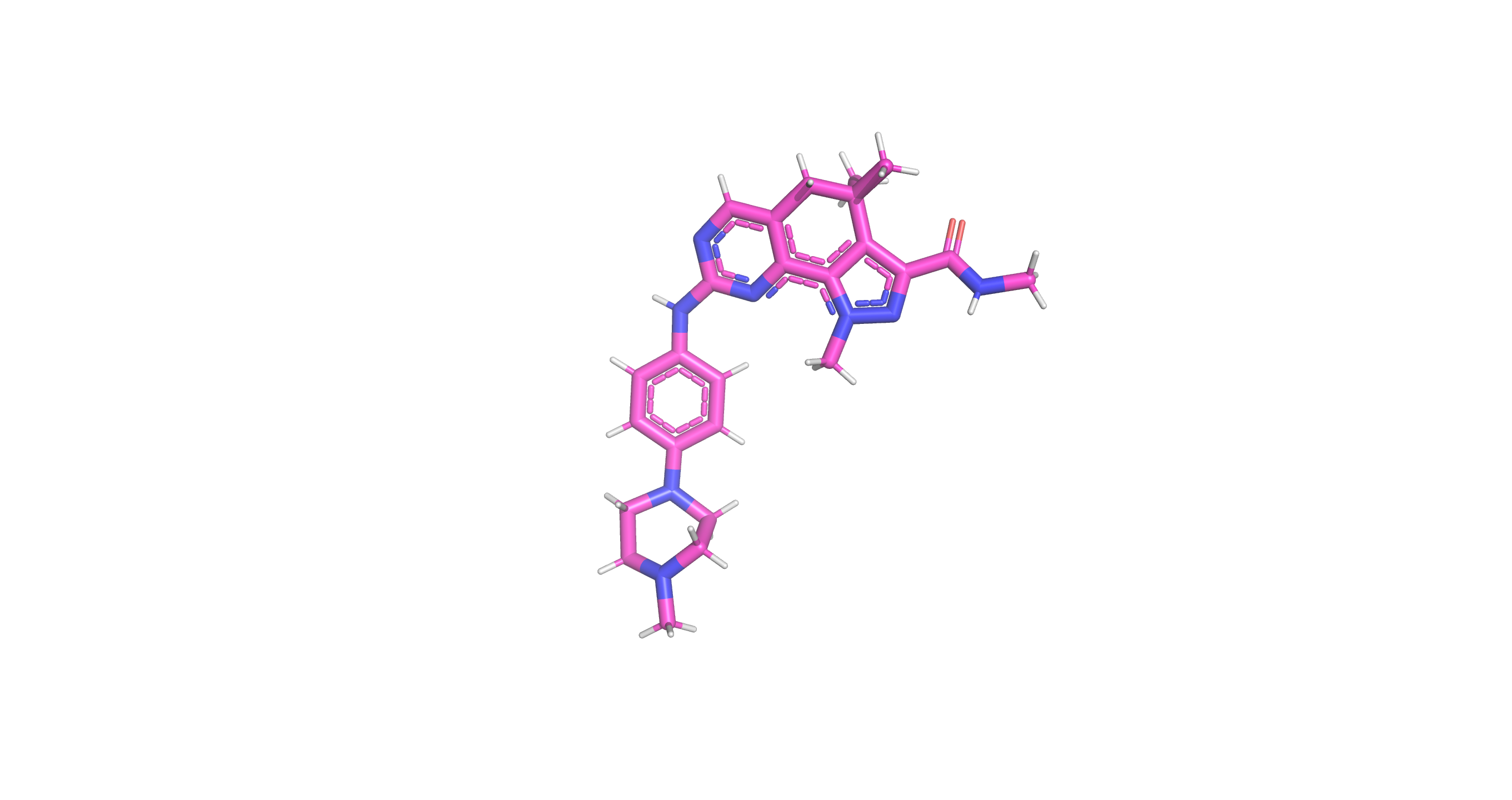
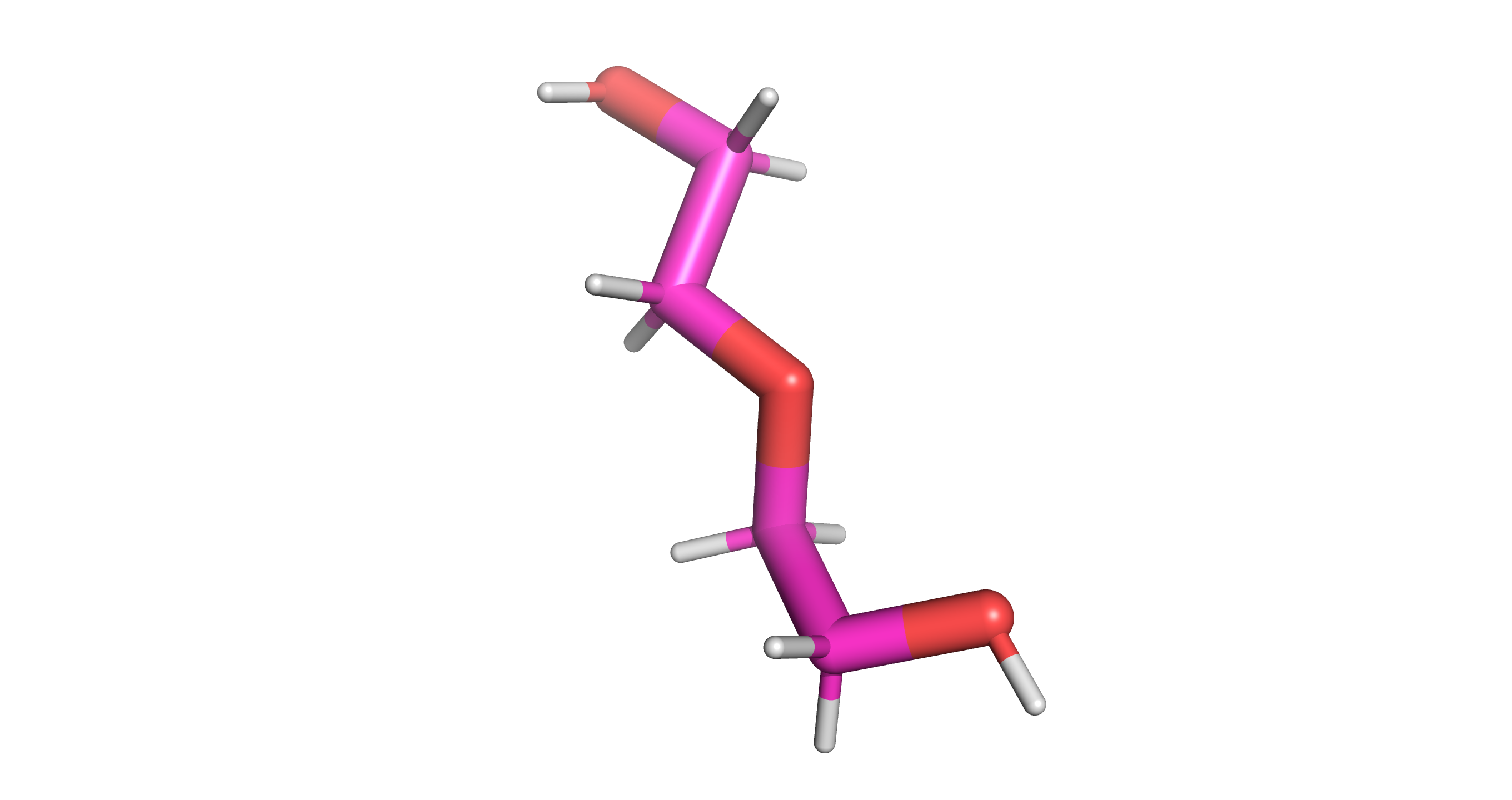Структура киназного домена человека MYT1 в комплексе с PHA-848125
PDB: 5VD1
Макромолекула
На рис1 представлена структура киназного домена человека MYT1
(мембраноассоциированной тирозин- и треонин-специфической cdc2-ингибирующей киназы)
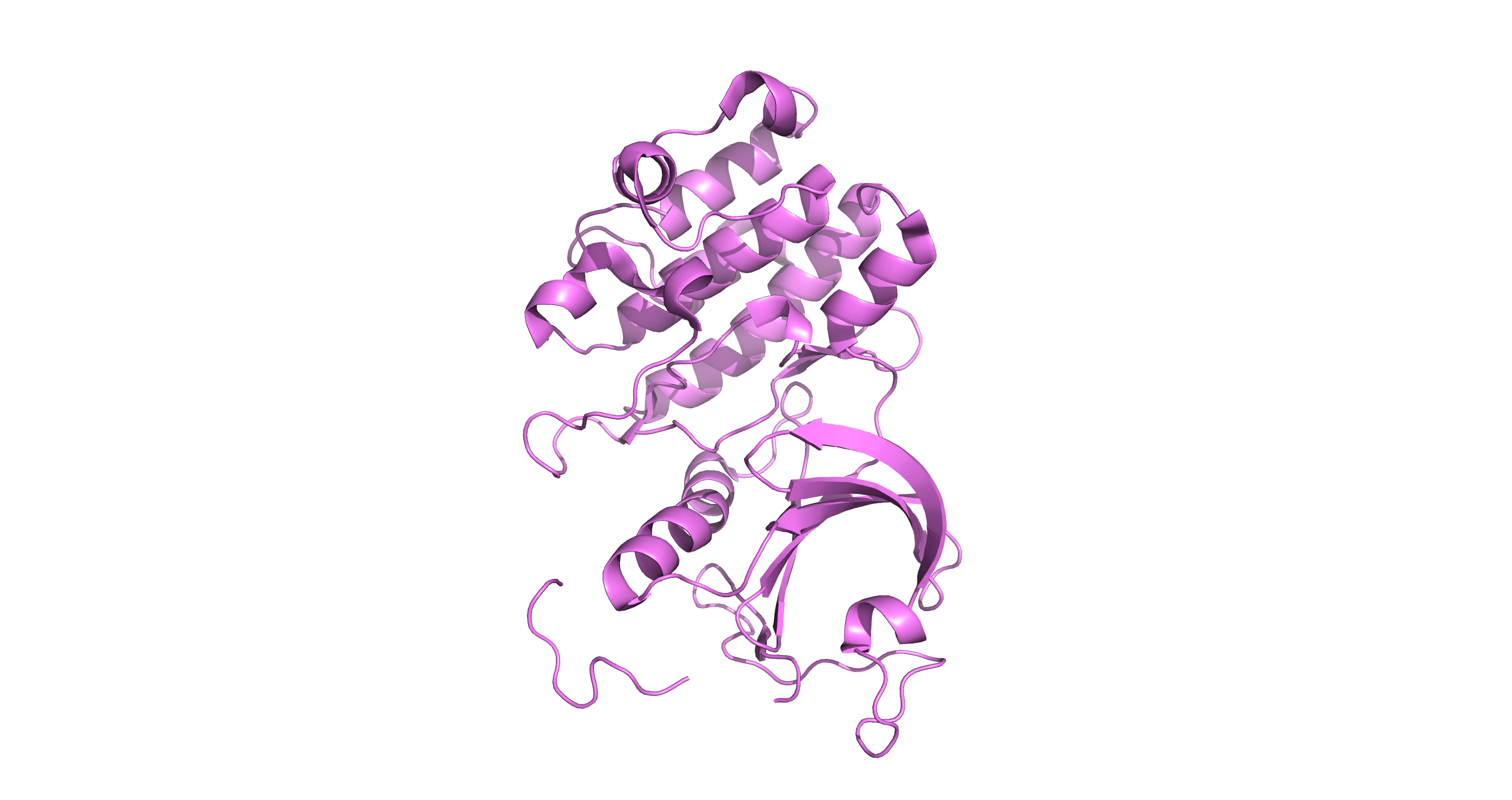
Рис1. Структура белка
Белок состоит из одной цепи. Биологическая единица совпадает с ассиметрической.
Согласно данным UniProt (ID: Q99640), белок действует как негативный регулятор вступления в митоз (переход от G2 к M) путем фосфорилирования киназы CDK1, в частности, когда CDK1 образует комплекс с циклинами. Также обеспечивает фосфорилирование CDK1 преимущественно на 'The-14'. Также участвует во фрагментации Гольджи. Может быть вовлечен в фосфорилирование CDK1 на 'Tyr15' в меньшей степени, однако активность тирозинкиназы неясна и может быть косвенной. Вероятно является нижестоящей мишенью сигнального пути Notch во время развития глаза.
Мутаций в последовательности относительно референсной из UniProt нет.
В составе цепи есть модифицированные аминоксилоты: N-ацетилметионин, фосфотреонин, фосфотирозин, фосфосерин.
На рис2 представлена вторичная структура киназного домена человека MYT1
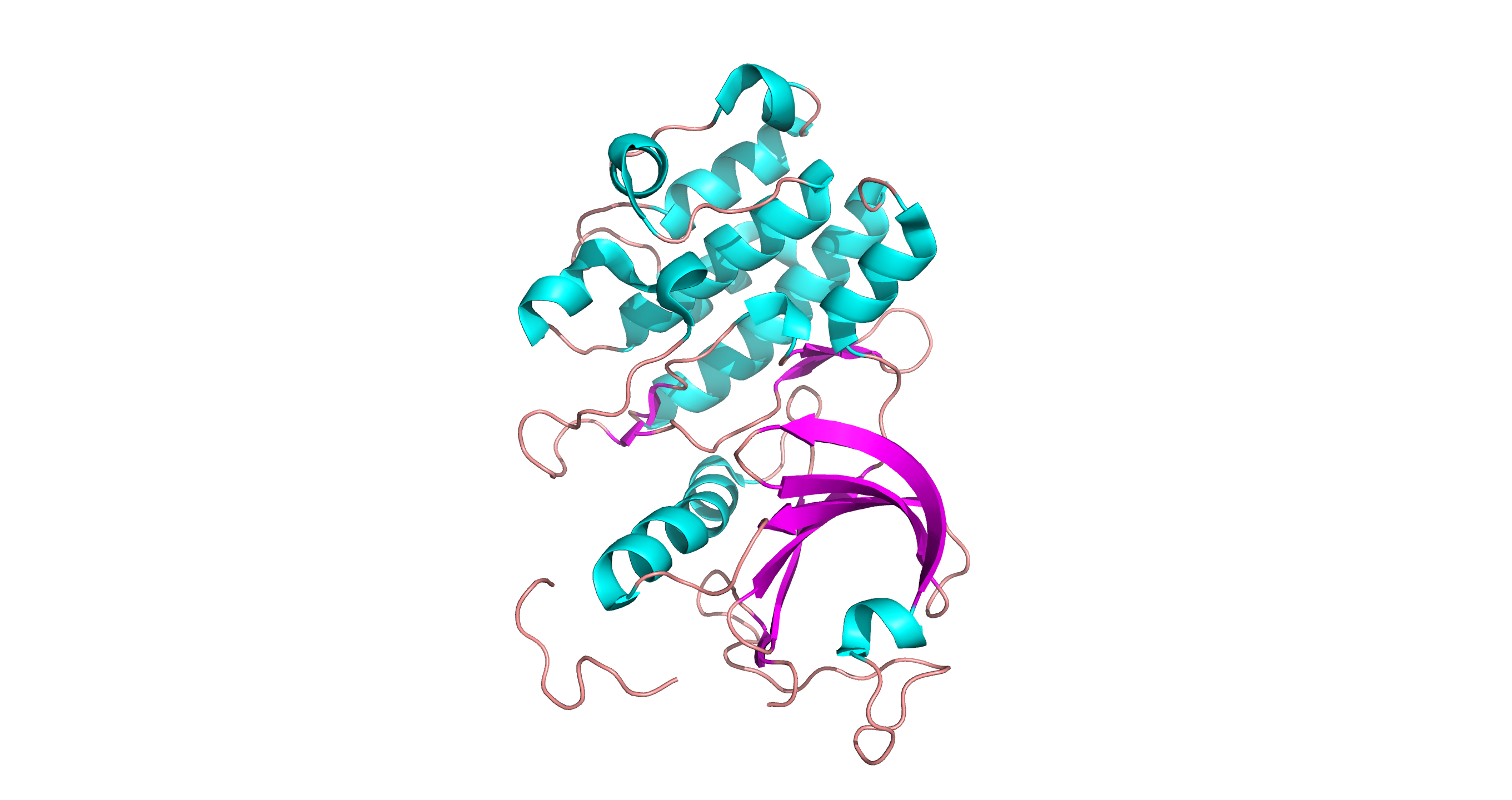
Рис2. Вторичная структура белка
Микромолекулы
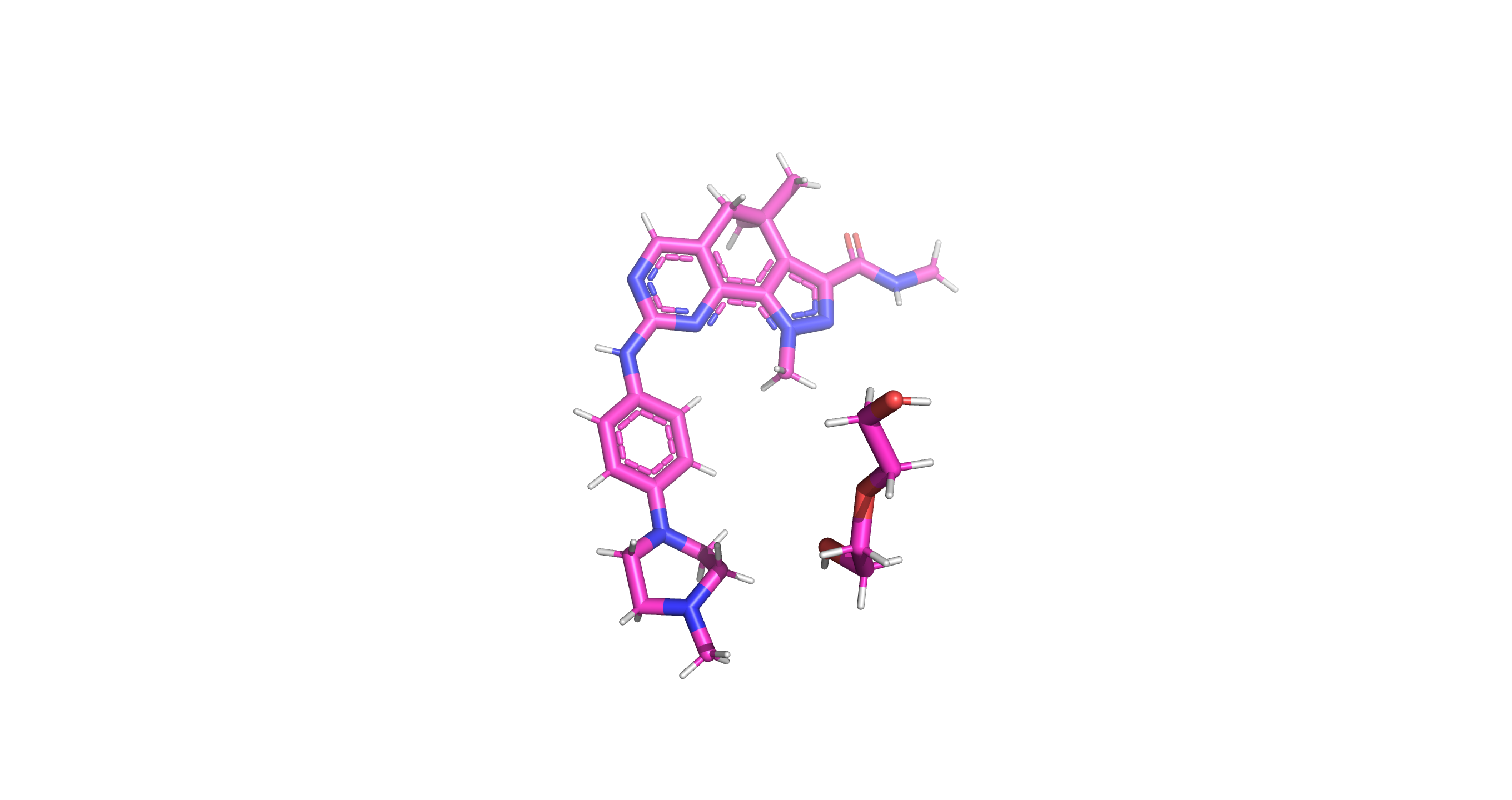
Рис3. Микромолекулы
Для микромолекулы P48 на рис4 и рис5 изображены аминокислотные остатки на расстоянии 5 ангстрем от молекулы лиганда
В окружении находятся такие аминокислотные остатки как: аргинин, аланин, аспарагин, аспартат, валин, гистидин, глицин, глутамин, лейцин, лизин, пролин, серин, треонин, цистеин
(к сожалению, это лучшиие из получившихся фотографий, слишком много аминокислот :(( )
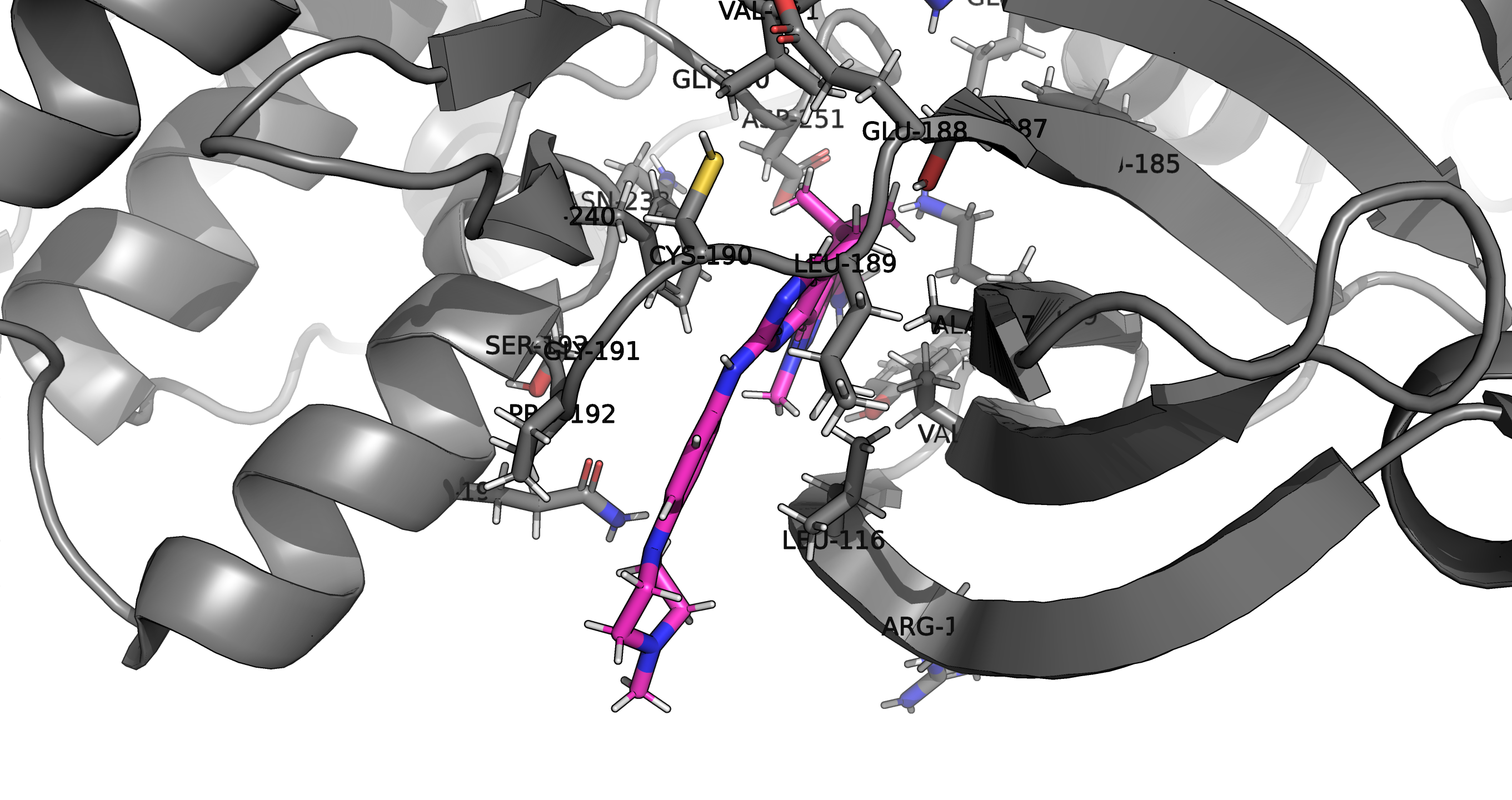
Рис4. Аминокислотное окружение (с остатками белковых цепей)
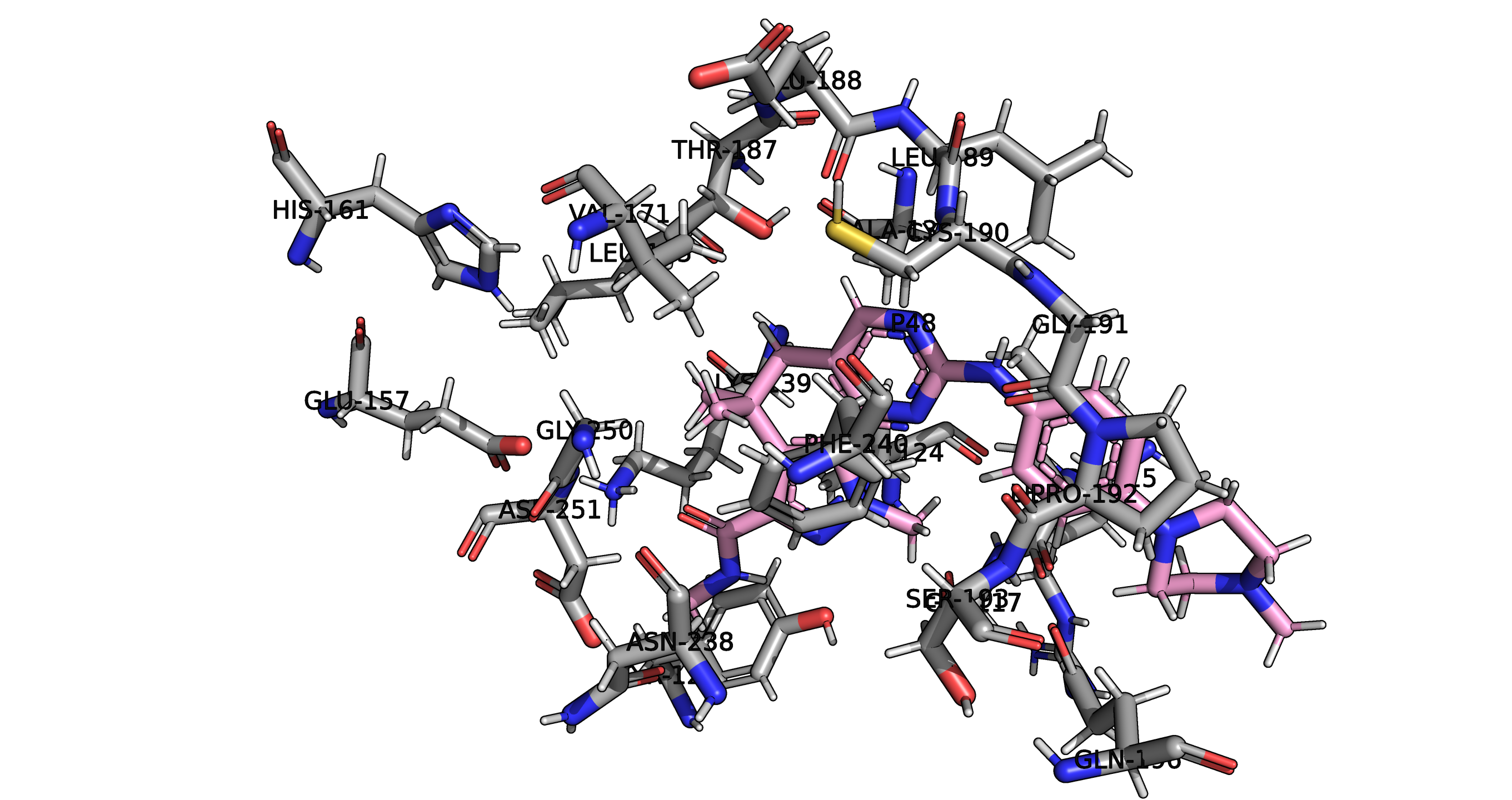
Рис5. Аминокислотное окружение
Взаимодействия между аминокислотами
В этом белке присутсвуют такие взаимодействия как: водородные связи, солевые мостики, pi-pi взаимодействия.
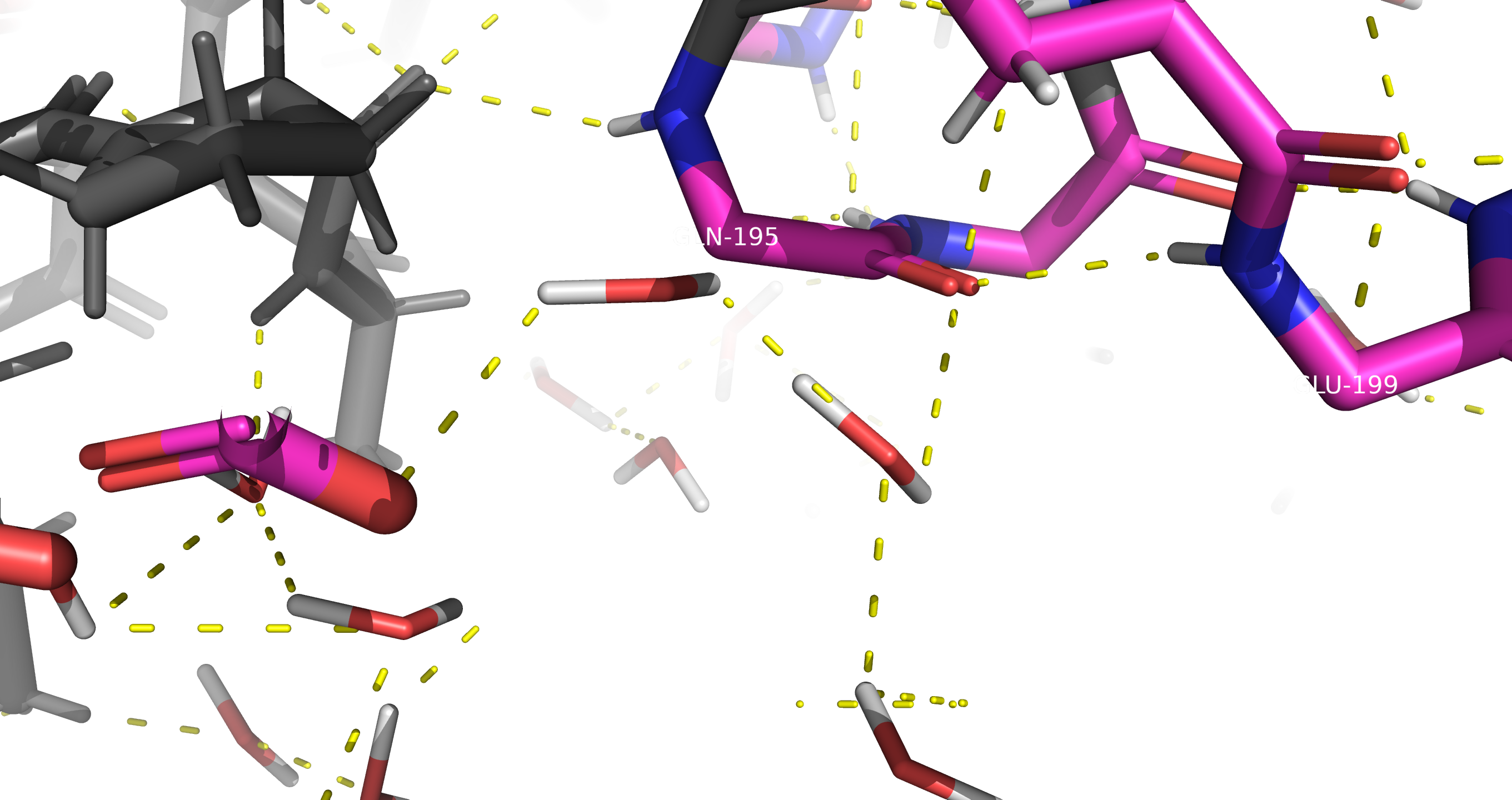
Рис6. Водородная связь, затрагивающая атомы остова белка
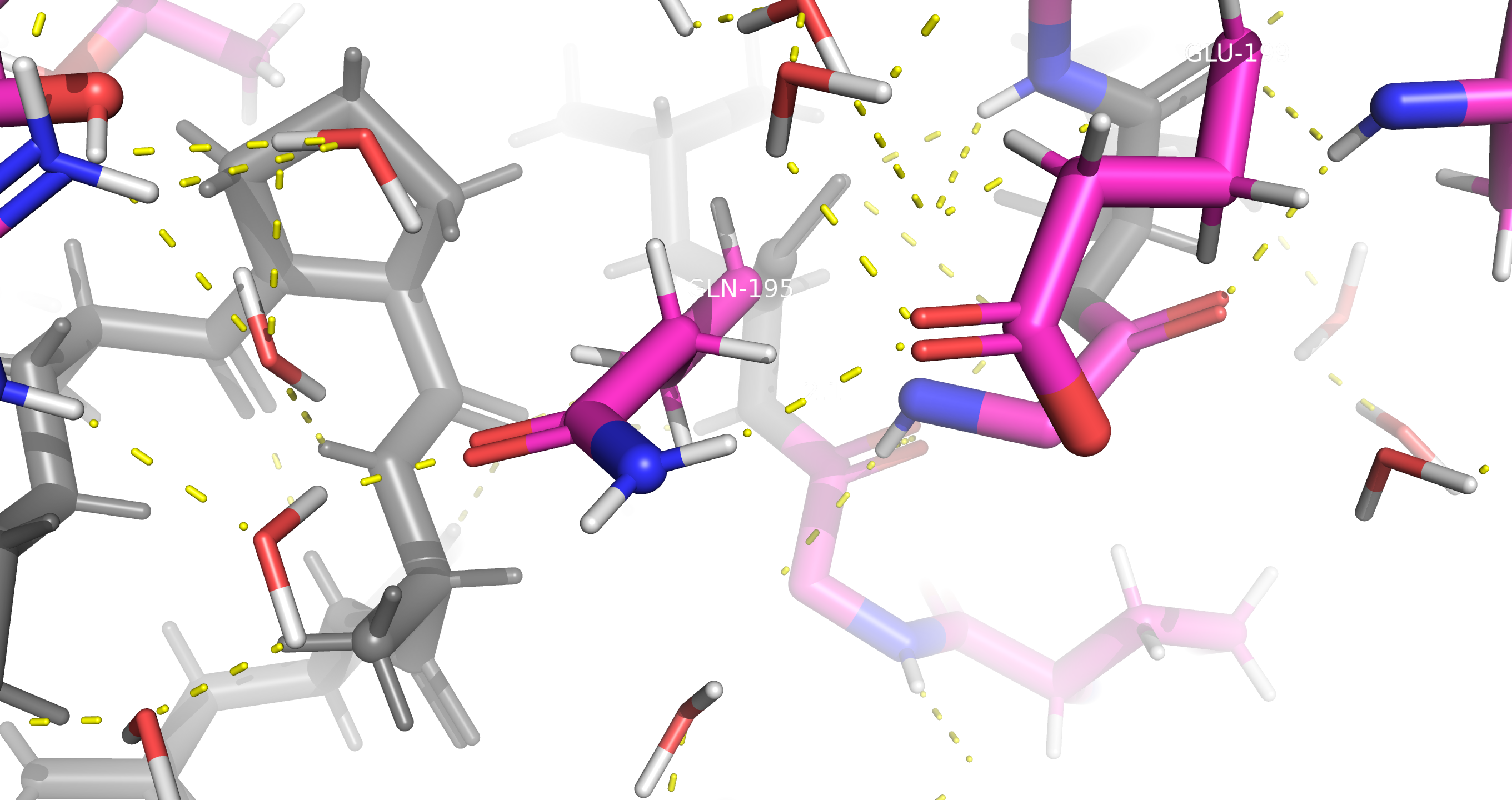
Рис7. Водородная связь, затрагивающая атомы боковых радикалов аминокислот
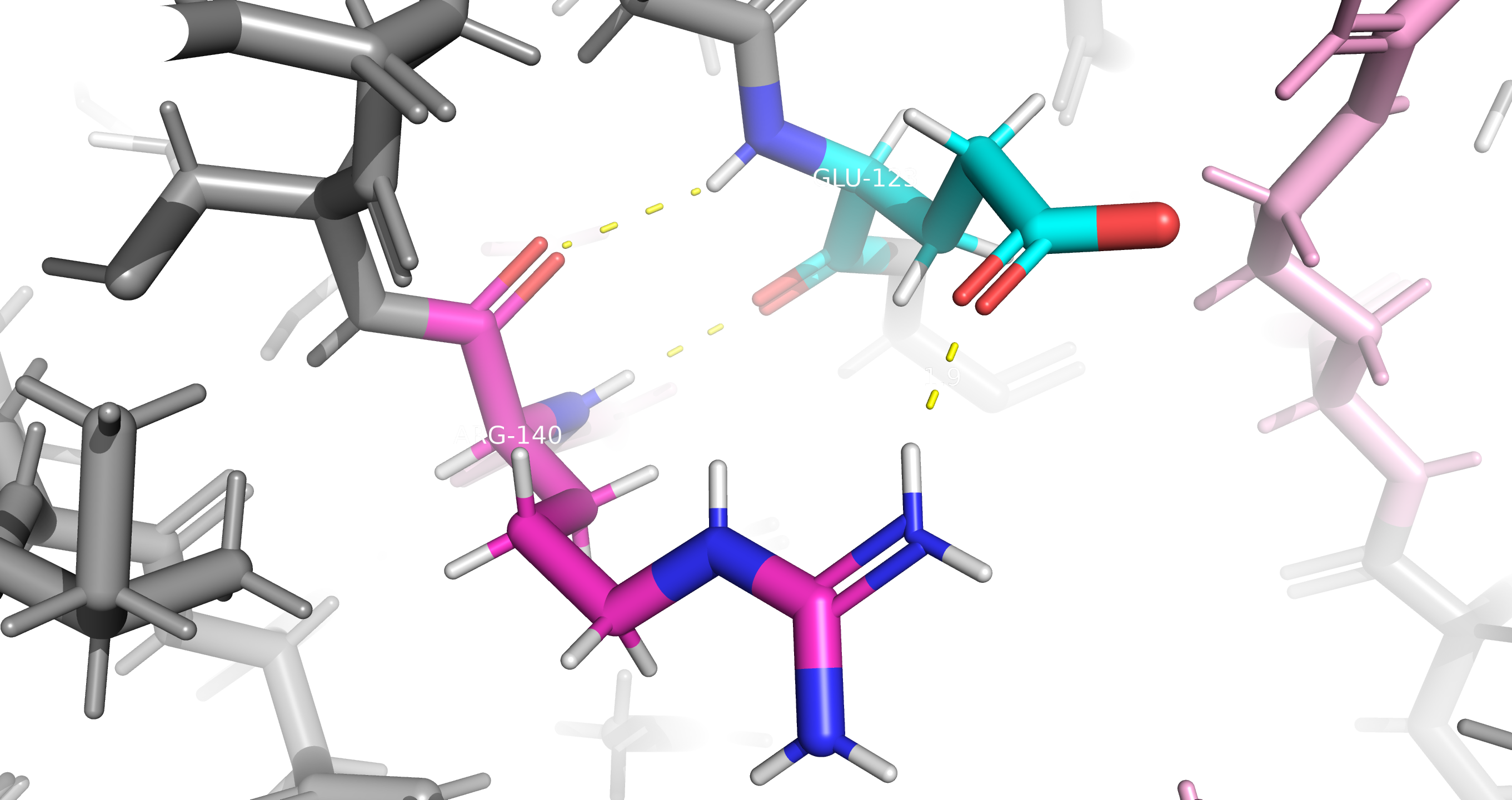
Рис8. Солевой мостик между Аргинином и Глутаматом
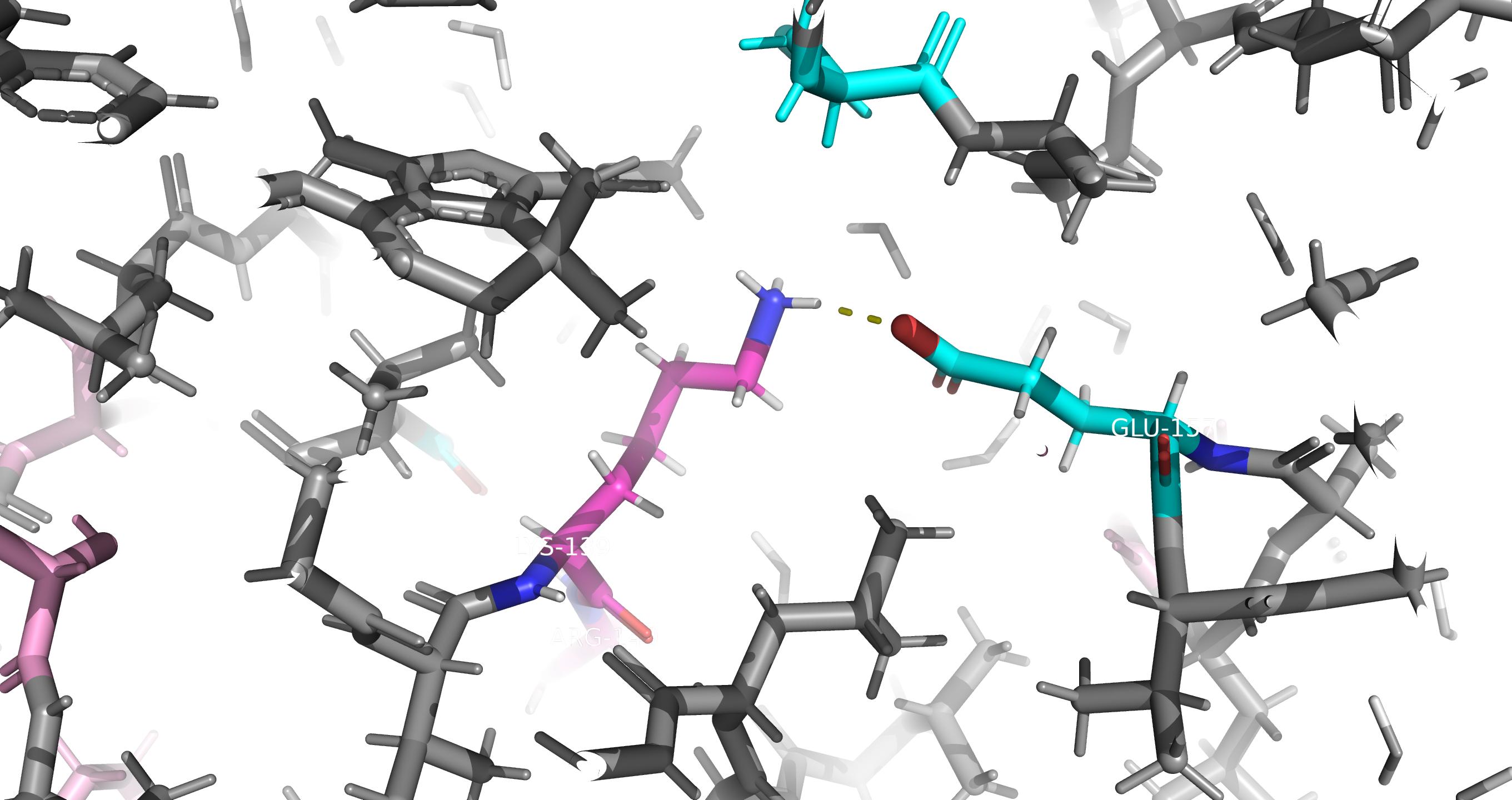
Рис9. Солевой мостик между Лизином и Глутаматом
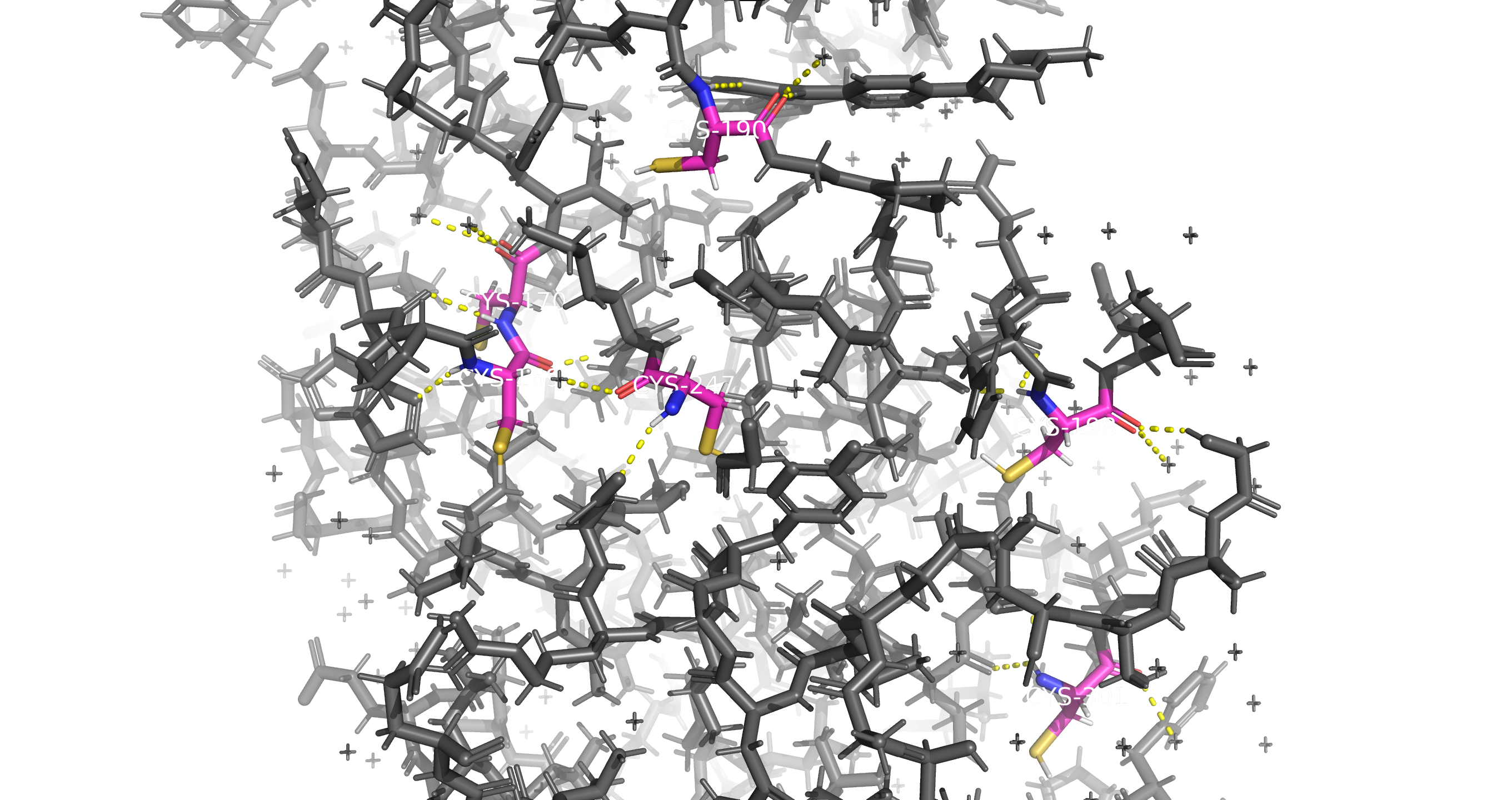
Рис10. Отсутсвие дисульфидной связи (все цистеины белка)
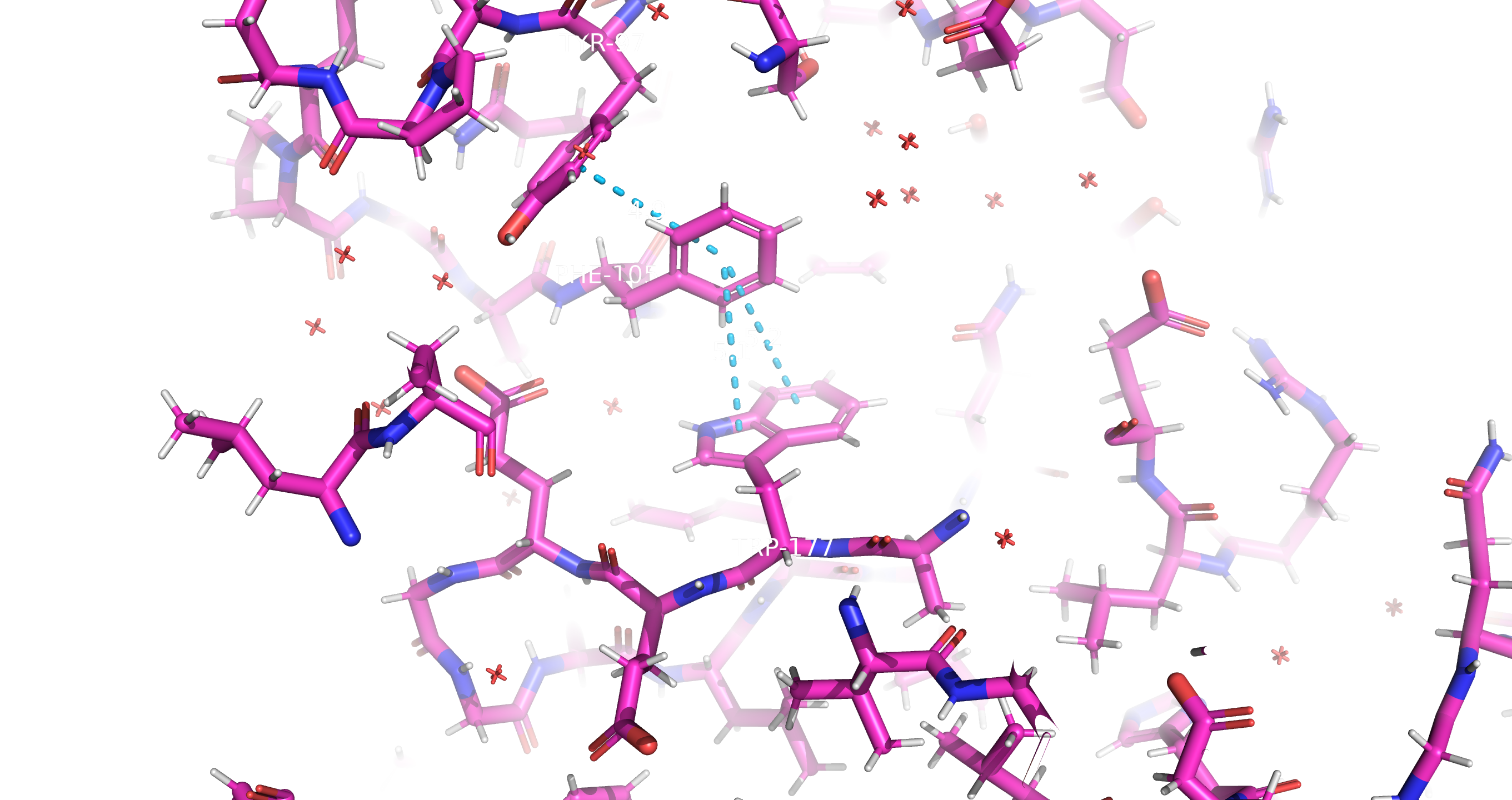
Рис11. Стекинг (pi-pi взаимодействия)
Каталитический центр
Неспецифическая серин/треониновая протеинкиназа (другое название этого белка) выполняет функцию фосфорилирования L-серина и L-треонина с использованием АТФ
Ссылка на EXPAZY с кратким описанием каталитической активности
Реакции:
ATP + L-seryl-[protein] <=> ADP + H(+) + O-phospho-L-seryl-[protein]
ATP + L-threonyl-[protein] <=> ADP + H(+) + O-phospho-L-threonyl-[protein]
Рассматривая подробную аннотацию последовательности белка, можно выяснить, что в состав каталитического центра этого фермента входит только аминокислота Аспартат (ASP на позиции 233).
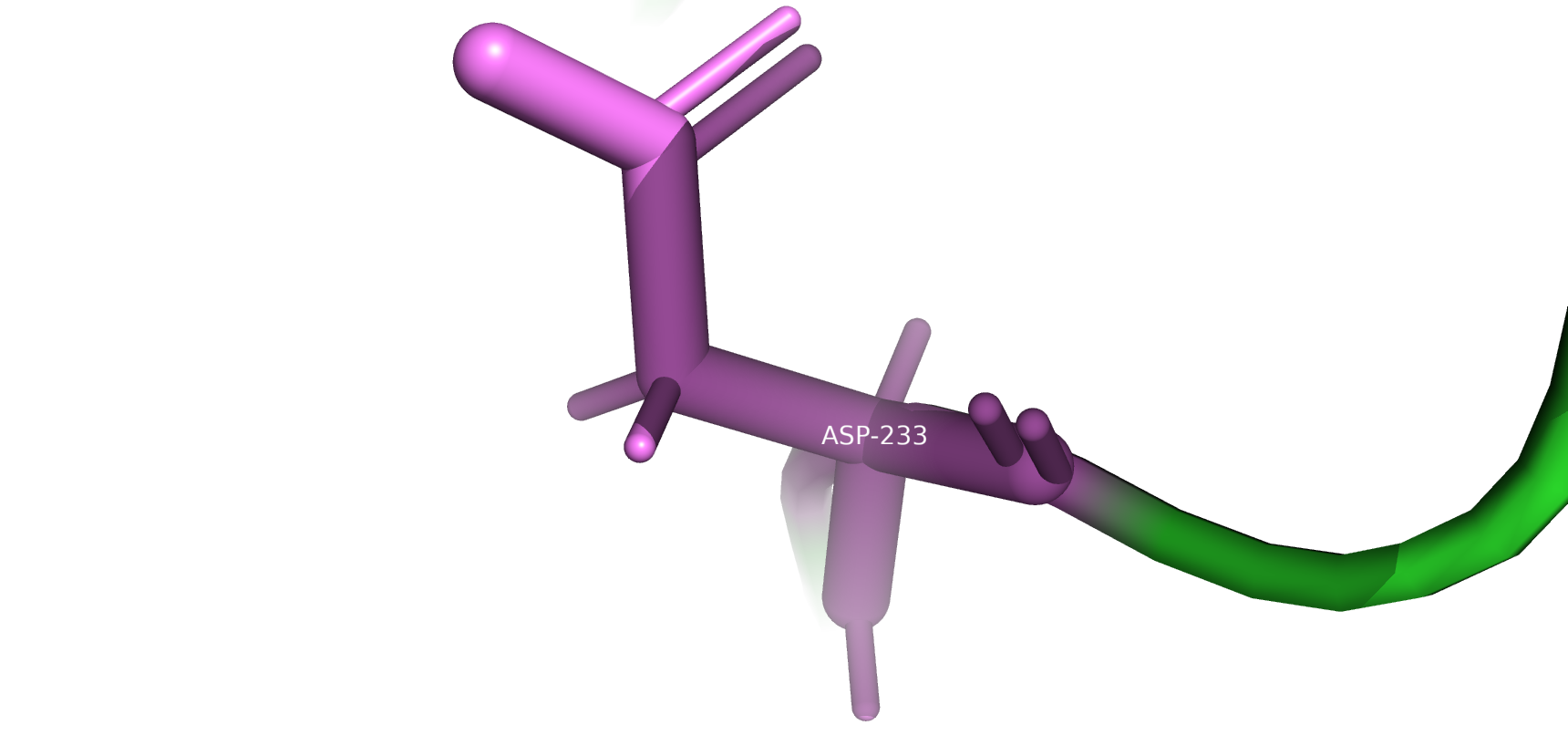
Рис12. Активный центр, аминокислота Изолейцин
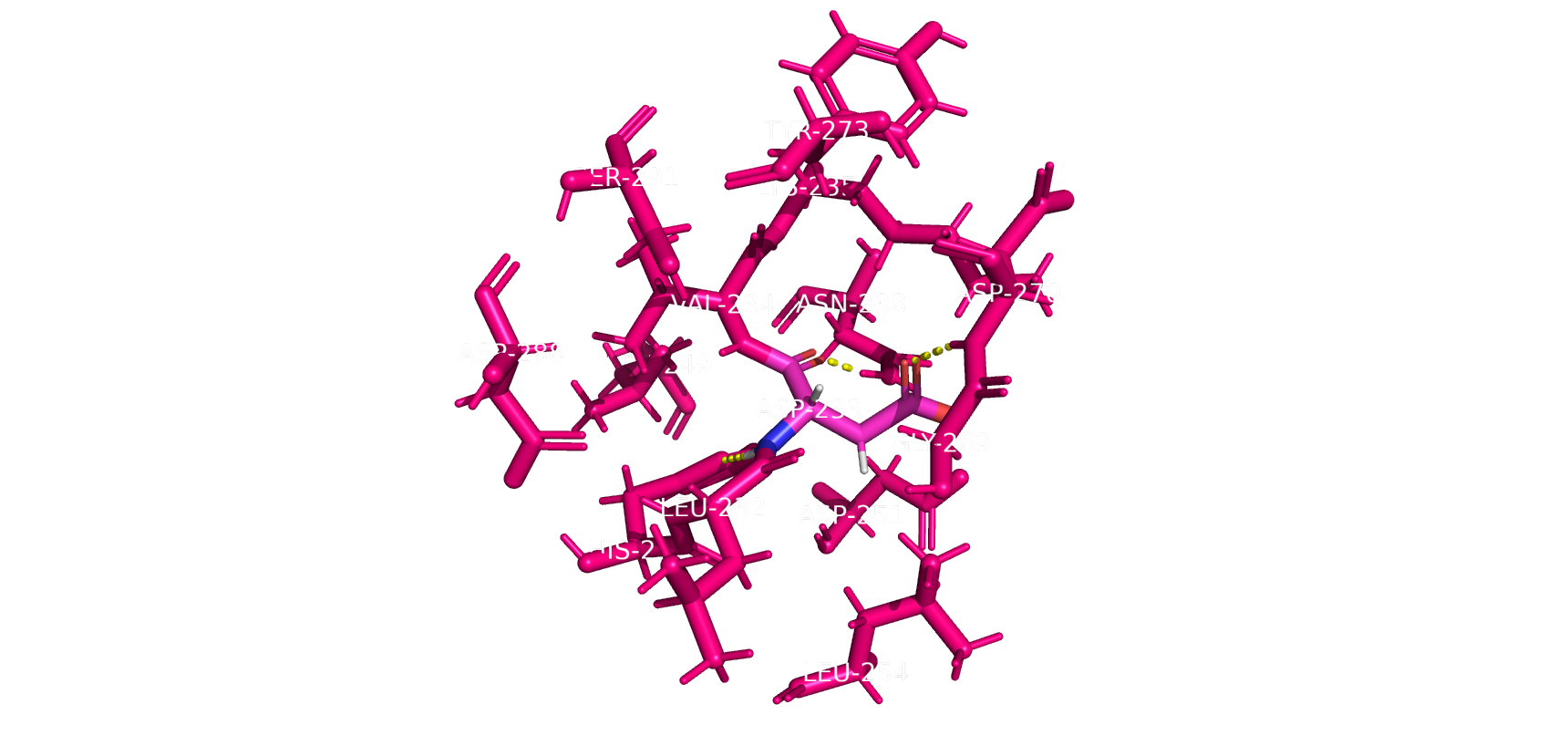
Рис13. Окружение активного (каталитичсекого) центра на расстоянии до 5 Ангстрем
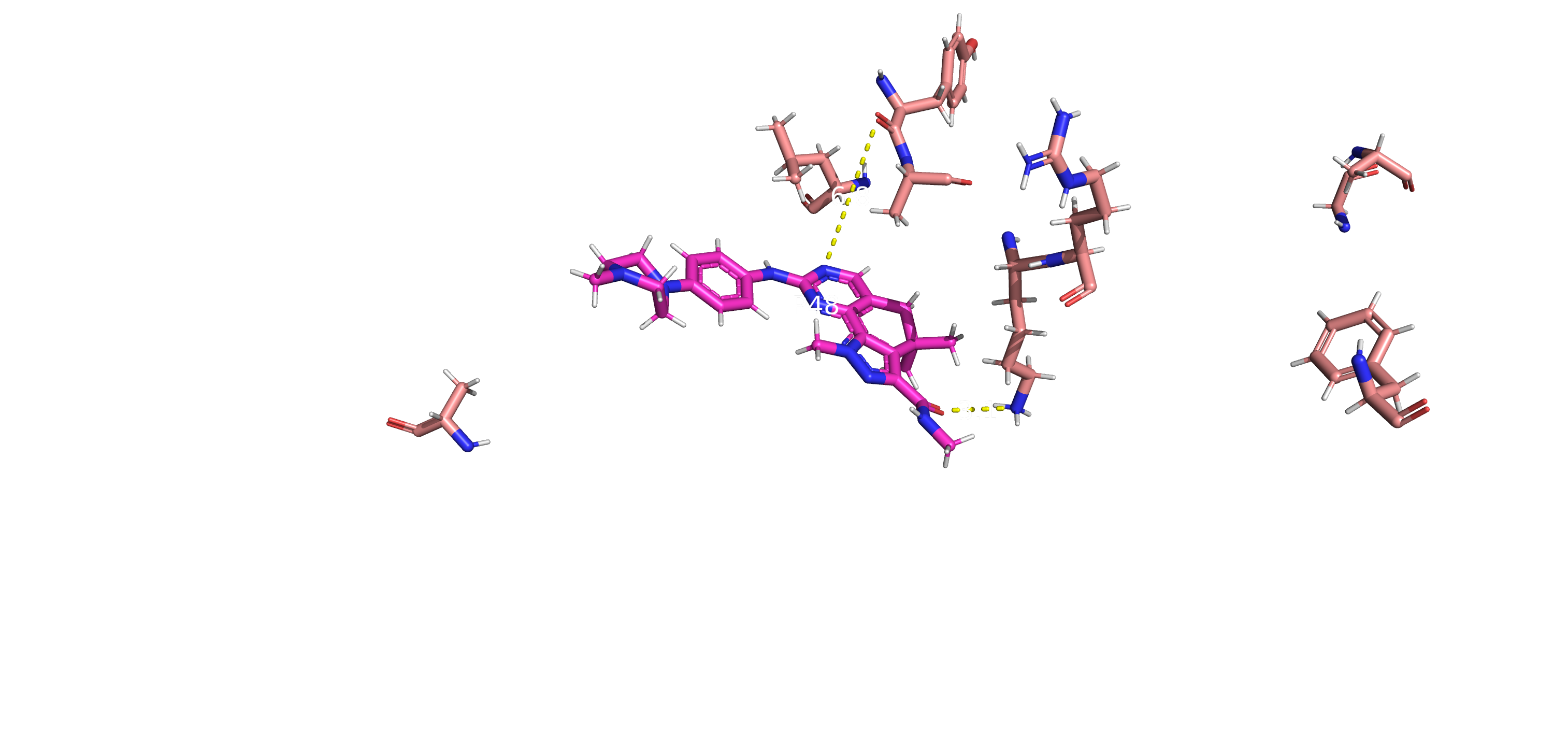
Рис14. Связь ингибитора с ферментом
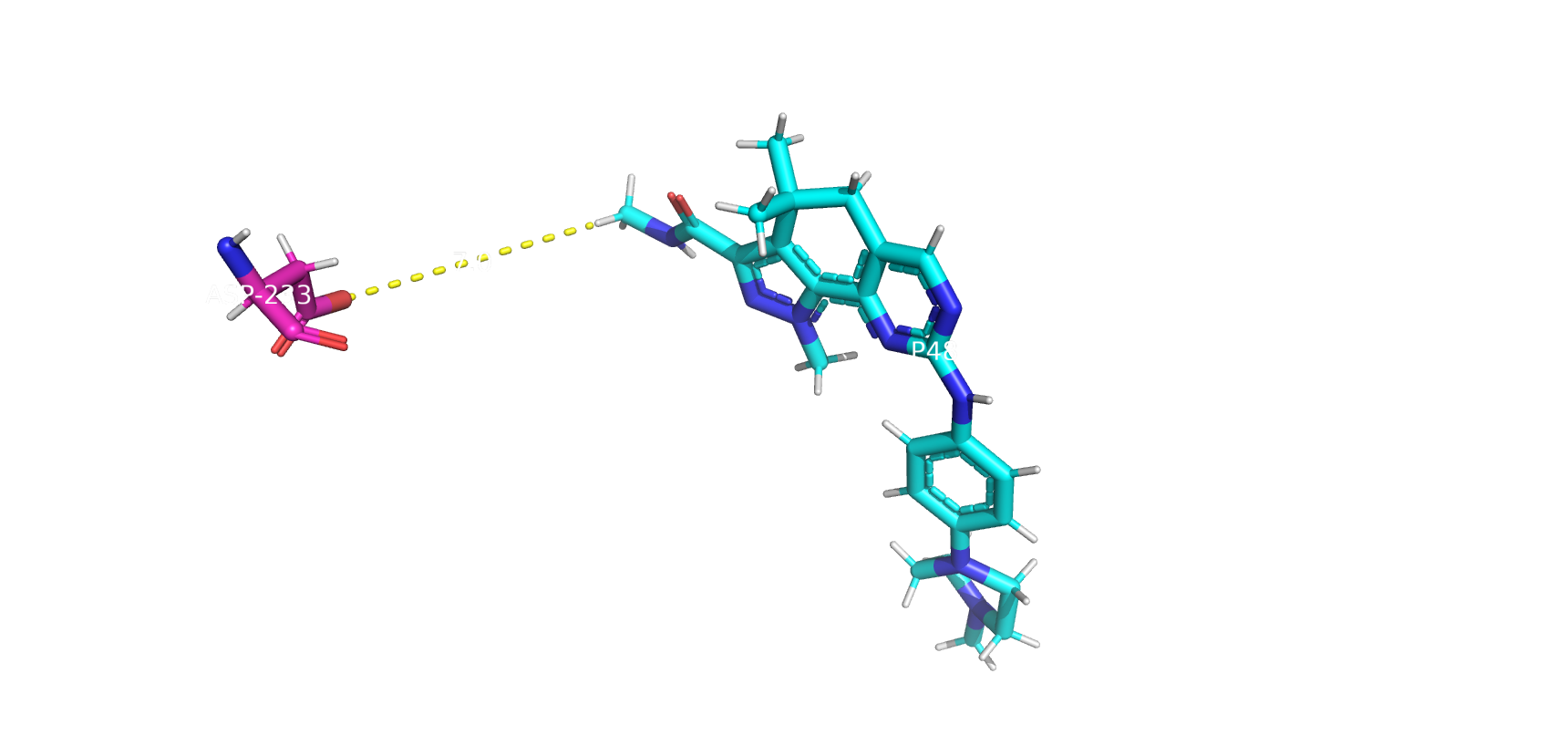
Рис15. Иллюстрация расстояния между активным центром и ингибитором
Так как ингибитор находится на большом расстоянии от активного центра фермента, то проявляется не конкурентное ингибирование