

В данном задании я выровняла 10 заданных структур относительно одной (1gzeA00, на рисунках далее покрашена в зеленый). На рис. 1 видно, что в целом третичные структуры этих белков весьма похожи, но есть и различия. Так, у всех них есть центральный бета-лист, тяжи которого хорошо совпадают у всех структур, а с альфа-спиралями дело обстоит иначе. А именно - у некоторых структур в областях, которые в остальных структурах соответствуют петле, находятся маленькие альфа-спирали (рис. 2, белая и голубая стрелки). Также участки с альфа-спиралями двух структур (на рисунках фиолетовая (3u0j00) и оранжевая (4elnA00)) не выравнялись с аналогичными участками зеленой структуры, по которой происходило выравнивание. На рис. 3 видно, что у этих двух структур альфа-спиралей в этом фрагменте больше, чем в зеленой структуре.


Рис. 1. Визуализация 10 выравненных структур с разных сторон.
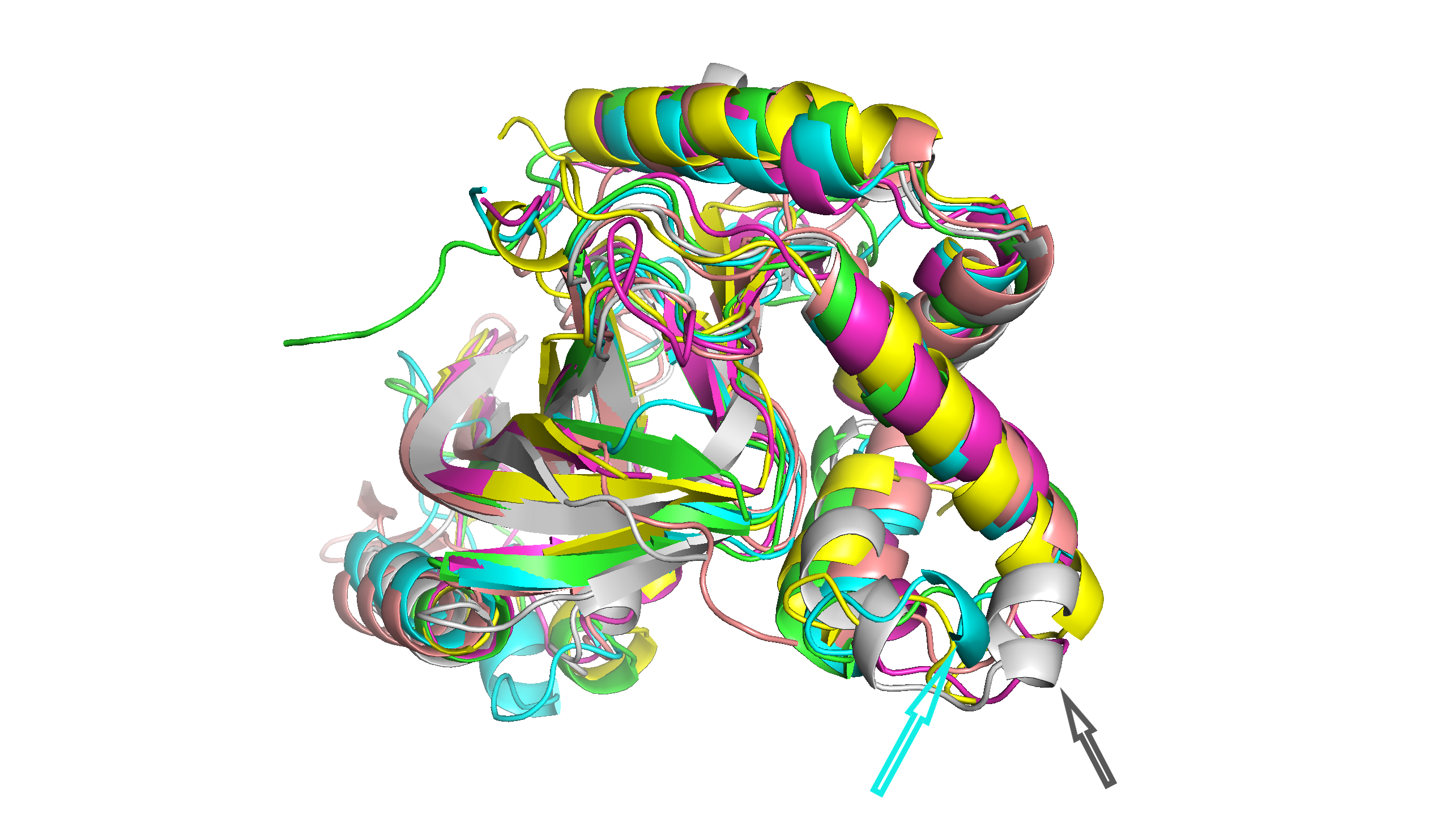
Рис. 2. Визуализация 6 из 10 выравненных структур с выделенными участками структур 1ojqA00 (голубая) и 2wn5A01 (белая).
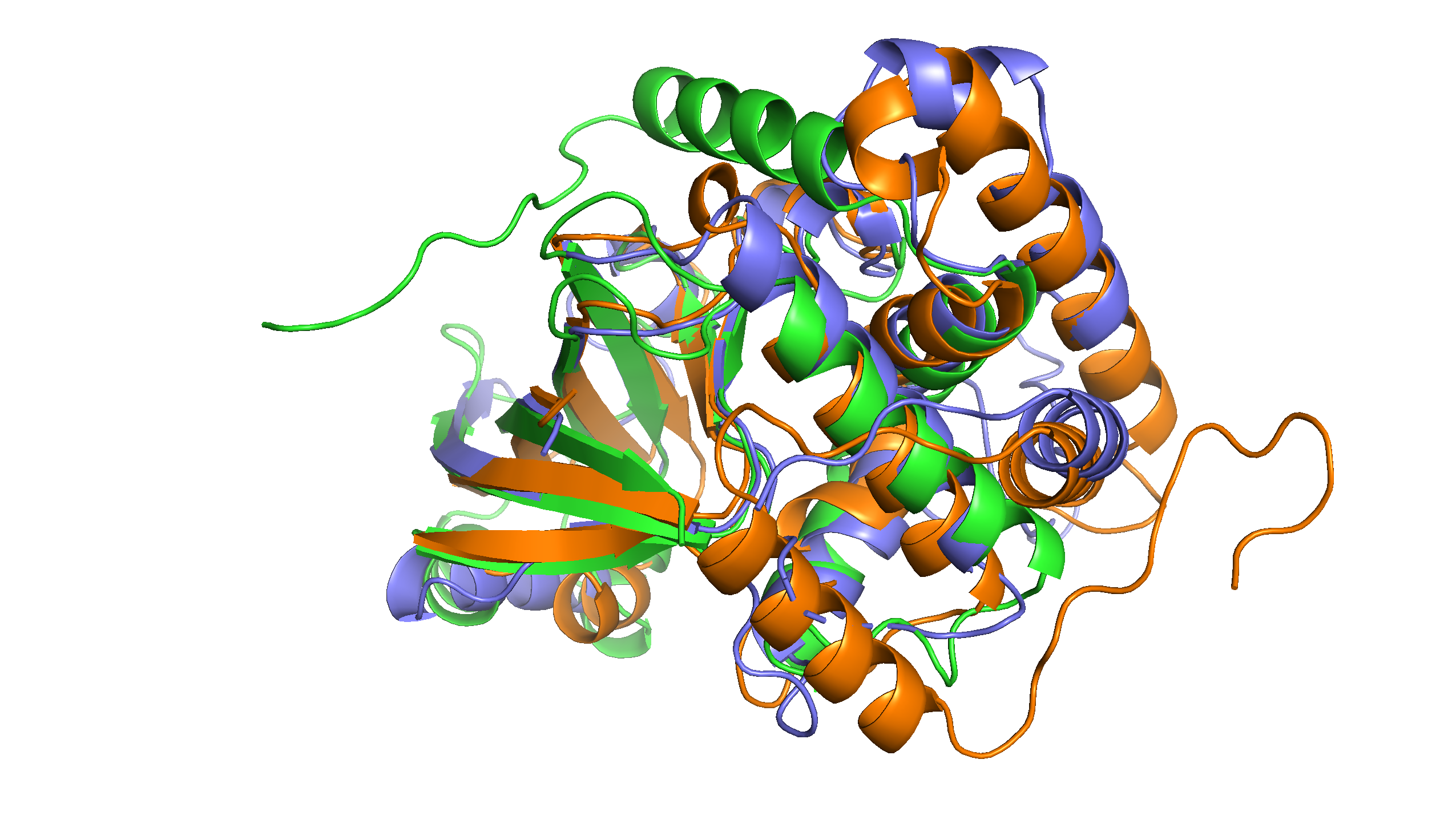
Рис. 3. Визуализация выравненных структур 1gzeA00 (зеленая), 3u0j00 (фиолетовая) и 4elnA00 (оранжевая).
Структуры 1gzeA00 (зеленая) и 2wn5A01 (белая) по разметке в выделенной на рис. 4 области: в зеленой структуре там находится петля, а в белой - маленькая альфа-спираль. Если рассмотреть эти участки поближе, то окажется, что в случае белой структуры (2wn5A01) наличие небольшой альфа-спирали оправдано, мы видим на рис. 5 несколько водородных связей между атомами остова, характерных для альфа-спирали. Если же говорить про аналогичный фрагмент в зеленой структуре (1gzeA00), то там это действительно похоже на петлю, хороших водородных связей между атомами остова не наблюдается. Поэтому разметка вторичных структур в этих фрагментах структур 1gzeA00 и 2wn5A01, на мой взгляд, оправдана.
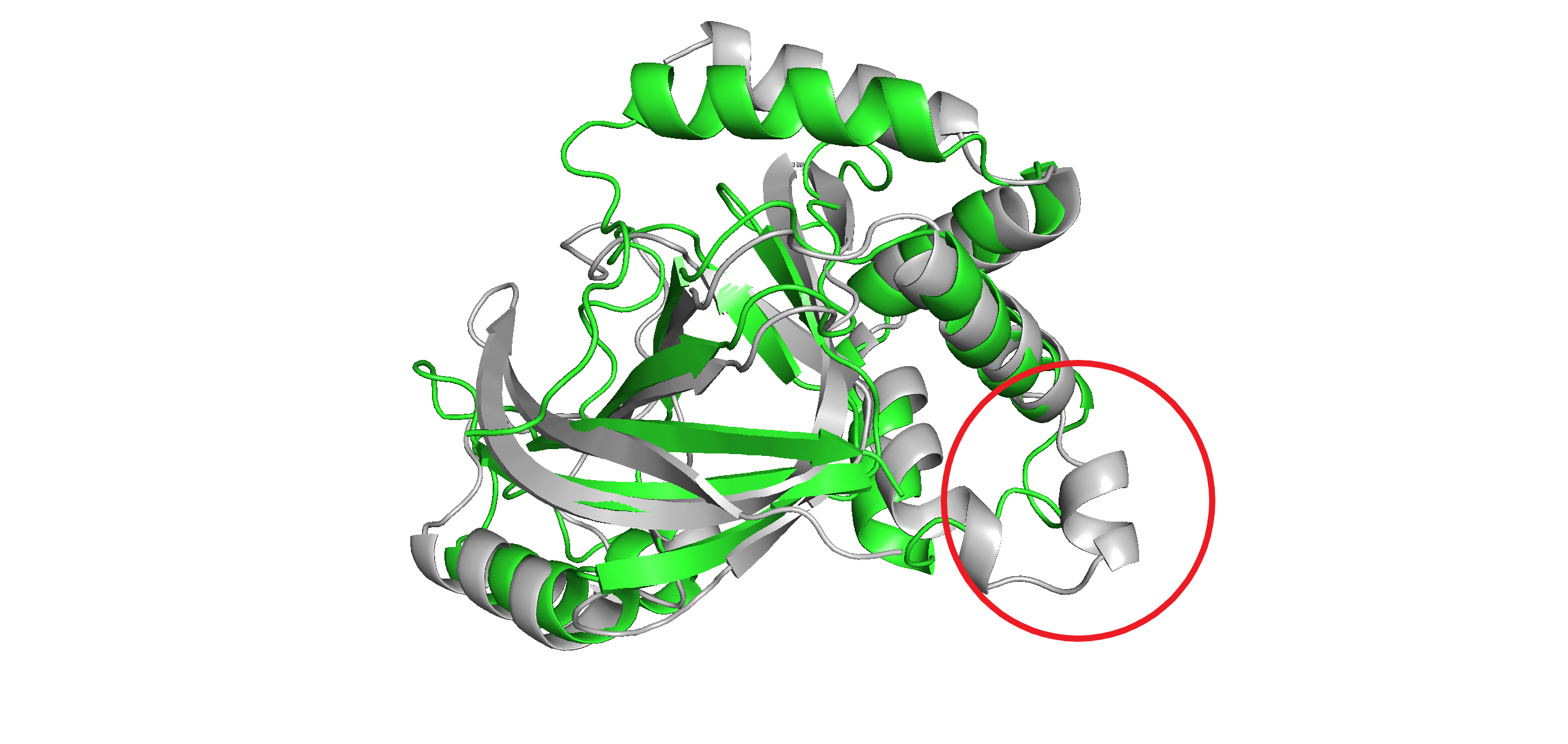
Рис. 4. Визуализация структур 1gzeA00 (зеленая) и 2wn5A01 (белая) с выделенной рассматриваемой в данном задании областью.
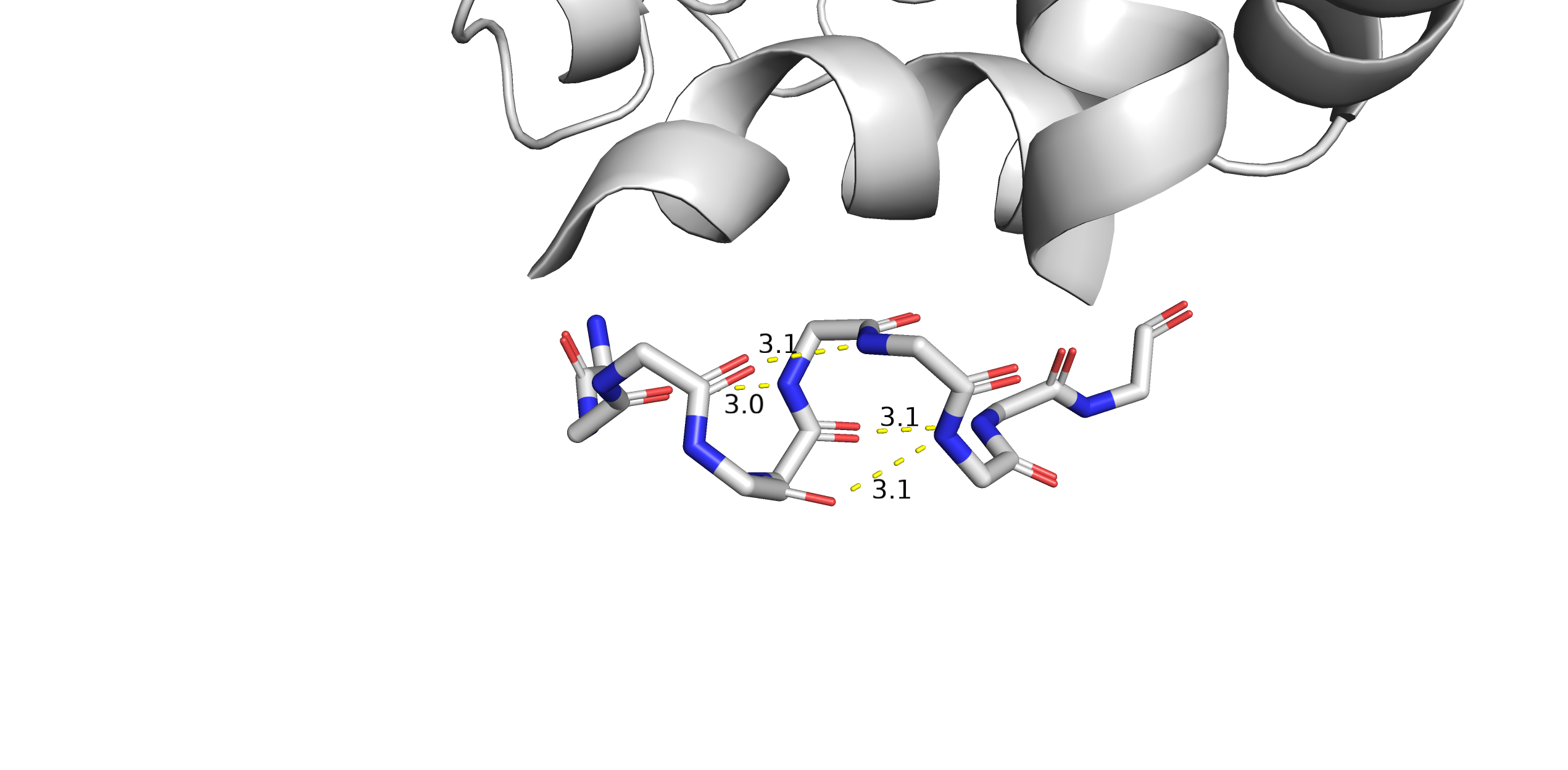
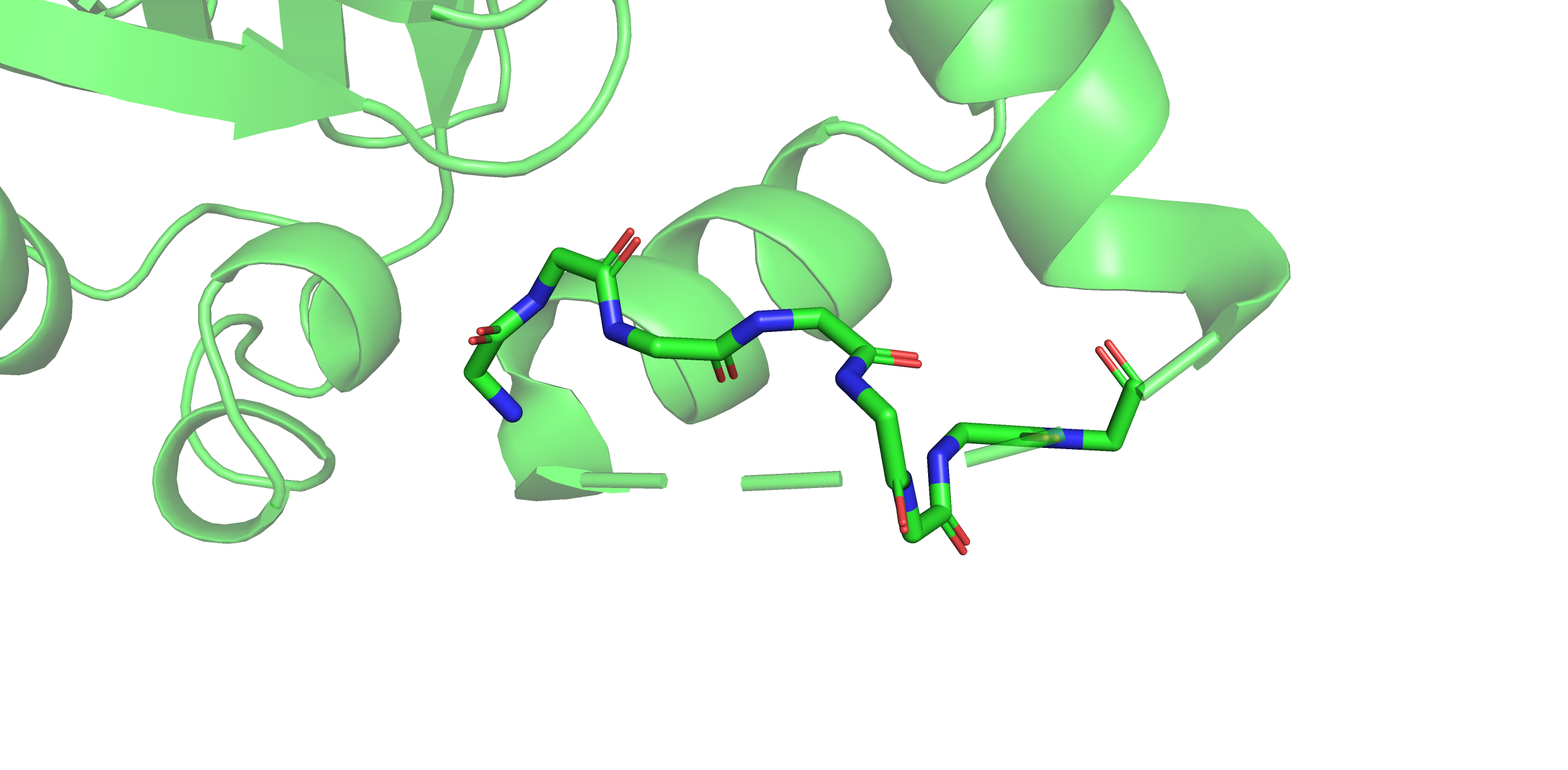
Рис. 5. Визуализация рассматриваемых в данном задании фрагментов структур 1gzeA00 (зеленая) и 2wn5A01 (белая); желтым пунктиром показаны водородные связи.
Для этого задания необходимо было каждого сгенерировать разметку вторичной структуры с помощью dssp и расчитать склонности каждого типа аминокислоты образовывать тот или иной тип вторичной структуры: петлю (С), альфа-спираль (Н) или бета-лист (Е).
| Аминокислота | C | E | H |
|---|---|---|---|
| A | 0.75 | 0.88 | 1.47 |
| G | 1.46 | 0.75 | 0.51 |
| V | 0.59 | 2.37 | 0.55 |
| I | 0.59 | 1.83 | 0.97 |
| L | 0.82 | 1.26 | 1.06 |
| M | 0.82 | 1.18 | 1.13 |
| C | 0.88 | 0.84 | 1.3 |
| P | 1.89 | 0.12 | 0.37 |
| S | 1.26 | 0.73 | 0.83 |
| T | 1.02 | 1.33 | 0.72 |
| F | 1.16 | 0.98 | 0.79 |
| Y | 0.97 | 1.34 | 0.78 |
| W | 0.38 | 0.37 | 2.39 |
| D | 1.22 | 0.67 | 0.93 |
| E | 0.83 | 0.85 | 1.36 |
| N | 1.47 | 0.21 | 0.91 |
| Q | 0.96 | 0.78 | 1.23 |
| R | 0.88 | 1.09 | 1.11 |
| H | 0.84 | 1.11 | 1.14 |
| K | 0.87 | 0.82 | 1.33 |
Остатки, заметно чаще образующие альфа-спирали - триптофан и аланин.
Остатки, заметно чаще образующие бета-листы - валин и изолейцин.
Остатки, заметно чаще образующие петли - пролин и глицин.
© Агаева Зара, 2021