Внутримолекулярные взаимодействия боковых цепей
Внутримолекулярные взаимодействия в белке β-лактамаза
Укладка белка не заканчивается на вторичной структуре. Дальше белок складывается в третичную структуру и она поддерживается не только водородными связями, но другими взаимодействиями. Такие как "гидрофобные взаимодействия", дисульфидные мостики, солевые мостики, Ван-дер-Вальсовы взаимодействия. Последние три и будут разобраны на этой странице.
Примером такой водородной связи между атомами в радикалах аминокислотных остатков приведён на рисунке 1. Он получен с помощью следующего скрипта.
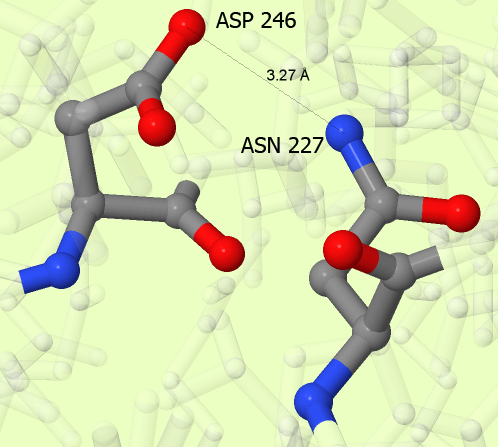 Рис.1. Водородная связь между двумя радикалами аминокислотных остатков. Атомы покрашены в соответствии со своей химической природой.
Рис.1. Водородная связь между двумя радикалами аминокислотных остатков. Атомы покрашены в соответствии со своей химической природой.
Аминокислоты могут иметь заряженные положительно или отрицательно радикалы. Если такие радикалы будут располагаться в белке рядом друг с другом то между ними образуется связь, аналогичная соли - связь между кислотой и основанием, такая структура называется солевой мостик. Используя скрипт, написанный на языке python, я написал скрипт jmol для выделения солевых мостиков в белке. Все солевые мостики показаны на рисунке 2 отдельно солевой мостик показан на рисунке 3.
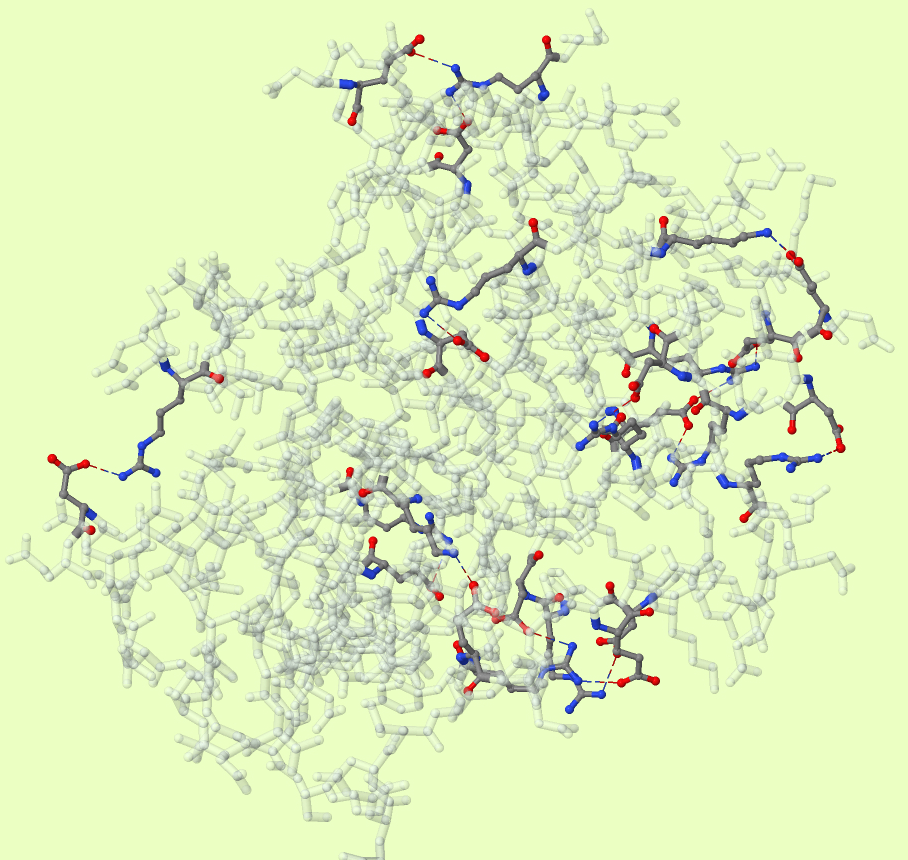 Рис.2. Солевые мостике в белке β-лактамаза. Белок показан полупрозрачным однотонным цветом. Аминокислотные остатки, образующие солевые мостики раскрашены в соответствии с химической природой атомов. Солевые мостики показаны пунктирными линиями.
Рис.2. Солевые мостике в белке β-лактамаза. Белок показан полупрозрачным однотонным цветом. Аминокислотные остатки, образующие солевые мостики раскрашены в соответствии с химической природой атомов. Солевые мостики показаны пунктирными линиями.
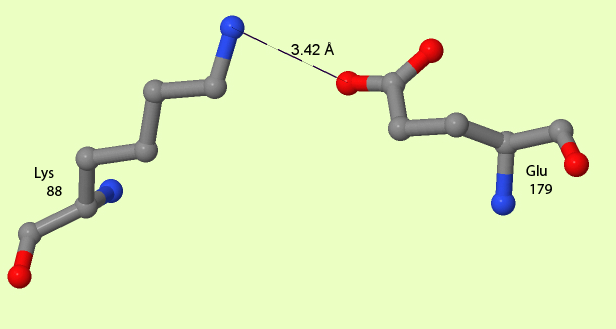 Рис.3.Солевой мостик. Атомы покрашены в соответствии со своей химической природой. Солевой мостик показан пунктирной линией.
Рис.3.Солевой мостик. Атомы покрашены в соответствии со своей химической природой. Солевой мостик показан пунктирной линией.
Другой тип взаимодействия между аминокислотными остатками - это дисульфидный мостик, который образуется между атомами серы двух остатков цистеина. Так как в β-лактамазе нет цистеина, и, соответственно, дисульфидных мостиков, то я для примера взял дисульфидный мостик в молекуле инсулина (идентификатор в базе данных PDB - 4INS). Как видно из рисунка 4 длина связи между атомами серы примерно в два раза меньше, чем у водородной связи или солевого мостика, следовательно связь между цистеинами ковалентная. Это довольно прочная связь, поддерживающая третичную структуру белка и часто "используемая" для сшивания разных цепей белка, как это и происходит в инсулине.
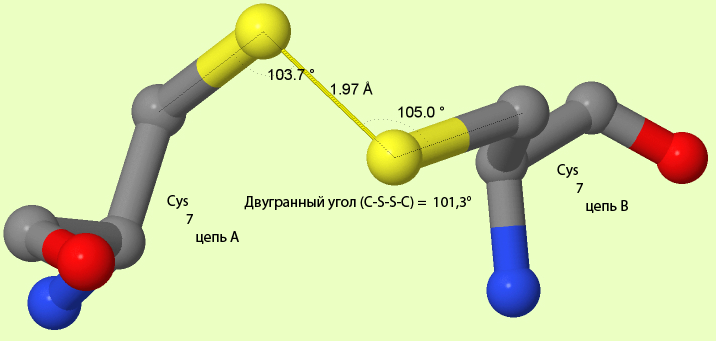 Рис.4. Дисульфидный мостик. Атомы покрашены в соответствии со своей химической природой. Связь между двумя атомами серы показана жёлтым цветом.
Рис.4. Дисульфидный мостик. Атомы покрашены в соответствии со своей химической природой. Связь между двумя атомами серы показана жёлтым цветом.
Некоторые атомы, способные образовывать водородную связь, расположены далеко друг от друга, но при этом они всё-таки могут быть связаны вместе водяным мостиком. Водяной мостик - это связь атомов друг с другом через водородную связь с водой. Для поиска потенцальных водяных мостиков я использовал тот же скрипт, написанный на языке python (используя другую функцию), который ищет среди атомов, способных образовывать друг с другом водородную связь те, которые расположены друг от друга дальше, чем 3,5 Å, и которые находятся на расстоянии не превышающем 3,5 Å от одной и той же молекулы воды. Из получившихся вариантов продолжился поиск вручную. Известно, что угол между водородами в молекуле воды равен 104,45 °, следовательно нужно искать угол, примерно равный этому значению. В результате был найден водяной мостик, показанный на рисунке 5.
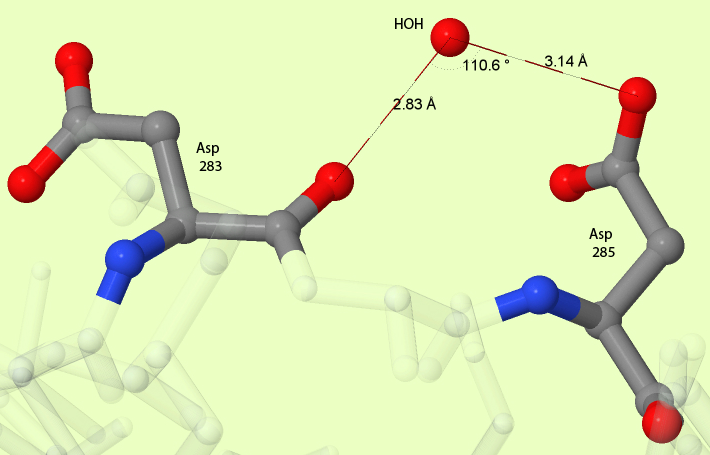 Рис.5. Водяной мостик. Атомы аминокислотных остатков, образующих водяной мостик покрашены в соответствии со своей химической природой. Остальной белок - полупрозрачный однотонный цвет.
Рис.5. Водяной мостик. Атомы аминокислотных остатков, образующих водяной мостик покрашены в соответствии со своей химической природой. Остальной белок - полупрозрачный однотонный цвет.