|
Карань Анна
студентка факультета биоинженерии и бионформатики
|
Краткое описание генома бактерии Neisseria meningitidis MC58
Классификация
| Домен: | Bacteria |
| Филум: | Proteobacteria |
| Класс: | Betaproteobacteria |
| Порядок: | Neisseriales |
| Семейство: | Neisseriaceae |
| Род: | Neisseria |
| Вид: | N. meningitidis |
| Штамм: | N. meningitidis MC58 |
Морфология
Клетки имеют округлую форму диаметром 0,6—1,0 мкм, располагаются попарно. (Рис. 1) Поверхности, обращённые друг к другу, вогнутые или ровные. Клетки полиморфны.
Грамотрицательны, но отношение к окраске по Граму выражено недостаточно четко, поэтому в мазках наблюдается неравномерное окрашивание — молодые клетки окрашиваются интенсивно,
а отмирающие и мёртвые клетки — очень слабо. Жгутиков не имеют, спор не образуют.
Клинические изоляты образуют макрокапсулу, которая утрачивается при росте на питательных средах.
|
|
Рис. 1 Бактерия на под электронным сканирующим микроскопом
[1]
|
Биохимическая активность
Биохимическая активность низкая. Разлагает глюкозу и мальтозу до кислоты,
не разжижает желатин, не образует индол и сероводород, не восстанавливает нитраты.
Ферментация глюкозы и мальтозы является дифференциально-диагностическим признаком.
В отличие от условно-патогенных нейссерий не образует крахмалоподобный полисахарид из
сахарозы. Данный признак выявляется на сывороточном агаре с 5 % сахарозы с помощью водного
раствора Люголя. Обладает, как и все аэробы, цитохромоксидазой и каталазой, что отличает его
от пневмококков и гемофилов.
Отсутствие 3-галактозидазы и наличие у-глютаминтрансферазы отличают менингококки от
N. lactamica , колонизирующей слизистую носоглотки у детей
[1].
Интересно, что у N. gonorrhoeae и N. meningitidis отсутствует супероксиддисмутаза
.
N. meningitidis требует минеральных солей, молочной кислоты, некоторые аминокислоты,
такие как цистеин и глутаминовая кислота, как источник углерода. Исследования гена gdhA, кодирующего
глутаматдегидрогеназу, подтвердили важность глутаминовой кислоты для роста и вирулентности.
помимо органических питательных веществ, железо также необходимо в качестве акцептора электронов,
о чем свидетельствует увеличение периода генераций при недостатке железа. В человеке-хозяине
это железо поставляется из гемового железа крови, где активный транспорт реальзуется TonB зависимым рецептором
[4]
. (Рис. 2)
|
|
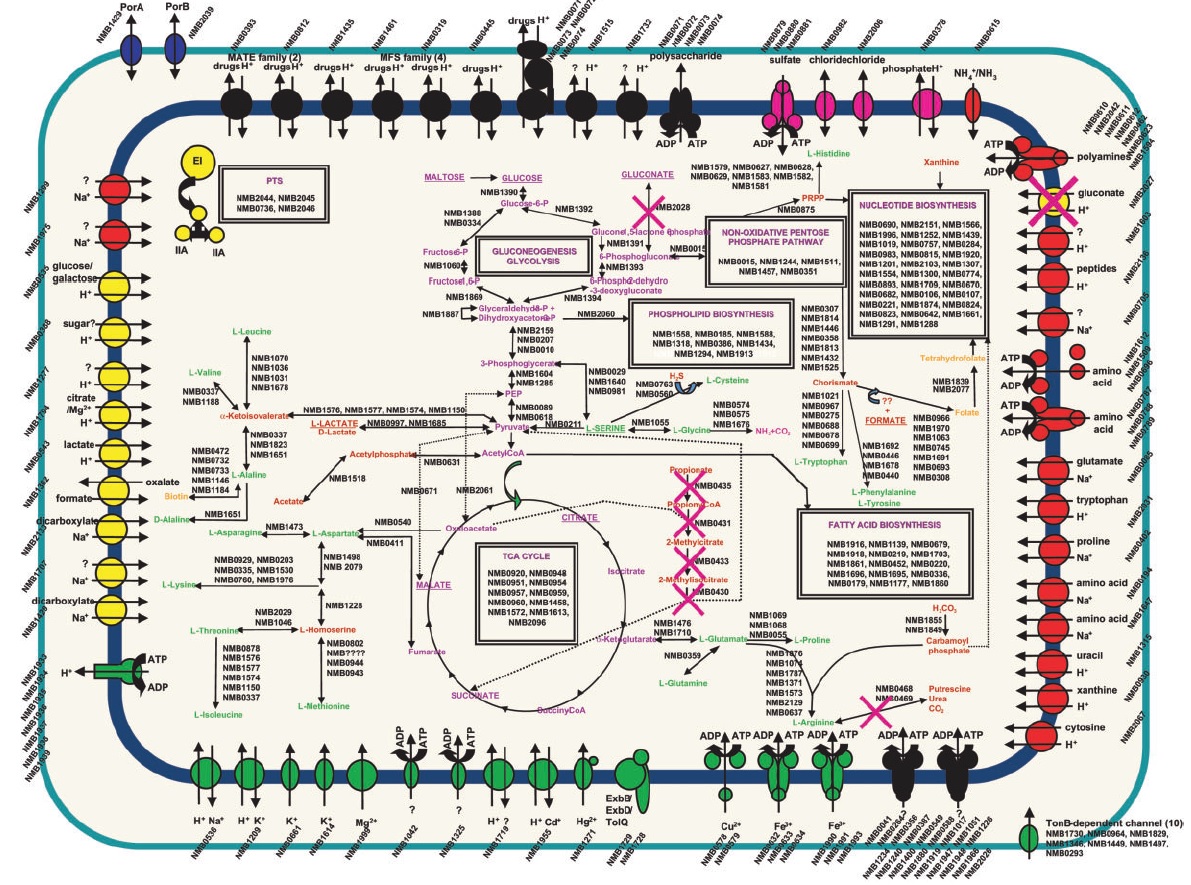
Рис. 2 Метаболизм N. meningitidis MC58. Соединения имеют цветовую маркировку
в зависимости от роли: гликолиз/глюконеогенез/интермедиаты цикла Кребса (фиолетовый),
аминокислоты (зеленый), витамины (оранжевый) и другие (красный).
Транспортеры группируются по субстратной специфичности: неорганических катионов (зеленый),
неорганических анионов (пурпурный), углеводы и карбоксилаты (желтый),
аминокислоты/пептиды/нуклеотиды/нуклеозиды (черный).
Вопросительные знаки рядом с транспортерами указывают на неопределенность в субстратной специфичности
или неопределенность в направлении транспорта
[4].
|
Эпидемиология
Экологической нишей для менингококка является слизистая оболочка носоглотки человека.
Источник инфекции — больной человек или носитель. Различают три группы источников инфекции:
больные генерализованными формами (около 1 % от общего числа инфицированных лиц),
больные назофарингитом (10—20 % от общего числа инфицированных лиц) и здоровые носители.
Основное значение имеют здоровые носители, которые составляют до 80—90 %. Здоровое
носительство у детей 1—2 лет встречается очень редко; с возрастом количество носителей
нарастает, достигая максимума к 14—19 годам.
Механизм передачи — аэрогенный, путь — воздушно-капельный. В отличие от других респираторных
инфекций заражение происходит при длительном и тесном контакте. Заболеваемость носит
сезонный характер, увеличиваясь в осенне-зимний период. Восприимчивость к менингококку
невысокая.
Возникновению вспышек способствует скученность детей в детских организованных коллективах,
учащихся школ и техникумов, студентов в общежитиях и т. п. Заболевания возникают при
низком распространении носительства менингококка в коллективе (2 % и ниже). В коллективах,
где носительство составляет 20 % и выше, заболевания не регистрируются, поскольку
интенсивная циркуляция менингококка обеспечивает
естественную иммунизацию населения в эндемичных очагах заболевания.
Упоминания об эпидемиях цереброспинального менингита встречаются в трудах античных врачей.
Первые клинические описания менингококкового менингита сделали в XVII в. Уйллис (Виллизии) и
Сиденхэм. В настоящее время менингококковая инфекция зарегистрирована более чем в 150
странах мира, в том числе в России. В Африке имеется гиперэндемическая зона заболеваемости
менингококковой инфекцией, так называемый "менингитный пояс", которая охватывает районы,
расположенные между югом Сахары и экваториальным лесом, Красным морем и Атлантическим океаном.
В "менингитном поясе" расположены 15 стран, через которые проходит трансконтинентальная дорога,
с которой связывают распространение менингококковой инфекции, — эпидемии отмечаются здесь через
каждые 10—15 лет [1].
Патогенез
Менингококки внедряются в организм человека через слизистые оболочки носоглотки. (Рис 3)
|
|
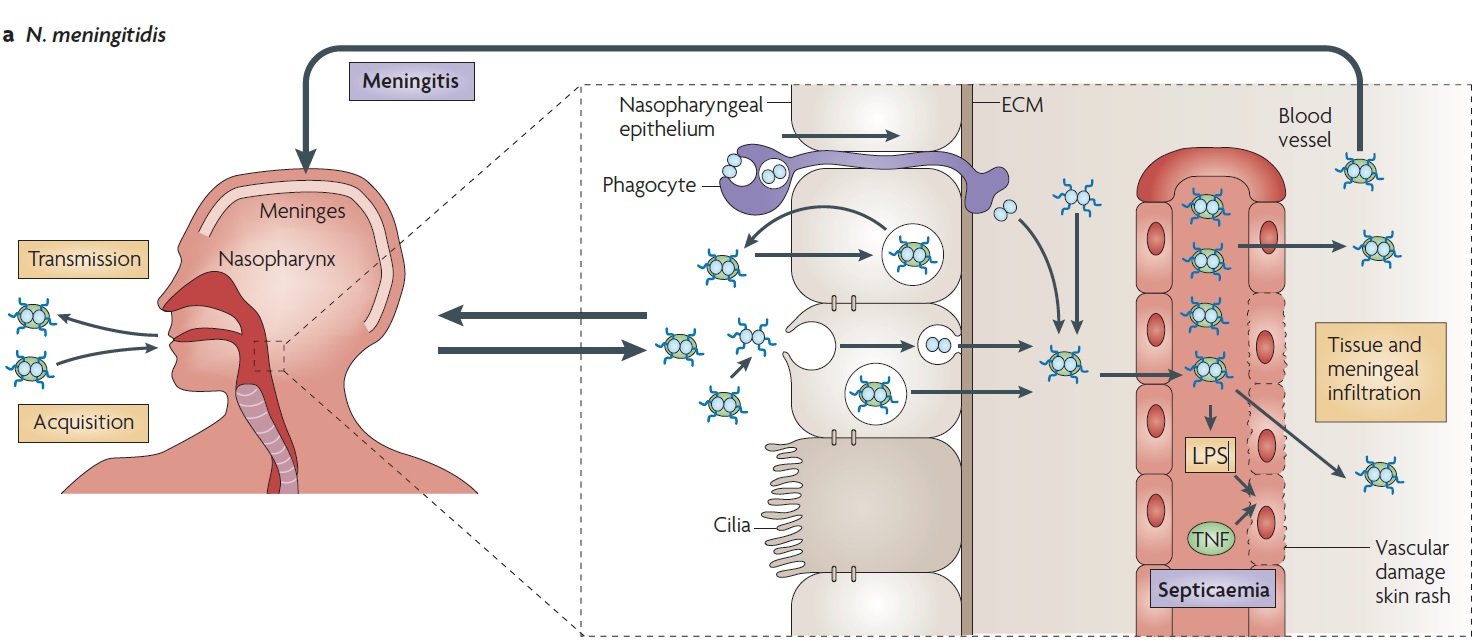
Рис. 3 Этапы в патогенезе N. meningitidis . Заражение происходит воздушно-капельным путем.
В организме устанавливается тесный контакт с нересничничными эпителиальными клетками слизистой оболочки верхних дыхательных путей,
где он может войти в клетке перед перенос в следующего хозяина. Бессимптомное носительтсво распространено
у здоровых взрослых.
Бактерия может пересечь эпителий либо непосредственно после повреждения его целостности, либо
через монослой фагоцитов. У восприимчивых индивидуумов N. meningitidis может выживать, размножаться
и распространяться по всему телу и мозгу. В результате может происходит инфицирование мозговых оболочек
и спиномозговой жидкости
[5].
|
Сейчас уже идентифицироны поверхностные лиганды, как раз позволяющие бактерии попасть в клетку
хозяина. (Рис. 4)
|
|
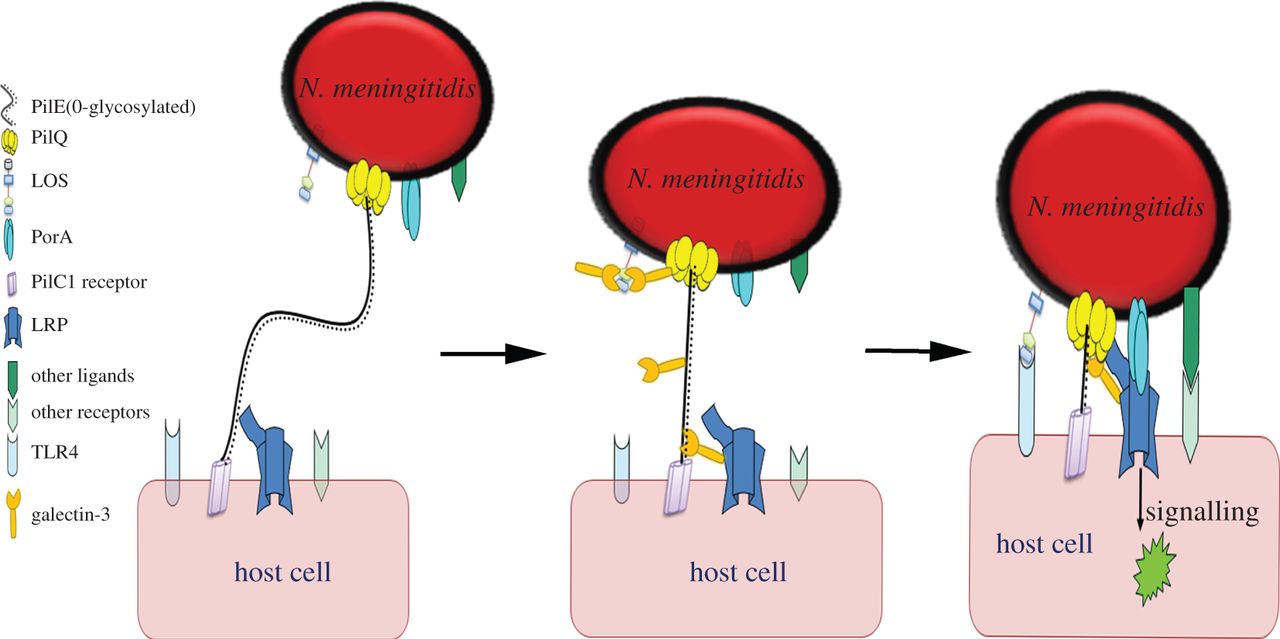
Рис. 4 Иллюстрация взаимодействия клетки-хозяина и менигококка с помощью поверхностных лигандов.
Первоначальный контакт опосредуется PilC1, связываущегося с его предполагаемым рецептором, далее
37LRP/Gal-3-PilE связывание, что усиливает первоначальный контакт, и втягивание пиля, который притягивает
клетки ближе к друг другу. PilQ на поверхности менингококка связывается с обоими 37LRP и Gal-3-PilE,
устанавливает тесный контакт, укрепляет взаимодействие и запускает сигнал в клетке хозяина
[6].
|
N. meningitidis - модельный организм для исследований бактерий, осуществляющих взаимодействие
с Gal-3 и 37LRP. Обе эти молекулы являются мишенью лиганда бактериальной поверхности - PilQ.
Последний образует десятисубъединичный комплекс с полостью, через которую пилевое волокно 4 типа втягивается и выпячивается.
PilE - основная субьединица, образующая это волокно. PilQ и PilE тесно расположены и окружены LOS
, который преобладает в липидной части наружной мембраны. PorA, другой специфический менигококковый лиганд для
37LRP, также порообразующий белок в наружней мембране, присутствующий в больших количествах.
Эволюция 37LRP- и Gal-3-свяывающих поверхностных лигандов тесно связана с изменениями вирулентности менингококков, и, возможно,
других бактериальных патогенов [6] .
Размножаясь, они формируют первичный очаг воспаления. По окончаниям обонятельного нерва
воспалительный процесс может распространиться на оболочки мозга. Возможно и гематогенное
распространение менингококка по организму. Основной фактор патогенности — капсула, защищающая менингококки от различных воздействий,
в первую очередь от фагоцитоза. AT, образующиеся к полисахаридам капсулы, проявляют
бактерицидные свойства. Важная роль в патогенезе принадлежит эндотоксину,
который участвует в развитии токсического шока и угнетении фагоцитарной активности нейтрофилов.
Кроме того эндотоксин запускает и поддерживает каскады провоспалительных реакций - свертывание крови, фибринолиз,
активацию комплемента и калликреин-кининовой системы, а также образование цитокинов
(ФНОальфа, Il-1, IL-6, IL-8, IL-10) и NO. В результате развиваются вазодилатация,
нарушение функции сердца , агрегация тромбоцитов, ДВС-синдром и повышение проницаемости капилляров.
Все это ведет к септическому шоку, РДСВ и полиорганной недостаточности. [8]
Патогенез заболевания включает поражения токсического и септического характера в сочетании с
аллергическими реакциями.
К другим факторам патогенности относятся пили, белки наружной мембраны, наличие
гиалуронидазы и нейроминидазы. Пили являются фактором адгезии к слизистой оболочке
носоглотки и, предположительно, тканям мозговой оболочки. Менингококки выделяют IgA-протеазы,
расщепляющие молекулы IgA в шарнирной области, что защищает бактерии от действия Ig.
Различают локализованные формы менингококкой инфекции - носительство, менингококковый нозофарингит и пневмонию,
и генерализованные формы - менингококцемию, менингококковый менингит и менингоэнцефалит, а также смешанные формы (артрит и др.)
Менингококковый нозофарингит, как правило, сопровождается появлением признаков ринита и незначительном повышении температуры.
Специфических признаков у него нет, поэтому его часто не диагностируют.
Пневмония протекает достаточно тяжело и длительно, и так же не имеет специфических признаков.
При генерализованных формах происходит заражение крови.
Признаками генерализованных форм являются симптомы интоксикации (лихорадка, головная боль, слабость, бледность
и т.д.), а также развитие характерной экзантемы (сыпь). [9]
Лечение
Препарат выбора — бензилпенициллин, эффективны также полусинтетические пенициллины
(ампициллин, оксациллин). Оптимально назначение антибиотиков в сочетании с диуретиками.
Антимикробную терапию
следует сочетать с симптоматическими средствами, корригирующими водно-солевой и
кислотно-щелочной баланс, а также с седативными средствами и глюкокортикоидами.
[2]
Некоторые особенности генома и протеома
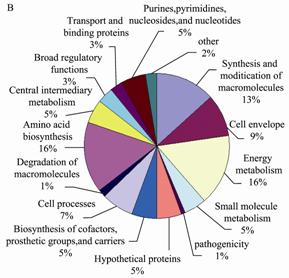
Самые крупные белки - porA, porB, and rmpM. После классификации по функциям, больше всего оказалось белков,
участвующих в энергетическом обмене, биосинтезе аминокислот, синтезе и модификации макромолекул и белков наружной
мембраны [7]. (Рис. 5)
|
|
Рис. 5 Распределение белков N.meningitidis согласно функциональной классификации, предсказанное на основе
анализа секвенсов.
[7]
|
|
|
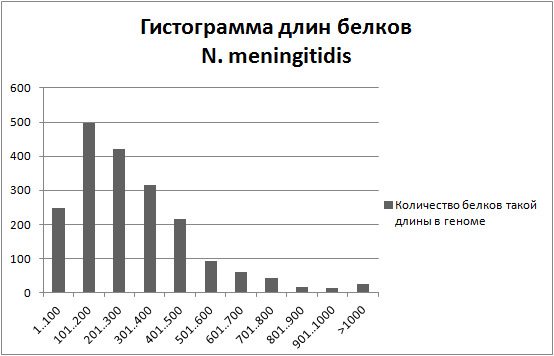
Рис. 6 Гистограмма длин белков N. meningitidis
|
В геноме N. meningitidis наиболее распространены белки с длинной от 100 до 200 нуклеотидов.
Далее число белков равномерно падает от длины 200, длиной >800 белков уже почти нет (Рис 6).
| Таблица 1. Основные особенности генома [3] |
| Тип | Размер | GC% | Белки | рРНК |
| Хромосома | 2272360 bp | 51,5% | 1943 | 12 |
| тРНК | Гены | Псевдогены | Дата секвенирования генома | |
| 59 | 2104 | 90 | 2000/02/25 | |
Источники:
[1] Microbewiki_Neisseria_meningitidis
[2] Wikipedia_Менингококк
[3] www.ncbi.nlm.nih.gov/genome/?term=Neisseria+meningitidis+MC58
[4] Comparative genomics of Neisseria meningitidis :core genome,
islands of horizontal transfer and pathogen-specific genes. Julie C. Dunning Hotopp, Renata Grifantini et al.
[5] Pathogenic neisseriae: surface modulation, pathogenesis and infection control. Mumtaz Virji. Nature reviews | Microbiology April 2009 | Volume 7
[6] Alqahtani F et al. 2014. Deciphering the complex three-way interaction
between the non-integrin laminin receptor,
galectin-3 and Neisseria meningitidis. Open Biol. 4: 140053.
[7] Proteome Analysis of Neisseria meningitidis Serogroup Strains C Associated with Outbreaks in China. Yuan HU, Zhu-Jun SHAO, Xiao-Mei YAN et al.
[8] Менингококковая инфекция: патогенез
[9] Клинические формы менингококковой инфекции:
генерализованная, локализованная, молниеносная, редкие формы





