| Главная | Семестры | Проекты | Заметки |
Контакты белка с лигандом
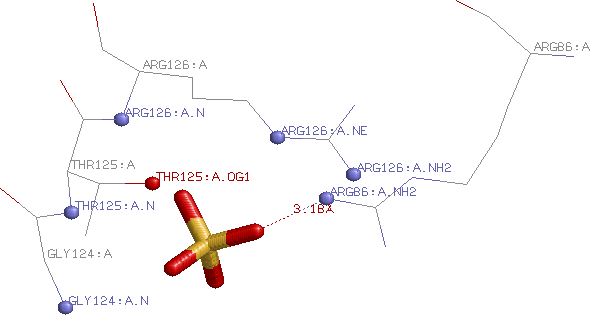
Контакты сульфат-иона с белком RNPH_BACSU
Для исследования выбран лиганд — сульфат-ион под номером 301.
| # | Имя атома контакта | Имя контактирующего атома белка | Расстояние в A | Предположительная природа контакта |
| 1 | O2 | ARG86:A.NH2 (азот гуанидиновой группы радикала аргинина) | 3.18 | Электростатическое взаимодействие? |
| 2 | O3 | GLY124:A.N (амидный азот глицина) | 3.23 | Водородная связь? |
| 3 | O3 | THR125:A.N (амидный азот треонина) | 3.02 | Электростатическое взаимодействие? |
| 4 | O4 | THR125:A.N (амидный азот треонина) | 3.34 | Водородная связь? |
| 5 | O3 | THR125:A.OG1 (кислород гидроксильной группы радикала треонина) | 2.99 | Электростатическое взаимодействие? |
| 6 | O4 | ARG126:A.N (амидный азот аргинина) | 2.85 | Электростатическое взаимодействие? |
| 7 | O4 | ARG126:A.NE (азот гуанидиновой группы радикала аргинина) | 3.21 | Водородная связь? |
| 8 | O2 | ARG126:A.NH2 (азот гуанидиновой группы радикала аргинина) | 3.45 | Водородная связь? |
В ## 2, 4, 7, 8 имеет место водородная связь по типу N–H ... :O (руководствуюсь только расстоянием — больше 3.2 A и меньше 3.5 A).
Однако гуанидиновая группа аргинина в нейтральной среде протонирована (заряжена положительно причем положительный заряд делокализован на все атомы азота группы). Поэтому в #1 существует электростатическое взаимодействие (расстояние меньше 3.2 A).
В #3 и #6 также возможно существование именно электростатического взаимодействия: расстояние меньше 3.2 A, атом азота пептидной группы имеет положительный заряд (правда, лишь в одной из двух резонансных форм амидной группы).
В #5 расстояние хоть и меньше 3.2 A (намек на электростатическое взаимодействие), но, т. к. положительного заряда на атоме кислорода гидроксогруппы нет, здесь возможна только водородная связь по типу O–H ... :O.
© Антон Васетенков
E-mail