Практическая работа 9
Глобальное парное выравнивание гомологичных белков
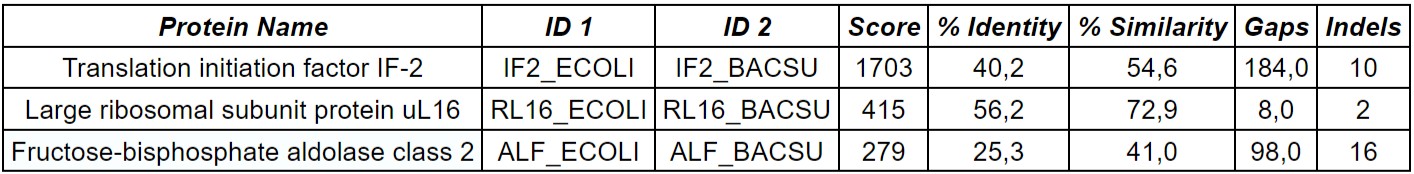
В Табл. 1 приведены результаты глобального выравнивания с помощью программы needle трех гомологичных белков(IF2, RL16 и ALF), полученных из Escherichia coli (strain K12) и Bacillus subtilis (strain 168). Как видно из представленных данных, наиболее консервативными оказались белки IF2 и RL16, связанные с реализацией генетической информации, в то время, как фермент ALF из гликолиза оказался менее консервативным.
Локальное парное выравнивание гомологичных белков
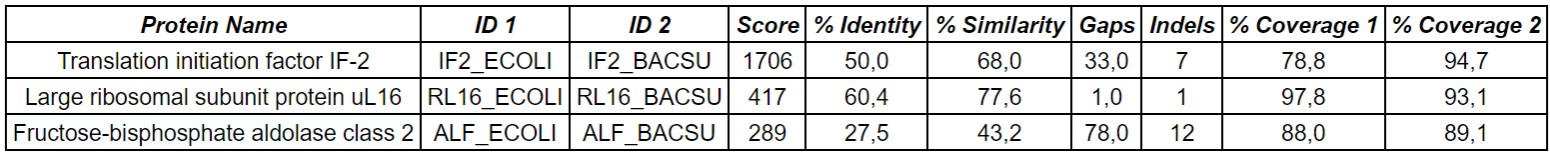
В Табл. 2 приведены результаты локального выравнивания с помощью программы water трех гомологичных белков(IF2, RL16 и ALF), полученных из Escherichia coli (strain K12) и Bacillus subtilis (strain 168). По сравнению с глобальным выравниванием, вес локального выравнивания оказался больше для всех трех последовательностей(как, собственно, всегда). Однако разница между весом глобального и локального выравнивания для IF2 и RL16 несущественна. Для ALF разница в весе более весома(10). Наиболее существенннная разница в проценте идентичности локального и глобального выравнивания(10%) наблюдается для последовательности транскрипционного фактора IF2. Её можно объяснить, если предположить, что у IF2 есть консервативный участок, связывающийся с ДНК, который и был выявлен как наиболее схожий между двумя последовательностями алгоритмом Смита-Ватермена.
Выравнивание негомологичных белков
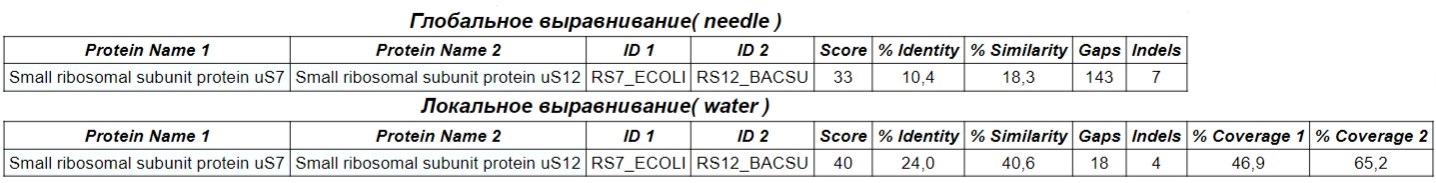
В Табл. 3 приведены результаты глобального и локального выравнивания негомологичных белков RS7 и RS12, полученных из Escherichia coli (strain K12) и Bacillus subtilis (strain 168). Процент идентичности, рассчитанный с помощью локального выравнивание, укладывается в диапозон 20-25%, что, на удивление, позволяет сделать вывод о наличии гомологичного участка в последовательности белков RS7 и RS12. Можно выдвинуть две гипотезы, объясняющие это:
- Сходные участки последовательностей белков RS7 и RS12 могли возникнуть в результате конвергенции на молекулярном уровне, то есть в результате появления похожих участков аминокислотной последовательности у негомологичных белков, обусловленных необходимостью похожих физико-химических свойств(например, для организации рибосомы).
- Возможно, когда-то гены белков RS7 и RS12 образовались из общего предкового гена в одном геноме в результате дупликации, а затем эволюционировали независимо друг от друга, получив набор различного рода мутаций. То есть, согласно этой гипотезе, данные белки нужно считать гомологичными.
Множественное выравнивание белков
Для множественного выравнивания последовательностей белков был выбран белок Large ribosomal subunit protein uL16(RL_16) из следующих организмов:
- Escherichia coli (strain K12)
- Bacillus subtilis (strain 168)
- Mycobacterium tuberculosis (strain ATCC 25618 / H37Rv)
- Chlamydia trachomatis (strain D/UW-3/Cx)
- Mycoplasma capricolum subsp. capricolum (strain California kid / ATCC 27343 / NCTC 10154)
- Borrelia garinii subsp. bavariensis (strain ATCC BAA-2496 / DSM 23469 / PBi) (Borreliella bavariensis)
- Acaryochloris marina (strain MBIC 11017)
Теперь перейдем к рассмотрению непосредственно полученного выравнивания. В первую очередь, хочется отметить крупные участки гомологии, имеющие следующие координаты: 40-70, 75-88, 93-100, 124-134. Кроме этого, существуют и другие более короткие участки гомологии, расположенные практически по всей длине выравнивания. Во-вторых, отметим, что от большей части выравнивания(1-134) гэпы не встречаются в то время, как в конце выравнивания(135-146) появляется много гэпов. Это может свидетельствовать о неконсервативности С-конца данного белка, который, по-видимому, не несет существенной функциональной нагрузки. В тоже время участок 1-134 в целом довольно консервативный(особенно некоторые его учатки, указанные выше). Больше информации можно получить, если окрасить выравнивание по физико-химическому сходству аминокислот(Clustal). Так, например, есть довольно много позиций, где аминокислоты хоть и разные, но одинаковые по физико-химическим свойствам(например: гидрофобные в позициях 64, 66, 68, 102, 103 ...). Таким образом, 'физико-химическая' гомология данных белков гораздо больше, чем формальная гомология их последовательностей.
Параметры для программ needle и water
Помимо имени файлов с двумя входными последовательностями для выравнивания и именем выходного файла с выравниванием, программы needle и water требуют указать:
- Gap openning penalty(GOP) – штраф за первый гэп в инделе(равен 10 по умолчанию)
- Gap extension penalty(GEP) – штраф за каждый последующий гэп в инделе(равен 0,5 по умолчанию)
- ASEQWFGGNTVILKQHWWRGKLYREQWSCC
- ASEQWGNTVILKQHWWRGKLYREQC