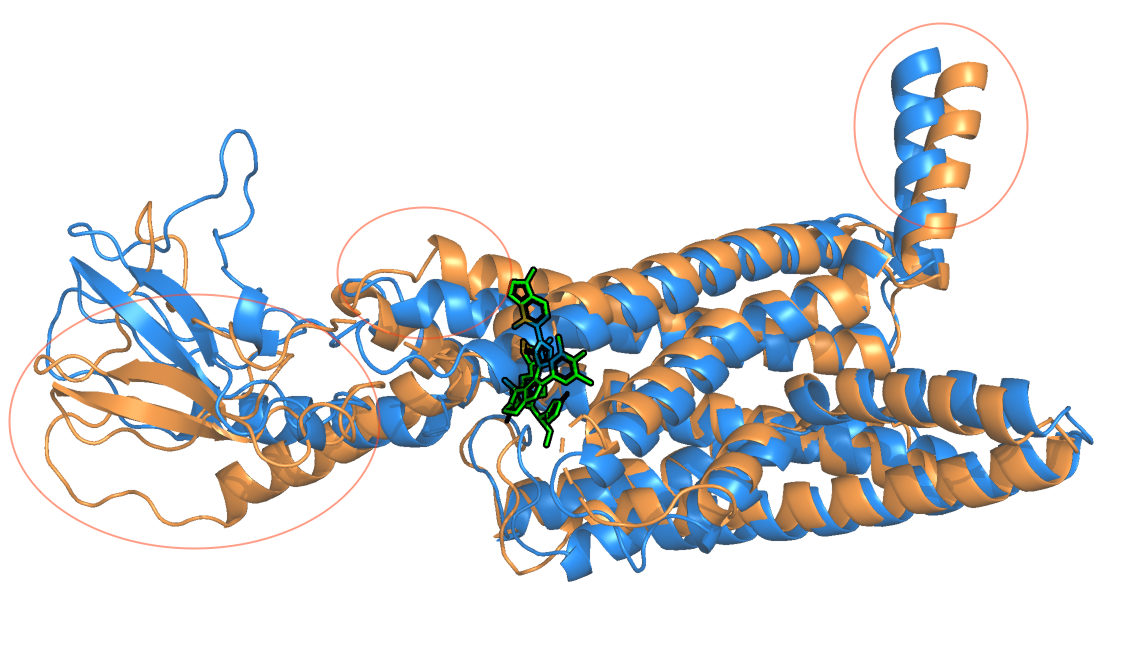
Для одного и того же белка я рассмотрела две структуры: свободную и связанную с лигандом UK1. В структуре присутствует 7 альфа-спиралей, что наводит на мысль, что этот белок трансмембранный, скорее всего рецептор. Когда я перешла на страницу с лигандом, то увидела, что он встречается только в одной структуре - 6X19 - это рецептор глюкагоноподобного пептида 1.
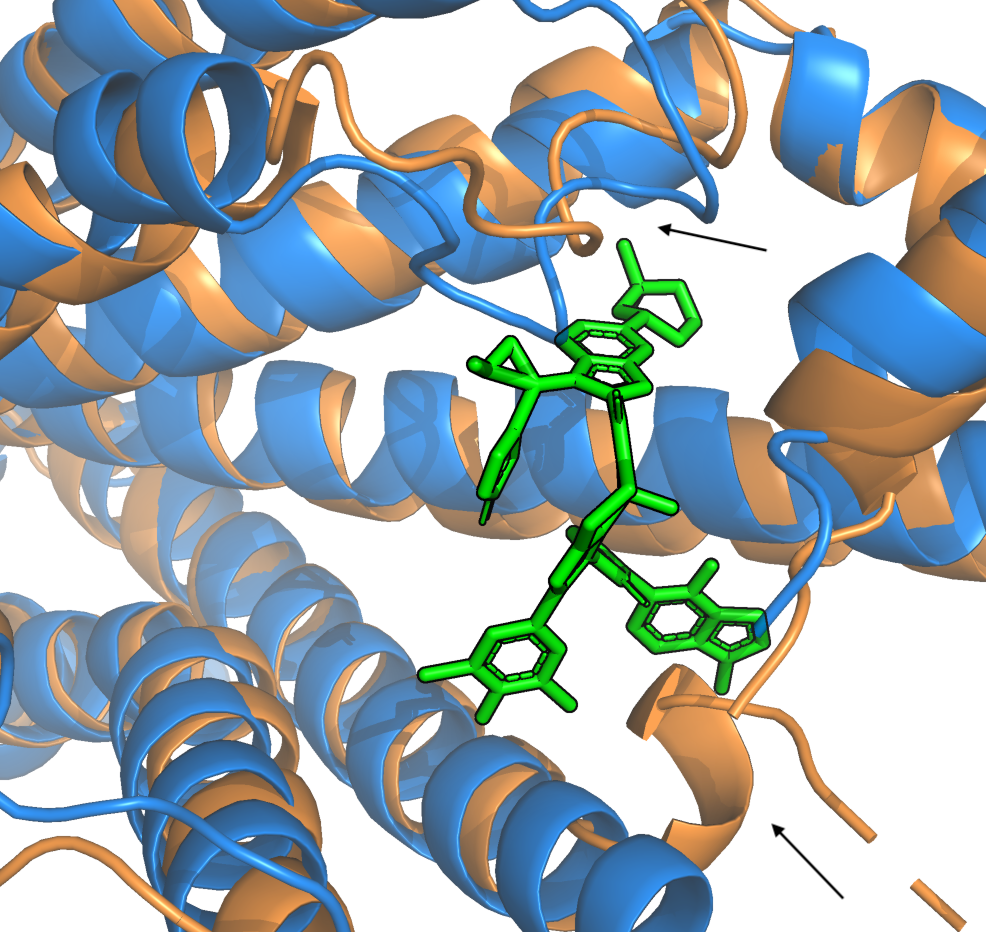
При первом взгляде на структуры можно увидеть, что они хорошо друг на друга накладываются. Однако видны довольно сильные изменения (выделены кругами на Рисунке 1) в разных частях структуры. При связывании с лигандом сдвигается наименее упорядоченная часть белка (слева), которая скорее всего обращена наружу от мембраны. Возможно, в таком положении она препятствует новому связыванию, когда карман уже занят. Также есть различия в положении альфа-спиралей близко к месту связывания с лигандом. На Рисунке 2 внизу (указано стрелкой) видно, что произошел разрыв водородных связей на конце длинной альфа-спирали, и отдельная спираль "развернулась" для связывания с лигандом. Другая стрелка указывает на перемещение белковой петли.


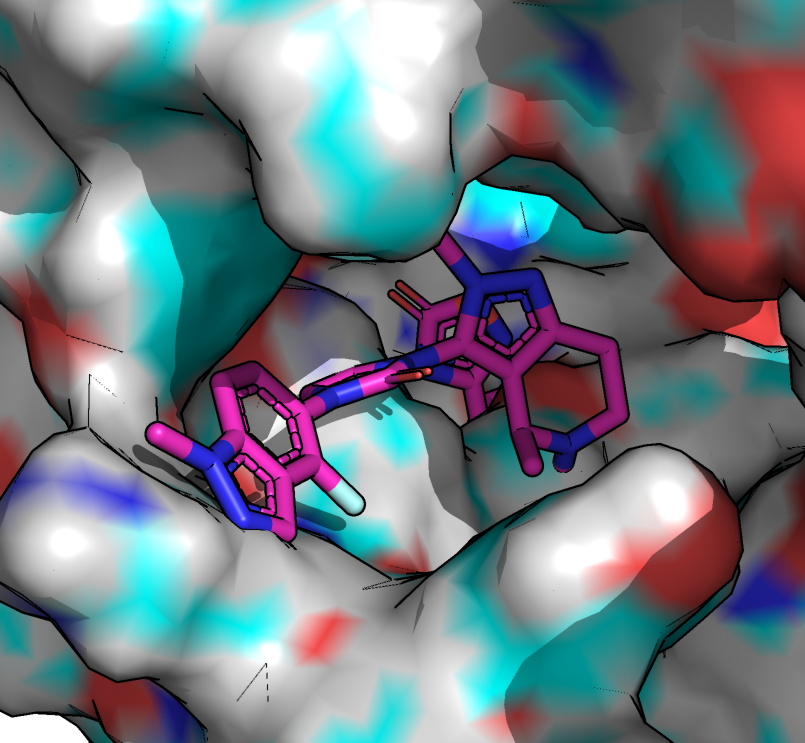
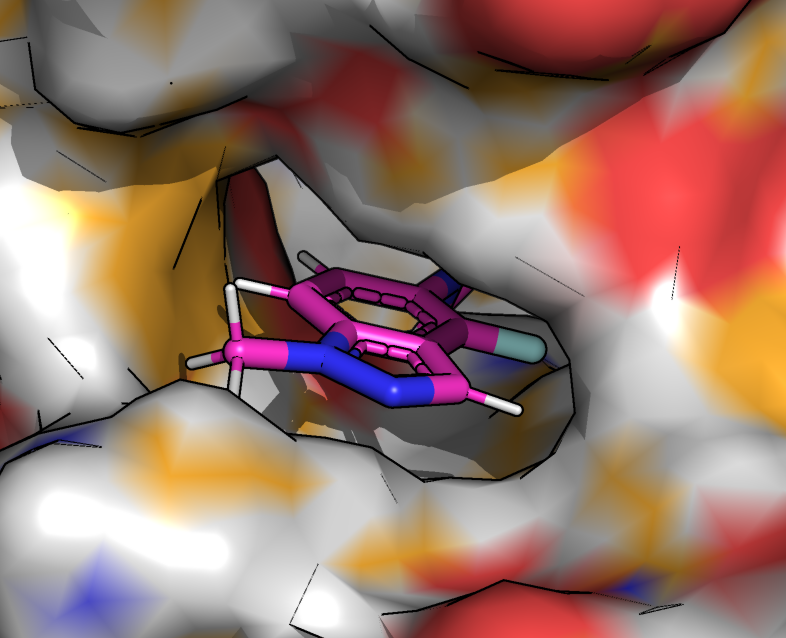
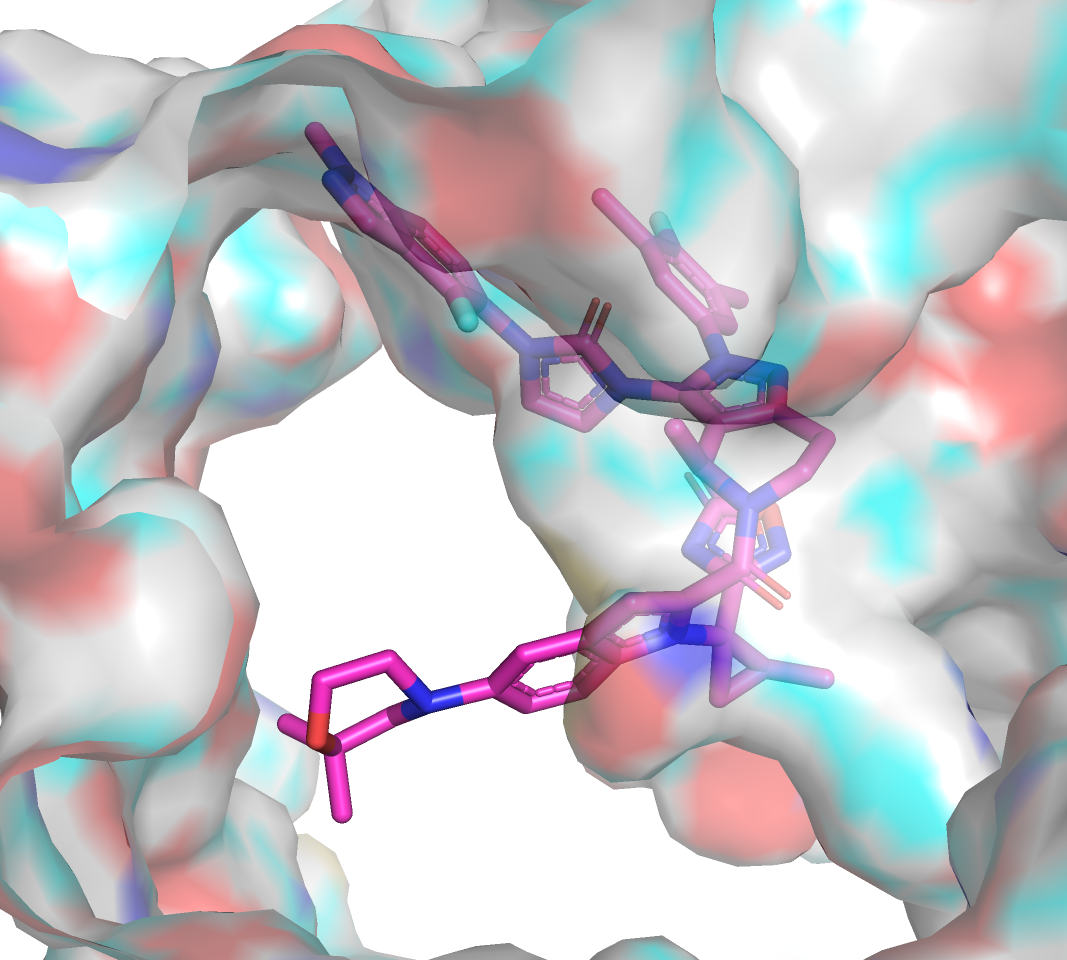
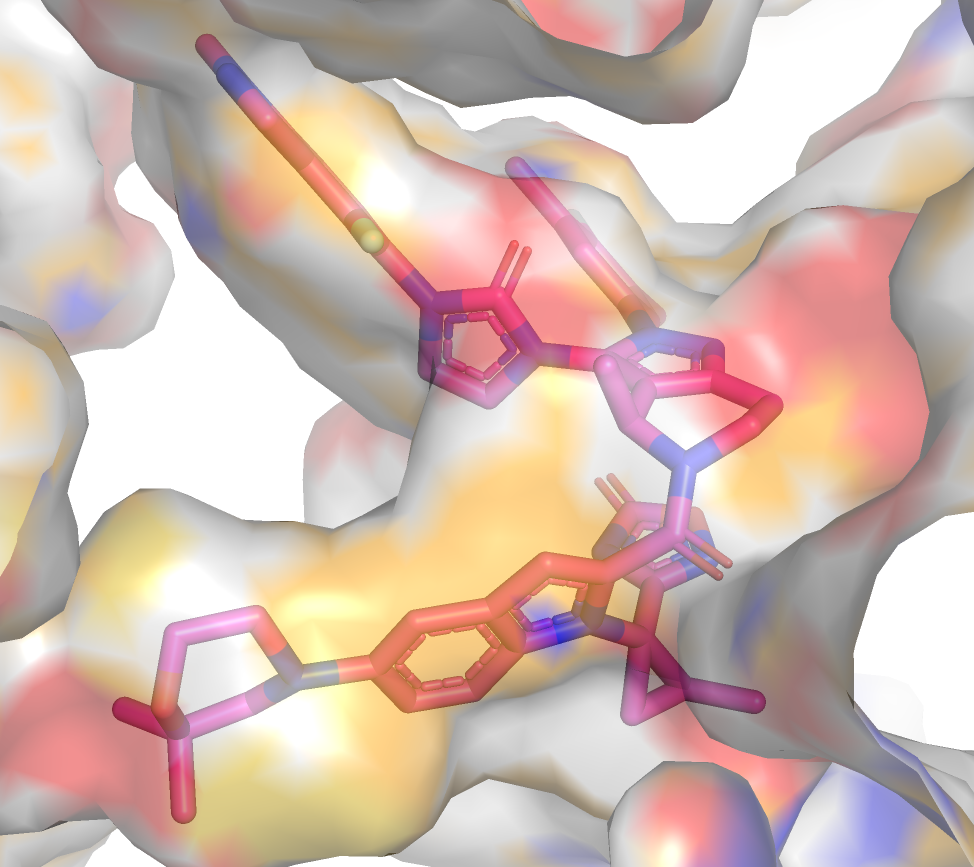
После связывания белок принимает закрытую конформацию, изменения удобно рассмотреть с помощью отображения surface. На Рисунках 3, 4 можно увидеть, что после связывания фермент "облегает" индазольное кольцо лиганда. На Рисунках 5, 6 показано, что фермент подстроился под структуру после связывания. Для плечей лиганда остались полости, при этом лишнего свободного места почти нет. Свободная форма хороша для досупа лиганда в карман, но еще слабо подстроена под лиганд.
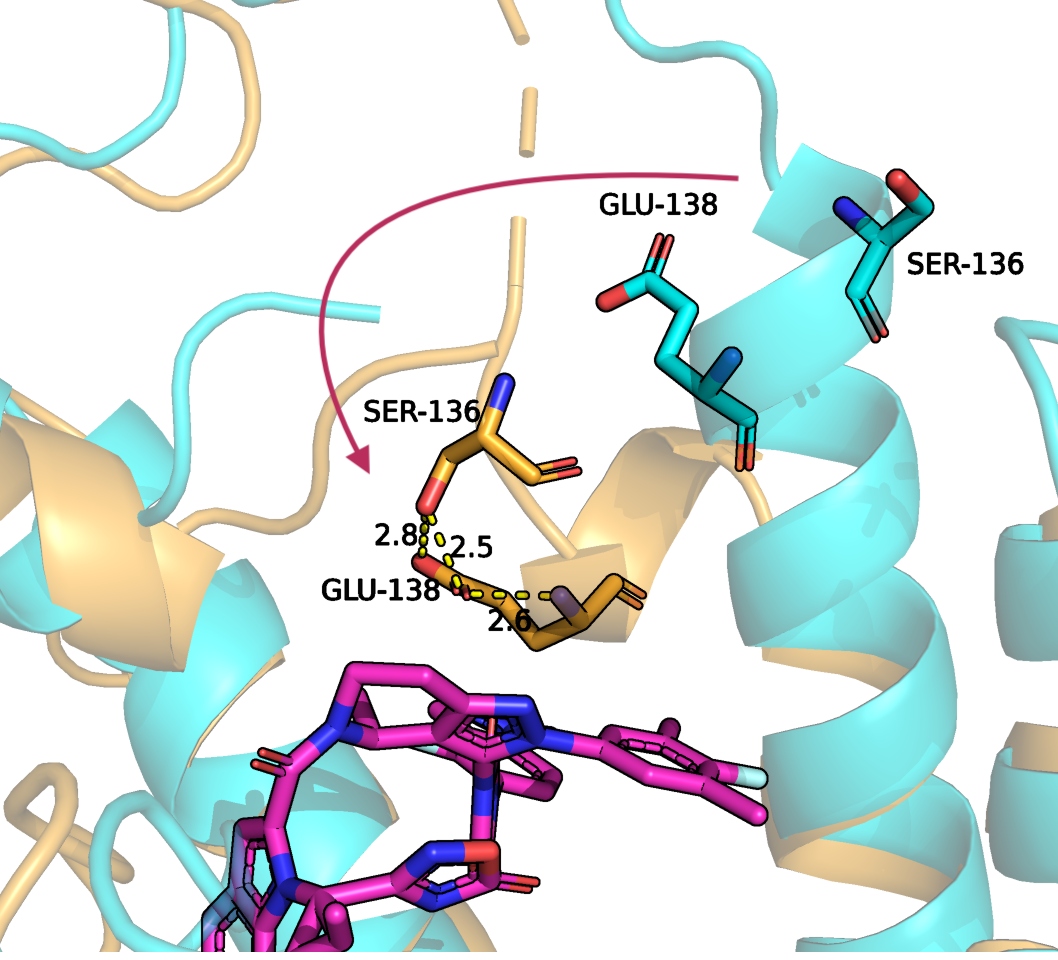
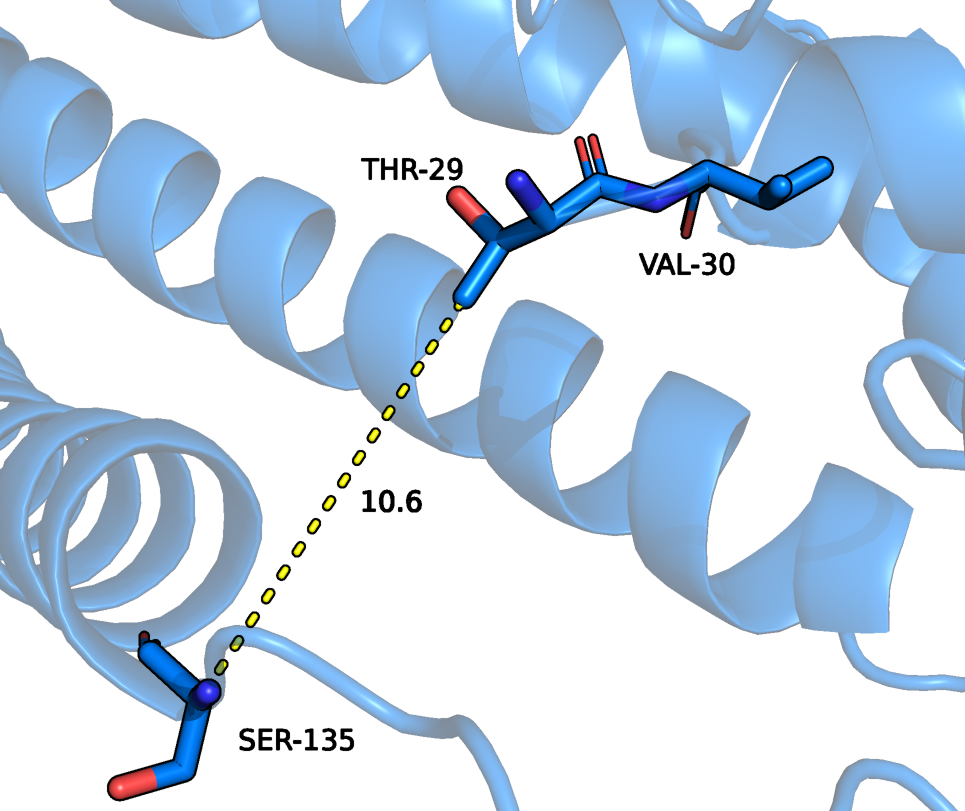
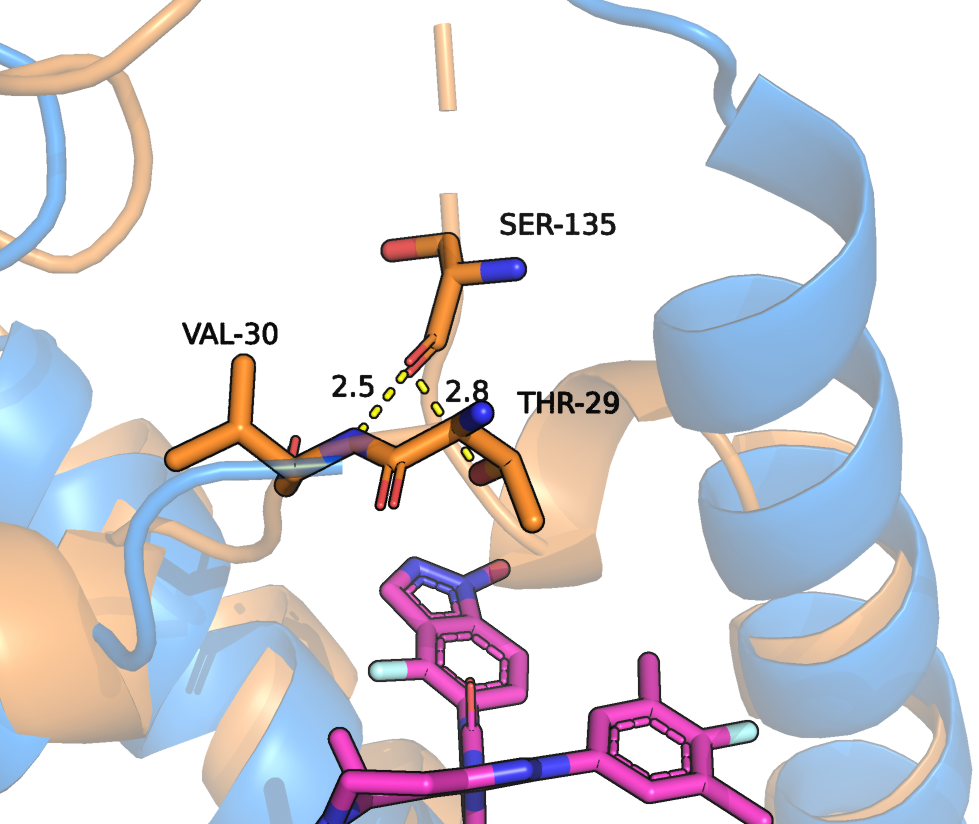
Рассмотрим подробнее некоторые изменения на уровне взаимодействия аминокислотных остатков. Длинная альфа-спираль расщепилась и ее часть развернулась, закрывая карман. В повороте спирали важную роль играют остатки GLU-138 и SER-136. Они сближаются в пространстве и удерживаются водородными связями. Кроме того, у остатка GLU-138 изменилась конформация бокового радикала (Рисунок 7). Гидрофобная часть бокового радикала GLU может участвовать в гидрофобных взаимодествиях [3], она сближена с ароматическим кольцом лиганда. Также в пространстве сближаются петли и взаимодействуют остатки THR-29, SER-135 и VAL-30 (Рисунок 8,9).
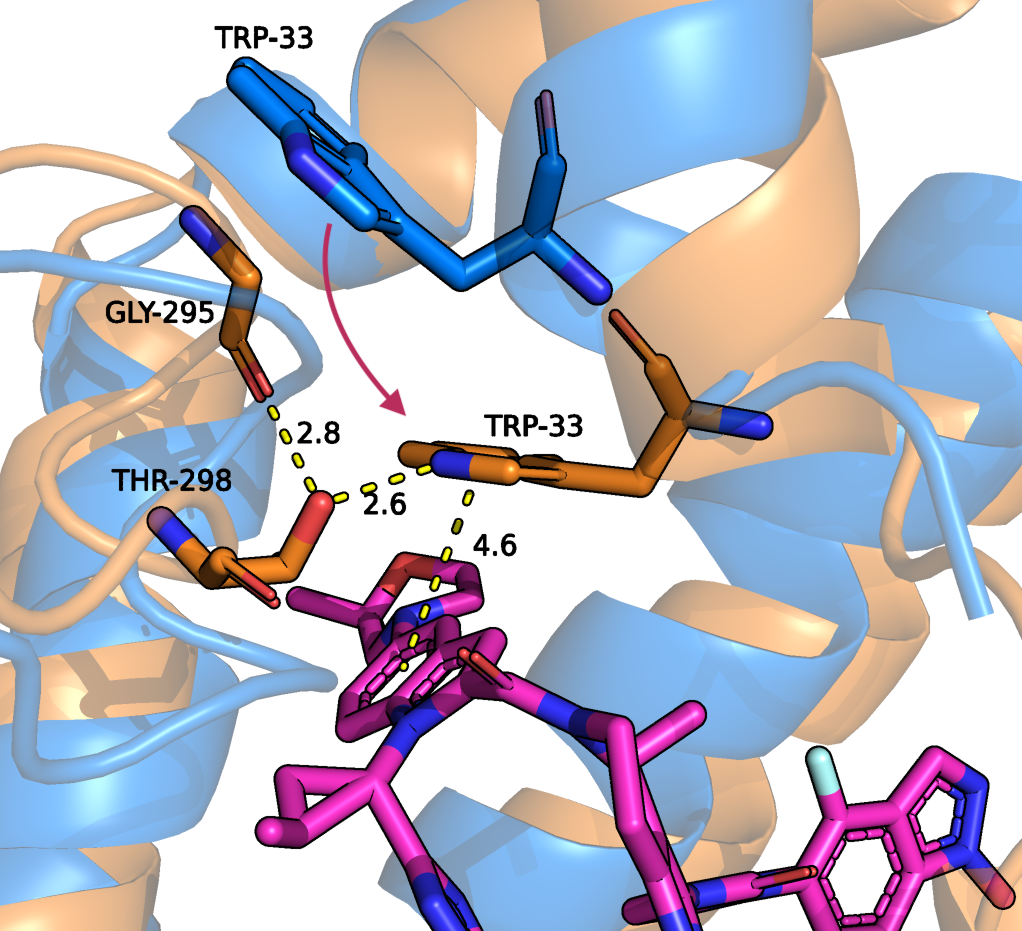
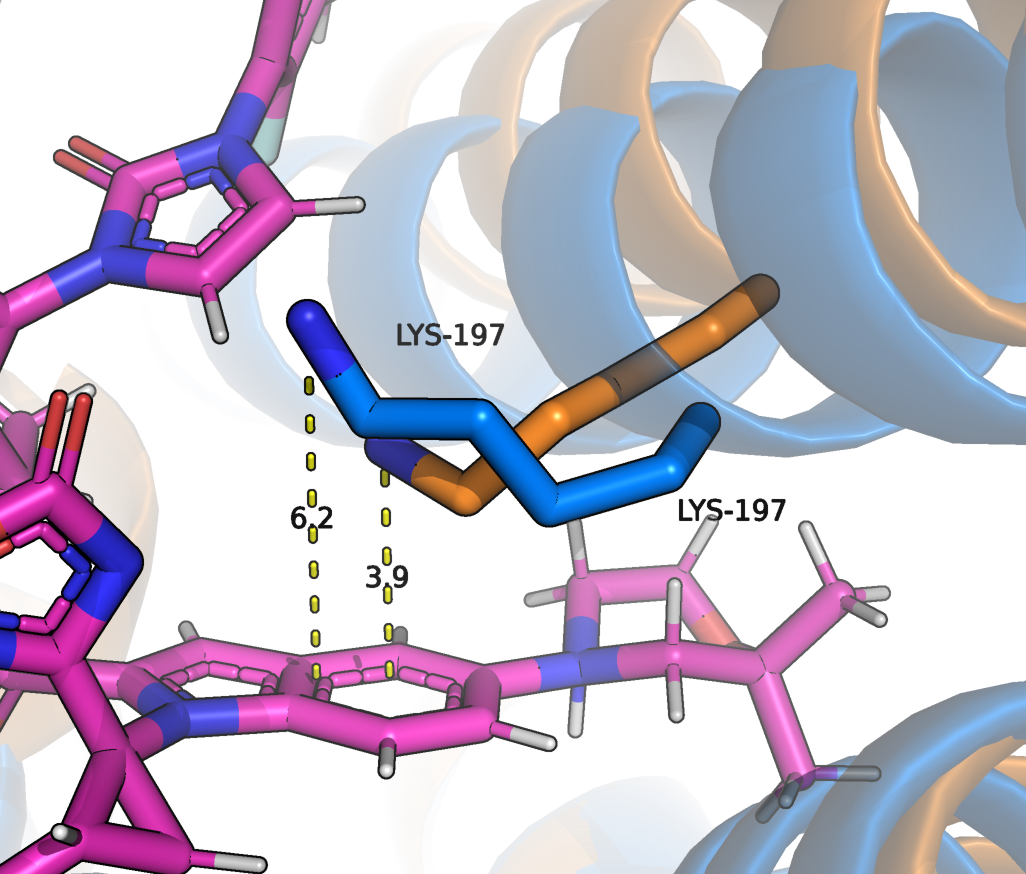
Также примером изменений может служить TRP-33, который в связанной форме ориентирован так, что возможна водородная связь между ним и THR-298 (Рисунок 10). Видно, что он сближается с лигандом и возможно стекинг-взаимодействие между ароматическим кольцом лиганда и остатком TRP-33. Также мне показалось интересным стягивание остатка LYS-197 для образования пи-катионного стекинга с пи-системой лиганда (Рисунок 11).
Далее я воспользовалась веб-сервером POCASA для поиска и анализа карманов в белке. Карманом обычно называют вогнутость (concavity) на поверхности белка. Полостью (cavity) - образование внутри белка (чаще бывают активными сайтами), а каналом - путь к этой полости.[2] Здесь есть пребладающая полость - щель между альфа-спиралями, и несколько небольших полостей. (Рисунок 12)
При предсказании, может ли карман/полость быть активным сайтом, стоит учитывать не только его объем, но и глубину. Для этого рассчитывается параметр Volume Depth (VD). Для каждой точки кармана рассчитывается кратчайшее расстояние от нее до поверхности. Глубина - это сумма кратчайших расстояний по всем точкам кармана. [1]
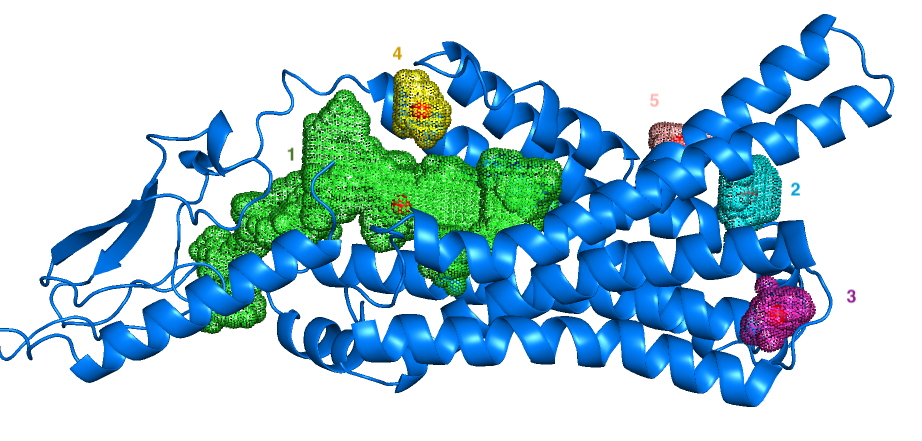
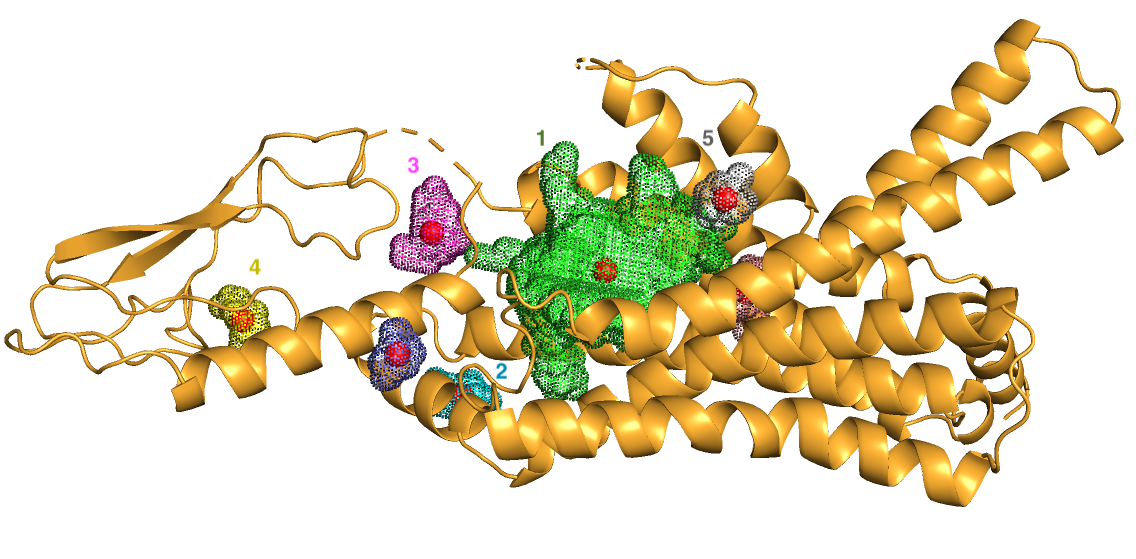
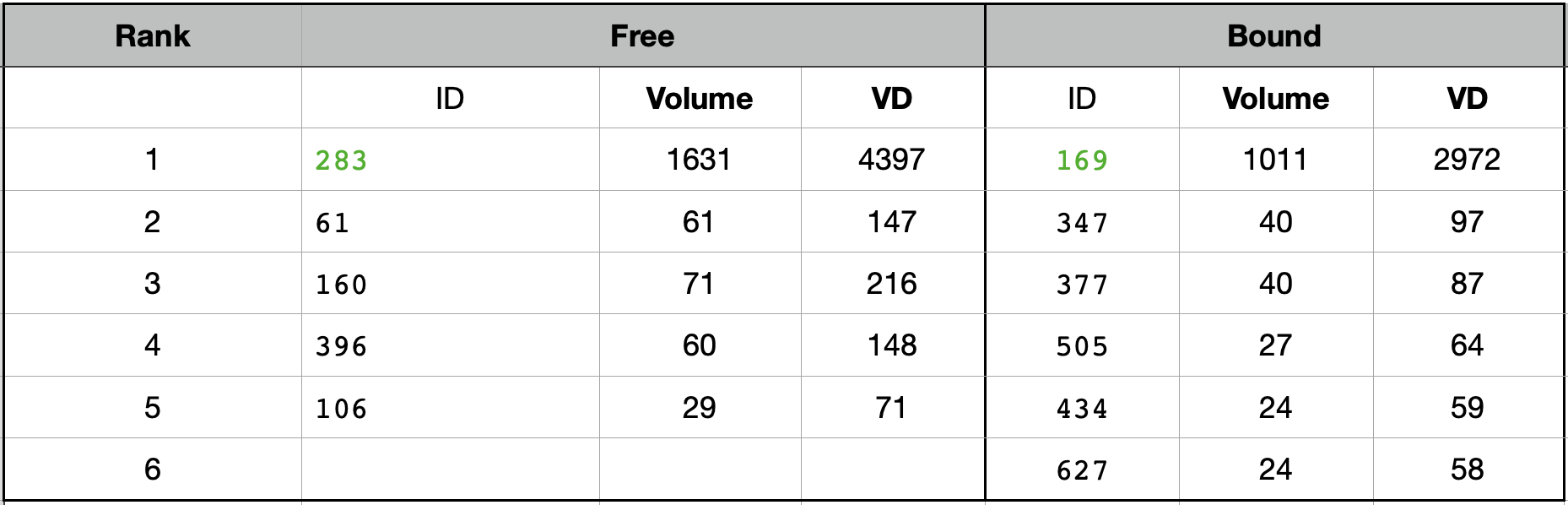
Результаты представлены на Рисунке 12 и в Таблице 1. Сервису удалось определить главную полость, где и происходит связывание с лигандом (номер 1 в Таблице 1). Можно заметить, что объем полостей, как и параметр VD, уменьшается при связывании белка с лигандом. Во втором случае определились новые карманы и исчезли некоторые старые. Большой карман, который соответствует месту связывания лиганда, расщепился на несколько карманов поменьше. Мне кажется, что это стягивание должно закрывать доступ в полость, при этом меняется форма самой полости из-за новых взаимодействий с лигандом. Стягивания, перекрывающие полость, могут возникать после связывания, а перестройки внутри полости могут происходить в то время, когда лиганд "зацепился" в кармане. Мелкие карманы не определились, скорее всего стали незначимы по объему после небольших сдвигов элементов вторичной структуры.
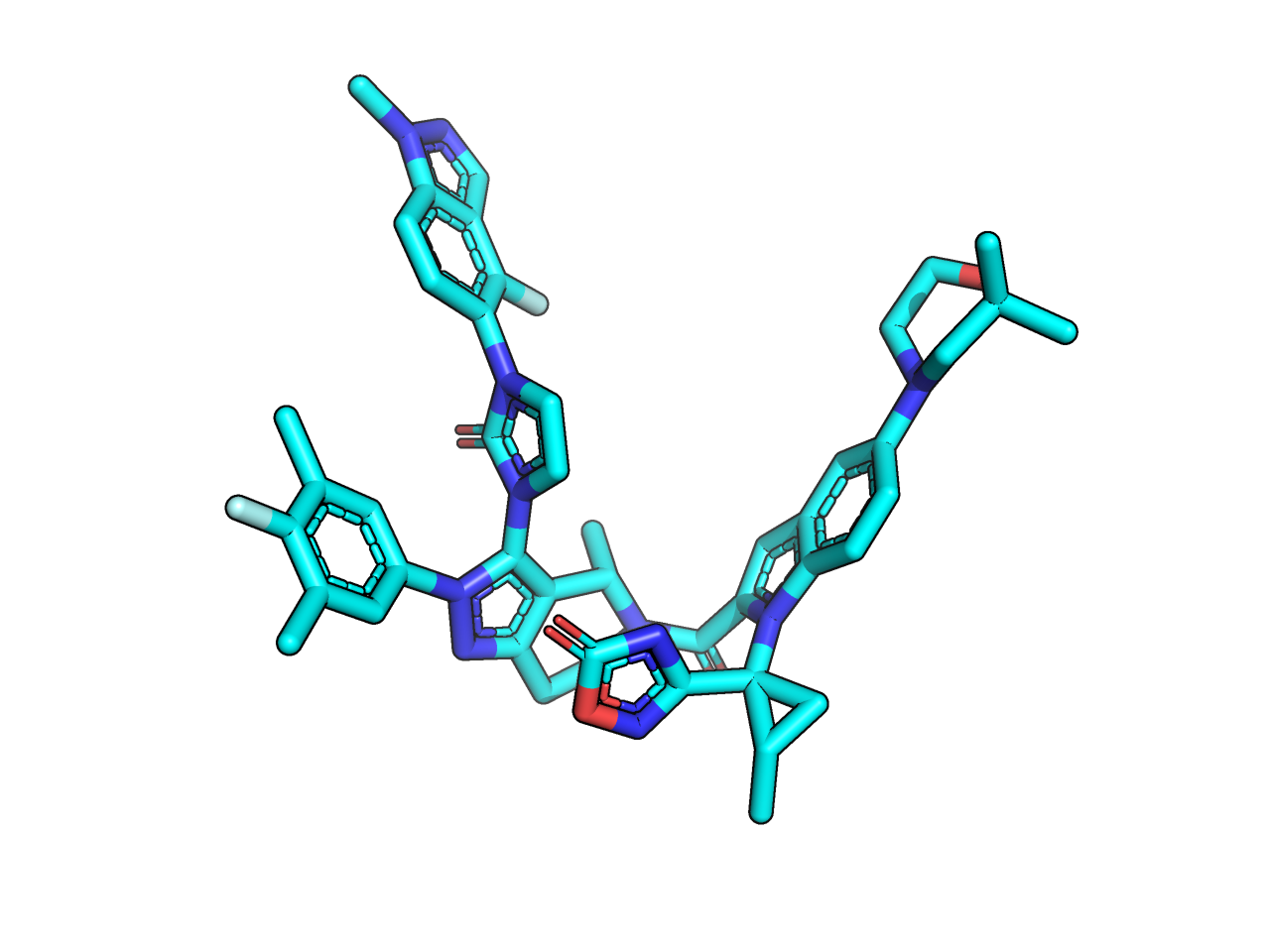
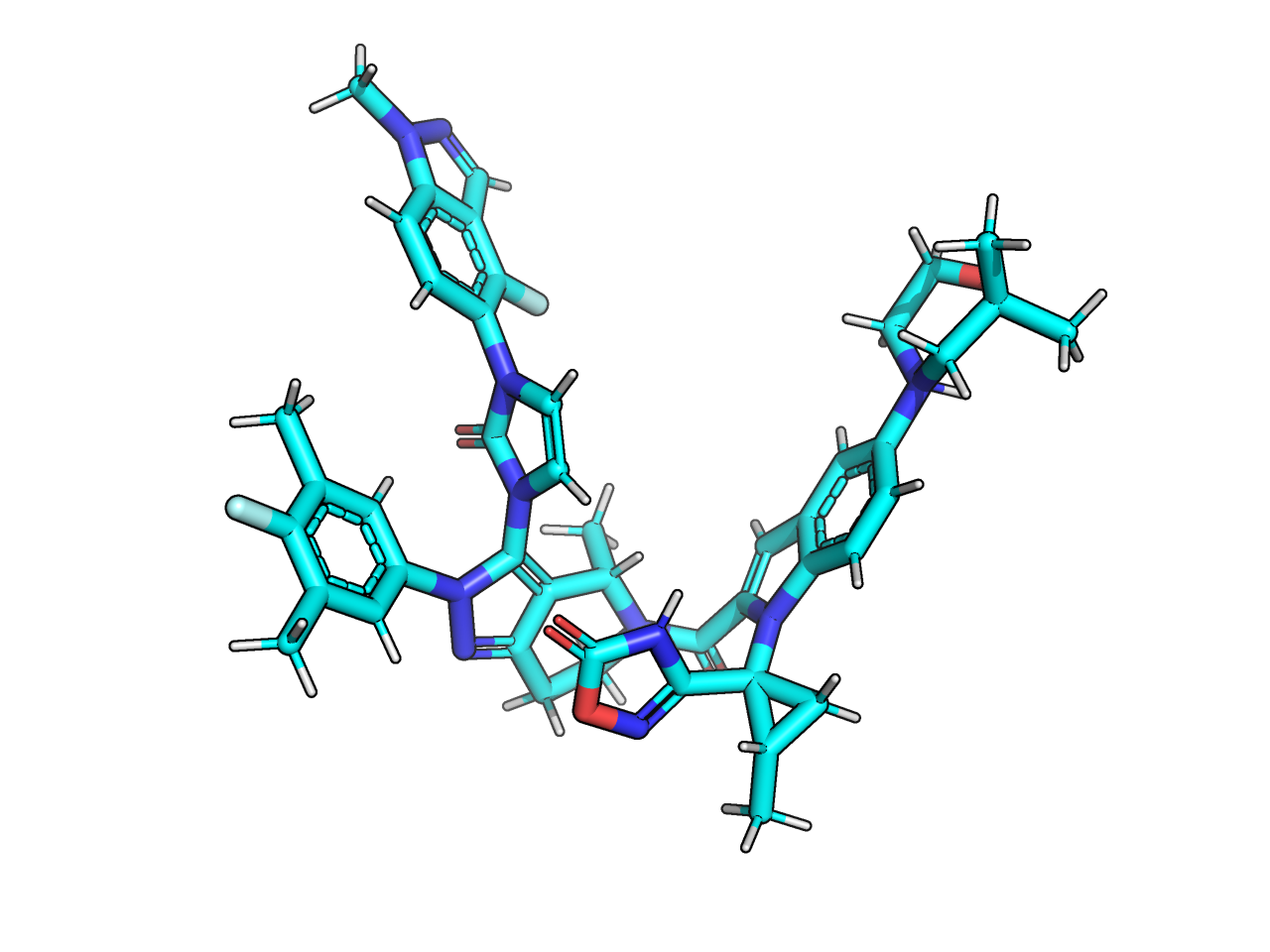
Протоны были добавлены осмыслено. Водороды программа расположила в плоскости колец, углы выглядят нормально.
Сама процедура докинга была проведена с параметрами по умолчанию. Webina было предложено 9 лучших поз. Они, а также исходная поза, изображены на Рисунке 14, 15.
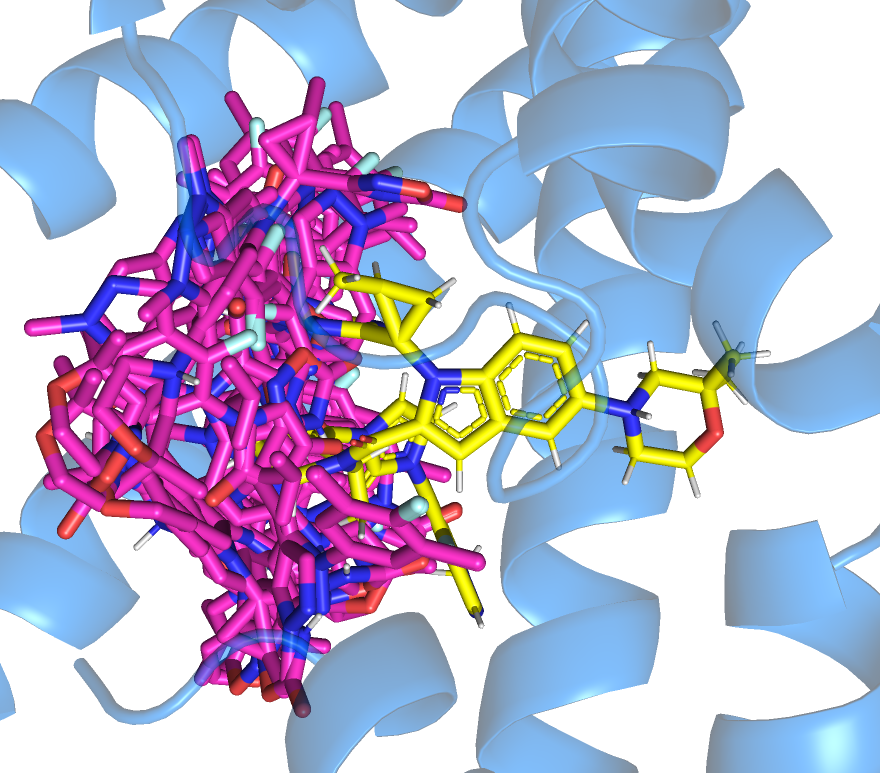
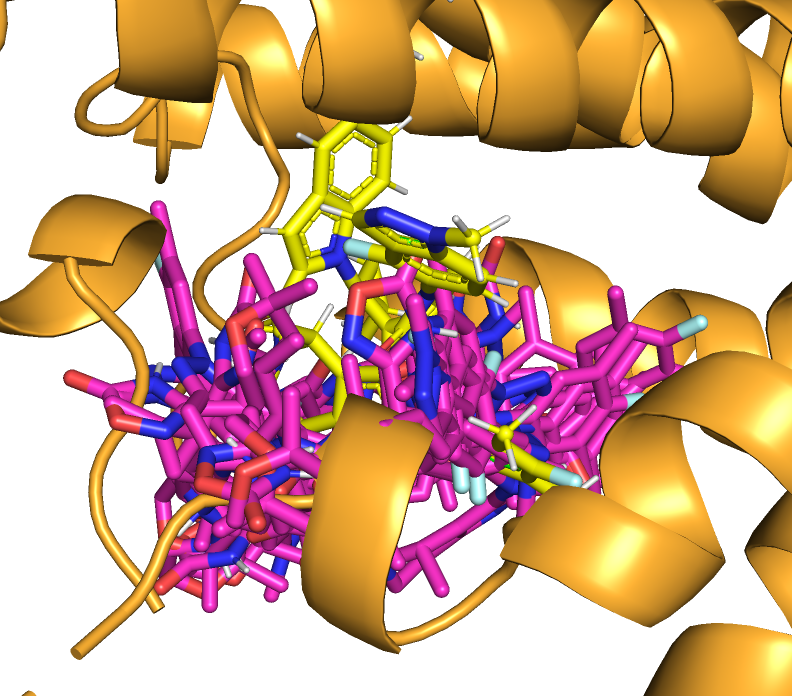
Видно, что ни одно предложенное положение не похоже на положение лиганда при связывании. Заметно, что для всех этих положений части молекул перекрываются со смещенной альфа-спиралью, которую я в том числе описывала в задании 1 (Рисунок 15). Получается, что молекула, полученная из связанного состояния не может быть похожа на предложенные. Если рассмотреть свободную форму рецептора, то можно увидеть, что предложенные молекулы занимают более внутреннее положение, а исходная молекула своей частью располагается ближе к поверхности.
Чтобы сравнить взаимодействия несвязанной формы белка с молекулой в исходной позе и лучшей позе по мнению Webina, я посторила диаграммы взаимодействий в PoseView. На Рисунках 17-18 представлены 2D карты взаимодействий. На наложение исходной и лучшей позы можно посмотреть на Рисунке 16 .
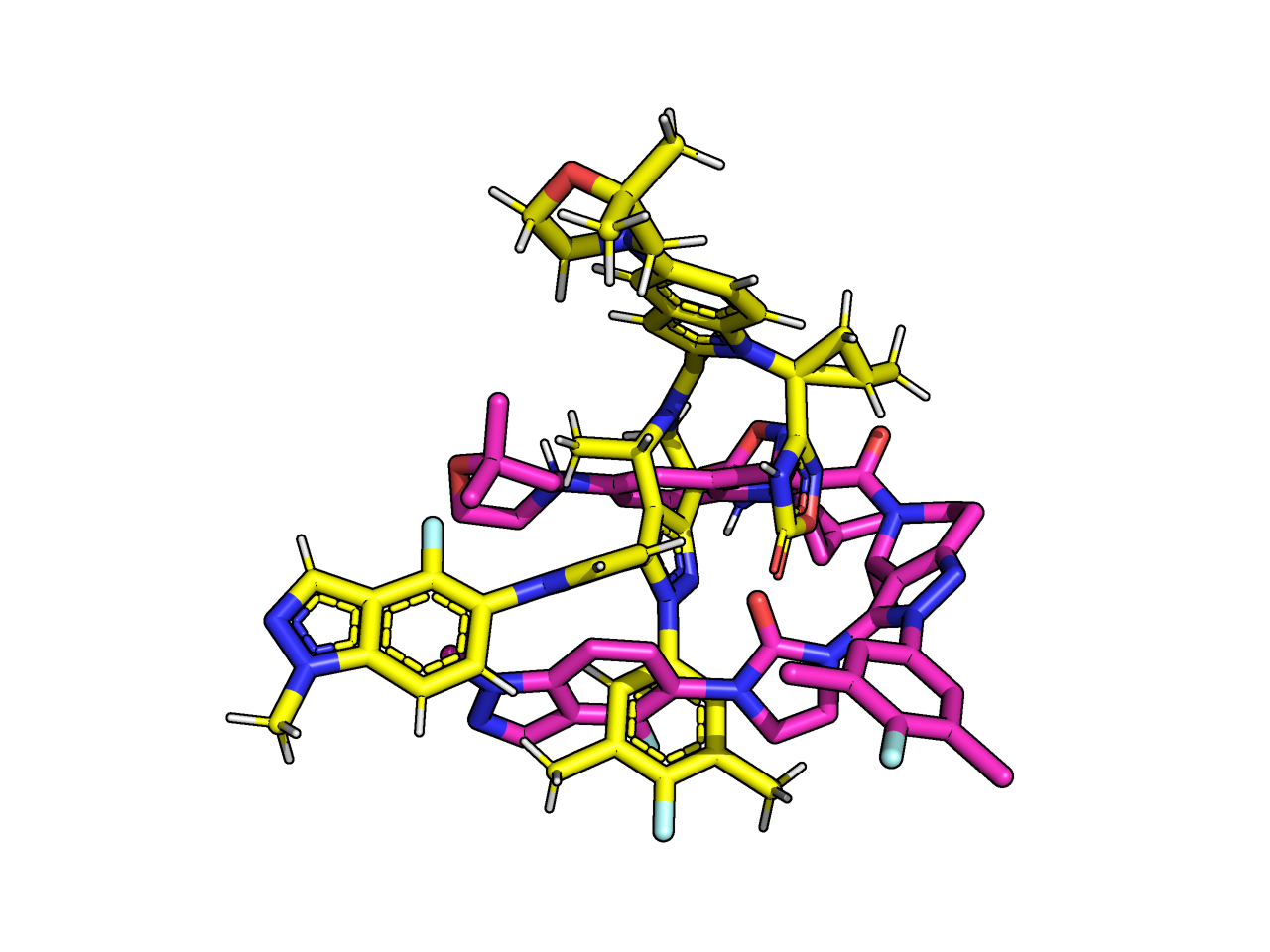
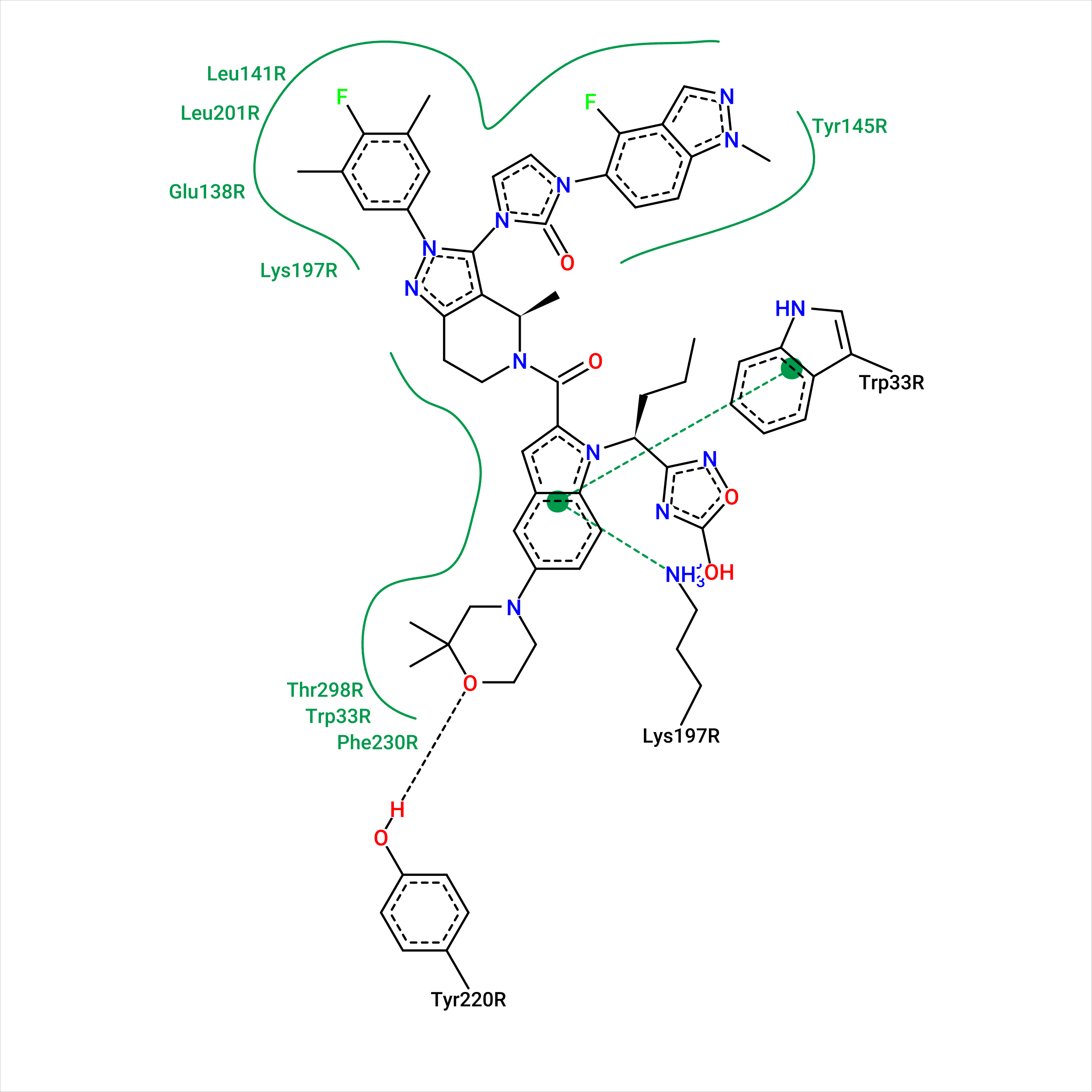
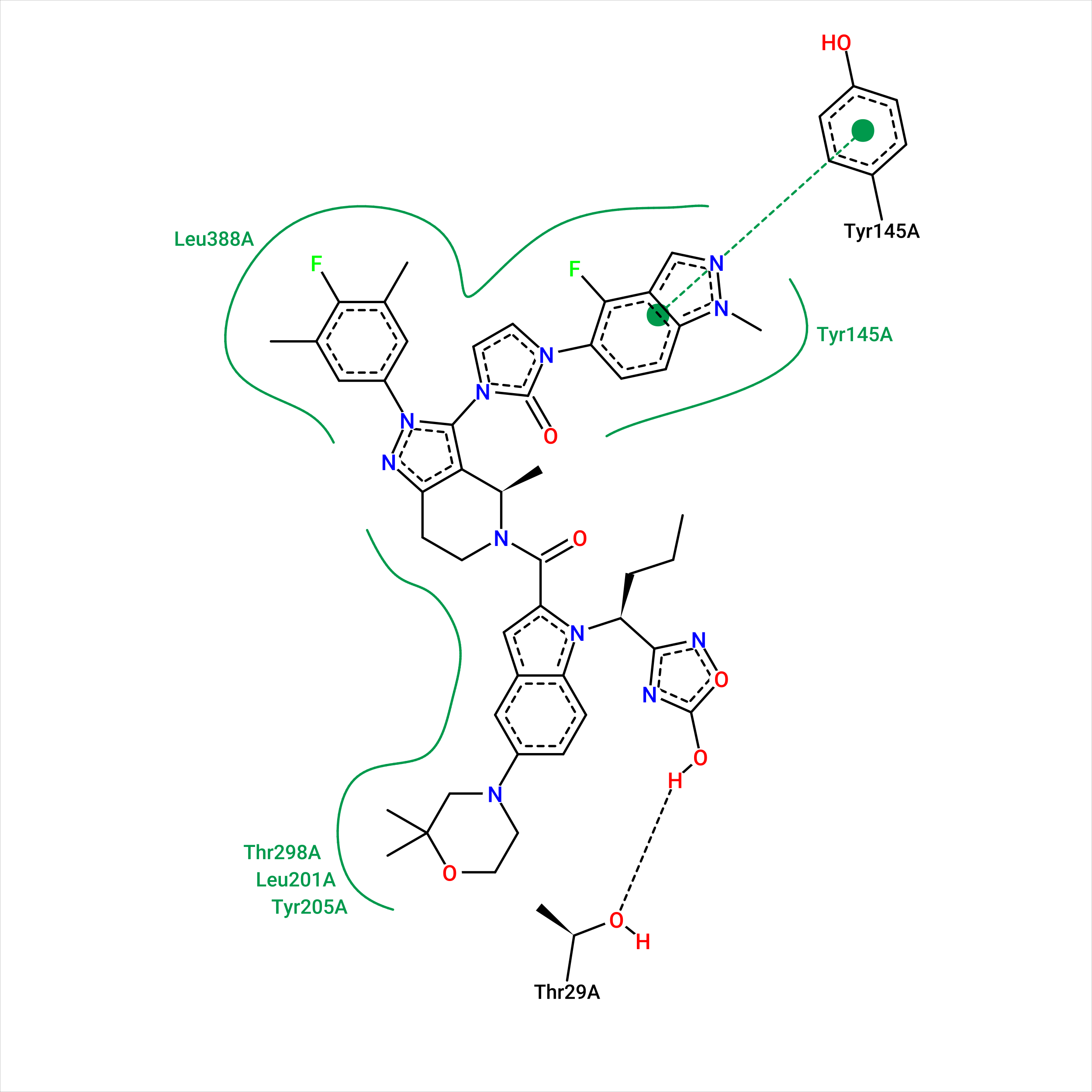
В обоих случаях лиганд был помещен в гидрофобное окружение, однако оно часто составлено из разных остатков. Для связанной формы наблюдаются два стекинг взаимодействия с TRP-33 и LYS-197. Также наблюдается водородная связь TYR с кислородом диметилморфолина лиганда, в свободной форме он не поддерживается полярными взаимодействиями. Также программа выдает отcутствие стекинг взаимодействия с TYR-145, но я предполагаю, что T-стекинг все-таки есть (Рисунок 19).
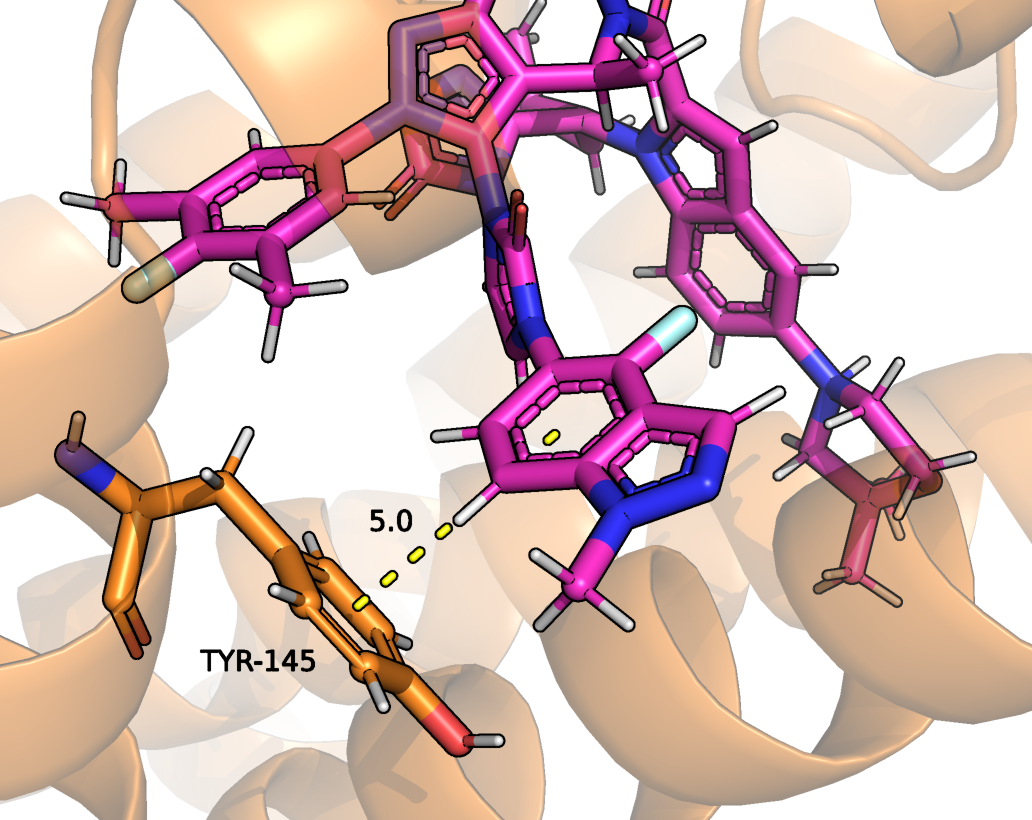
Скорее всего, важную роль играет при связывнии играет индуцированное соответствие. Как мы увидели выше, лиганд не может занять свою позицию, пока не произойдут изменения в белке. Первичным якорем могут служить гидрофобные взаимодействия, не обязательно они будут окончательными, но могут задержать лиганд. Также определящим взаимодействием может служить стекинг взаимодействие с кольцом Tyr145. Окончательное положение, вероятно, лиганд может занять только после перестроек в кармане связывания.
[1] Roll: a new algorithm for the detection of protein pockets and cavities with a rolling probe sphere
[2] Computing cavities, channels, pores and pockets in proteins from non-spherical ligands models
[3] The role of hydrophobic interactions in initiation and propagation of protein folding