Трансмембранные белки
Последующие задания выполнялись с YDHB_BACSU - предположительным белком-транспортером мембраны Bacillus subtilis. Для работы была скачана последовательность белка и предсказание его трехмерной структуры.
База данных OPM
Для выполнения задания был выбран трансмембранный белок Outer membrane protein H (OprH), отвечающий за связывание липополисахаридов. Липополисахарид-связывающие белки важны для опосредования ответа хозяина на липополисахарид.
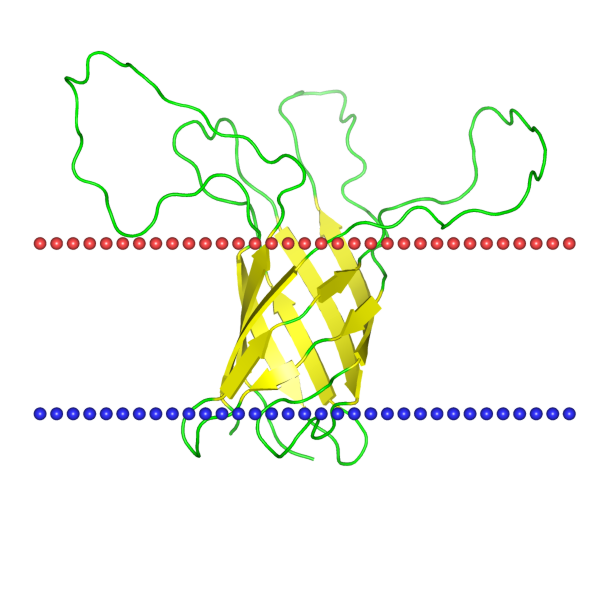
Для выполнения задания был выбран трансмембранный белок Outer membrane protein H (OprH), отвечающий за связывание липополисахаридов. Липополисахарид-связывающие белки важны для опосредования ответа хозяина на липополисахарид.
Трансмембранная часть этого белка представлена 8 β-тяжами, формирующими β-бочонок, заякоренный в мембране. Каждый сегмент в среднем состоит из 8 остатков. По сведениям из базы данных OPM, гидрофобная часть этого белка имеет толщину 20.6 Å. Эта величина отражает расстояние между внутренней и внешней частями мембраны. Измерения в Jmol показали такой же резульат. Также в базе данных указаны следующие координаты сегментов: 1( 5- 12), 2( 41- 48), 3( 55- 60), 4( 74- 83), 5( 91- 101), 6( 119- 130), 7( 137- 144), 8( 170- 177).
| Тип | Трансмембранный |
| Класс | Трансмембранный β-бочонок |
| Суперсемейство | Непрозрачные порины |
| Семейство | Непрозрачные порины |
| Организм | Pseudomonas aeruginosa |
| Локализация | внешняя мембрана грамотрицательных бактерий |
| Толщина гидрофобной части | 20.6 Å |
| Угол изгиба | 15° |
| Топология | субъединица А (N-конец внеклеточный) |
DeepTMHMM
Белок(α): YDHB_BACSU
Последовательность | Выдача программы
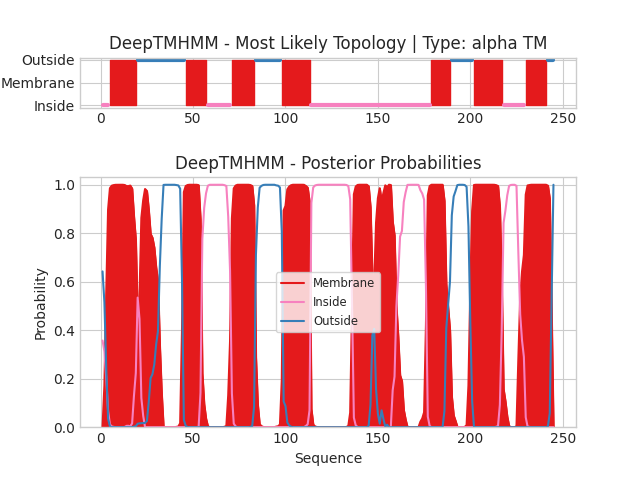
В графической выдаче по горизонтали отложены координаты остатков белка, на вертикальной оси показаны предсказание положение определенных участков (верхний рисунок) и вероятность принадлежности конкретного остатка к той или иной топологии (нижний рисунок). Каждый цвет означает определенную локализацию участка: Membrane - трансмембранный, Inside - внутриклеточный, Outside - внеклеточный. Для выданного белка показано 10 трансмембранных сегментов, а N- и C-концевой домены являются внутриклеточными. Также нетрудно заметить, что для региона с 110 по 180 остаток предсказание положения участка затруднено, в то время как на вероятностном графике мы видим трансмембранный сегмент.
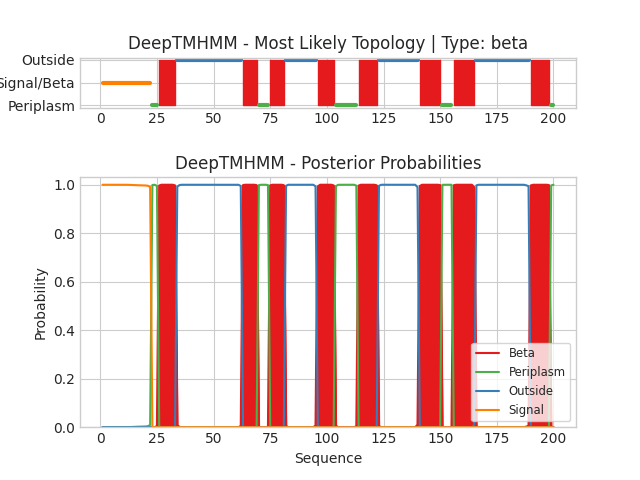
Белок(β): YDHB_BACSU
Последовательность | Выдача программы
Здесь каждый цвет также означает определенную локализацию участка: Beta - бета-слой (мембранный), Periplasm - периплазматический (аналог внутриклеточной части), Outside - внеклеточный, Signal - сигнальный пептид для периплазматической локализации. Для выбранного в первом задании трансмембранного белка программа нашла 8 трансмембранных сегментов. N-конец белка является сигнальным пептидом, а за ним согласно предсказанию следует периплазматический участок.
PPM
Были выбраны следующие параметры программы PPM 3.0:
- Number of Membranes: 1
- Type of membrane: Gram-negative bacteria outer membrane
- Allow curvature: no
- Topology (N-ter): out (по предсказанию DeepTMHMM)
Выдачу можно посмотреть по ссылке
| Толщина гидрофобной части | 26.3 ± 1.3 Å |
| ΔG | -67.7 kcal/mol |
| Угол изгиба | 7 ± 1° |
| Трансмембранные сегменты | 1(3 - 17), 2(22 - 33), 3(39 - 57), 4(69 - 88), 5(98 - 116), 6(130 - 149), 7(172 - 193), 8(199 - 219), 9(226 - 243) |
| Средняя длина трансмембранного сегмента | 18 |
Сравнение алгоритмов предсказания
DeepTMHMM
- 3 - 19
- 22 - 31
- 45 - 54
- 71 - 83
- 99 - 113
- 137 - 146
- 148 - 157
- 177 - 186
- 200 - 217
- 226 - 243
PPM
- 3 - 17
- 22 - 33
- 39 - 57
- 69 - 88
- 98 - 116
- 130 - 149
- 172 - 193
- 199 - 219
- 226 - 243
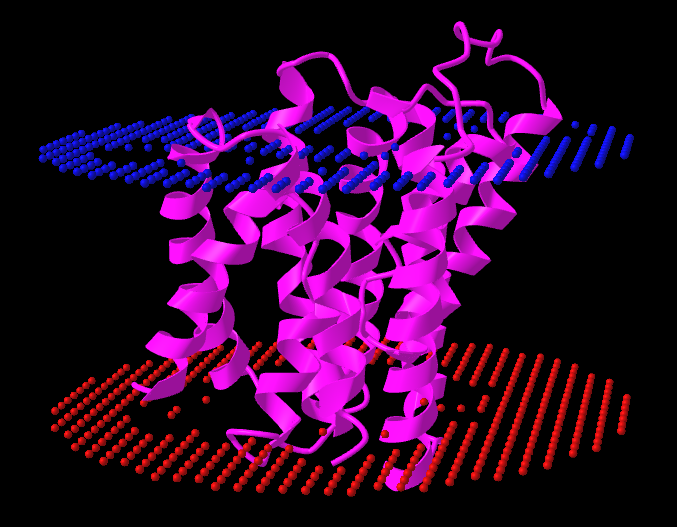
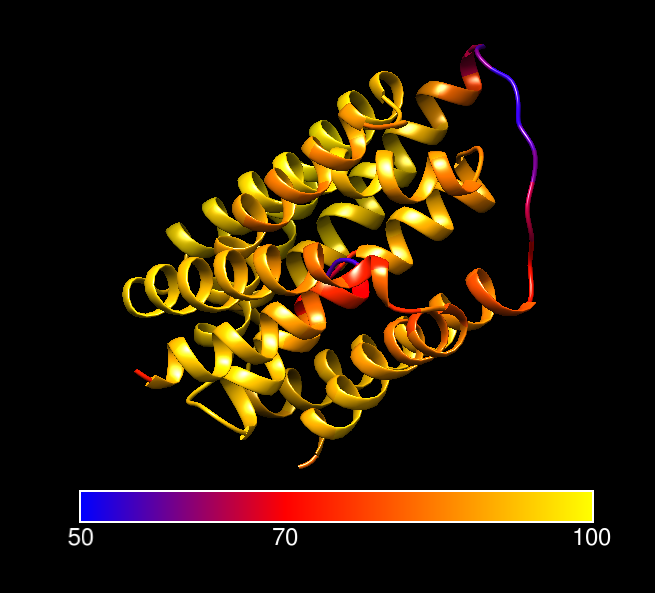
Программа DeepTMHMM нашла на один трансмембранный сегмент больше. Координаты остальных сегментов у DeepTMHMM и PPM похожи (в разной степени). На картинке справа можно увидеть покраску структуры по b-фактору (уверенность в предсказании). Уверенность предсказания AlphaFold для белка высока для всех трансмембранных участков. Для остальных частей структуры предсказаны менее достоверно. Скорее всего, PPM не использует данные из колонки b-фактора pdf-файла, поэтому качество предсказания AlphaFold по-видимому не влияет на результат.
База данных TCDB
К сожалению, для обоих белков я получил сообщение, что записи о них не содержатся в базе данных.