|
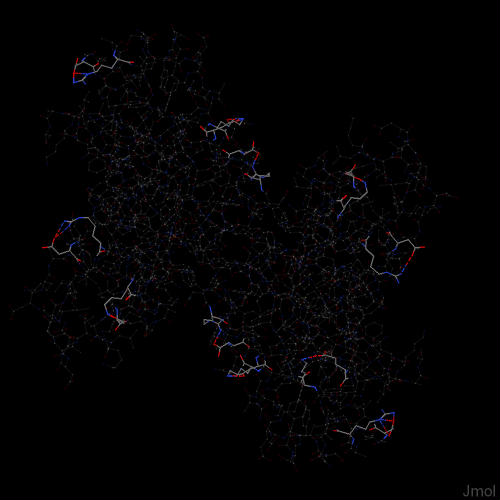
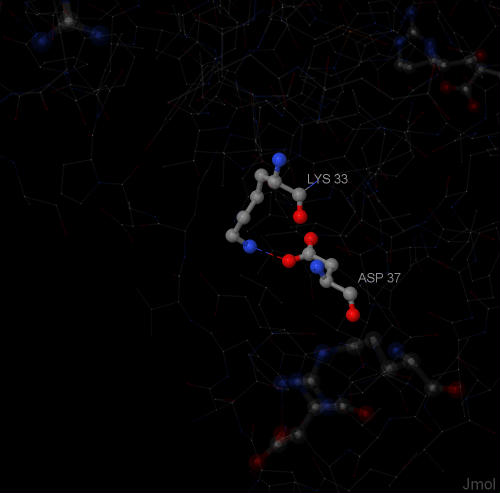
Третичная структура формируется в результате нековалентных взаимодействий (электростатические, ионные, силы Ван-дер-Ваальса и др.) боковых радикалов альфа-спирали и вета-тяжами. Среди связей, удерживающих третичную структуру следует отметить: а) дисульфидный мостик ( - S - S - ) б) сложноэфирный мостик (между карбоксильной группой и гидроксильной группой) в) солевой мостик (между карбоксильной группой и аминогруппой) г) водородные связи. Солевой мостики образованны между положительно и отрицательно заряженными аминокислотными остатками. На рис1 изображены все солеввые мостики белка sodB. Всего в белке представлено 11 солевых мостиков. На рис2 показан один из солевых мостиков. Эти изображения получены с помощью скрипта и еще команды "select within(GROUP,within(3.5,hbpositive) and hbnegative, within(3.5,hbnegative) and hbpositive)", где hbnegative-это гидрофобные кластеры, а hbpositive-гидрофильные кластеры.
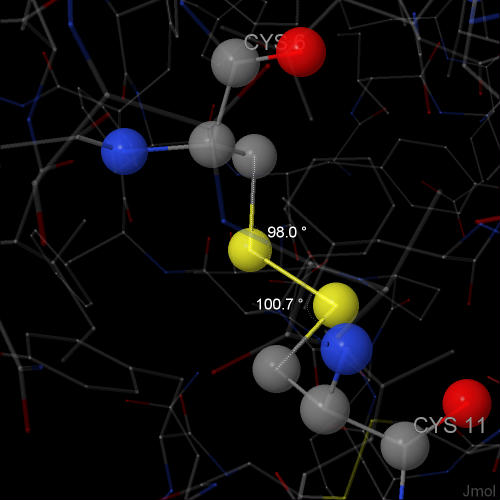
Дисульфидные мостики Дисульфидные мостики образуются между атомами S.Так как в белке sodB не было найдено дисульфидных мостиков. Ярким примером SS-мостиков является белкок инсулин (идентификатор 2DTG на сайте PDB). На рис3 показан два цистеина, который образуют дисульфидный мостик, при этом образуются углы примерно равные 90°.
Рис3.SS-мостик между двумя цистеинами. Водородные связи, не являющиеся солевыми мостиками Такие связи образуются между могут незаряженными остатками аминокислот На рис. изображены водородные связи между аланина 119 и глутамин 123. |