Взаимодействия. Субстратная специфичность
PoseView
PDB ID структуры - 5RNF
В практикуме 1 рассматривались взаимодействия лиганда 1-ацетил-N-метил-N-фенилпиперидин-4-карбоксамида (UPJ) с белком.
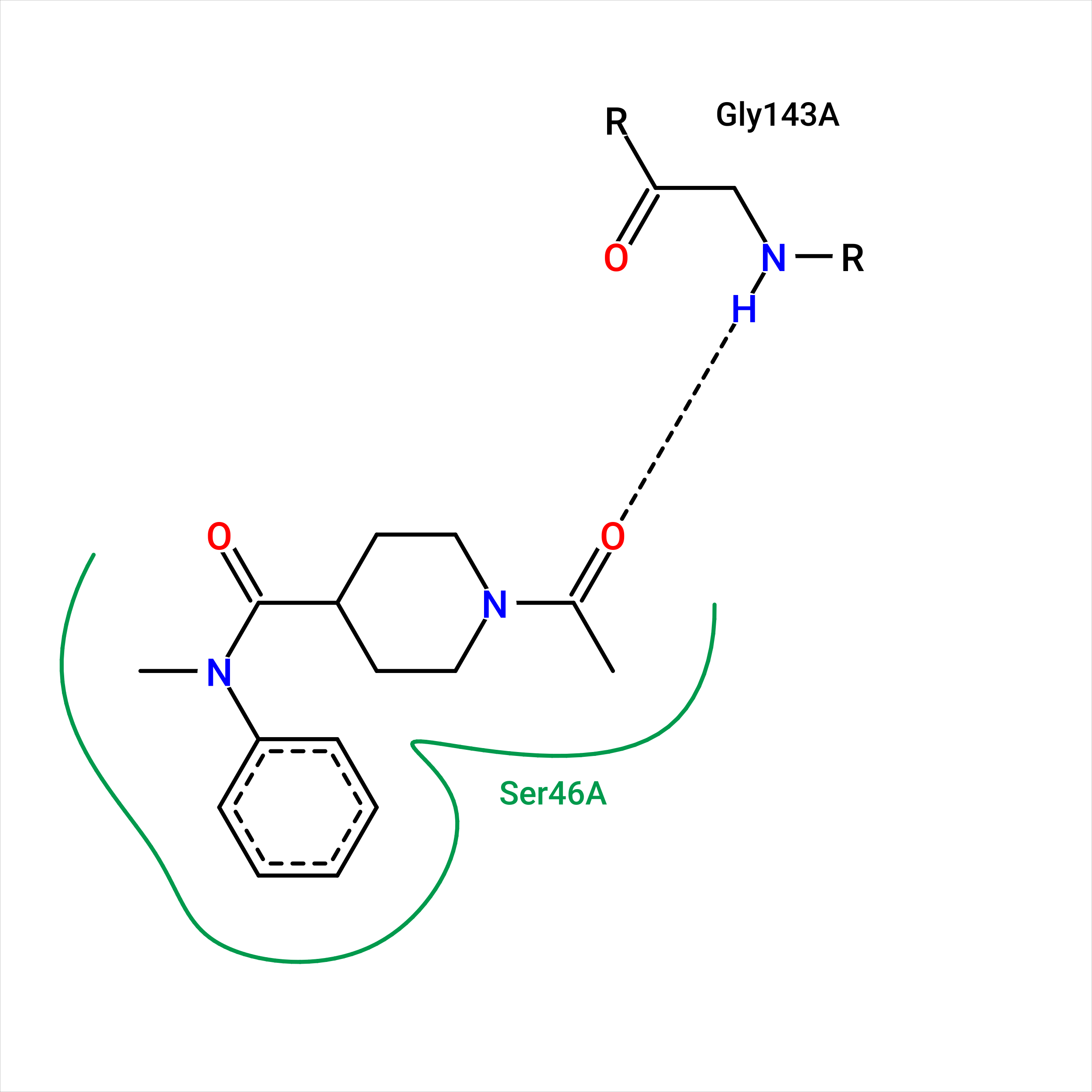
Ниже показаны взаимодействия лиганда, полученные с помощью Poseview
Взаимодействие с глицином-143, представленное на диаграмме, не было упомянуто в практикуме 1. Также в структуре, изображённой в Proteins.Plus, отсутствует ковалентная связь с цистеином, которая была показана в Pymol.
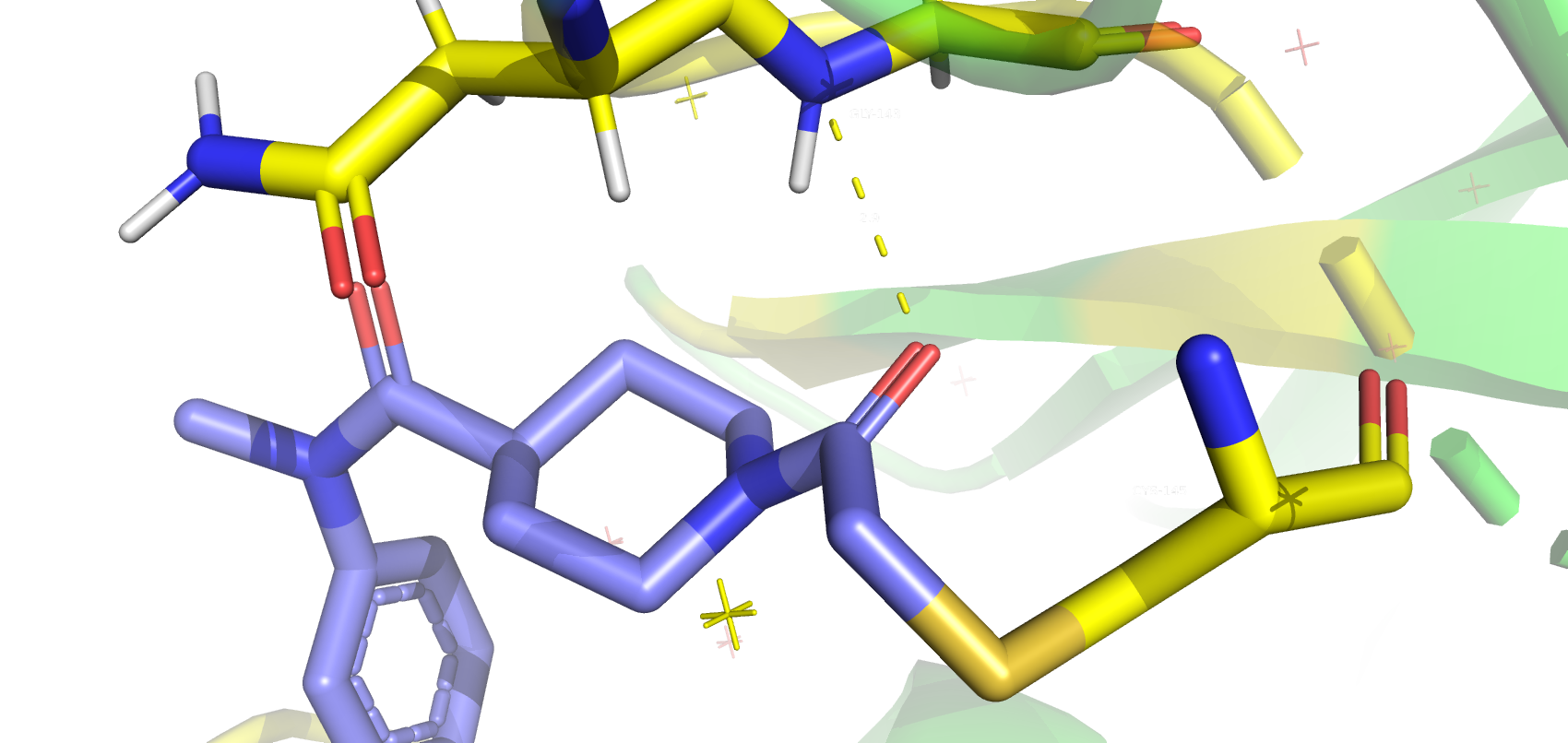
Изображение отличительного взаимодействия в Pymol показано ниже
На рисунке видно, что азот глицина-143 находится на комфортном расстоянии от кислорода, но геометрия данного взаимодействия далека от идеальной. Также серин-46, изображённый на диаграмме, в Pymol находится на некотором отдалении от лиганда.
Из этого можно сделать вывод, что при выявлении потенциально взаимодействующих остатков экспертный взгляд не менее важен, чем выдача различных программ.
PyMol mutagenesis
Структура 1 (0005)
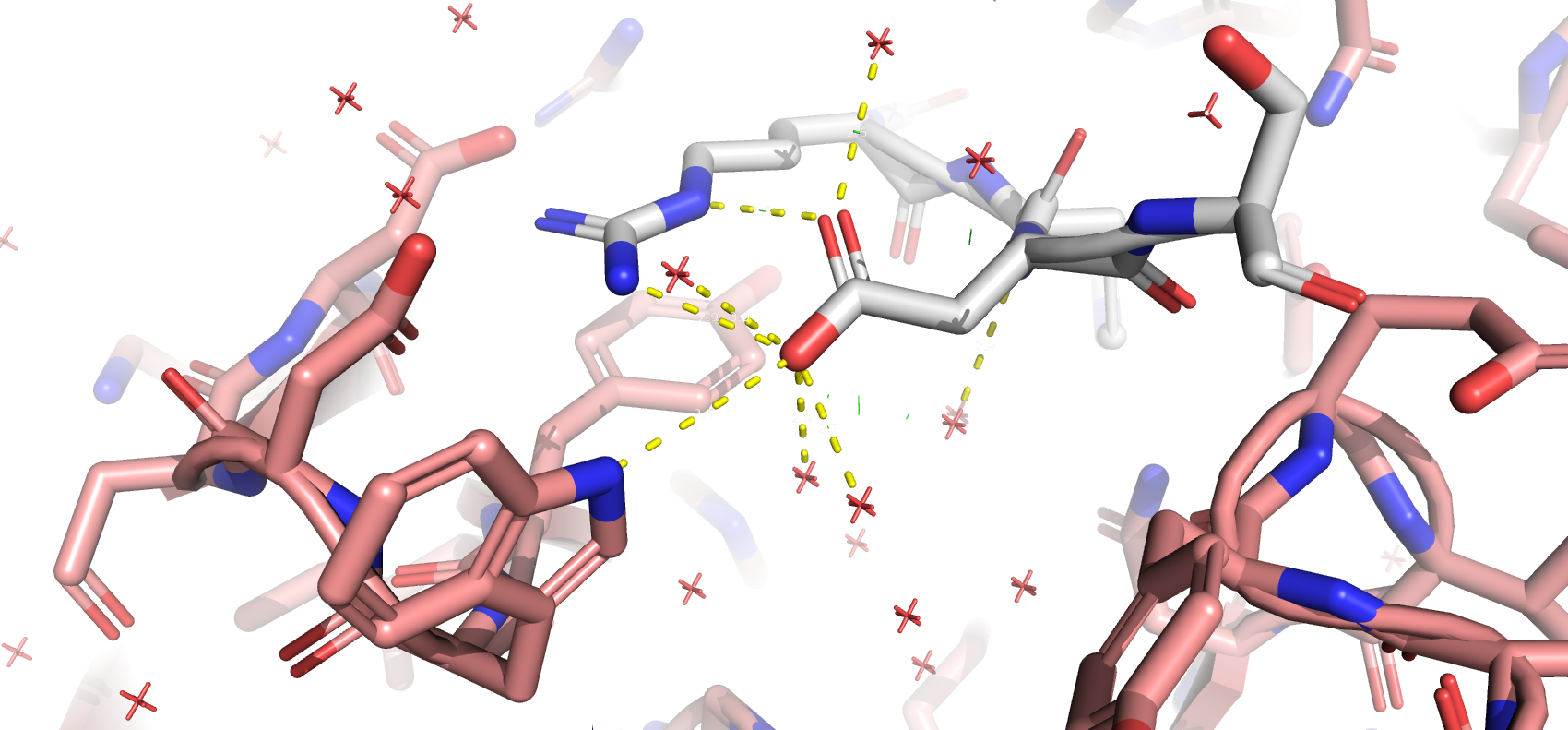
Поскольку структура является комплексом антитела с пептидным антигеном, постараемся найти такую аминокислоту, которая имеет много связей с атомами белка, по возможности минимизируя параметр strain и максимизируя вероятность встретить ротамер в PDB.
Здесь в месте бокового радикала предположительной аминокислоты видно большое количество полярных групп, с которыми можно образовать водородную связь. Большие аминокислоты (trp, his, lys, arg и т.п.) стерически плохо подходят. Малые аминокислоты (asp, asn, ser, cys и т.п.) образуют мало связей и пустоты, в которых должна быть вода, которой нет. Аминокислоты glu и gln плотно контактируют с белком и образуют с ним водородные связи. Но именно 3й ротамер глутамина образует водородные связи с лучшей геометрией, чем глутамат, он имеет strain=23.08 и вероятность встречи в PDB = 9.1%
Структура 2 (0072)
Здесь в месте бокового радикала видно большое количество молекул воды, что исключает присутствие гидрофобных аминокислот. Вода и боковой радикал аргинина не предполагают большого бокового радикала. 1й ротамер аспартата образует водородные связи с аргинином и водой, имеет strain=14.39 и вероятность встречи в PDB = 40.6%