Поверхности, карманы, pKa
SASA, MSA
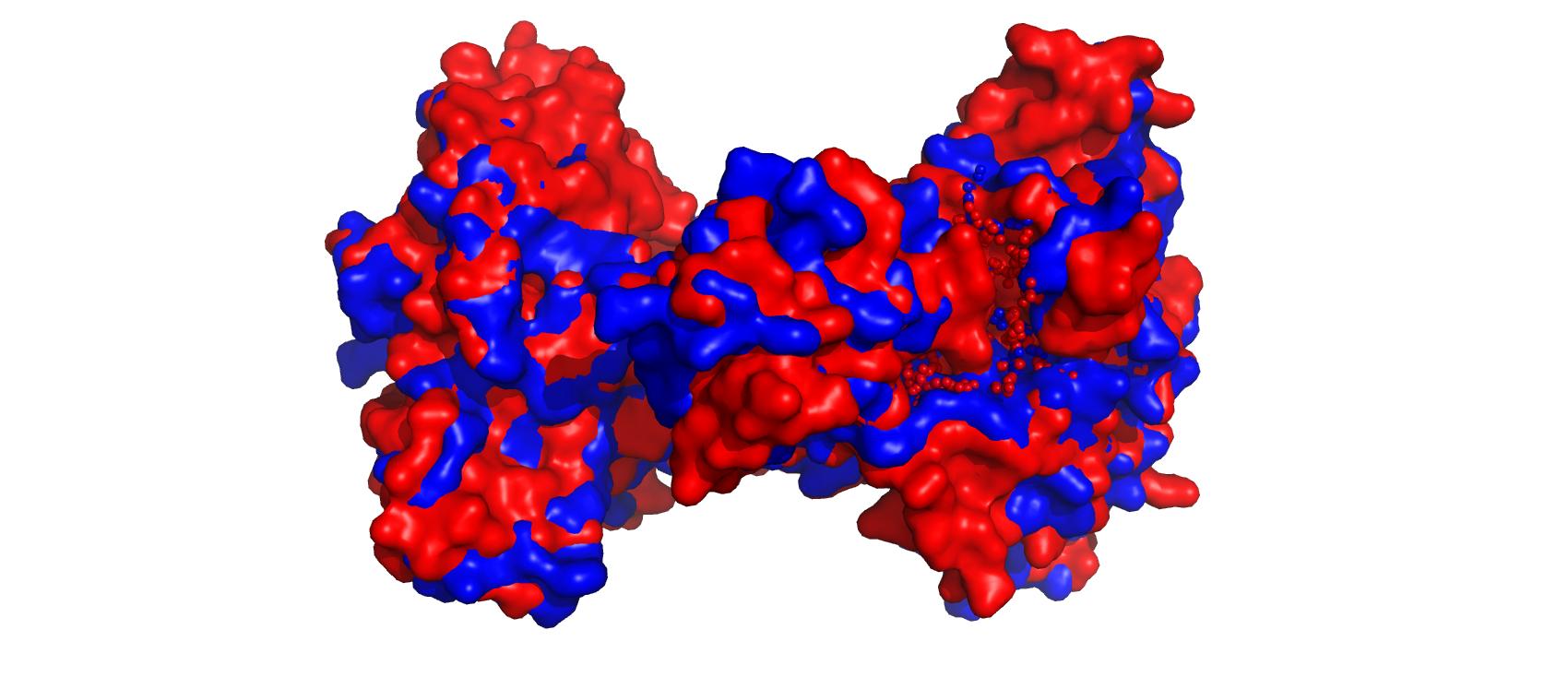
PDB ID данного практикума: 2CKQ (закрытая форма), 2CKP (открытая форма)
Структуры, в целом, схожи друг с другом. Присутствуют различия в положении петель и некоторых альфа-спиралей.
Площадь молекулярной поверхности(MS): 75719.945 Angstroms^2 (закрытая форма), 61343.219 Angstroms^2 (открытая форма)
Площадь поверхности, доступной растворителю(SAS): 34492.875 Angstroms^2 (закрытая форма), 31921.102 Angstroms^2 (открытая форма)
Площадь молекулярной поверхности гораздо больше, чем площадь поверхности, доступной растворителю. Это связано с тем, что "растворитель" не может контактировать со всей молекулярной поверхностью.
Площадь закрытой формы больше, чем открытой. Это может быть связано с тем, что некоторые остатки, экспонированные в закрытой форме, погружены в белок в открытой форме.
Карманы, объем
С помощью fpocket были предсказаны положения и параметры карманов на поверхности молекул. Определён основной карман связывания. Его изображение и параметры показаны ниже.
Программа показала 52 кармана для открытой формы и 49 для закрытой.
Объём основного кармана связывания: 6825.7437 (закрытая форма), 5105.3809 (открытая форма)
Объём кармана в закрытой форме больше из-за того, что при изменении конформации белка появляются полости, которые программа считает частью основного кармана связывания, или же карманы, считаемые программой разными для открытой конформации, воспринимаются как один для закрытой формы белка.
Экспонированность
Была посчитана экспонированность для каждого остатка обеих форм белка. Также для каждого остатка, присутствующего в обеих формах, была посчитана разность экспонирования открытой и закрытой формы. Получившееся распределение прказано на рисунке 3.1
Из распределения видно, что большинство остатков незначительно изменило свою экспонированность, но есть остатки, для которых экспонированность при зактытии белка существенно изменилась.
Рассмотрим остатки с наибольшим изменением экспонированности:
| Аминокислота | Открытая форма | Закрытая форма |
|---|---|---|
| 89 ARG | 176 | 43 |
| 259 GLU | 138 | 35 |
| 373 LYS | 76 | 178 |
| 271 ILE | 150 | 57 |
| 272 LYS | 63 | 154 |
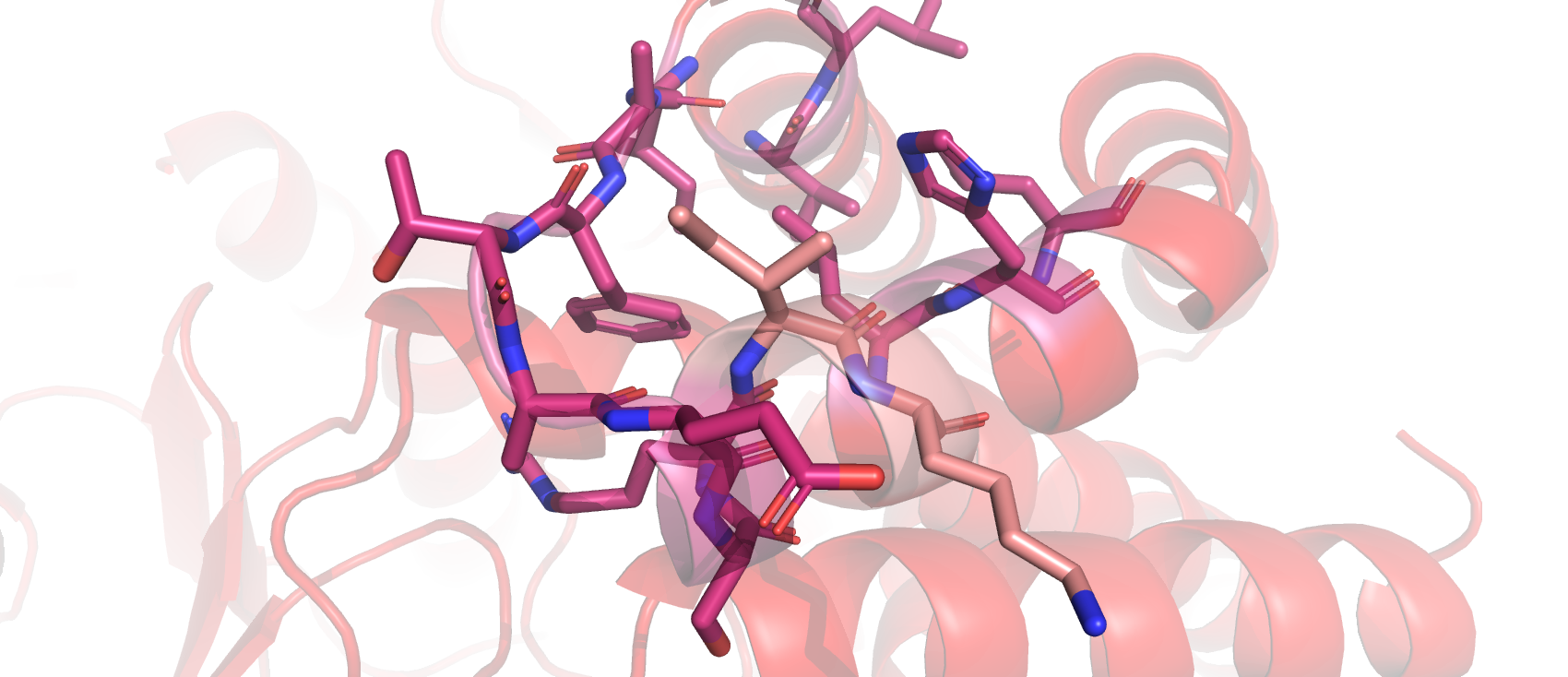
Из приведённых выше остатков только один, изолейцин-271, имеет все атомы в структуре. Его изображение представлено на рисунке 3.2
Здесь для открытой формы видно, что петля, соединяющая две альфа-спирали, не разрешена. Видимо, из-за этого экспонированность данного остатка настолько большая для данной формы. Для закрытой формы данный участок хорошо разрешён. Рядом с изолейцином-271 присутствует несколько гидрофобных отатков, которые, по-видимому, стабилизируют эту часть белка.
Из этого можно сделать вывод, что экстремальное изменение экспонированности обусловлено больше факторами подготовки структуры белка, чем его биологической функцией.