| Главная страница | Обучение | Обо мне | Ссылки |
Построение и анализ поверхностей | |||
|
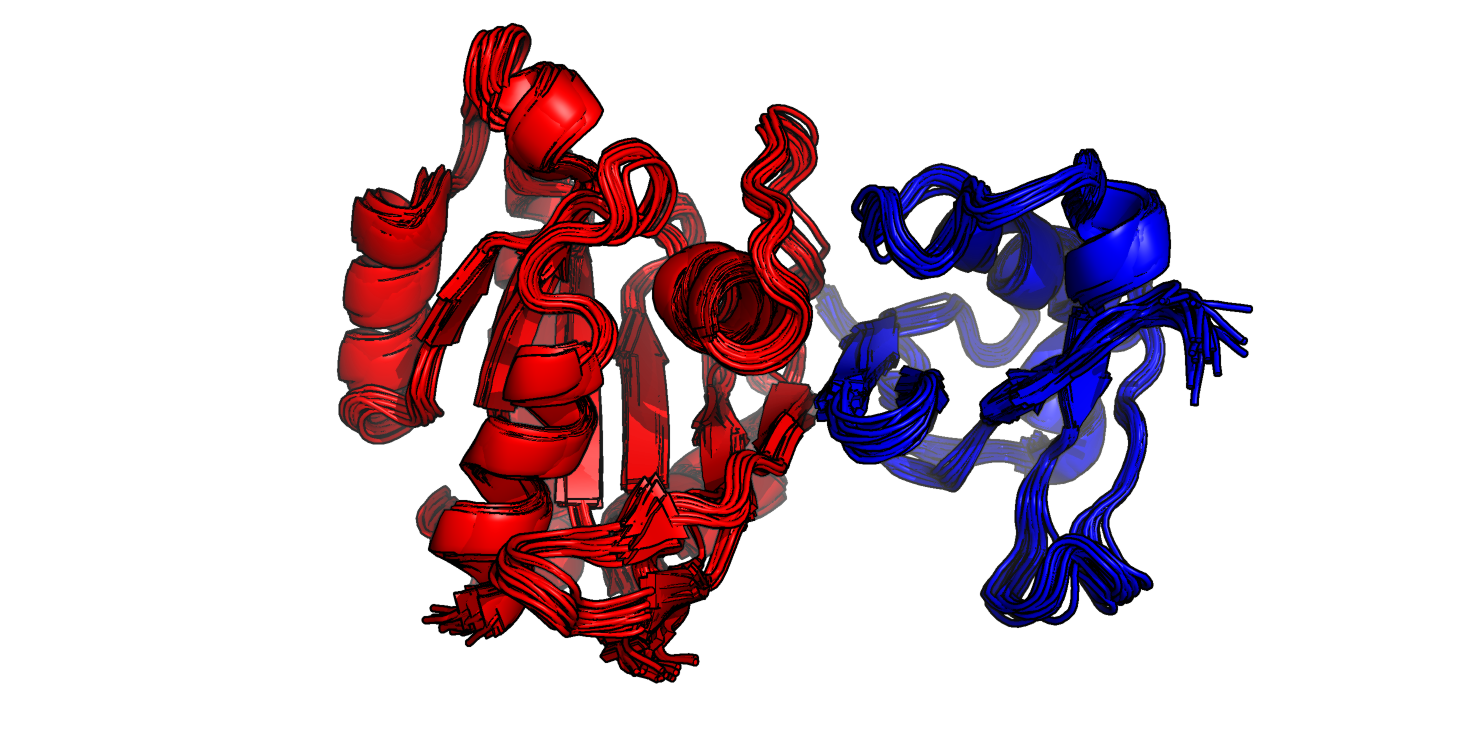
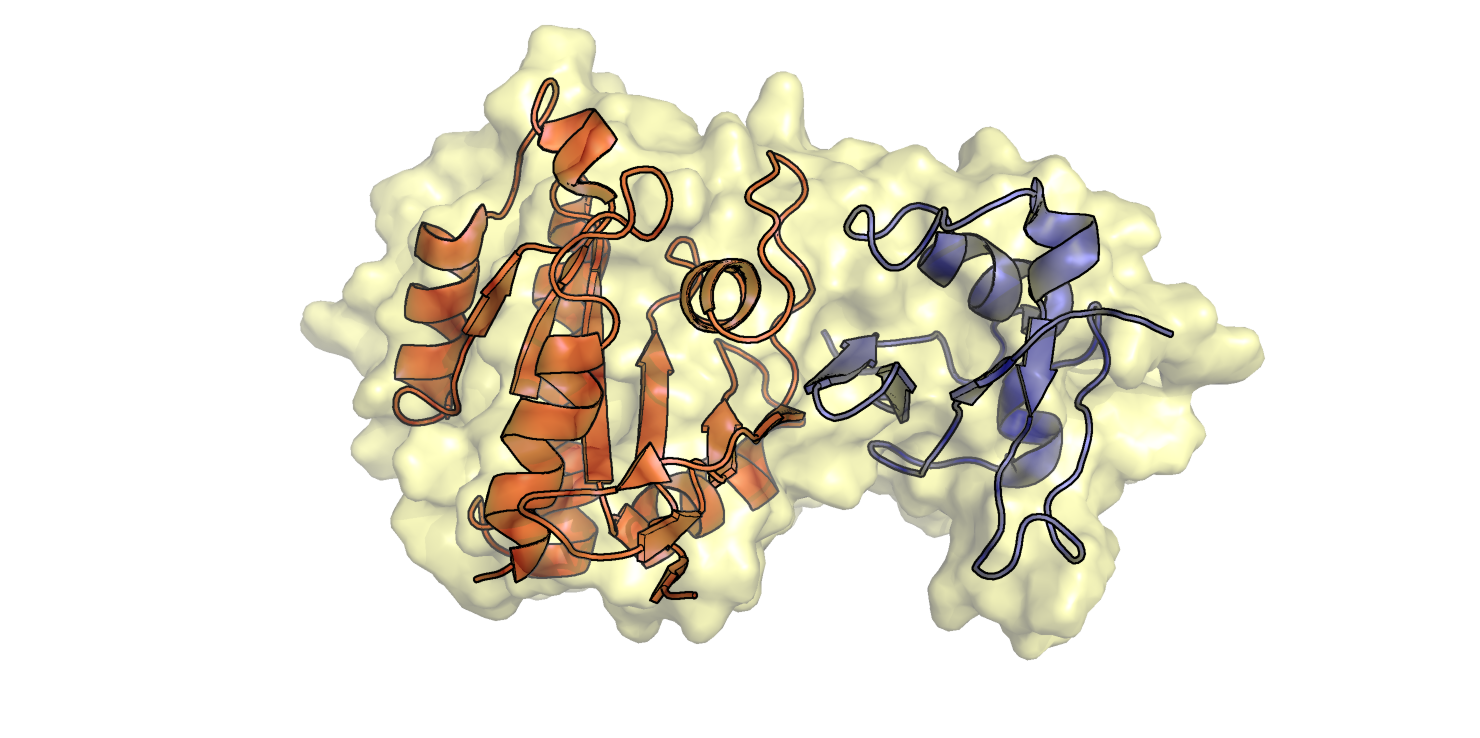
Для построения поверхностей была выбрана структура комплекса мембрансвязанной малой ГТФазы Rap1 с субдоменом F0 талина - белка, связывающего интегрины с актиновым цитоскелетом в фокальных контактах. Структура (6BA6) была разрешена с помощью ЯМР (файл содержит 20 моделей). 3D-структура комплекса, а также молекулярная поверхность комплекса изображены на Рис. 1.
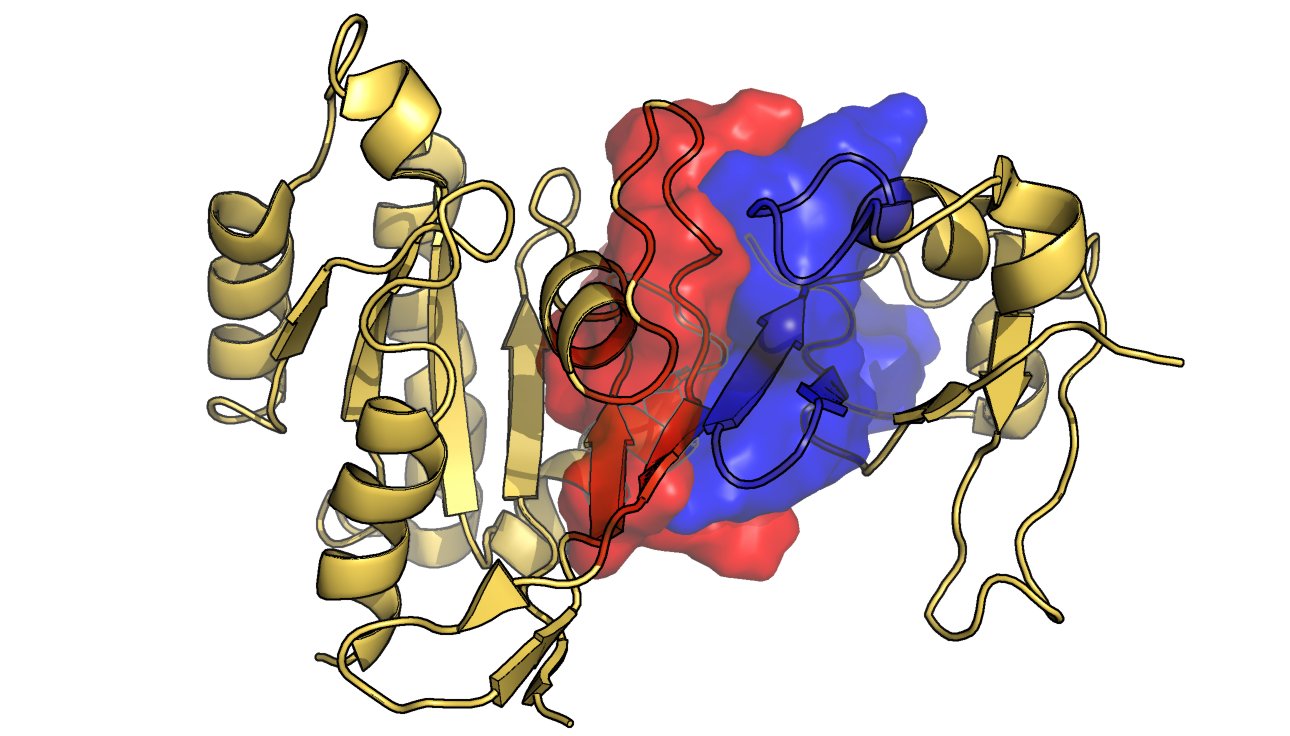
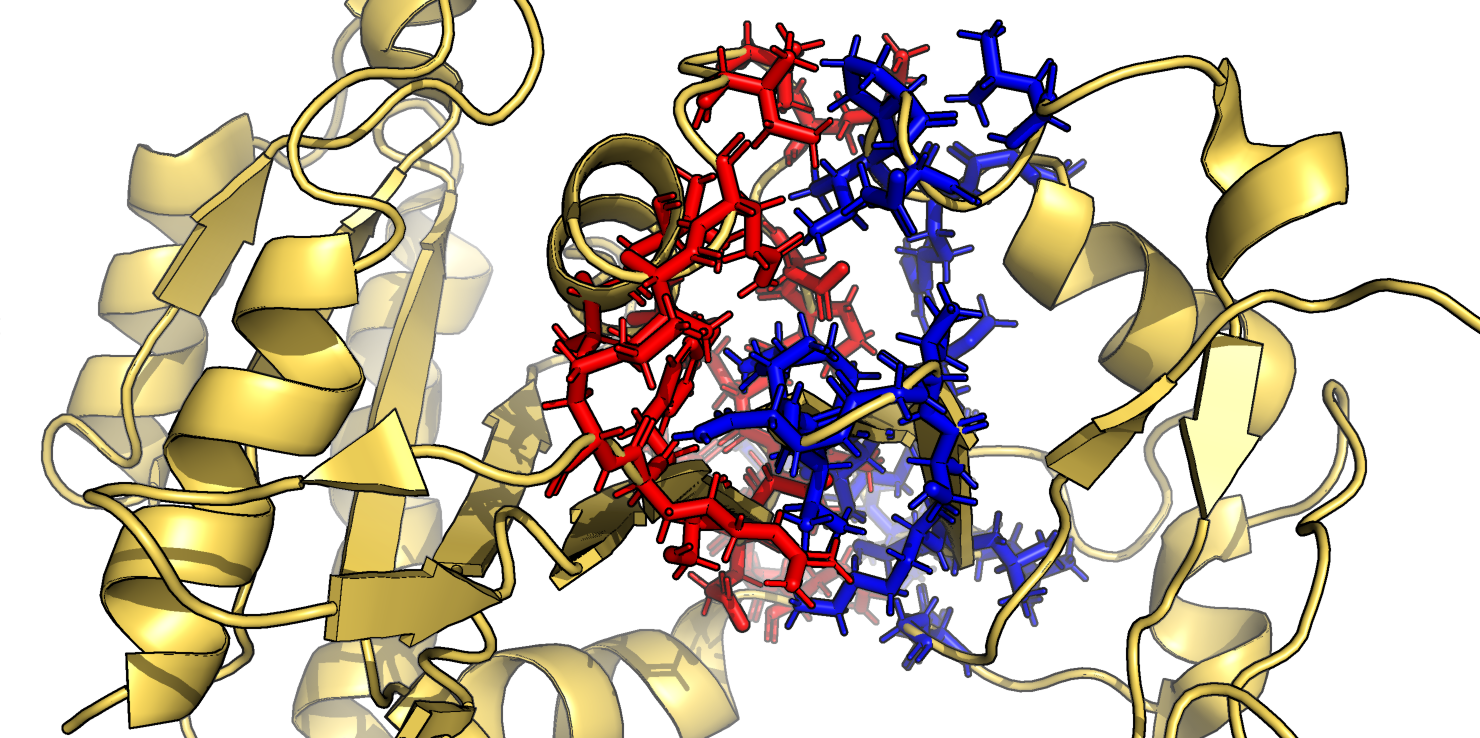
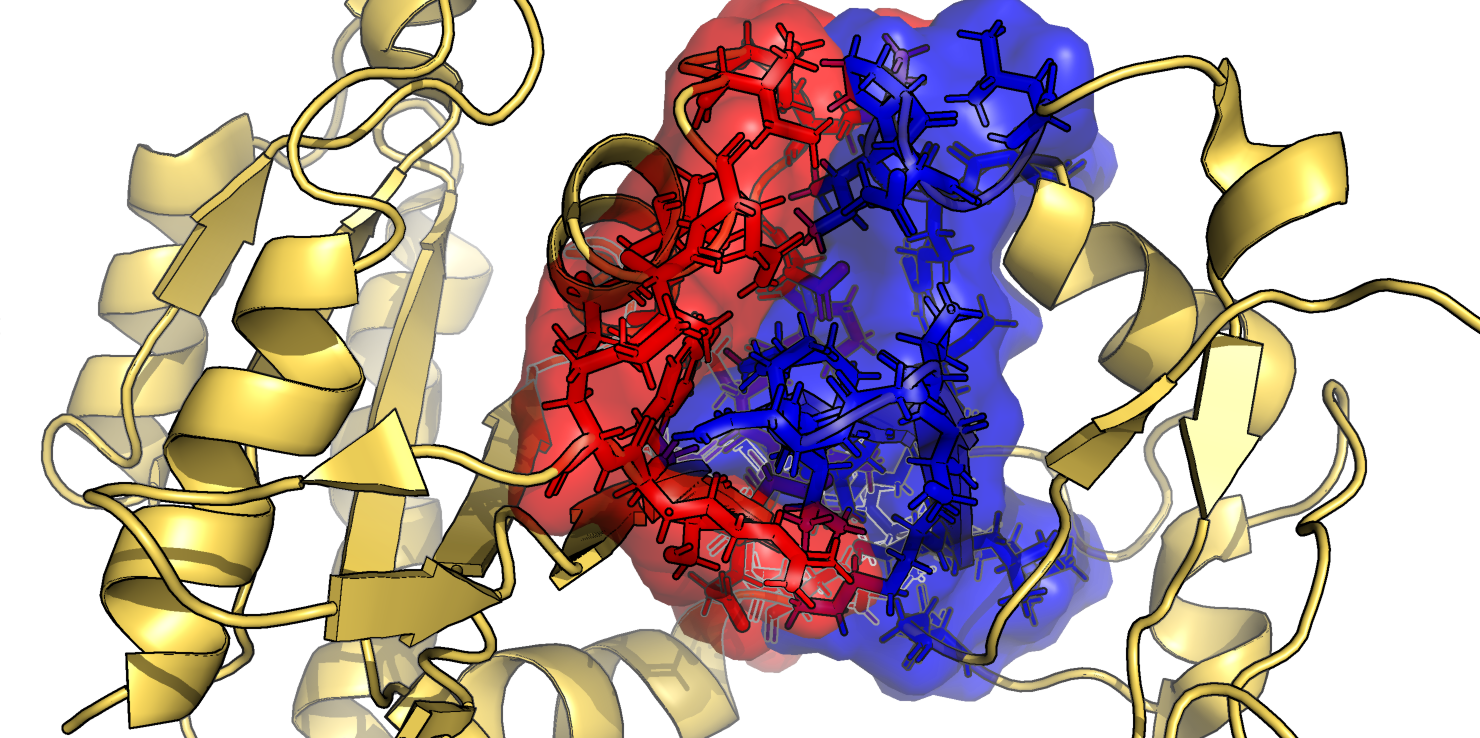
Далее для всех моделей были посчитаны молекулярная поверхность и поверхность, доступная для растворителя (SASA). Это было сделано с помощью команды get_area в PyMol при set dot_solvent, off и set dot_solvent, on для молекулярной повехности и SASA, соответственно. Построенные по результатам графики приведены на Рис. 2. Заметно, что два типа расчитанных поверхностей отличаются - поверхность SASA по площади более чем в 2 раза меньше молекулярной. Очень грубо можно сказать, что в целом при большей молекулярной поверхности SASA также больше. Однако зависимость не так проста и очевидна. Например, для модели 7 приведена самая высокая поверхность SASA, однако площадь молекулярной поверхности для нее средняя. При этом нет принципиальных конформационных различий между всеми моделями. Площадь SASA равна 12528 ± 112 Å2, молекулярной поверхности - 27342 ± 90 Å2 (средние и стандартные отклонения), то есть значения варьируют в пределах 1% (или меньше) от среднего. Таким образом, вероятнее всего, изменения поверхностей объясняются случайными флуктуациями отдельных фрагментов комплекса в растворе - в частности, движением поверхностных петель. Затем была рассмотрена поверхность контакта между Rap1 и талином на примере модели 14 (Рис. 3). Видно, что контакт между двумя белками очень тесный, выемки в поверхности одного белка очень хорошо соответствуют выступающим частям другого и наоборот.
| |||
| © Alexandra Boyko, 2014. Faculty of Bioengineering and Bioinformatics, MSU. | |||