Yersinia Pestis
Таксономия:
Домен: Бактерии
Тип: Протеобактерии
Класс: Гамма-протеобактерии
Порядок: Enterobacteriales
Семейство: Энтеробактерии
Род: Иерсиния (Yersinia)
Вид: Чумная палочка
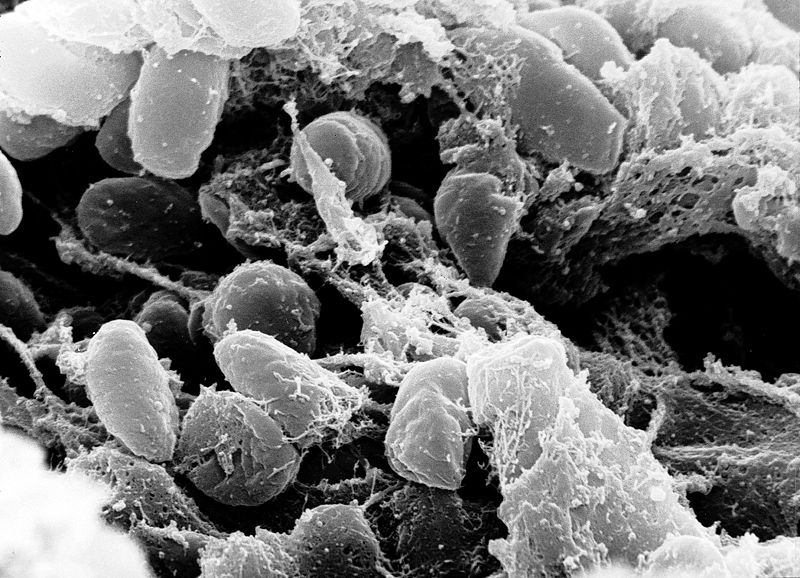
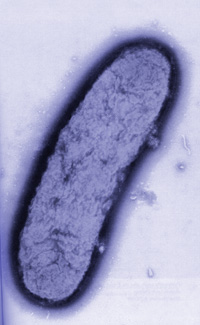
Чумная палочка (лат. Yersinia pestis) — грамотрицательная бактерия из семейства энтеробактерий.
Инфекционный агент бубонной чумы, также может вызывать пневмонию (легочную форму чумы) и
септическую чуму. Все три формы ответственны за высокий уровень смертности в эпидемиях, имевших
место в истории человечества, например таких как Великая чума и «Чёрная смерть», на счету
последней из которых — смерть трети населения Европы за промежуток с 1347 по 1353 годы.
Доступны полные генетические последовательности для различных подвидов бактерии: штамма KIM
(из биовара Medievalis), штамма CO92 (из биовара Orientalis, полученного из клинического
изолятора в США), штамма Antiqua, Nepal516, Pestoides F. Хромосомы штамма KIM состоят из 4 600 755
пар оснований, в штамме CO92 — 4 653 728 пар оснований. Как и родственные Y. pseudotuberculosis
и Y. enterocolitica, бактерия Y. pestis содержит плазмиды pCD1. Вдобавок, она также содержит плазмиды
pPCP1 и pMT1, которых нет у других видов рода Yersinia. Перечисленные плазмиды и остров патогенности,
названный HPI, кодируют белки, которые и являются причиной патогенности бактерии. Помимо всего прочего
эти вирулентные факторы требуются для бактериальной адгезии и инъекции белков в клетку «хозяина»,
вторжения бактерии в клетку-хозяина, захвата и связывания железа, добытого из эритроцитов. Полагают,
что бактерия Y. pestis произошла от Y. pseudotuberculosis, отличие только в присутствии специфичных
вирулентных плазмид.
Традиционным средством первого этапа лечения от Y. pestis были стрептомицин, хлорамфеникол
или тетрациклин. Также есть свидетельства положительного результата от использования
доксициклина или гентамицина. Надо заметить, что выделены штаммы, устойчивые к одному или
двум перечисленным выше агентам и лечение по возможности должно исходить из их восприимчивости
к антибиотикам. Для некоторых пациентов одного лишь лечения антибиотиками недостаточно, и может
потребоваться поддержка кровоснабжения, дыхательная или почечная поддержка.
En:
Yersinia pestis is a Gram-negative rod-shaped bacterium belonging to the family Enterobacteriaceae.
It is a facultative anaerobe that can infect humansand other animals.Human Y. pestis infection takes
three main forms: pneumonic, septicemic, and the notorious
bubonic plagues. All three forms are widely believed to have been responsible for a number of
high-mortality epidemics throughout human history, including the Plague of Justinian in 542
and the Black Death that accounted for the death of at least one-third of the European
population between 1347 and 1353.
The complete genomic sequence is available for two of the three sub-species of Y. pestis:
strain KIM (of biovar Medievalis), and strain CO92 (of biovar Orientalis, obtained from a
clinical isolate in the United States). As of 2006, the genomic sequence of a strain of biovar
Antiqua has been recently completed. Similar to the other pathogenic strains, there are
signs of loss of function mutations. The chromosome of strain KIM is 4,600,755 base pairs long;
the chromosome of strain CO92 is 4,653,728 base pairs long. Like its cousins Y. pseudotuberculosis
and Y. enterocolitica, Y. pestis is host to the plasmid pCD1. In addition, it also hosts two other
plasmids, pPCP1 (also called pPla or pPst) and pMT1 (also called pFra) which are not carried by
the other Yersinia species. pFra codes for a phospholipase D that is important for the ability of
Y. pestis to be transmitted by fleas. pPla codes for a protease, Pla, that activates plasminogen
in human hosts and is a very important virulence factor for pneumonic plague. Together, these
plasmids, and a pathogenicity island called HPI, encode several proteins which cause the
pathogenesis, for which Y. pestis is famous. Among other things, these virulence factors are
required for bacterial adhesion and injection of proteins into the host cell, invasion of bacteria
in the host cell (via a Type III Secretion System), and acquisition and binding of iron that is
harvested from red blood cells (via siderophores). Y. pestis is thought to be descendant from
Y. pseudotuberculosis, differing only in the presence of specific virulence plasmids.
The traditional first line treatment for Y. pestis has been streptomycin, chloramphenicol,
tetracycline, and fluoroquinolones. There is also good evidence to support the use of doxycycline
or gentamicin. Resistant strains have been isolated; treatment should be guided by antibiotic
sensitivities where available. Antibiotic treatment alone is insufficient for some patients,
who may also require circulatory, ventilator, or renal support.
(Материал с
http://ru.wikipedia.org/wiki/Yersinia_pestis)
Yersinia pestis, the Gram-negative coccobacillus belonging to the Enterobacteriaceae is the causative
agent of plague and is arguably the deadliest pathogen in history. At least 200 million deaths have
been attributed to this disease in modern times.
Yersinia pestis was named after Andre Yersin the French bacteriologist sent by Institute Pasteur to
the Far East (Hong Kong) to study plague where he first isolated plague bacillus in 1894.
Yersinia pestis is primarily a rodent pathogen, with humans being an accidental host when bitten by
an infected rat flea. The flea draws viable Y. pestis organisms into its intestinal tract. These organisms
multiply in the flea and block the flea's proventriculus (digestive chamber). Some Y. pestis in the flea
are then regurgitated when the flea gets its next blood meal thus transferring the infection to a new host.
Within hours of the initial flea bite, the infection spills out into the bloodstream, leading to involvement
of the liver, spleen, and lungs. The patient develops a severe bacterial pneumonia, exhaling large numbers
of viable organisms into the air during coughing fits. 50 to 60 percent of untreated patients will die if
untreated. As the epidemic of bubonic plague develops (especially under conditions of severe overcrowding,
malnutrition, and heavy flea infestation), it eventually shifts into a predominately pneumonic form, which
is far more difficult to control and which has 100 percent mortality.
The sequencing has revealed Y. pestis to be a highly dynamic and adaptable pathogen that has undergone rapid
genetic changes. It appears to have evolved in a remarkably short time from a relatively harmless stomach
bug to a blood-borne pathogen. Over time, Y. pestis acquired genes from other bacteria and viruses that
allowed it to live in the blood instead of the intestine, altogether, the researchers identified 21 regions,
or adaptation islands, that were probably acquired from other organisms.
Conversely, gene acquisition has been balanced by gene loss. 149 deactivated genes,
or pseudogenes, were discovered, that once enabled Y. pestis to thrive in the human
gut, but are no longer needed in the new environment. These include genes associated with adhesion,
mobility and colonization of the gut.
RUS:
Yersinia pestis, грамотрицательная коккобацилла из семейства Энтеробактерий, - возбудитель чумы и, возможно,
смертельнейший патоген в истории. По крайней мере 200 млн. смертей приписано этому заболеванию к настоящему
времени.
Yersinia pestis была названа в честь Андрэ Ерсина, французского бактериолога из Института Пастера на
Дальнем Востоке (Гонконг), где он впервые открыл чумную палочку в 1894 году.
Yersinia pestis - это преимущественно разъедающий патоген, человек стал ее случайным хозяином, когда
был укушен инфицированной крысиной блохой. Блоха несла жизнеспособных организмов Yersinia pestis в кишечном
тракте.Эти организмы размножились в блохе и закупорили ее провентрикулум (многокамерный пищеварительный канал).
Некоторые Yersinia pestis затем переносятся от блохи к новому носителю инфекции, когда у нее был следующий
кровавый обед.В течение часа после укуса блохи инфекция разносится по кровотоку, попадая в печень, селезенку и
легкие. У пациента развивается острая бактериальная пневмания, выдыхая огромное количество жизнеспособных
организмов во время кашля. От 5о до 60 % пациентов умирает, если не лечатся. Поскольку эпидемия бубонной чумы
развивается (особенно в условиях перенаселенности, недоедания и сильной инвазии блохами), это в конечном
счете переходит в преимущественную пневманическую форму, которую намного сложнее контролировать и которая
имеет стопроцентную смертность.
Последствия показали, что Yersinia pestis - чрезвычайно динамичный и приспосабливаемый патоген,
подверженный быстрым генетическим изменениям. С течением времени Yersinia pestis приобрелагены от других бактерий и вирусов,
которые позволили ей жить не в кишечнике, а в крови; всего исследователи идентифицировали 21 область, или
остров адаптации, которые мы, возможно, приобрели от других организмов.
Напротив, приобретение одних генов компенсируется утратой других. Было открыто 149 дезактивированных генов,
или псевдогенов, которые некогда позволяли Yersinia pestis процветать в человеческом кишечнике, но не
пригодившиеся больше в новом окружении. Эти включенные гены связаны с прилипанием, подвижностью и
колонизацией кишечника.
(информация с http://www.ebi.ac.uk/2can/genomes/bacteria/Yersinia_pestis.html )
запрос в БД PubMed: yersinia pestis complete genome 2000:2010 [DP]
найдено: 30 статей
аннотация одной из статей: Sadovskaia NS, Mironov AA, Gel'fand MS.
Abstract
One of the main trends in the prokaryote genomics is the comparative analysis of metabolic pathways.
This method can be used for the analysis of experimentally studied systems of co-regulated genes,
as well as genes with unknown regulatory signals. In this study we apply the comparative analysis
of regulatory signals to the genes of the enzymes for fatty acid metabolism from Escherichia coli,
Haemophilus influenzae, Vibrio cholerae, Yersinia pestis. Transcription of these genes is regulated
by the FadR protein. We describe the FadR regulation of the long-chain fatty acid oxidation and partially
that of the fatty acid biosynthesis. We also demonstrate that the gene yafH encoding acyl-CoA dehydrogenase
is identical to the gene fadE, previously identified by genetic techniques.
EN:
Одна из главных черт генома прокариотического организма - это сравнительный анализ типов метаболизма.
Этот метод может быть использован для анализа экспериментальных данных о ко-регулируемых генах так же
хорошо, как для генов с неизвестными регуляторными функциями. В этом исследовании мы применяем
сравнительный анализ регуляторных сигналов к генам ферментов метаболизма жирных кислот у Escherichia coli,
Haemophilus influenzae, Vibrio cholerae, Yersinia pestis. Транскрипция этих генов регулируется FadR-белком.
Мы описываем FadR-регуляцию окисления длинных цепочек жирных кислот и частично то, что они синтезируют.
Мы также показываем, что ген yafH, кодирующий ацил-CoA дегидрогеназу идентичен гену FadR, идентифицированному
ранее с помощью генетической техники.
(http://www.ncbi.nlm.nih.gov/pubmed/11771124)
PMID: 11771124 [PubMed - indexed for MEDLINE]
задание №4(5)
Component info:
| Component name | Protein count | Type | Length (bp) | Av. CDS Length | GC content | CDS coverage | Gene count |
| Chromosome | 3837 | 4504254 | 902.147 | 47.6% | 77% | 3837 | |
| Plasmid pMT-pPCP | 120 | 114570 | 726.55 | 50% | 76% | 120 | |
| Plasmid new_pCD | 88 | 68190 | 575.489 | 44.6% | 74% | 88 | |
| 3821 |
http://www.eiu.org/experiments/dispersion/pathogens.html
http://en.wikipedia.org/wiki/File:Yersinia_pestis.jpg
E-mail: yan1303@yandex.ru
Официальный сайт ФББ
Ваши предложения :)))
Проекты
Главная страница