Практикум 2. Альтернативные положения, B-фактор, кристалл
1. Альтернативные положения
Альтернативные конформации или альт-локи возникают, если какая-то химическая группа в ячейках кристалла располагалась по-разному, и такое состояние встречалось достаточно часто. В белке 6AF7 аминокислота Lys-63 встречается в двух альтернативных положениях (рис.1).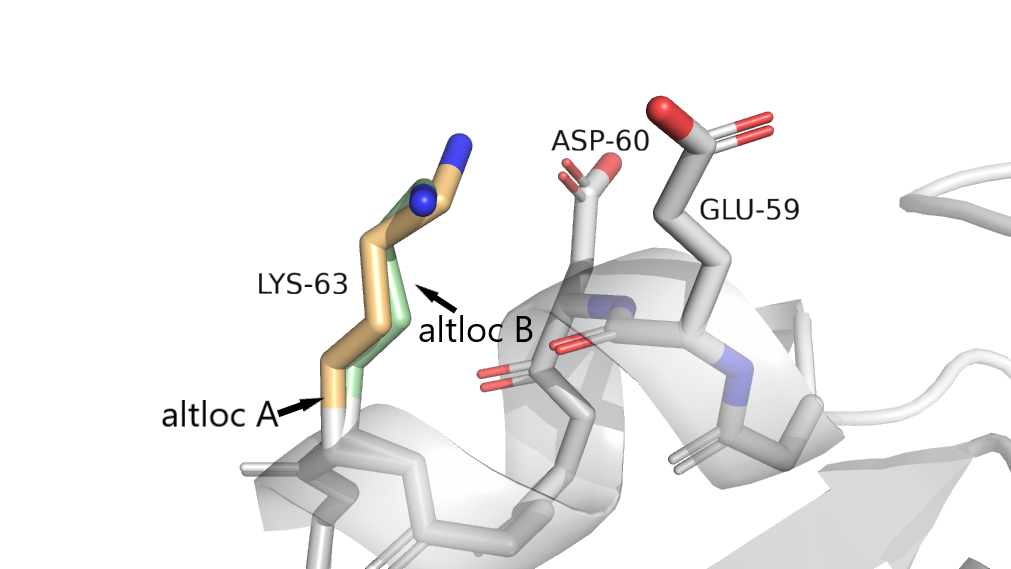
Рис.1 Общий вид. Оранжевый - альт-лок А, зеленый- альт-лок В.
Вариант А показан оранжевым цветом. Для этого альт-лока возможно стабилизирующее взаимодействие в виде водородной связи с кислородом ASP-60. Также между лизином и аспартатом есть солевой мостик (рис.2).
Вариант В показан зеленым цветом. Расстояния от азота лизина до двух отрицательных аминокислот - ASP-60 и GLU-59 слишком большие, чтобы можно было говорить о солевых мостиках. Но населенность альт-локов - 0.50 по всем атомам радикала и по С-альфа атому остова.
ATOM 468 C LYS A 63 13.093 -15.837 -2.435 1.00 31.26 C
ATOM 469 O LYS A 63 12.623 -15.930 -1.288 1.00 35.12 O
ATOM 470 CB ALYS A 63 13.020 -13.344 -2.888 0.50 37.26 C
ATOM 471 CB BLYS A 63 12.768 -13.605 -3.373 0.50 33.20 C
ATOM 472 CG ALYS A 63 13.695 -12.126 -3.524 0.50 39.37 C
ATOM 473 CG BLYS A 63 13.275 -12.374 -4.093 0.50 39.73 C
ATOM 474 CD ALYS A 63 12.636 -11.004 -3.713 0.50 44.42 C
ATOM 475 CD BLYS A 63 12.166 -11.300 -4.049 0.50 44.18 C
ATOM 476 CE ALYS A 63 13.010 -10.034 -4.848 0.50 50.31 C
ATOM 477 CE BLYS A 63 12.629 -10.005 -4.709 0.50 49.80 C
ATOM 478 NZ ALYS A 63 11.875 -9.532 -5.705 0.50 48.00 N
ATOM 479 NZ BLYS A 63 13.914 -9.489 -4.143 0.50 51.58 N
Значит, какой-то контакт, стабилизирующий это взаимодействие, есть.
И это предположительно водяной мостик - взаимодействие "белок-вода-белок" через водородные связи (рис.3).
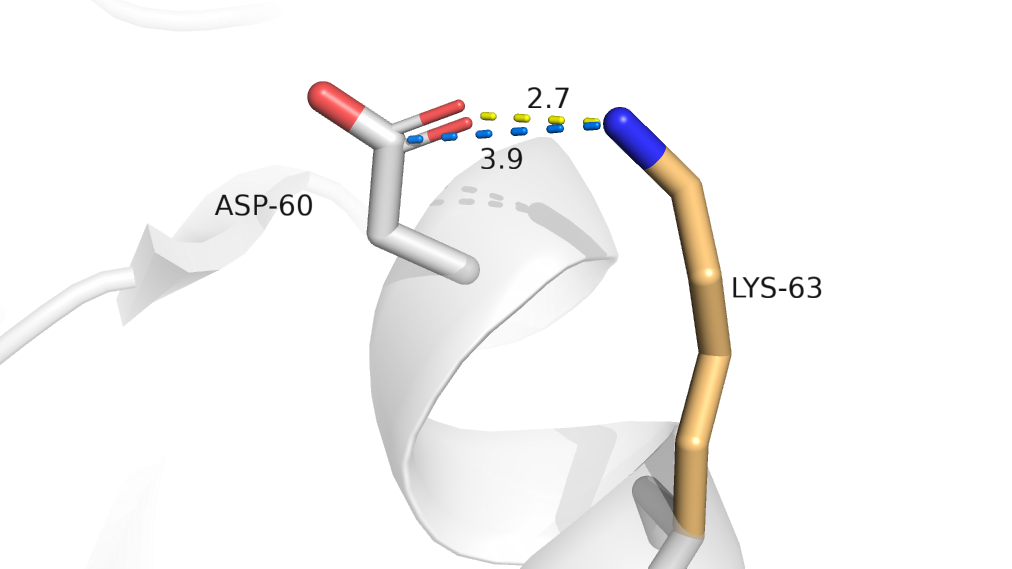 Рис.2 Контакты, стабилизирующие альт-лок А.
Рис.2 Контакты, стабилизирующие альт-лок А.
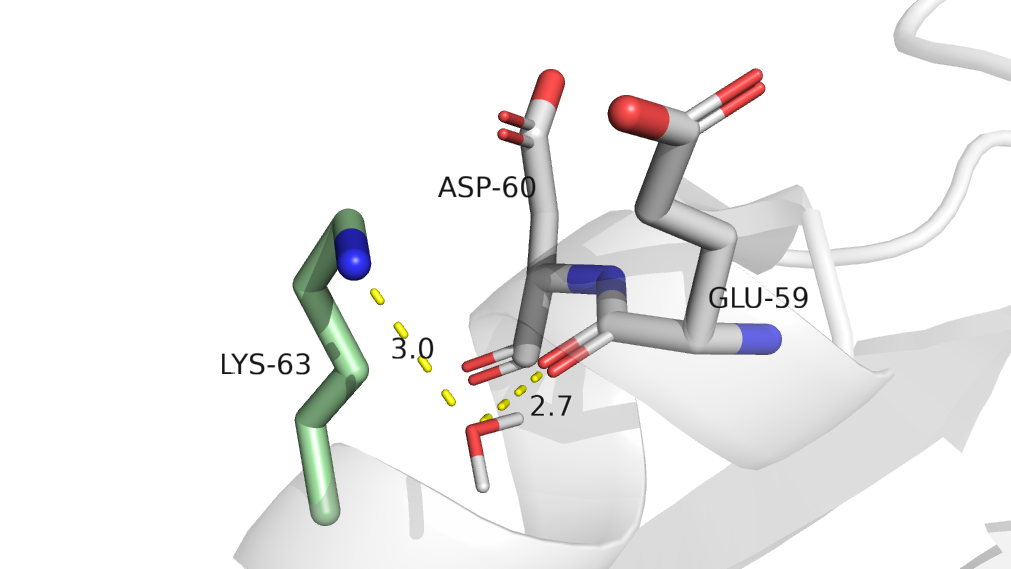 Рис. 3 Контакты, стабилизирующие альт-лок В.
Рис. 3 Контакты, стабилизирующие альт-лок В.
Какой из альт-локов стабильнее? Исходя из данных по населенности - конформации равновероятны.
Задание 2. B-фактор
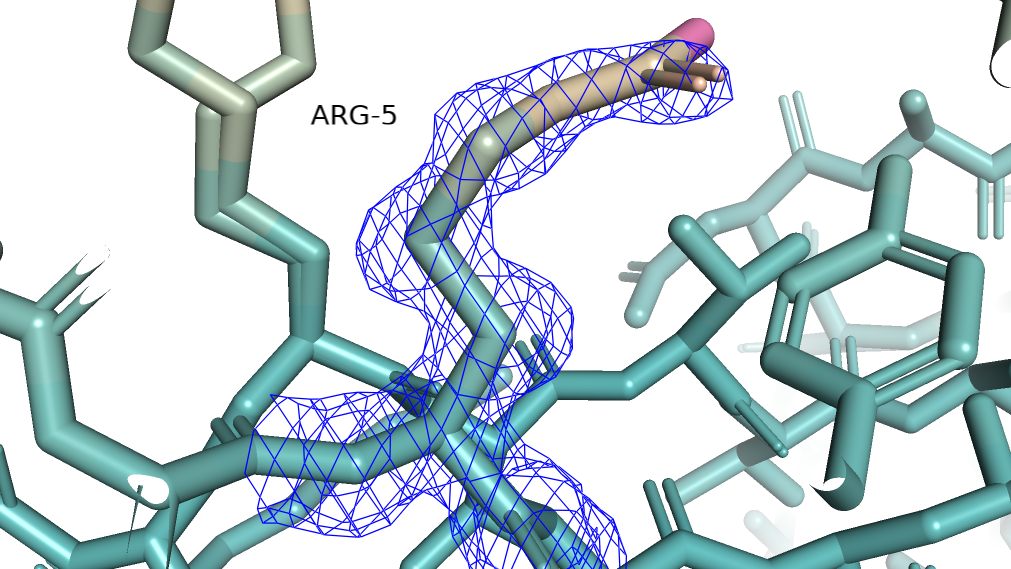
Была выбрана раскраска marine_wheat_magenta. На картинке ниже атомы с низким В-фактором покрашены в зеленый цвет, а атомы с высоким значением В-фактора покрашены в розовый (рис.4).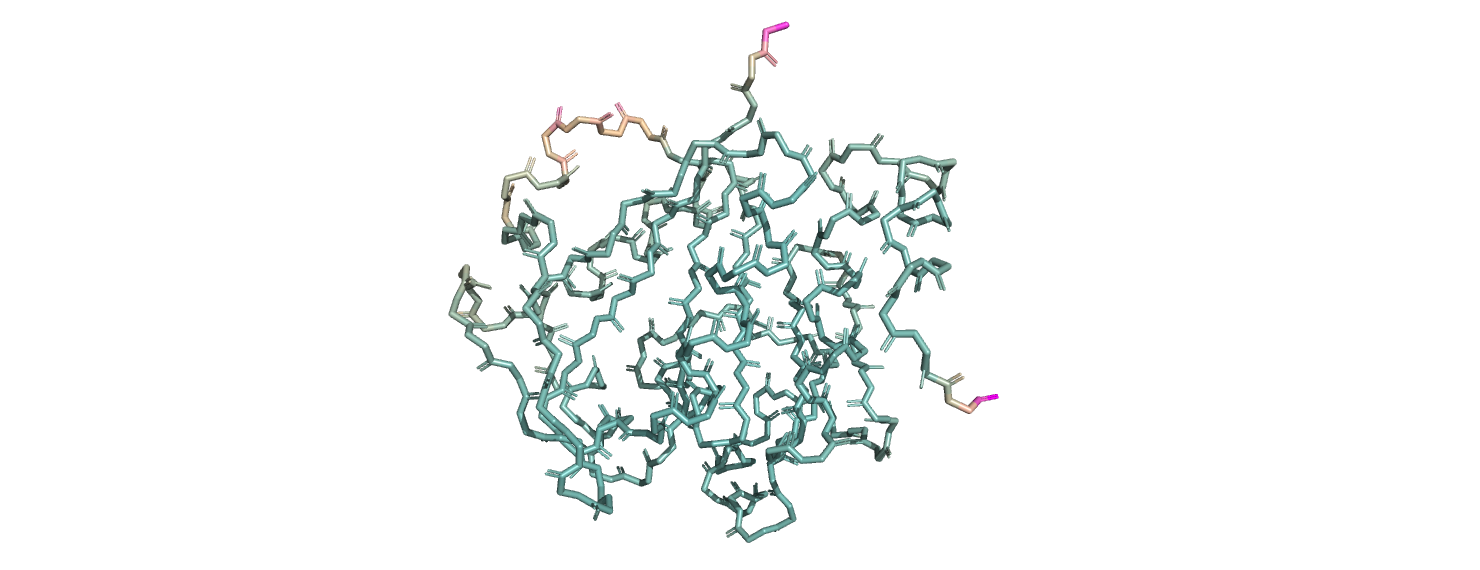 Рис.4 Раскраска по В-фактору.
Рис.4 Раскраска по В-фактору.
Сильнее всего розовеют части остова по краям от глобулы. Внутри глобулы преобладают зеленые оттенки. Скорее всего, значение B-фактора связано с подвижностью атома и размытием его электронной плотности.
После покраски по В-фактору всего белка с аминокислотными остатками, был выбран ARG-5 для дальнейшего
рассмотрения.
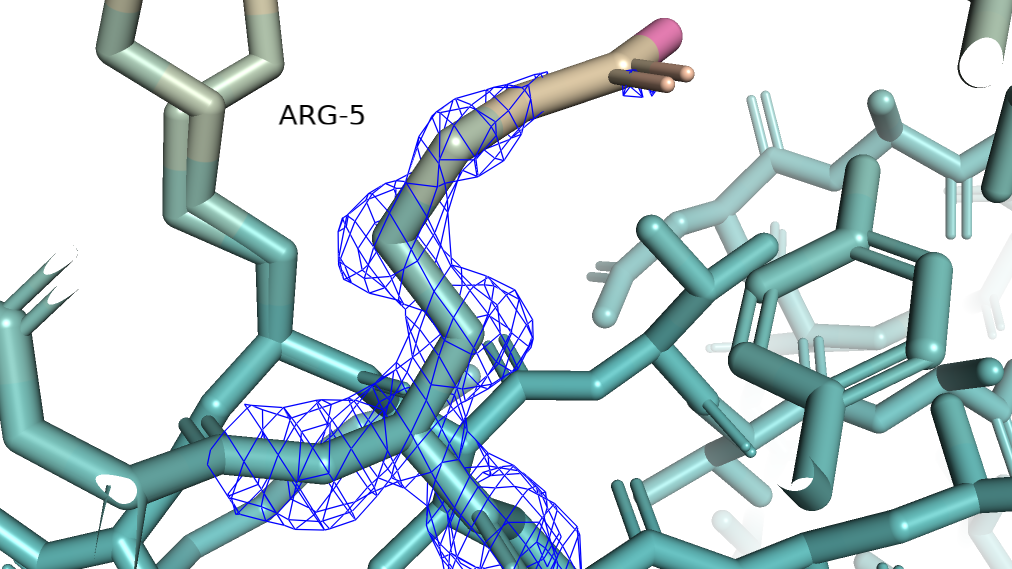
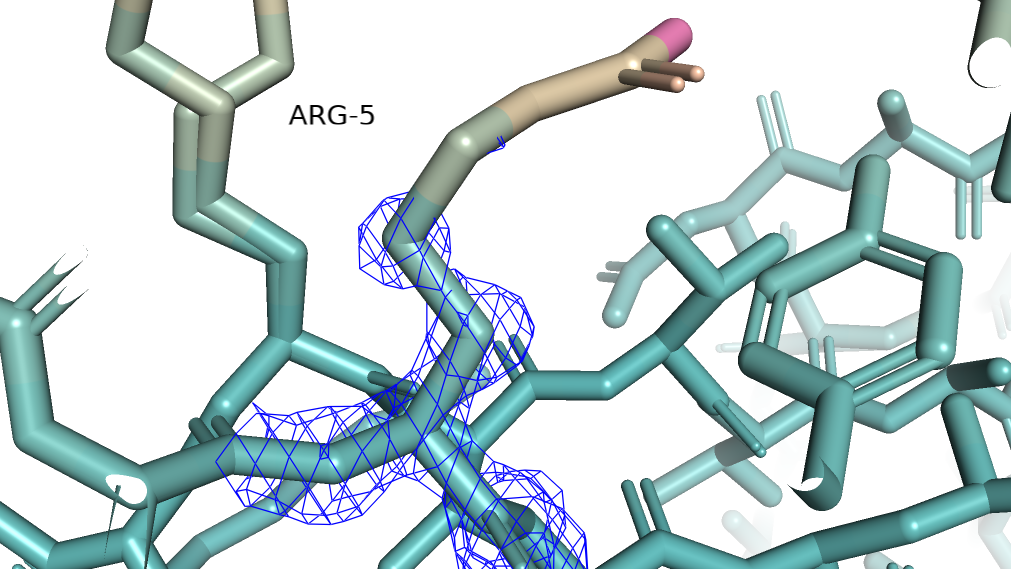
Посмотрим на его электронную плотность на разных уровнях подрезки. Carve = 1.5.
Электронная плотность уползает первой с самого розового азота. Затем оболочки лишается второй азот, он более бледный.Чем ближе атомы находятся к остову, тем более зеленого они цвета, тем дольше они остаются покрытыми электронной плотностью при увеличении уровня подрезки. Это объясняется тем, что атомы ближе к остову имеют меньше микросостояний и более четкое положение в пространстве. Ниже приведены значения B-фактора для атомов ARG-5. Для самого розового атома - NH2, значение В-фактора составляет 57,98, и электронная плотность на нем не наблюдается даже на уровне подрезки 1. Следовательно он обладает наибольшим числом разных состояний, электронная плотность для него размыта. И здесь наблюдается уменьшение B-фактора по мере приближения к остову.
Электронная плотность уползает первой с самого розового азота. Затем оболочки лишается второй азот, он более бледный.Чем ближе атомы находятся к остову, тем более зеленого они цвета, тем дольше они остаются покрытыми электронной плотностью при увеличении уровня подрезки. Это объясняется тем, что атомы ближе к остову имеют меньше микросостояний и более четкое положение в пространстве. Ниже приведены значения B-фактора для атомов ARG-5. Для самого розового атома - NH2, значение В-фактора составляет 57,98, и электронная плотность на нем не наблюдается даже на уровне подрезки 1. Следовательно он обладает наибольшим числом разных состояний, электронная плотность для него размыта. И здесь наблюдается уменьшение B-фактора по мере приближения к остову.
ATOM 27 N ARG A 5 13.955 -28.868 -4.745 1.00 12.09 N
ATOM 28 CA ARG A 5 13.878 -27.684 -5.558 1.00 12.43 C
ATOM 29 C ARG A 5 15.201 -27.435 -6.228 1.00 11.89 C
ATOM 30 O ARG A 5 16.279 -27.546 -5.605 1.00 13.04 O
ATOM 31 CB ARG A 5 13.508 -26.447 -4.715 1.00 16.24 C
ATOM 32 CG ARG A 5 12.160 -26.617 -3.976 1.00 18.93 C
ATOM 33 CD ARG A 5 11.998 -25.486 -3.019 1.00 27.95 C
ATOM 34 NE ARG A 5 11.612 -24.261 -3.702 1.00 37.38 N
ATOM 35 CZ ARG A 5 12.103 -23.044 -3.392 1.00 37.52 C
ATOM 36 NH1 ARG A 5 13.078 -22.894 -2.474 1.00 45.20 N
ATOM 37 NH2 ARG A 5 11.670 -21.975 -4.094 1.00 57.98 N
Таким образом, чем более подвижен атом, тем большее значение B-фактора он имеет, тем более он розовый.
Соседи. Кристалл
Далее было рассмотрено сколько соседей существует у белка, с которыми есть непосредственный контакт. Для начала я попробовала понять какая структура получается у кристалла. Получилась вот такая красота. (Рис.6-7)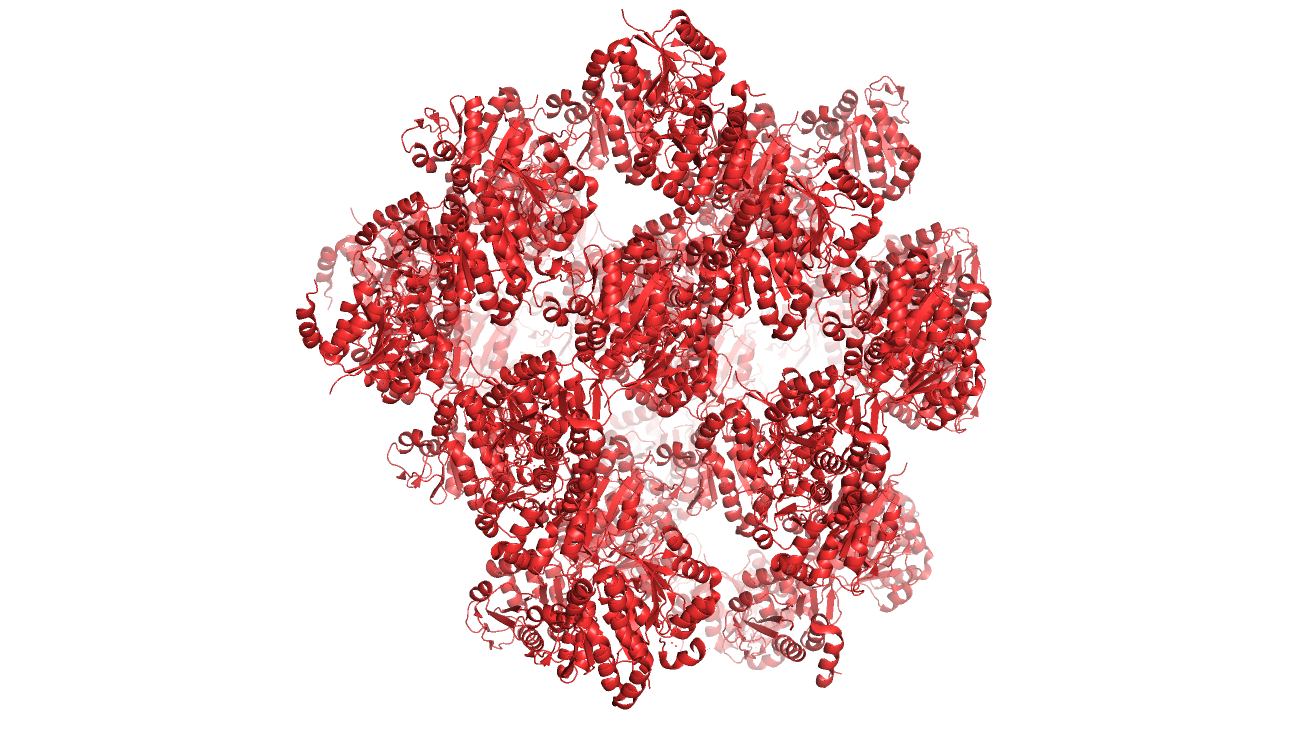 Рис.6 Общий вид кристалла сбоку.
Рис.6 Общий вид кристалла сбоку.
 Рис.7 Общий вид кристалла сверху.
Рис.7 Общий вид кристалла сверху.
Непосредственно контактирующих соседей было найдено 5 штук. Начальная молекула белка покрашена красным и находится в центре.
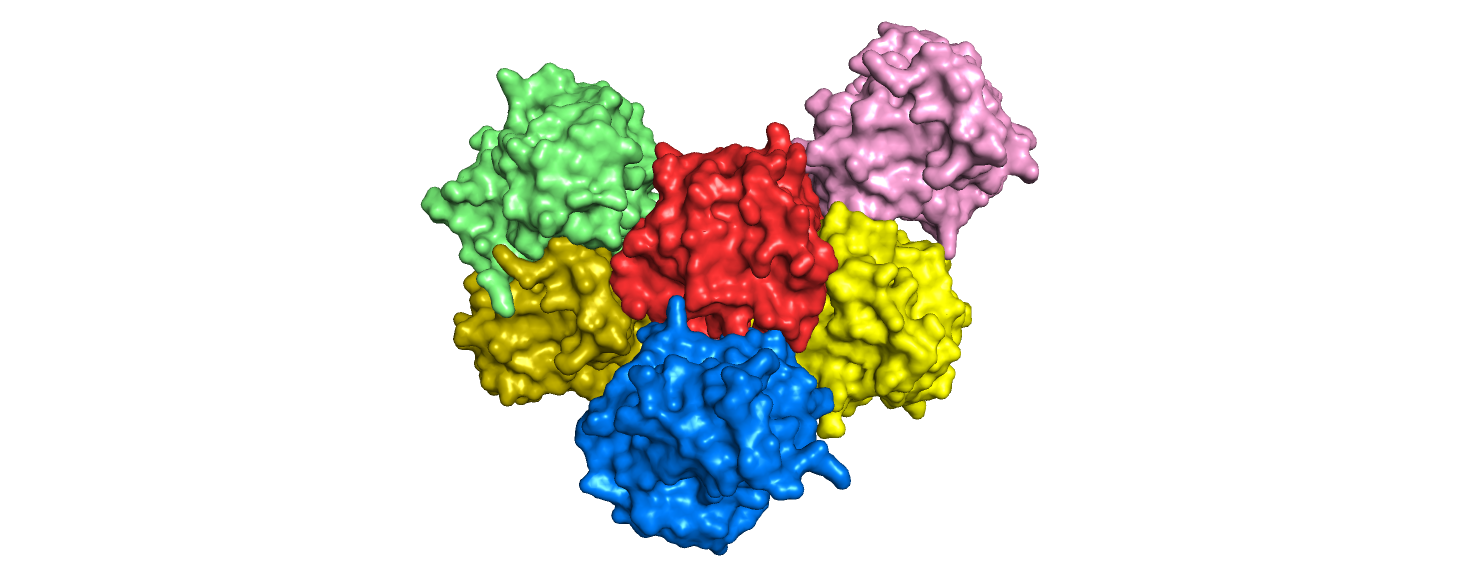 Рис.7 Соседи белка 6AF7.
Рис.7 Соседи белка 6AF7.
© Нестеренко Екатерина 2017-2020