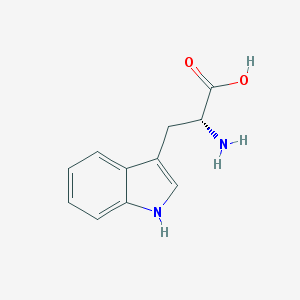
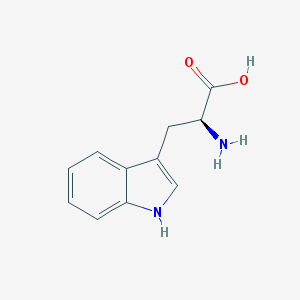
Структурные формулы D- (слева) и L-изомеров (справа) триптофана
Ароматическая неполярная α-аминокислота, входящая в состав многих белков. Содержащаяся в ее структуре индольная функциональная группа во многом определяет ее свойства. Эта кислота является предшественником нейромедиатора серотонина витамина В3. Триптофан кодируется единственным кодоном UGG. Кислота существует в виде двух оптических изомеров: D- и L-Триптофана и в виде рацемата (DL).[1]


Структурные формулы D- (слева) и L-изомеров (справа) триптофана
В синтезе белков человека участвует только L-Триптофан, однако сама кислота не синтезируется человеческим организмом - таким образом, L-Триптофан человек может получить только извне. Изомер входит в перечень 20 основных аминокислот, необходимых для нормального функционирования человеческого организма. L-Триптофан – преобладающая форма этой аминокислоты. Однако D-стереоизомер встречается в природных соединениях, таких как полипептид контрифан.По свойствам триптофан схож с фенилаланином и тирозином. Как и эти аминокислоты, триптофан содержит большую и устойчивую ароматическую группу в боковой цепи. Триптофан, фенилаланин и тирозин (вместе с изолейцином, лейцином и валином) гидрофобны и, как правило, ориентированы внутрь свернутой белковой молекулы.[1]
Номенклатура по IUPAC |
(2S)-2-амино-3-(1H-индол-3-yl)пропановая кислота |
||
Буквенные обозначения |
Trp, W |
||
Брутто-формула |
C11H12N2O2 |
||
Молекулярная масса |
204.22518 г/моль |
||
Температура плавления |
289°C |
||
Плотность |
1.34 г/см3 (тверд) |
||
pK |
pK1 (-COOH) |
pKa 2 |
pKa R |
2.4 |
9.4 |
- |
|
pI |
5.89 |
||
PubChem |
6305 |
||
Тип взаимодействия |
Характеристика |
Ковалентная связь |
Со всеми аминокислотами образует пептидную связь |
Водородная связь |
Взаимодействует с Gly и Glu |
Солевые мостики |
Нет (радикал ароматический) |
Гидрофобные ядра |
Кислота ароматическая, поэтому она может образовывать гидрофобные ядра.[3] |
© Кучеренко Варвара 2015