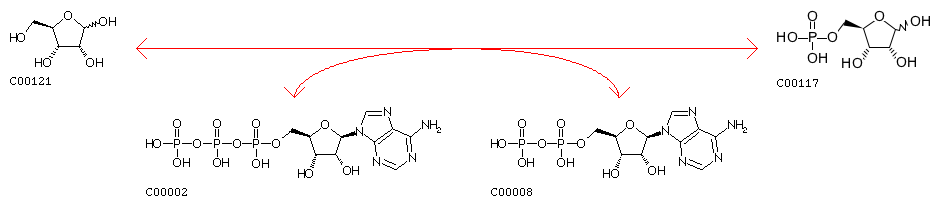
EC 2.7.1.15
EC 2.7.1 Phosphotransferases with an alcohol group as acceptor
EC 2.7 Transferring phosphorus-containing groups
EC 2 Transferases

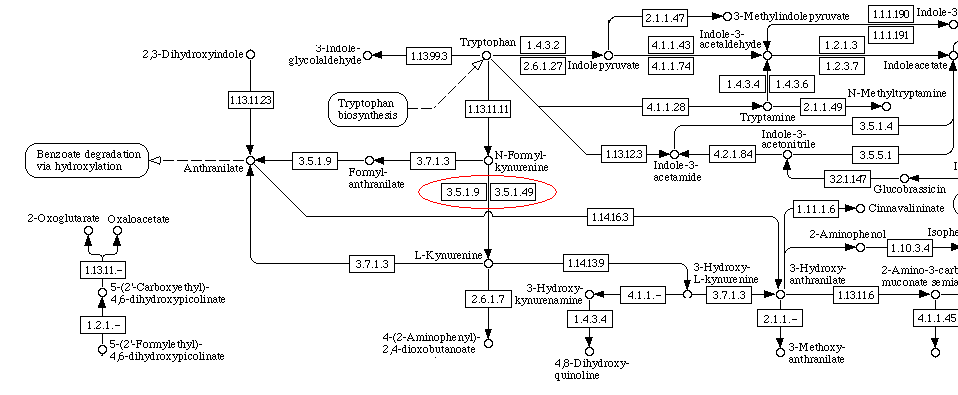
Сравнение выбранных ферментов
| EC-код | EC 3.5.1.9 | EC 3.5.1.49 |
| Название | arylformamidase (арилформамидаза); kynurenine formamidase; formylase; formylkynureninase; formylkynurenine formamidase; formamidase I; formamidase II |
formamidase (формамидаза) |
| Расшифровка кода | 3 гидроксилазы 3.5 Воздействуют на связи C-N, отличные от пептидных 3.5.1 В линейных амидах |
3 гидроксилазы 3.5 Воздействуют на связи C-N, отличные от пептидных 3.5.1 В линейных амидах |
| Катализируемая реакция | Н-формил-L-кинуренин + H2O = формиат + L-кинуренин | формамид + H2O = формиат + NH3 |
| Субстрат | Н-формил-L-кинуренин | формамид |
| Продукт | формиат | формиат |
| Комментарий | Также воздействует на другие ароматические формамилазы. | Также (но медленнее) воздействуют на ацетамид, пропанамид и бутанамид. Also acts, more slowly, on acetamide, propanamide and butanamide |
| Участие в метаболических путях | Tryptophan metabolism Glyoxylate and dicarboxylate metabolism |
Tryptophan metabolism Glyoxylate and dicarboxylate metabolism Nitrogen metabolism |
| Литература |
|
|
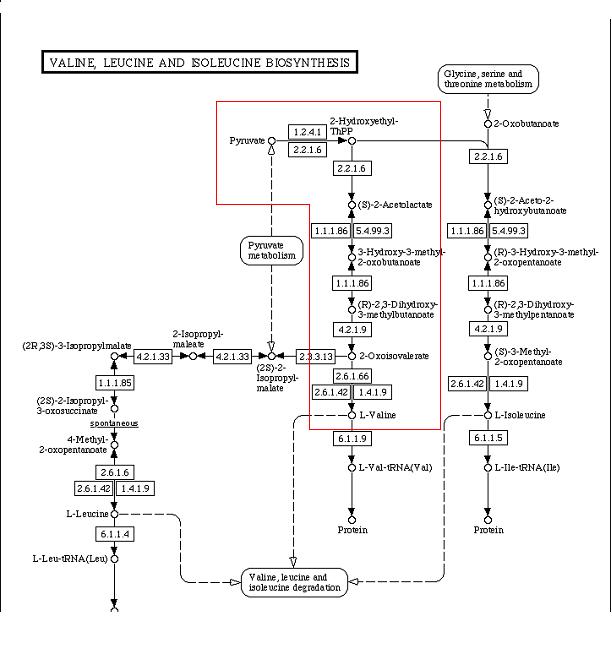
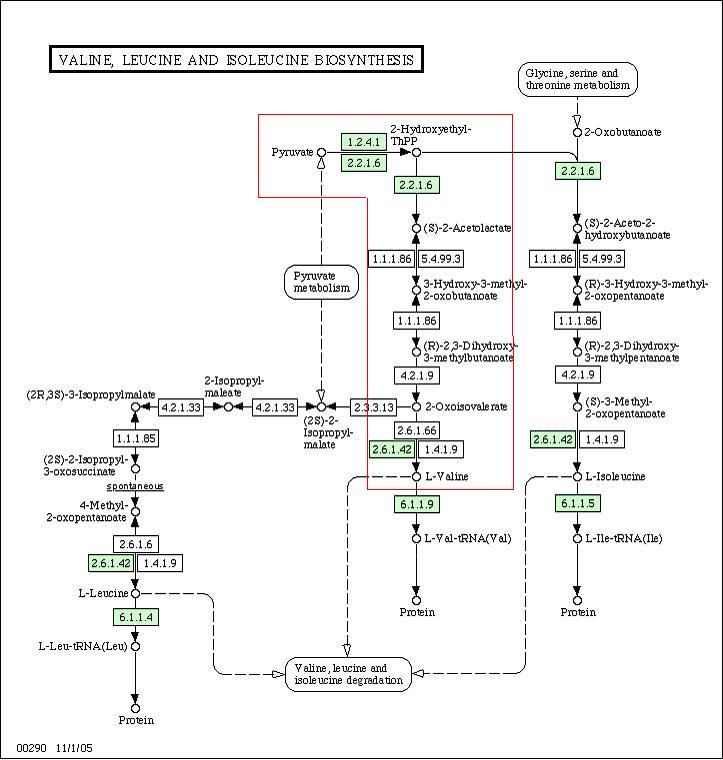
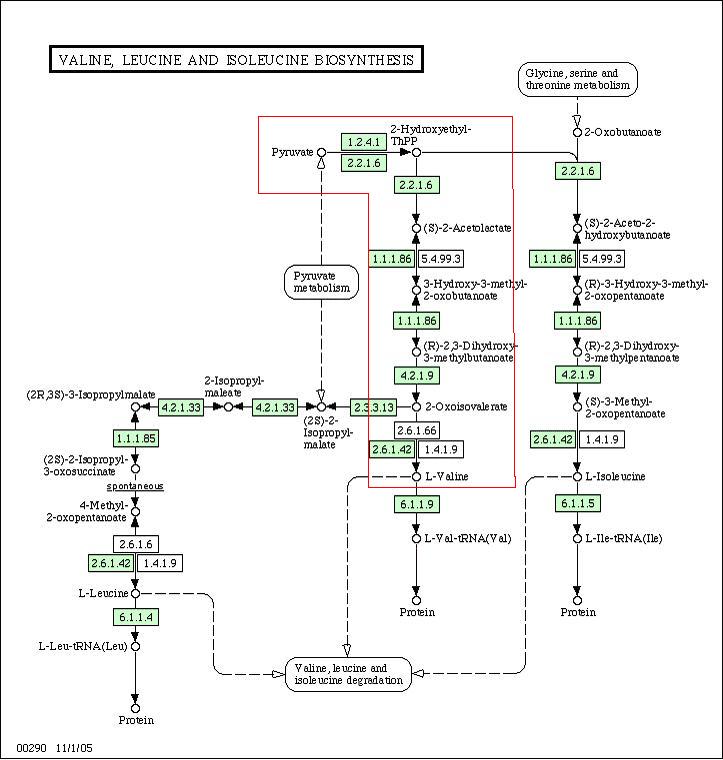
У Arabidopsis присутствуют все необходимые для биосинтеза Валина ферменты.