Электронная плотность
Задание 1. ЭП: хорошая и плохая расшифровки
В данном задании я рассматривал две различные структуры металло-бета-лактамазы Нью-Дели (PDB-ids 6lip & 5a5z). Это белок позволяющий бактериям расщеплять беталактамные антибиотики. На первый взгляд, существенных различий в структурах не видно (кроме того, что 5a5z содержит информацию о двух цепях, а 6lip об одной). Для более подробного изучения брался фрагмент с аминокислотами GIDGTDIA (197-204). Для изображения электронной плотности использовался инструмент isomesh с параметрами carve=1.5 и уровнем подрезки 2.
.
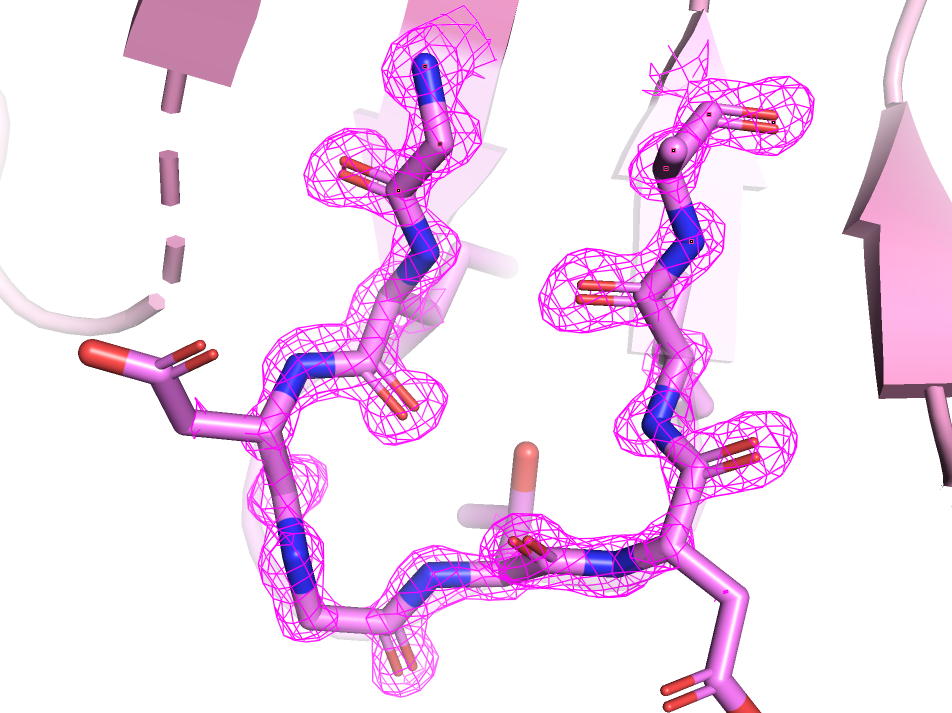
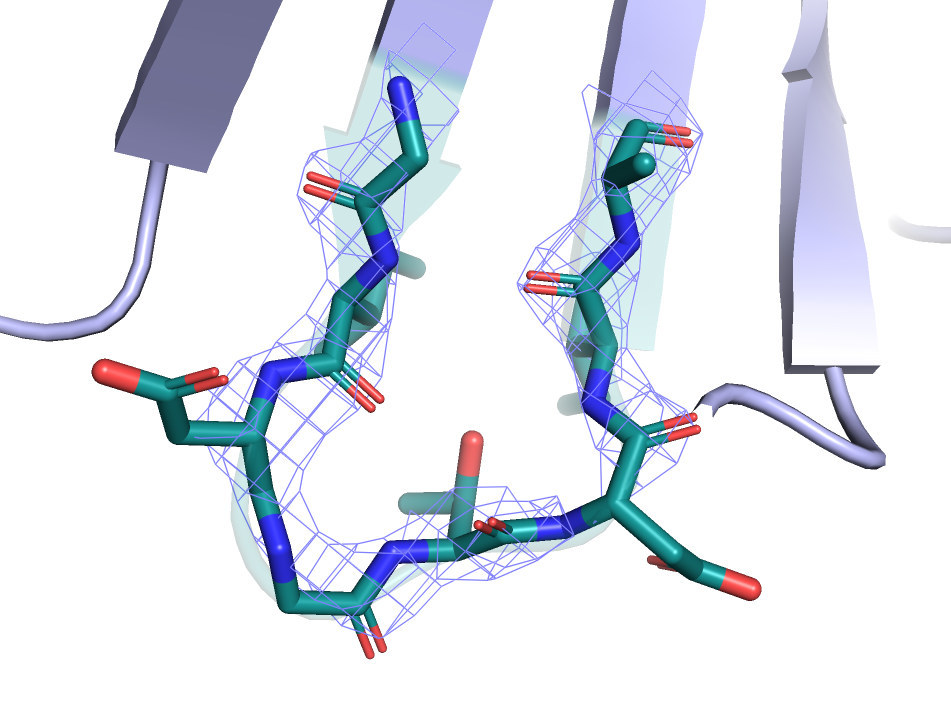
Фрагмент структур 6lip и 5a5z
.
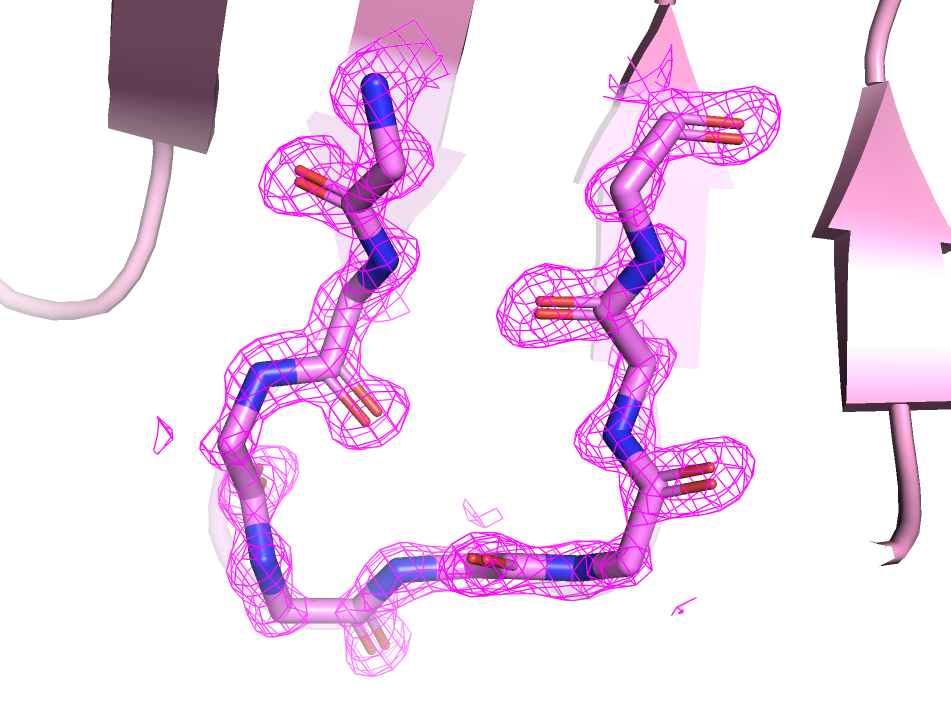
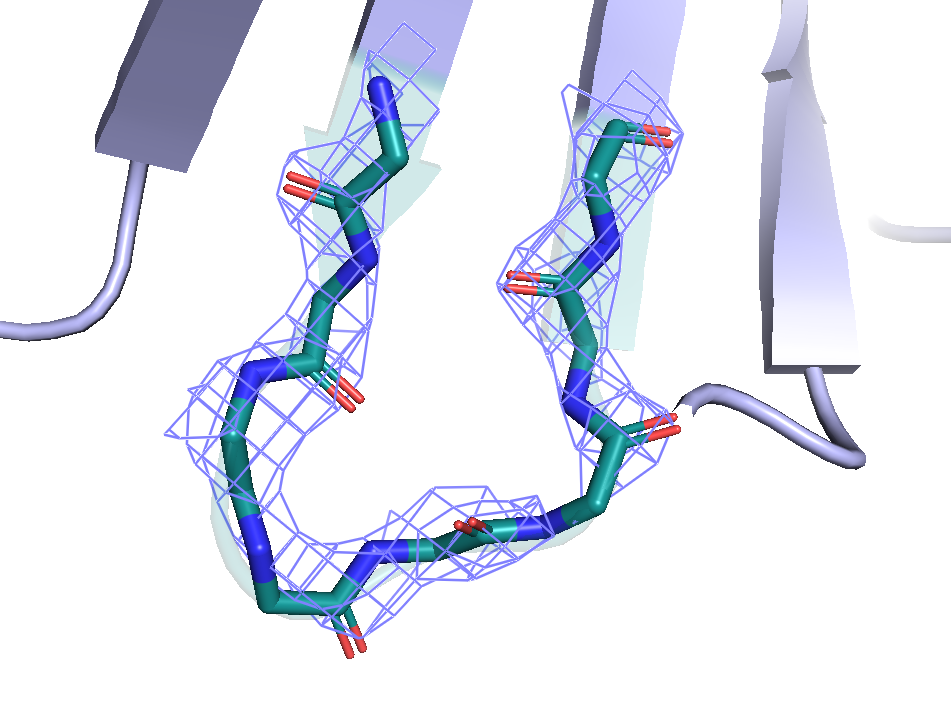
Атомы остова фрагмента структур 6lip и 5a5z
Можно заметить, что для структуры 6lip электронная плотность для каждого атома представлена в виде достаточно легко отличимой сферы, тогда как для 5a5z она явных сфер не образует и просто общей поверхностью покрывает атомы, и может быть сложно выделить отдельные из них. Из этого можно сделать вывод, что разрешение было выше для структуры 6lip. Это подтверждается данными с сайта PDB: разрешение для 6lip составляло 0.98А, в то время как для 5aza оно составило 2.6А. Также заметно, что некоторые атомы остова из структуры 5a5z вообще не попадают в границы электронной плотности (из данных изображений можно предположить, что это атомы расположенные на перефирической части белка в месах "изгиба" остова) , тогда как для 6lip каждому атому соответствует своя сфера.
Задание 2. ЭП и положение в структуре.
В данном задании рассматривалась структура другой бета-лактамазы (OXA-48 беты-лактамазы, PDB-id 7aux). Изучалась зависимость электронной плотности от параметра подрезки функции isomesh.
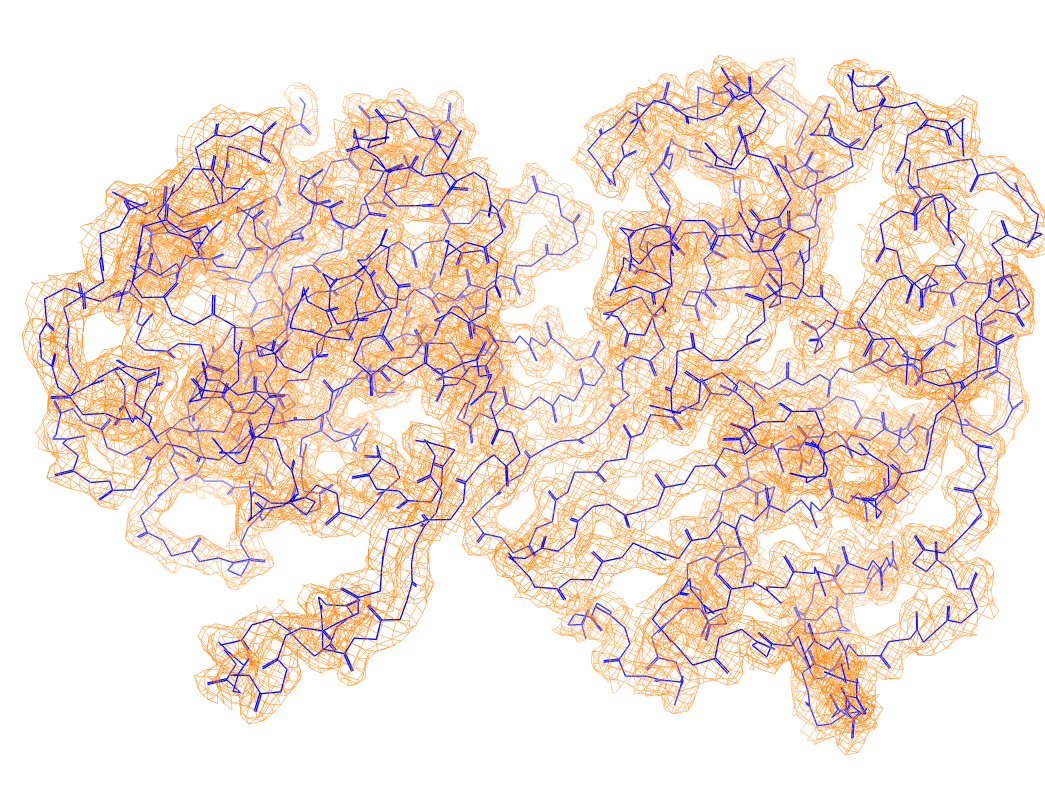
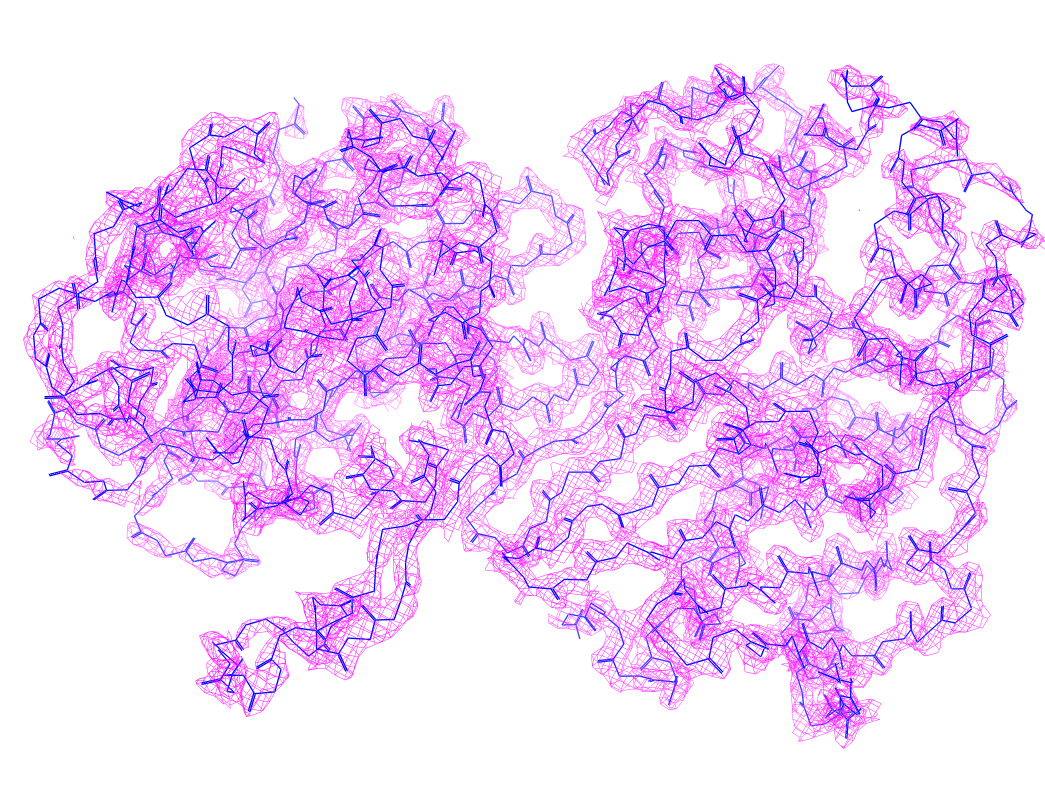
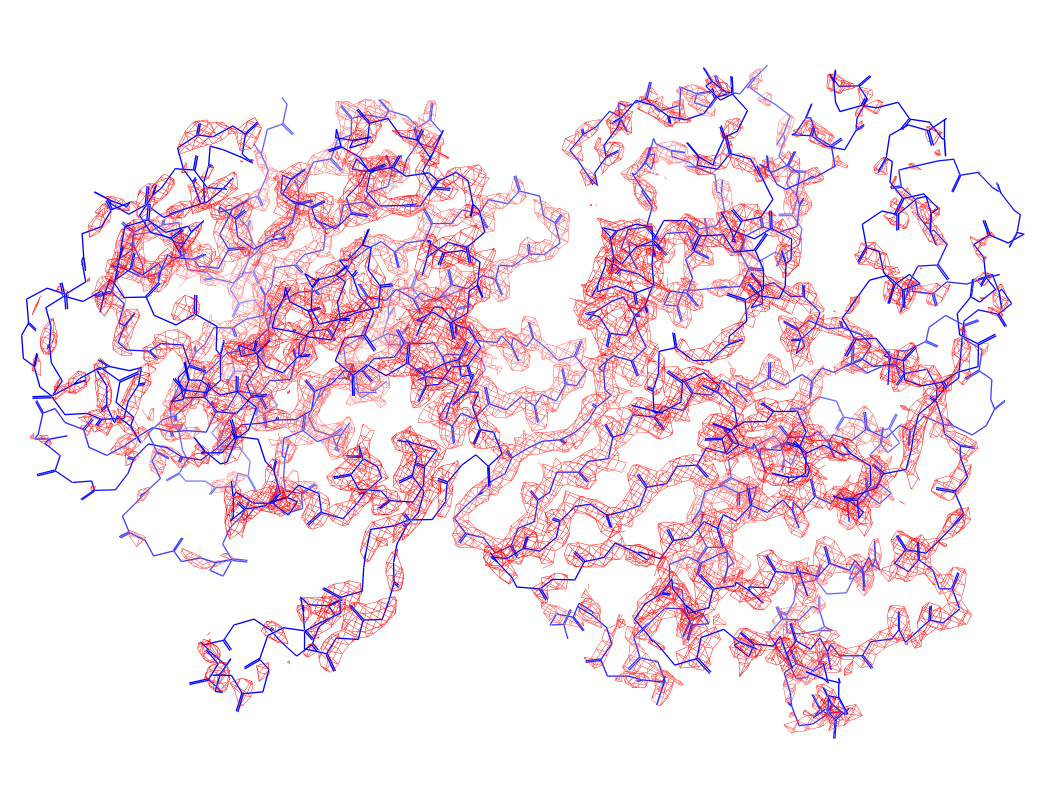
.
Остов структуры 7aux с различными значениями подбрезки (На левой картинке 1, на центральной 2, на правой 3)
Для уровня подрезки 1 электронная плотность покрывает все атомы белка. Для уровня подрезки 2 покрывает также почти все атомы, за исключением некоторых, расположенных на переферийной части белка. Для уровня подрезки 3 исчезает отображение электронной плотности целых участков белка, расположенных далеко от центра. Это может свидительствовать о том, какие участки белка более подвижны (расположенные скраю белка), а какие более фиксированы (находящиеся ближе к центру)
Задание 3. ЭП и типы атомов.
В данном задании изучалась электронная плотность для лиганда и изучалась зависимость от типа атомов. Для этого была использована функция isomesh с значениями подрезки 1, 2 и 3.
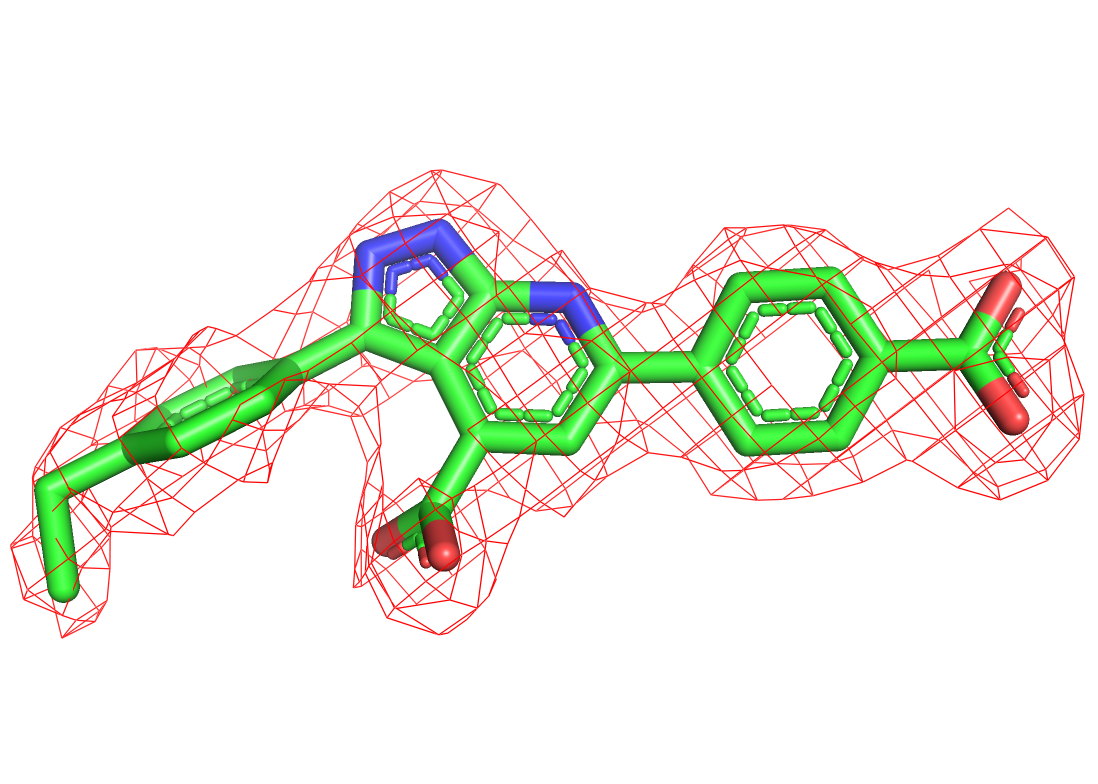
.
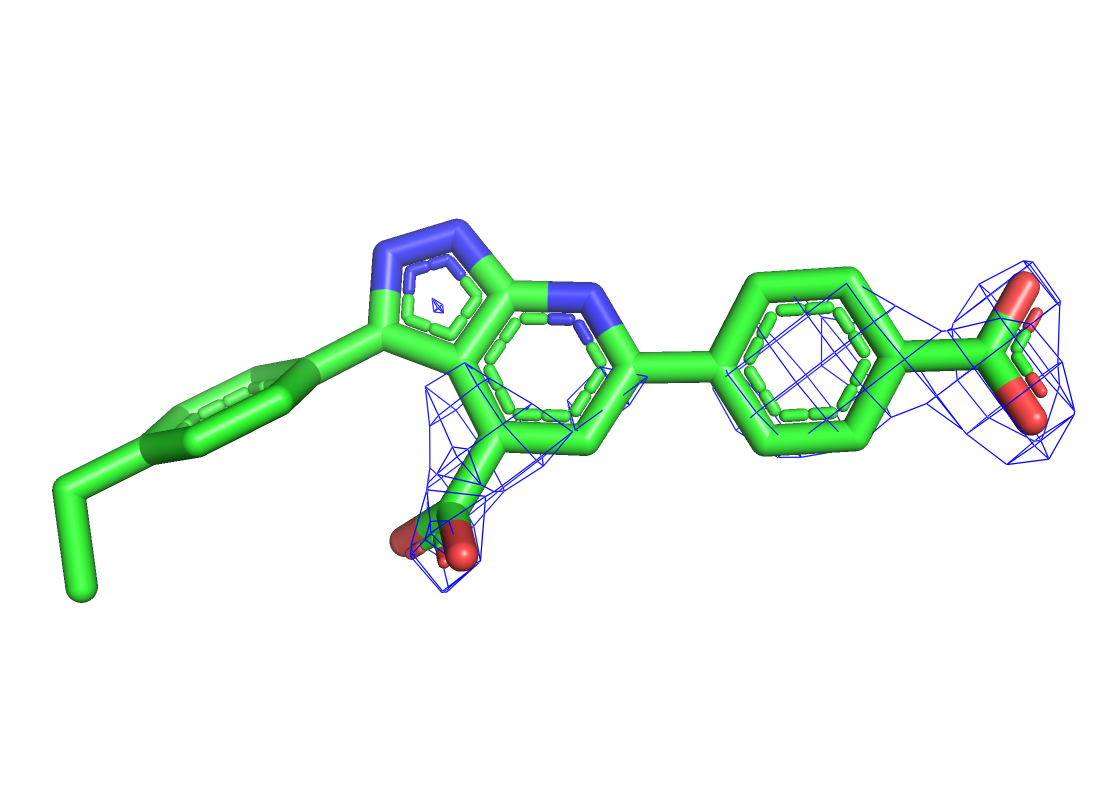
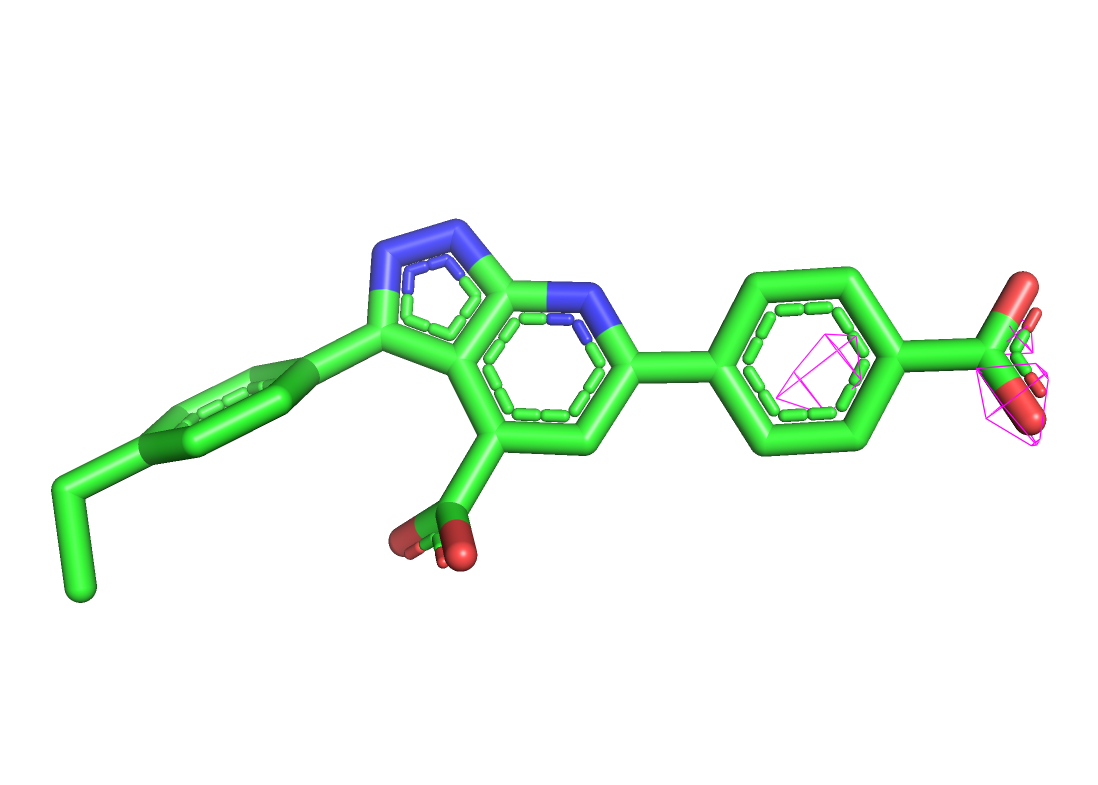
Лиганд из структуры 7aux с различными значениями подрезки (На левой картинке 1, на центральной 2, на правой 3)
На уровне подрезки 1 электронная плотность окружает все атомы. При увеличении этого параметра электронная плотность остается только на наиболее электроотрицательных атомах (на карбоксильной группе) и в рядом расположенных пи-системах в той их части, куда стягивается электронная плотность в соответствии с влиянием заместителей.