Семестр 2. Практикумы 3 & 4. Анализ и визуализация PDB-структуры 3AII
Содержание
1. Структура в целом
- Тип макромолекул: Фермент глутамил-тРНК синтетаза (Glutamyl-tRNA synthetase).
- Количество полимерных цепей: одна цепь, обозначенная в PDB как
CHAIN: A.
Цветовая легенда
CHAIN Aполимерная цепь - красныйACY- уксусная кислота - желтыйEDO- этиленгликоль - фиолетовыйCA- кальций - серо-голубойZN- цинк - зеленыйHOH- вода - синий
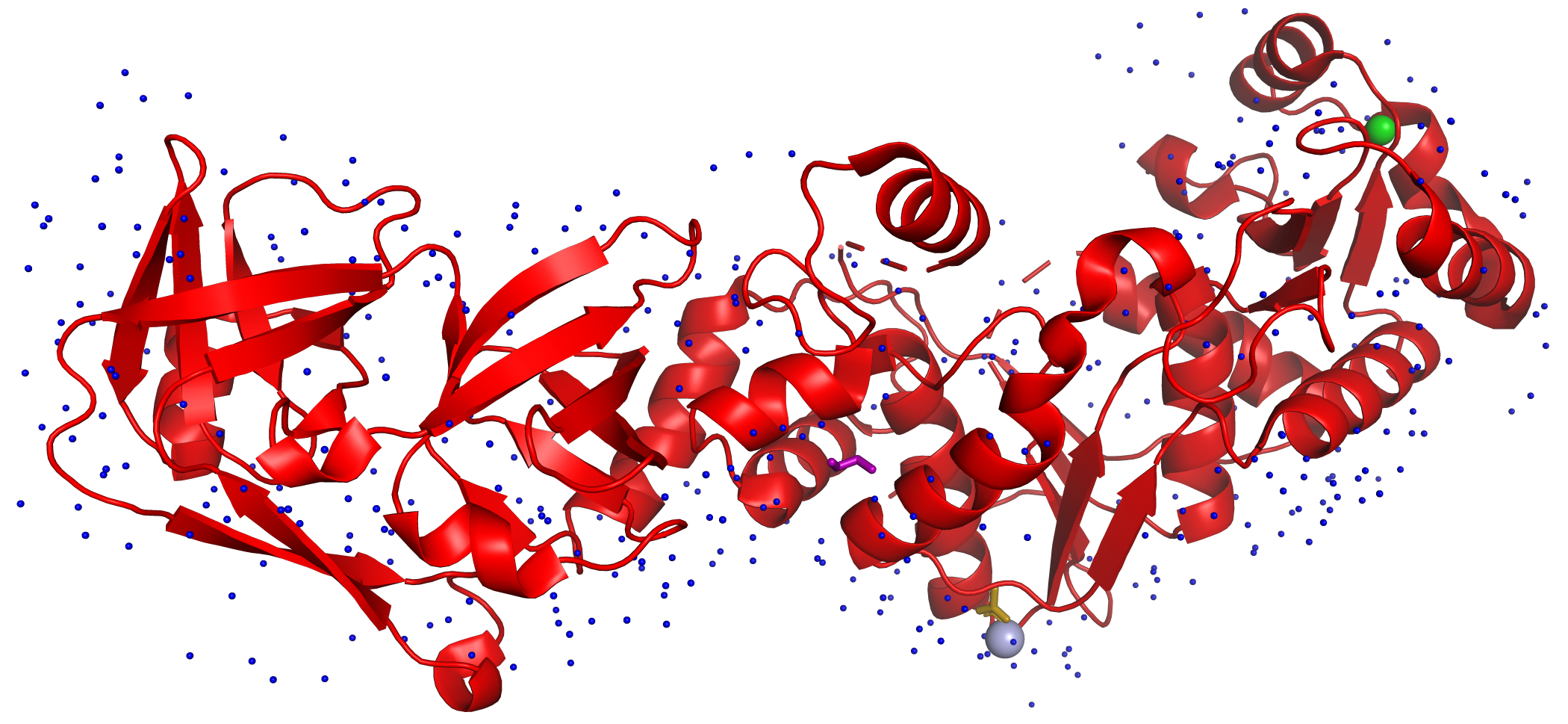
Рисунок 1. Общий вид структуры 3AII
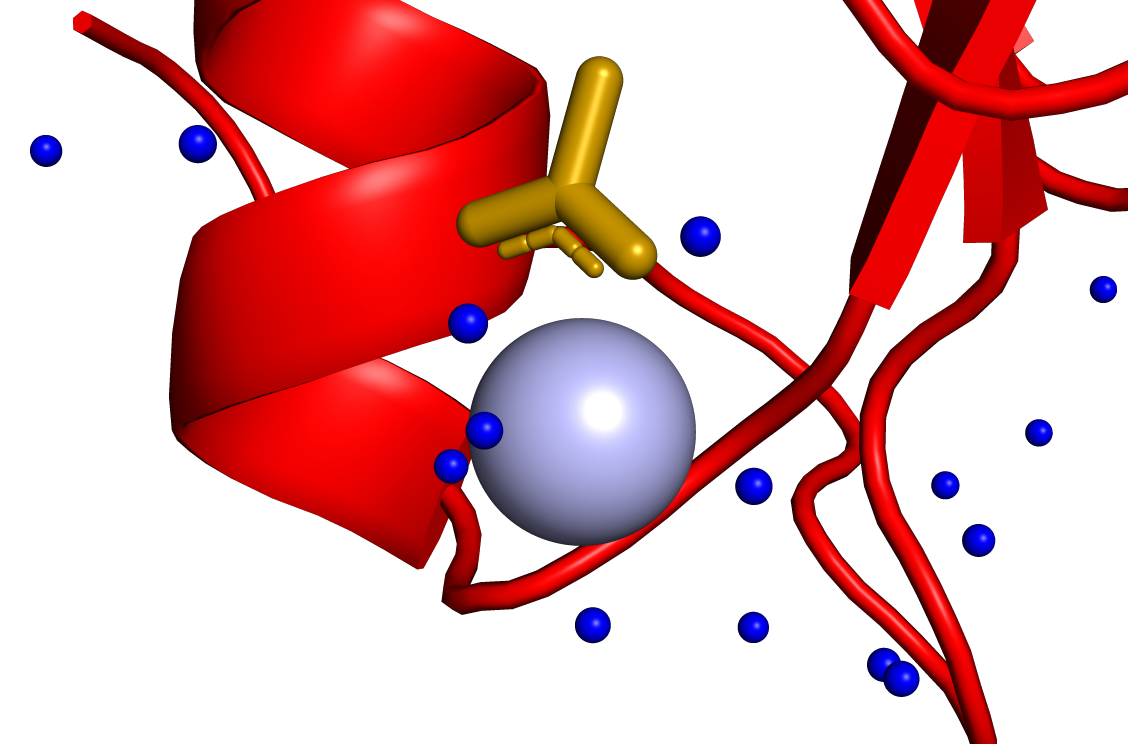
Рисунок 2. Детализация ACY, CA.

Рисунок 3. Детализация ZN.
2. Биологическая единица
Биологическая единица определена как мономерная:
REMARK 350 BIOMOLECULE: 1
REMARK 350 AUTHOR DETERMINED BIOLOGICAL UNIT: MONOMERIC
REMARK 350 SOFTWARE DETERMINED QUATERNARY STRUCTURE: MONOMERIC
REMARK 350 SOFTWARE USED: PISA
REMARK 350 APPLY THE FOLLOWING TO CHAINS: A
REMARK 350 BIOMT1 1 1.000000 0.000000 0.000000 0.00000
REMARK 350 BIOMT2 1 0.000000 1.000000 0.000000 0.00000
REMARK 350 BIOMT3 1 0.000000 0.000000 1.000000 0.00000 3. Отдельные цепи (Цепь A)
- Организм: Methanothermobacter thermautotrophicus (штамм Delta H), домен Archaea
- Uniprot:
- ID: O26157.
- Название: Глутамил-тРНК синтетаза (Glutamyl-tRNA synthetase), также известная как глутамат—тРНК лигаза.
- Функция: фермент катализирует реакцию присоединения аминокислоты глутамата к соответствующей транспортной РНК (тРНК(Glu)). Реакция происходит в два этапа: сначала образуется глутамил-аденилат (Glu-AMP), который затем переносится на тРНК.
4. Мутации в последовательности относительно референса из Uniprot
В разделе REMARK 465 перечислены аминокислотные остатки, которые не были обнаружены в экспериментальной структуре. Это означает, что эти участки белка являются гибкими или неупорядоченными и не видны на карте электронной плотности. Это не мутации, а техническая особенность метода рентгеноструктурного анализа.
5. Аминокислотные остатки
В файле не найдены модифицированные аминокислотные остатки. Все остатки являются стандартными:
СТАНДАРТНЫЕ АМИНОКИСЛОТЫ (всего: 20 типов, 3749 атомов): ARG: 595 GLU: 465 LEU: 333 VAL: 256 TYR: 240 ILE: 200 ASP: 200 PRO: 182 ALA: 175 GLY: 152 HIS: 150 LYS: 127 PHE: 121 TRP: 112 SER: 108 MET: 101 ASN: 88 THR: 84 GLN: 36 CYS: 24 МОДИФИЦИРОВАННЫЕ АМИНОКИСЛОТЫ (всего: 0 типов, 0 атомов).
6. Вторичная структура
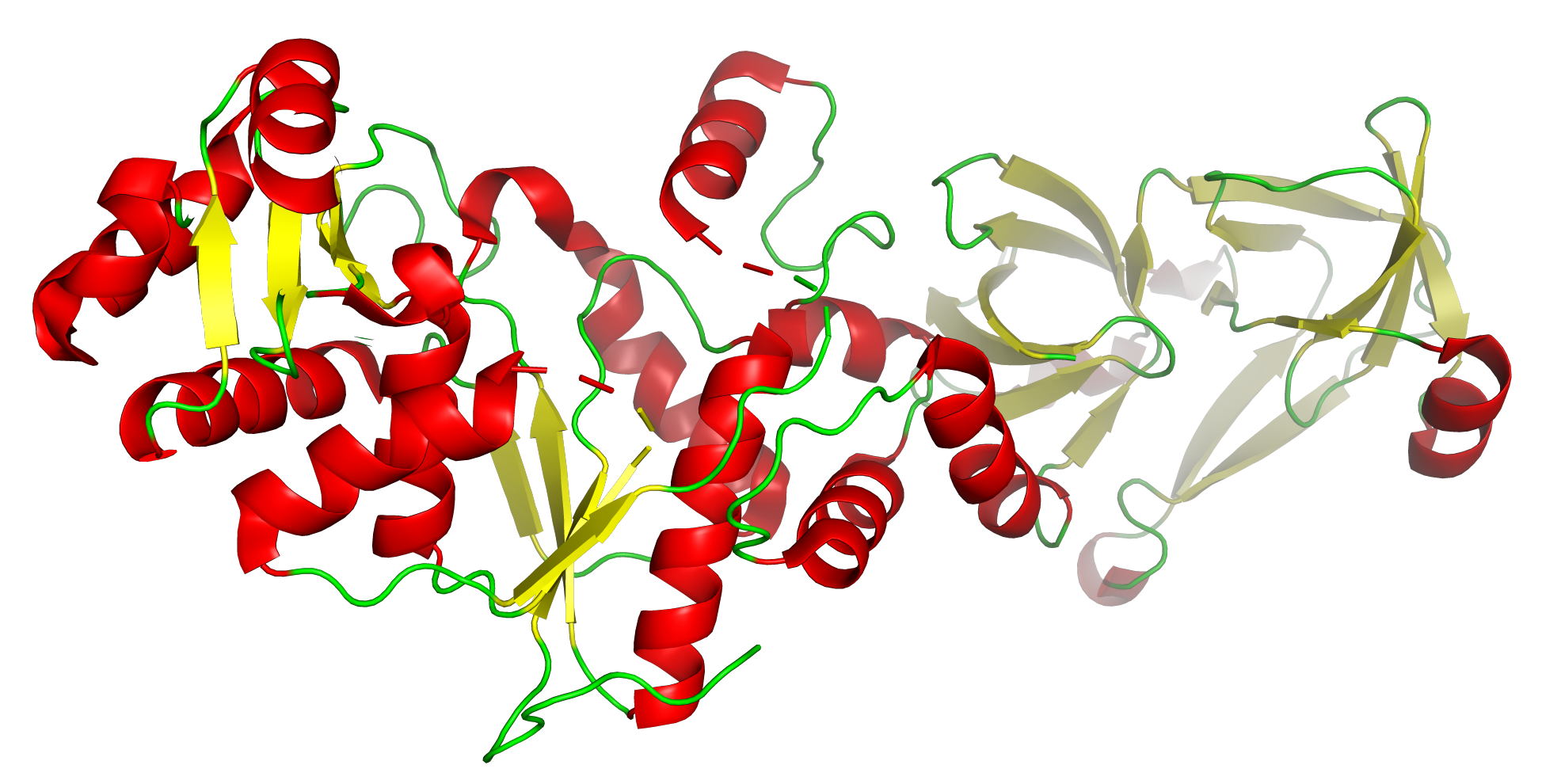
Рисунок 4. Детализация вторичной структуры
(Альфа-спирали: красный, Бета-тяжи: желтый, Петли/витки: зеленый)
Статистика вторичной структуры:
Всего остатков: 466
Альфа-спирали (ss h):
Остатков: 192
Процент: 41.2%
Бета-тяжи (ss s):
Остатков: 124
Процент: 26.6%
Петли/витки (ss l+):
Остатков: 150
Процент: 32.2%
7. Малые молекулы
В записи присутствуют следующие низкомолекулярные соединения HETATM:
- Ионы металлов:
ZN(Zinc Ion) — Один ион цинка (Zn²⁺). Выполняет каталитическую и структурную роль[1].CA(Calcium Ion) — Один ион кальция (Ca²⁺). Участвует в стабилизации структуры.
- Компоненты кристаллизационной среды:
ACY(Acetic Acid) — Молекула уксусной кислоты. Компонент буферного раствора.EDO(1,2-Ethanediol) — Молекула этиленгликоля. Фермент полиэтиленгликоля из кристаллизационного раствора.
- Растворитель:
HOH- 420 молекул воды. Формируют гидратную оболочку белка.
Сводный TXT-файл с детализацией.
Визуализация белкового окружения ACY
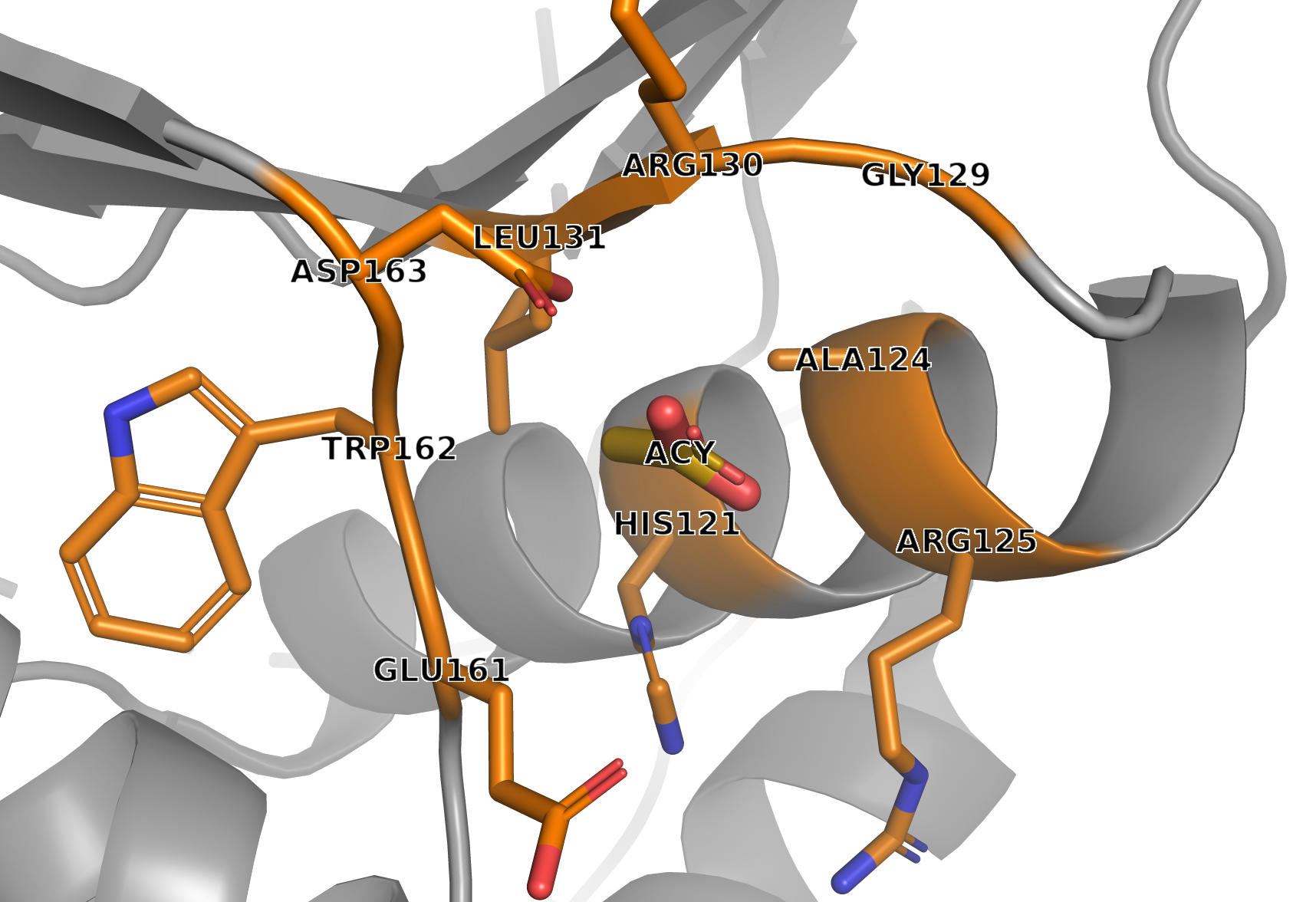
Рисунок 5. Белковое окружение лиганда ACY
Аминокислотные остатки в радиусе 5Å от ACY:
1. HIS121 2. ALA124 3. ARG125 4. GLY129 5. ARG130 6. LEU131 7. GLU161 8. TRP162 9. ASP163
Визуализация белкового окружения EDO
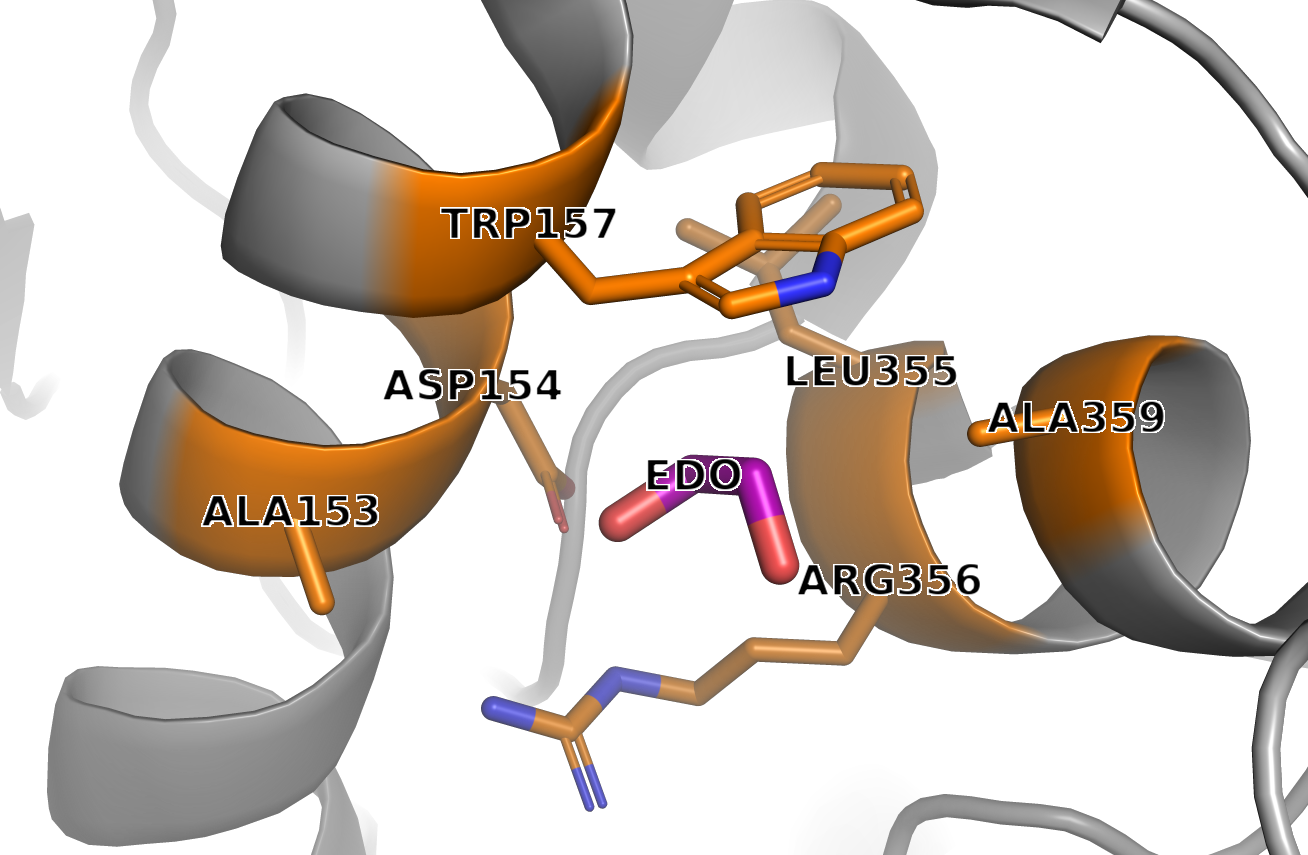
Рисунок 6. Белковое окружение лиганда EDO
Аминокислотные остатки в радиусе 5Å от EDO:
1. ALA153 2. ASP154 3. TRP157 4. LEU355 5. ARG356 6. ALA359
Визуализация белкового окружения CA
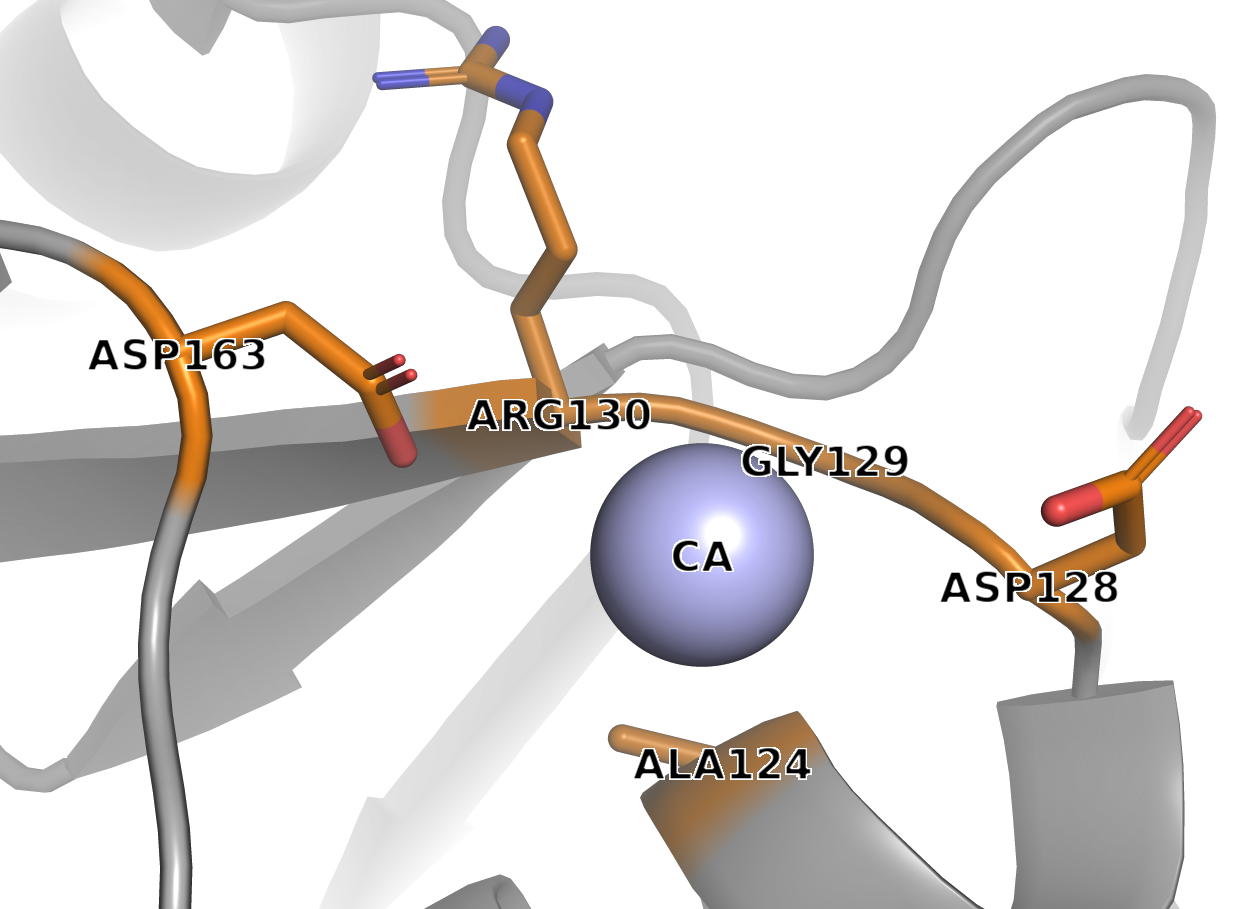
Рисунок 7. Белковое окружение CA
Аминокислотные остатки в радиусе 5Å от CA:
1. ALA124 2. ASP128 3. GLY129 4. ARG130 5. ASP163
Визуализация белкового окружения ZN
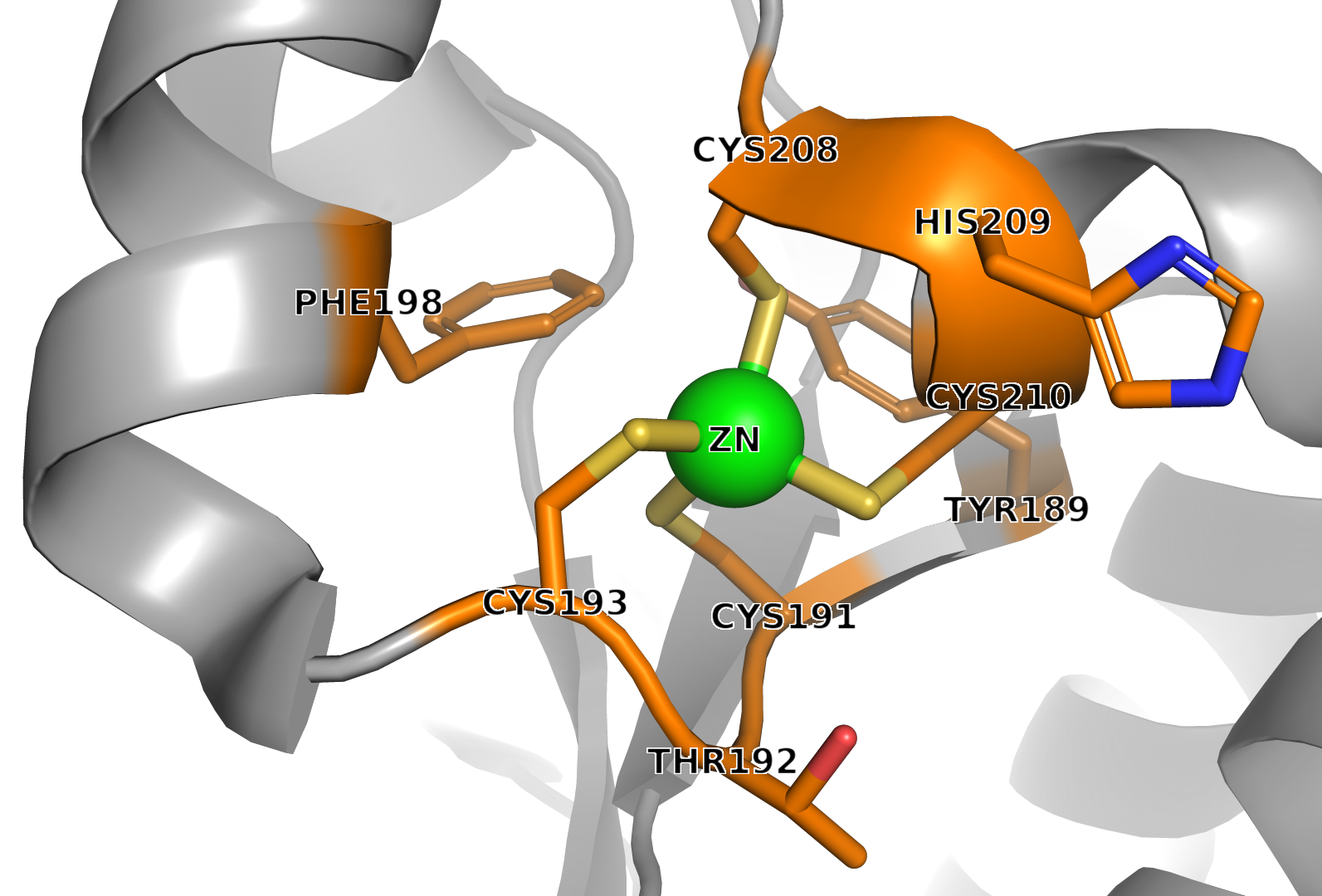
Рисунок 8. Белковое окружение ZN
Аминокислотные остатки в радиусе 5Å от ZN:
1. TYR189 2. CYS191 3. THR192 4. CYS193 5. PHE198 6. CYS208 7. HIS209 8. CYS210
8. Список литературы
- Nureki O, O'Donoghue P, Watanabe N, Ohmori A, Oshikane H, Araiso Y, Sheppard K, Soll D, Ishitani R. Structure of an archaeal non-discriminating glutamyl-tRNA synthetase: a missing link in the evolution of Gln-tRNAGln formation. Nucleic Acids Res. 2010 Nov;38(20):7286-97. doi: 10.1093/nar/gkq605. Epub 2010 Jul 8. PMID: 20601684; PMCID: PMC2978372.