Семестр 2. Практикум 5. Визуализация взаимодействий между аминокислотными остатками в 3AII
Содержание
1. Демонстрация водородной связи атомов остова
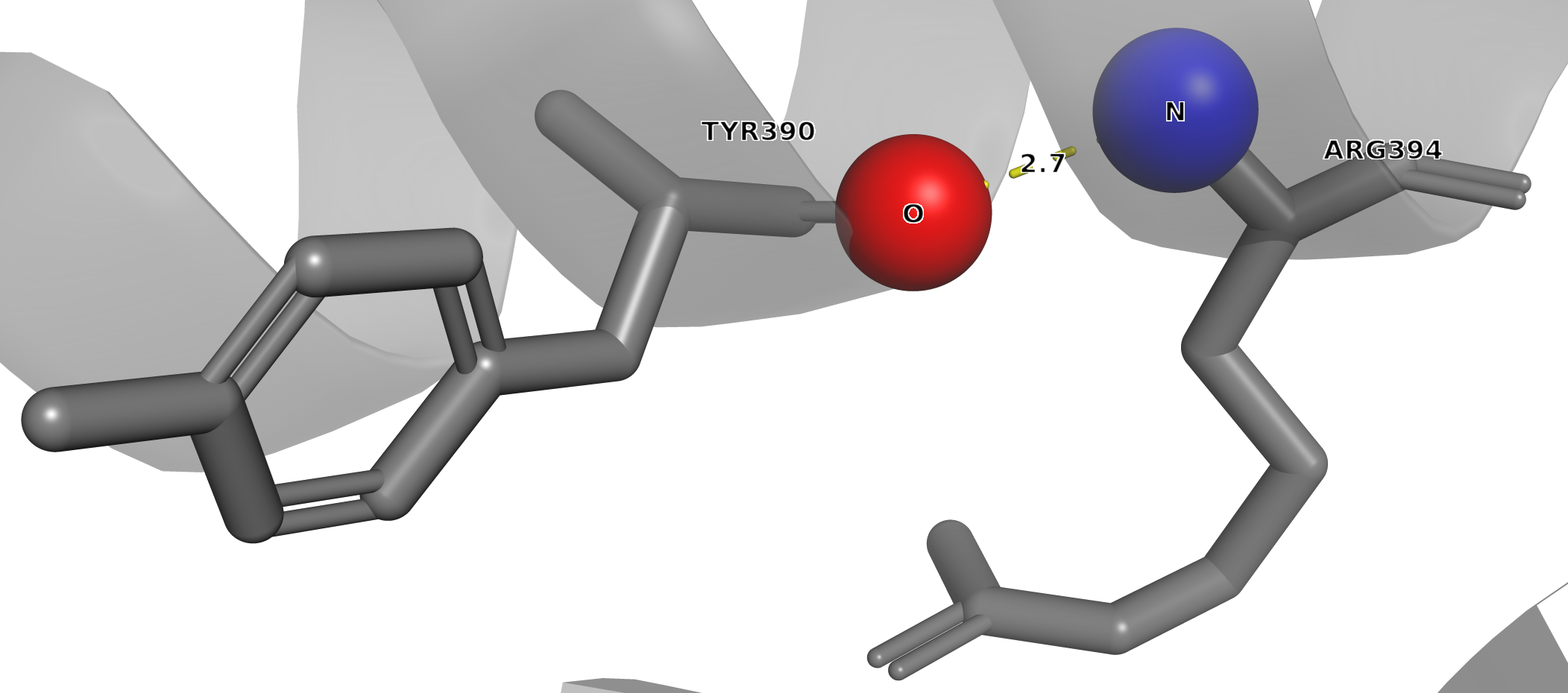
Рисунок 1. Водородная связь остова белка 3AII
Донор: ARG 394 (N-H) Акцептор: TYR 390 (C=O) Цепь: A Расстояние N···O: 2.69Å REMARK 2 RESOLUTION. 1.65 ANGSTROMS
Водородная связь: O···H-N. В рентгеновской кристаллографии (X-ray) при заданном разрешении 1.65Å атомы H, имеющие размер 0.529Å не видны.
Сводный TXT-файл с детализацией по найденным водородным связям остова.
2. Визуализация водородной связи для боковых радикалов аминокислот
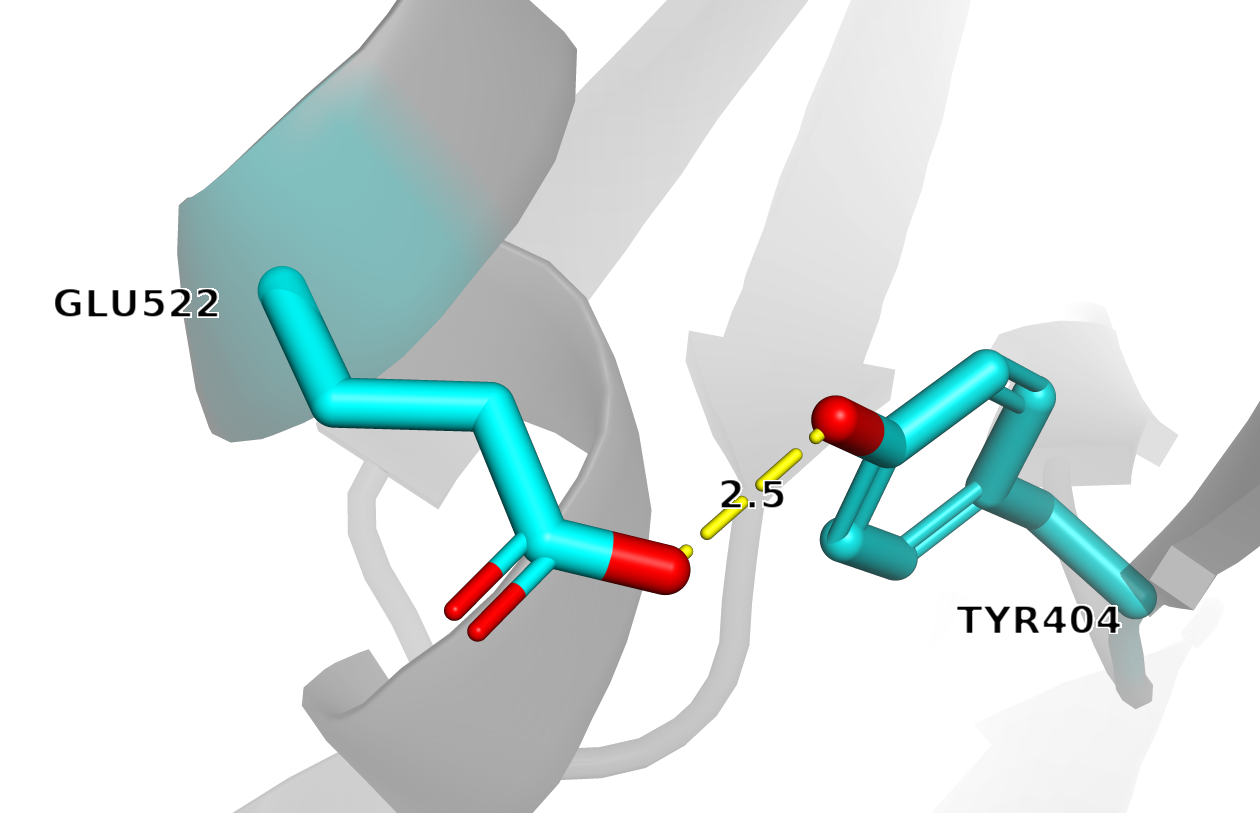
Рисунок 2. SC-SC H-cвязь между TYR404(OH) и GLU522(OE2)
Всего SC-SC H-связей найдено : 101 Минимальное расстояние : 2.5 Максимальное расстояние : 3.5
Сводный TXT-файл с детализацией по найденным водородным связям для боковых радикалов аминокислот.
3. Солевой мостик
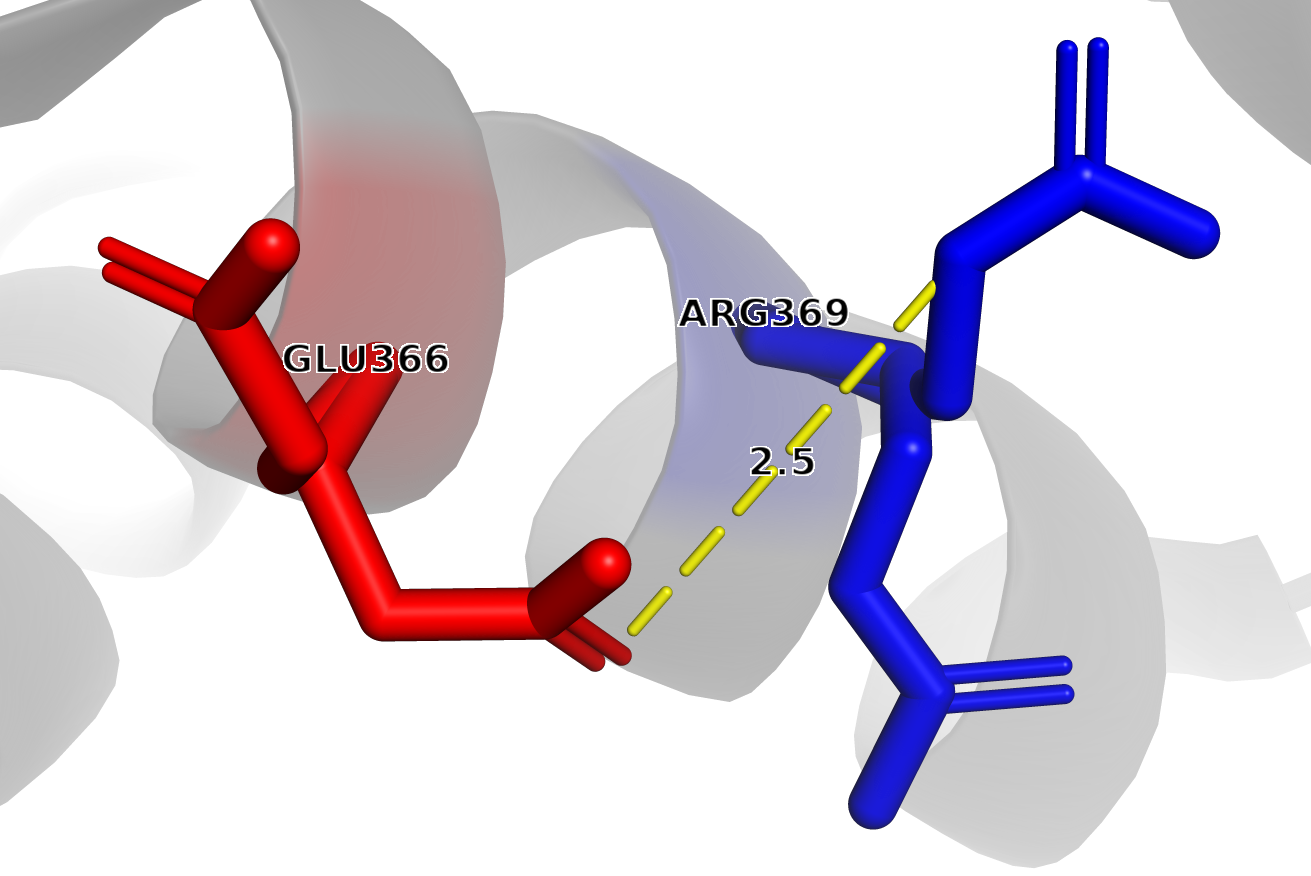
Рисунок 3. Мостик между ARG369(NE) и GLU366(OE1)
Сводный TXT-файл с детализацией по найденным солевым мостикам.
4. Дисульфидная связь
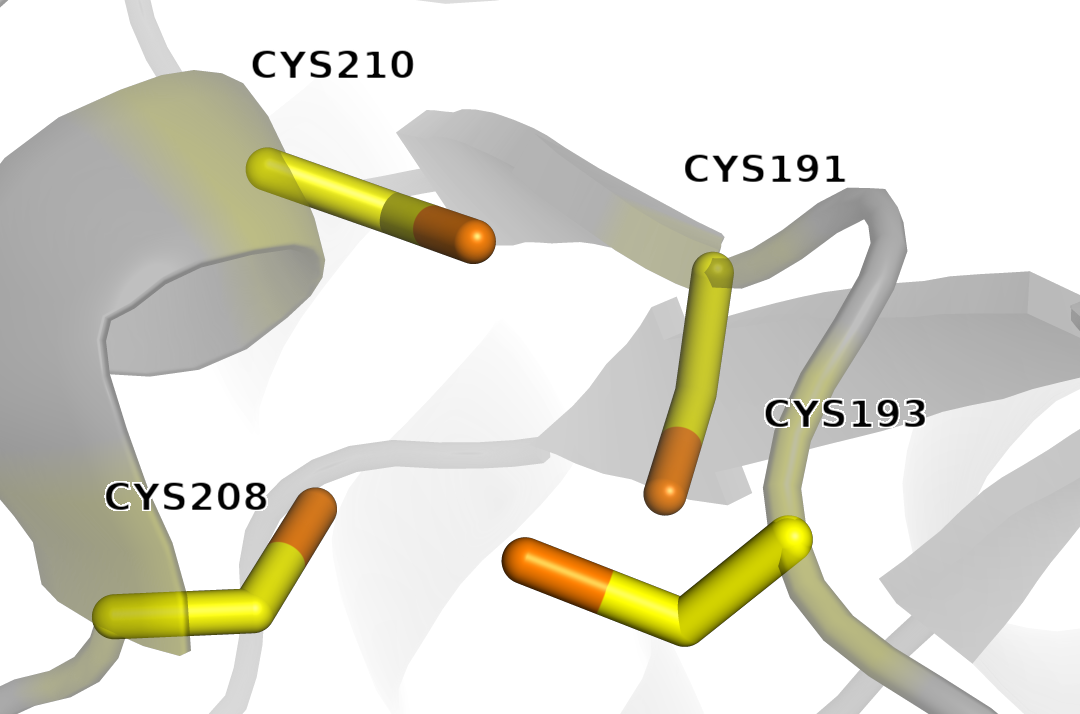
Рисунок 4. Цистеины CYS в 3AII
Дисульфидных связей не найдено (порог S-S ≤ 2.3Å) Найдено цистеинов в структуре CHAIN A: 4 CYS191 CYS193 CYS208 CYS210
Ион цинка координируется всеми четырьмя цистеинами, поэтому они не способны к образованию дисульфидных связей. Выступая в роли структурного центра, цинк жестко фиксирует эти аминокислотные остатки, создавая устойчивый тетраэдрический мотив и формируя характерный цинковый палец (кластер) с лигандным окружением Cys₄. Вместе с цинком - см. рисунок из Практикума №4.
5. Стекинг
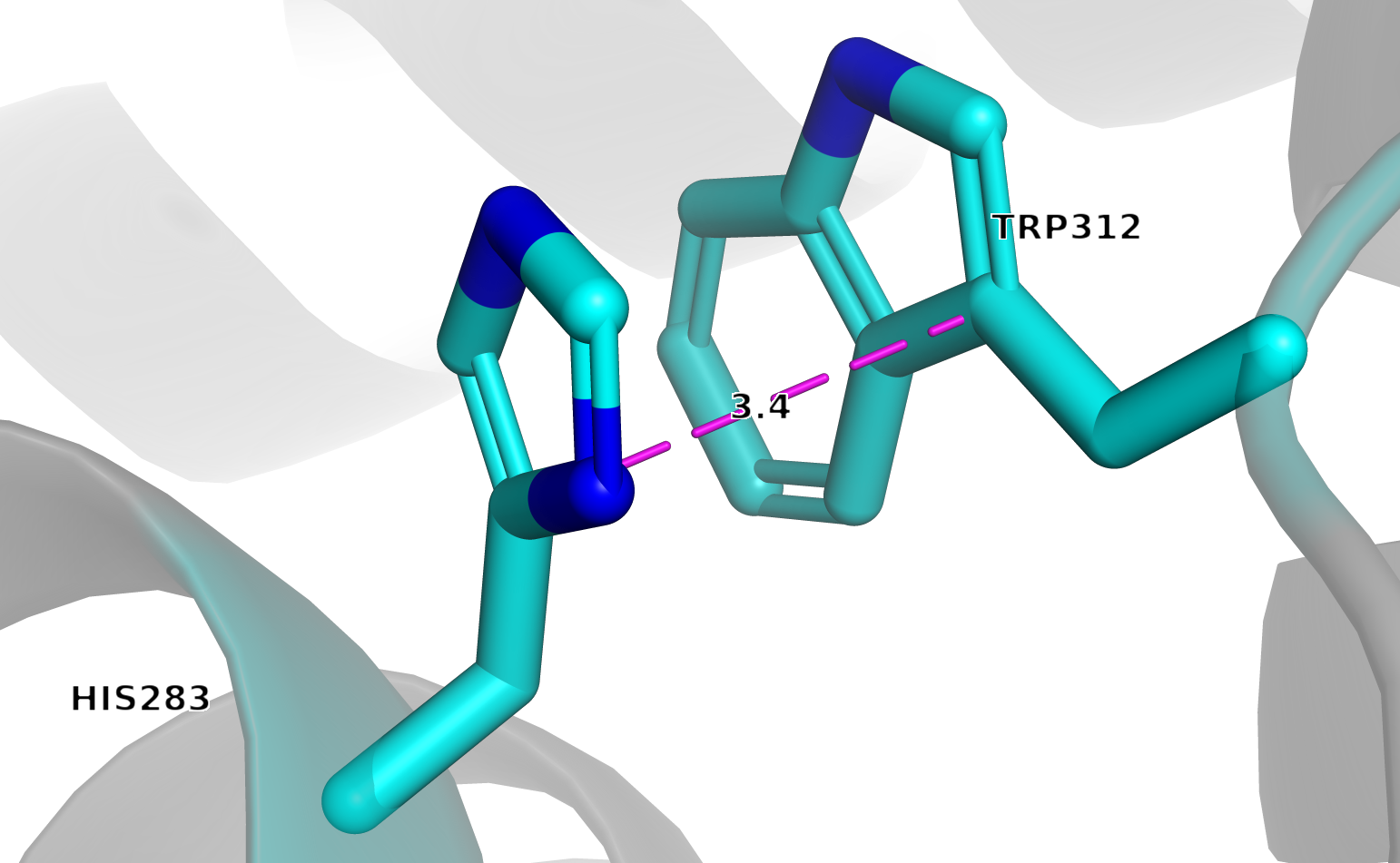
Рисунок 5. Пример параллельной стекинг-пары 3AII
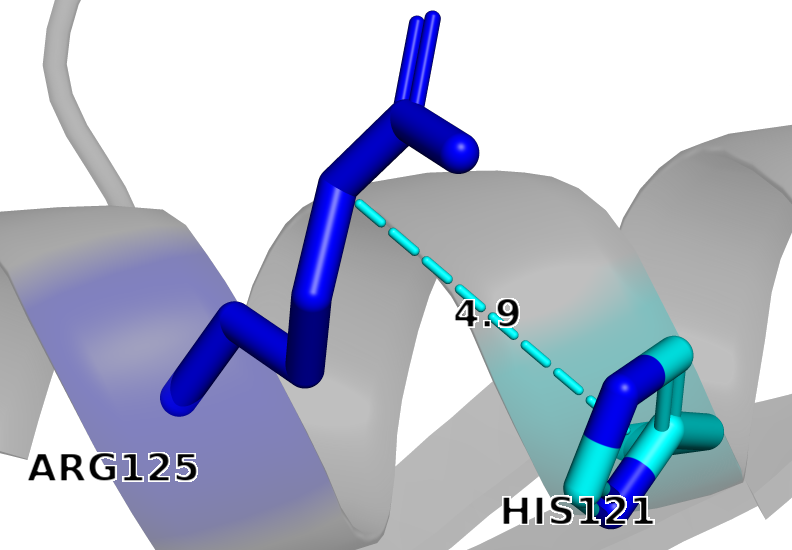
Рисунок 6. Пример пи-катионной стекинг-пары 3AII
Стекинг-пар найдено : 1 (параллельных: 1, T-образных: 0) 1. TRP312(A) ... HIS283(A) d=3.4 угол=8.1 [параллельный] <- Пи-катионных пар найдено : 7 1. PHE405(A) ··· ARG438(A,NH1) d=3.5 угол=6.3 2. PHE198(A) ··· ARG236(A,NE) d=3.5 угол=14.9 3. TYR549(A) ··· ARG360(A,NE) d=3.8 угол=16.1 4. PHE198(A) ··· ARG236(A,NH2) d=4.1 угол=35.8 5. TYR320(A) ··· ARG115(A,NE) d=4.3 угол=37.0 6. TYR148(A) ··· ARG263(A,NE) d=4.7 угол=22.6 7. HIS121(A) ··· ARG125(A,NE) d=4.9 угол=35.4 <-
Расстояние в 3.4Å указывает на наличие ван-дер-ваальсового контакта между ароматическими кольцами (типичный диапазон 3.3–3.8Å).
Угол между кольцами триптофана TRP и гистидина HIS составляет 8.1°, что демонстрирует параллельную (сэндвич) ориентацию.
Обнаружено 7 пи-катионных взаимодействий между ароматическими кольцами (PHE, TYR, HIS) и гуанидиниевыми группами остатков аргинина (ARG). Расстояния в диапазоне 3.5–4.9 Å и малые углы между нормалью кольца и вектором катион→центроид (6–37°) указывают на геометрически корректные пи-катионные контакты, вносящие вклад в стабилизацию третичной структуры белка.