Анализ структуры белка с помощью PDB
СТРУКТУРА В ЦЕЛОМ
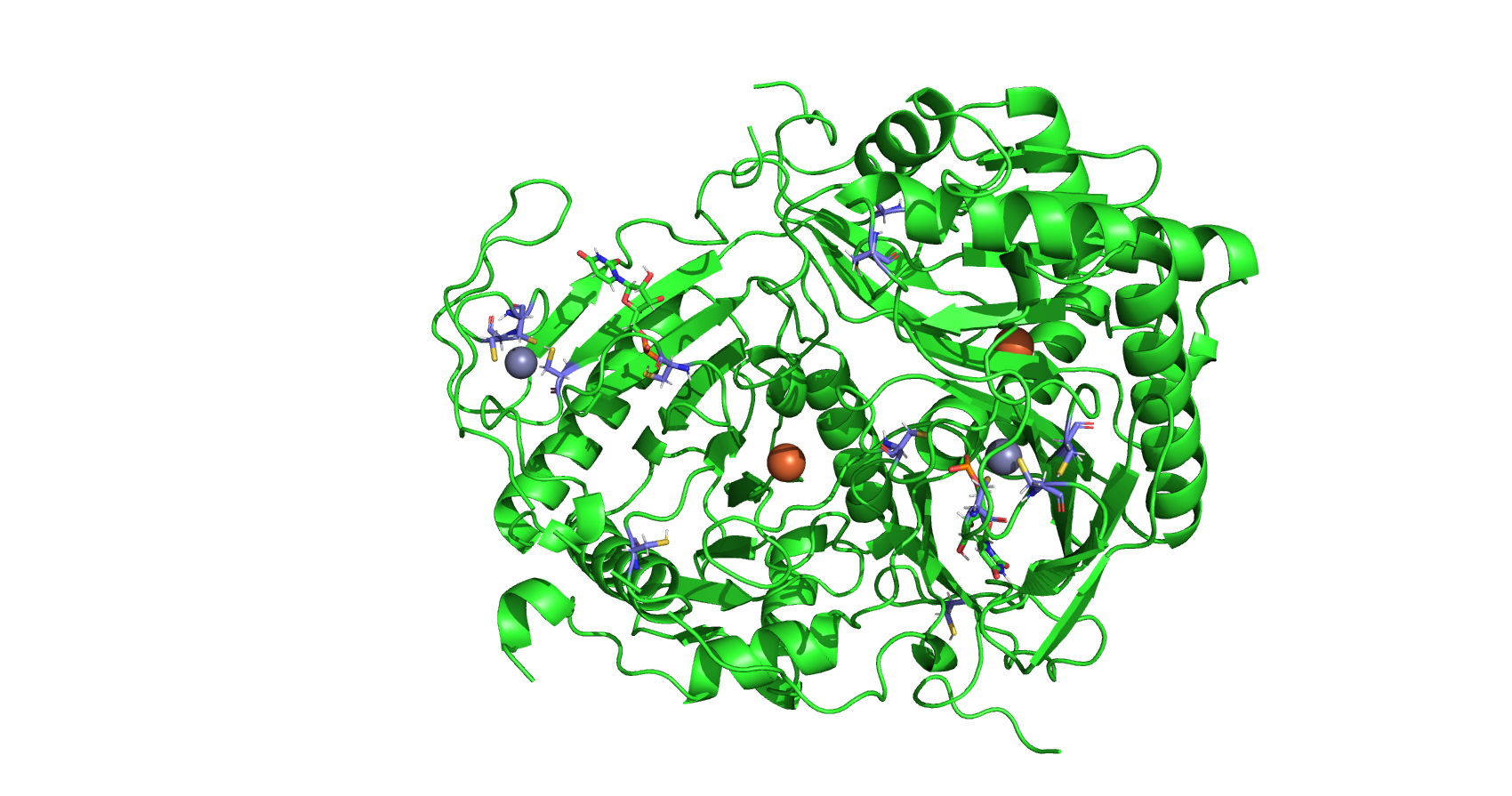
Идентификатором 1HXQ в базе данных PDB обозначен белок бактерии Escherichia coli галактозо-1-фосфат уридилтрансфераза (GALACTOSE-1-PHOSPHATE URIDYLYLTRANSFERASE), относящийся к нуклеотидтрансферазам. В структуре присутствуют две полимерные цепи, А и В (см. рис. 1, различные цепи покрашены различными цветами), идентичные по последовательности. Данный белок является гомодимером, то есть в биологическую единицу входят обе (две) цепи: А и В.
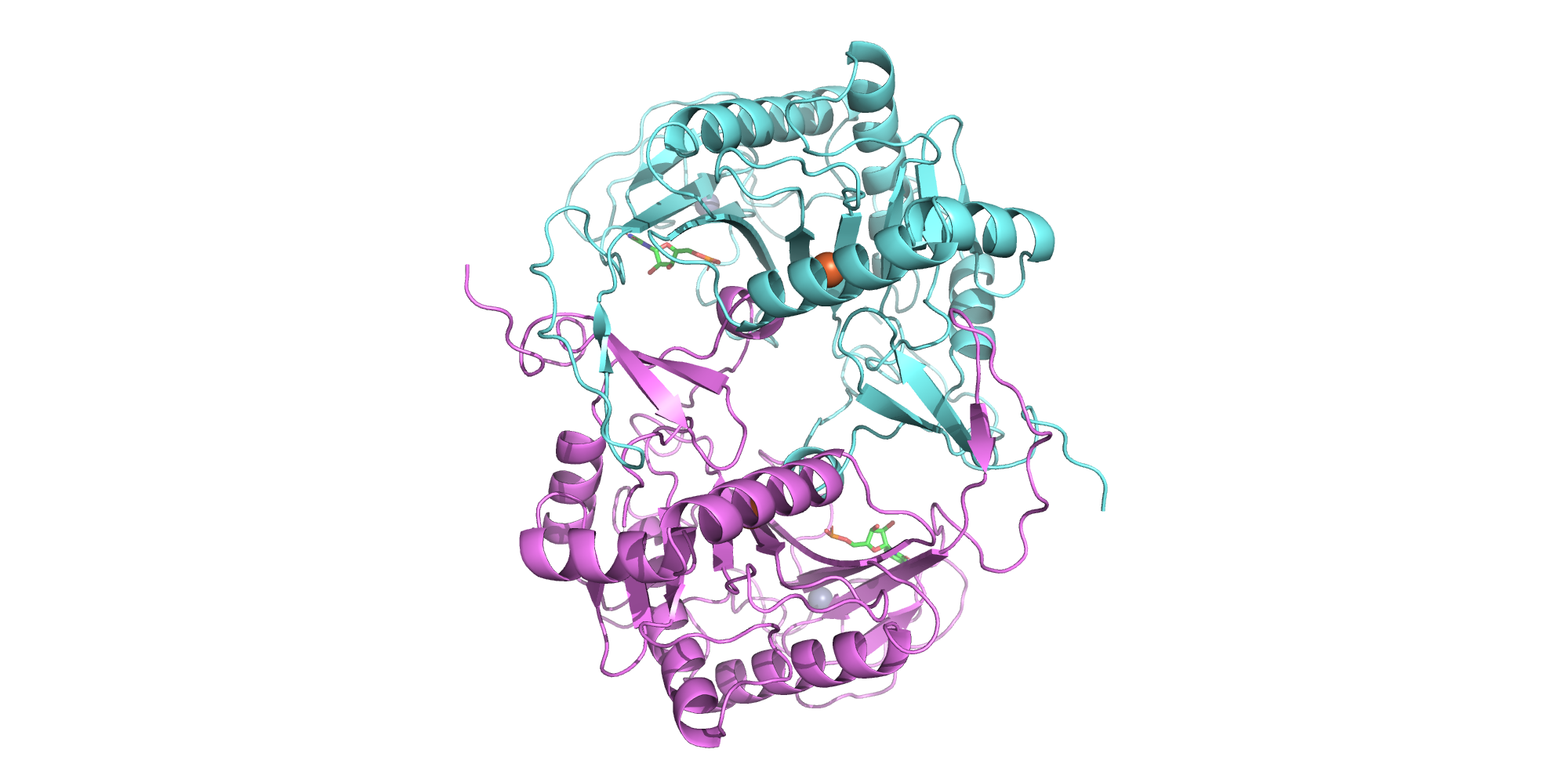
ОТДЕЛЬНЫЕ ЦЕПИ
Для каждой из полимерных цепей А и В, в силу гомодимерности описываемого белка, верно, что они относятся к организму Escherichia coli штамма К12 и имеют uniprot_id P09148. Каждая цепь имеет название галактозо-1-фосфат уридилтрансфераза (GALACTOSE-1-PHOSPHATE URIDYLYLTRANSFERASE) и выполняет функцию катализа совместного превращения УДФ-глюкозы и галактозо-1-фосфата в УДФ-галактозу и глюкозо-1-фосфат. Таким образом, обе цепи данного фермента участвуют в метаболизме углеводов, в частности, играя важную роль в метаболизме галактозы. Мутаций в последовательности относительно референса из Uniprot, согласно PDB, нет, как и модифицированных аминокислотных остатков в составе цепи.
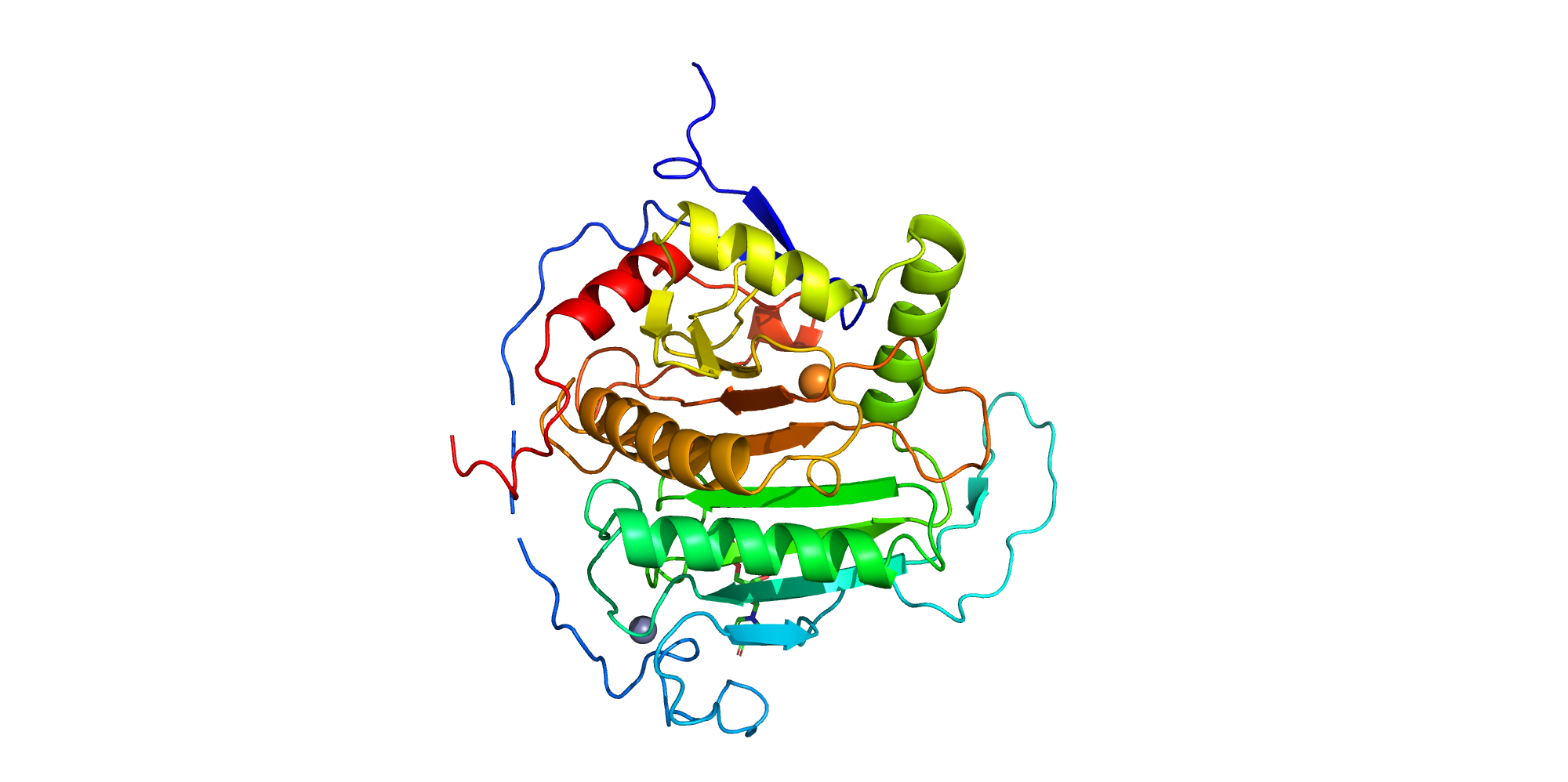
ВТОРИЧНАЯ СТРУКТУРА
Во вторичной структуре белка присутствует 12 альфа-спиралей и 4 бета-листа, а также часть объема занимают неупорядоченные участки с первичной структурой. Несмотря на то, что спиральных фрагментов в ферменте по количеству больше, нежели складчатых, и те, и другие имеют примерно одинаковый объем в общей структуре.
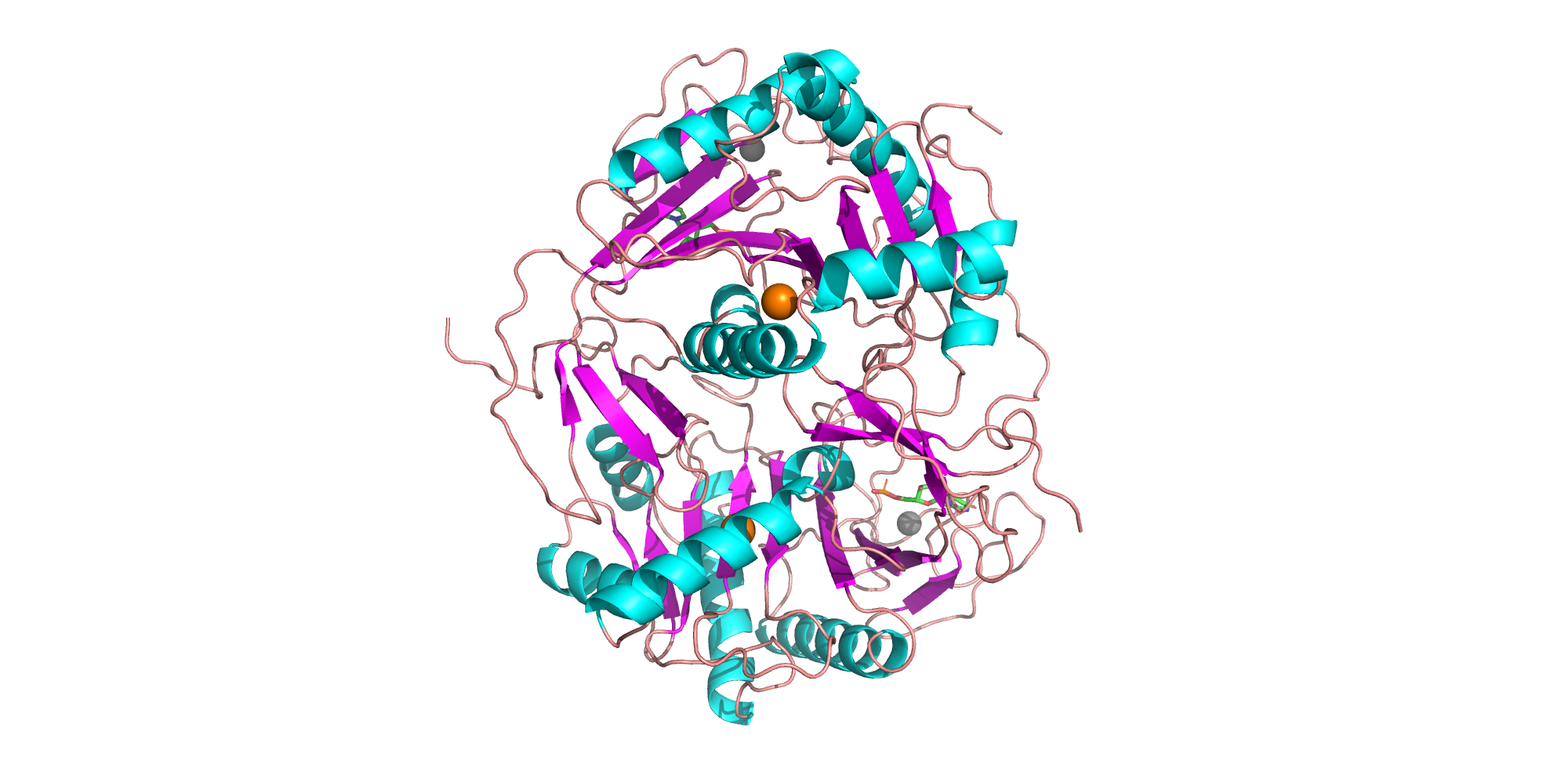
ВНУТРИБЕЛКОВЫЕ ВЗАИМОДЕЙСТВИЯ
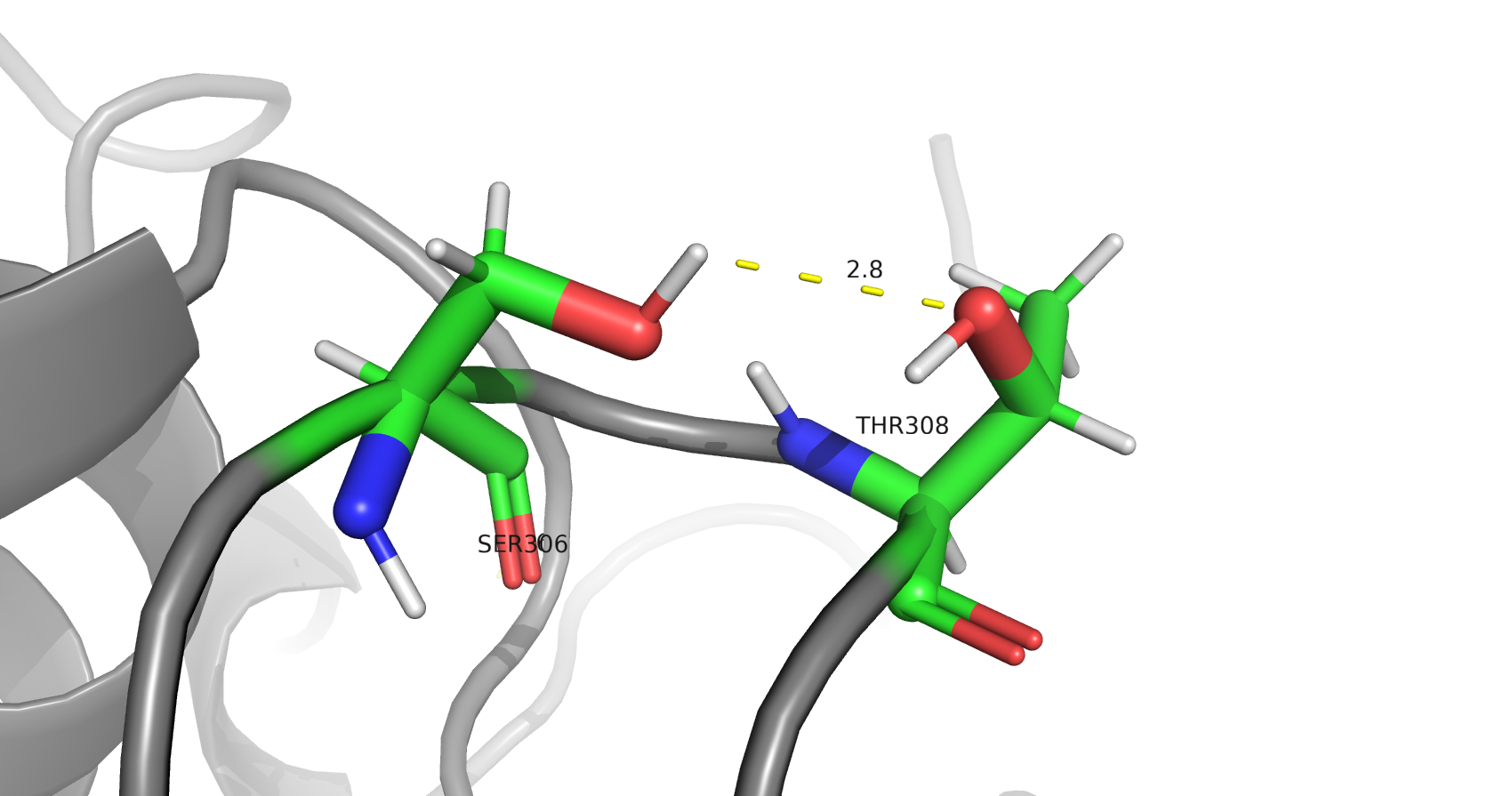
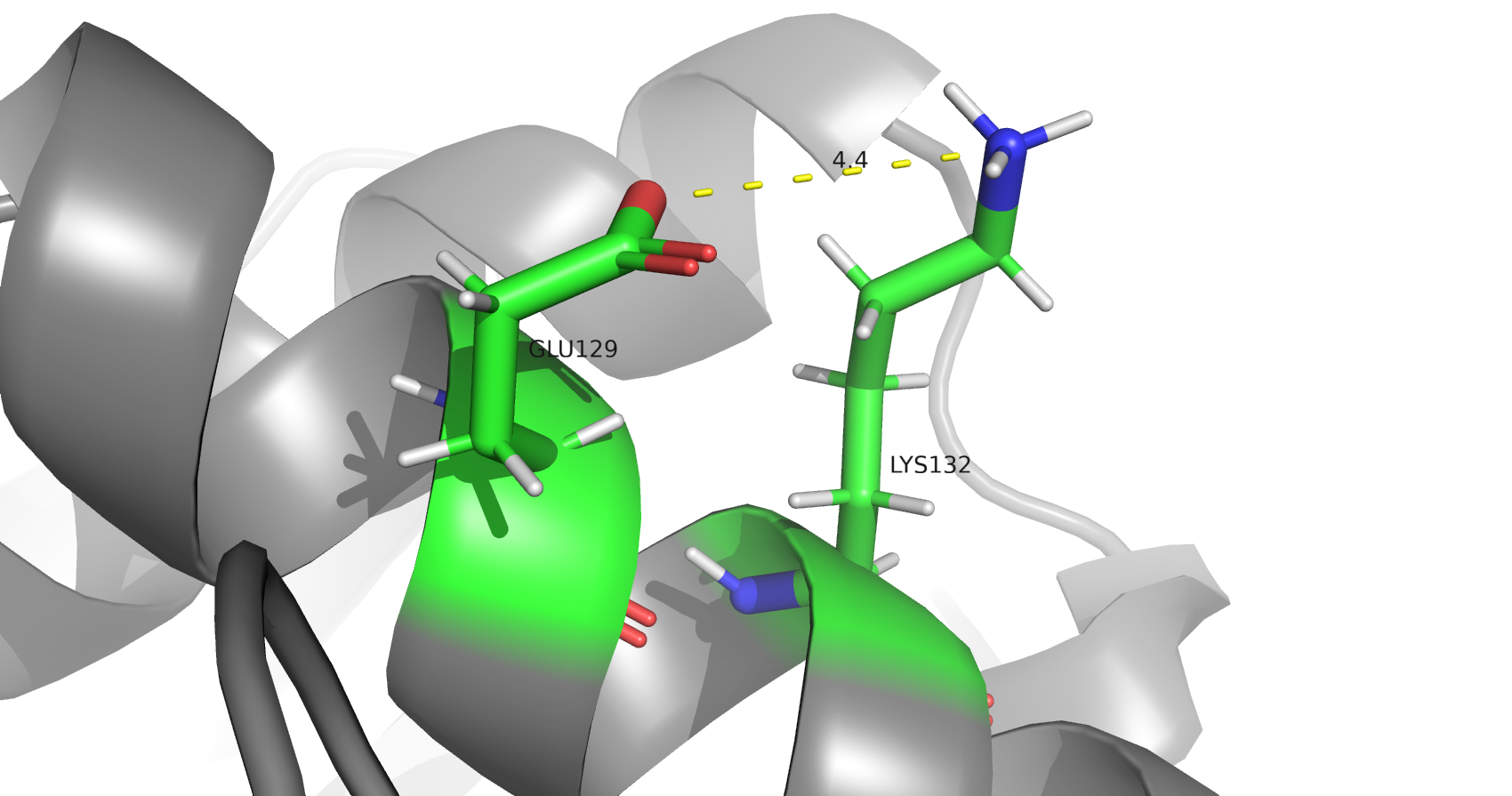
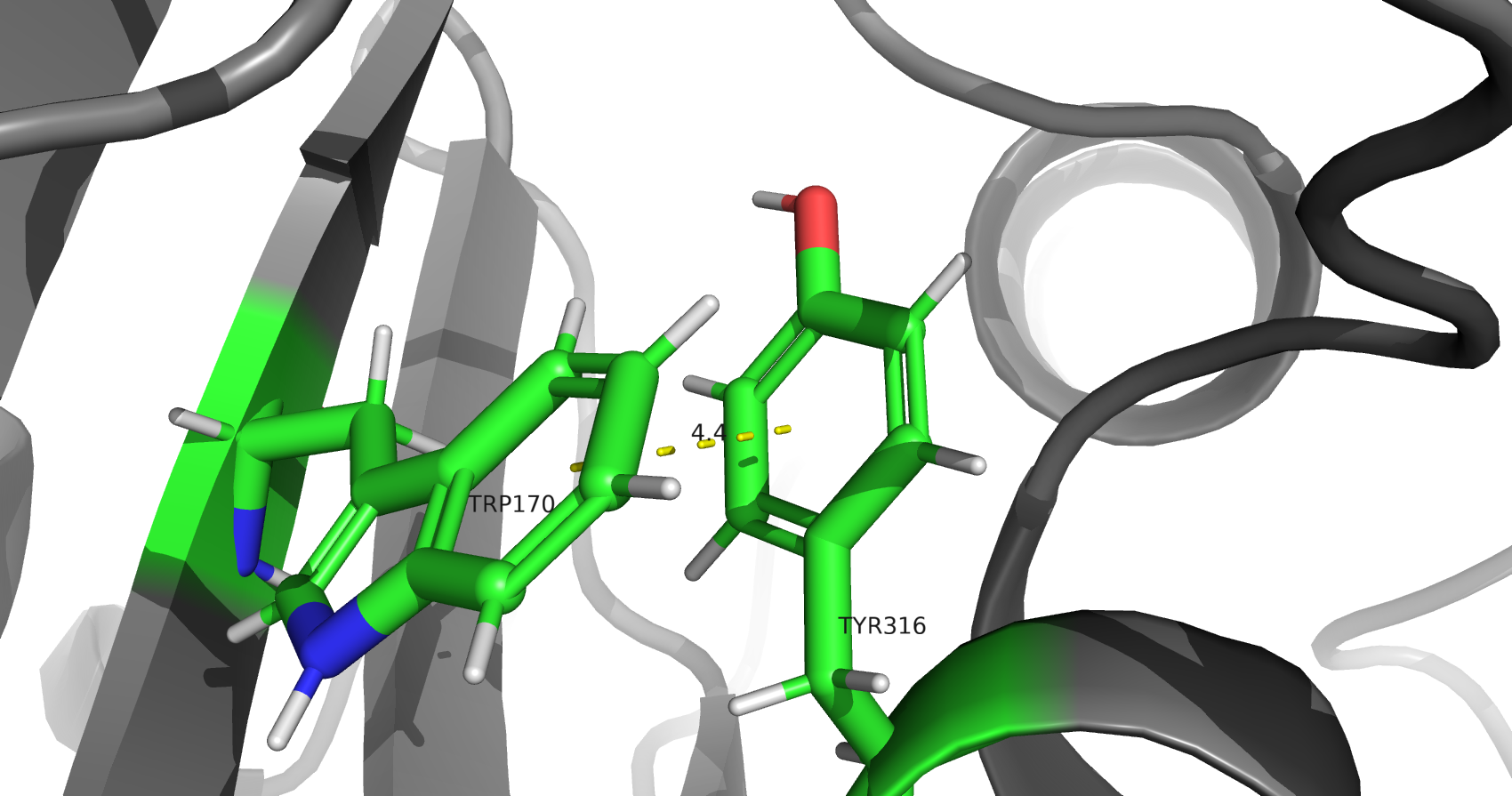
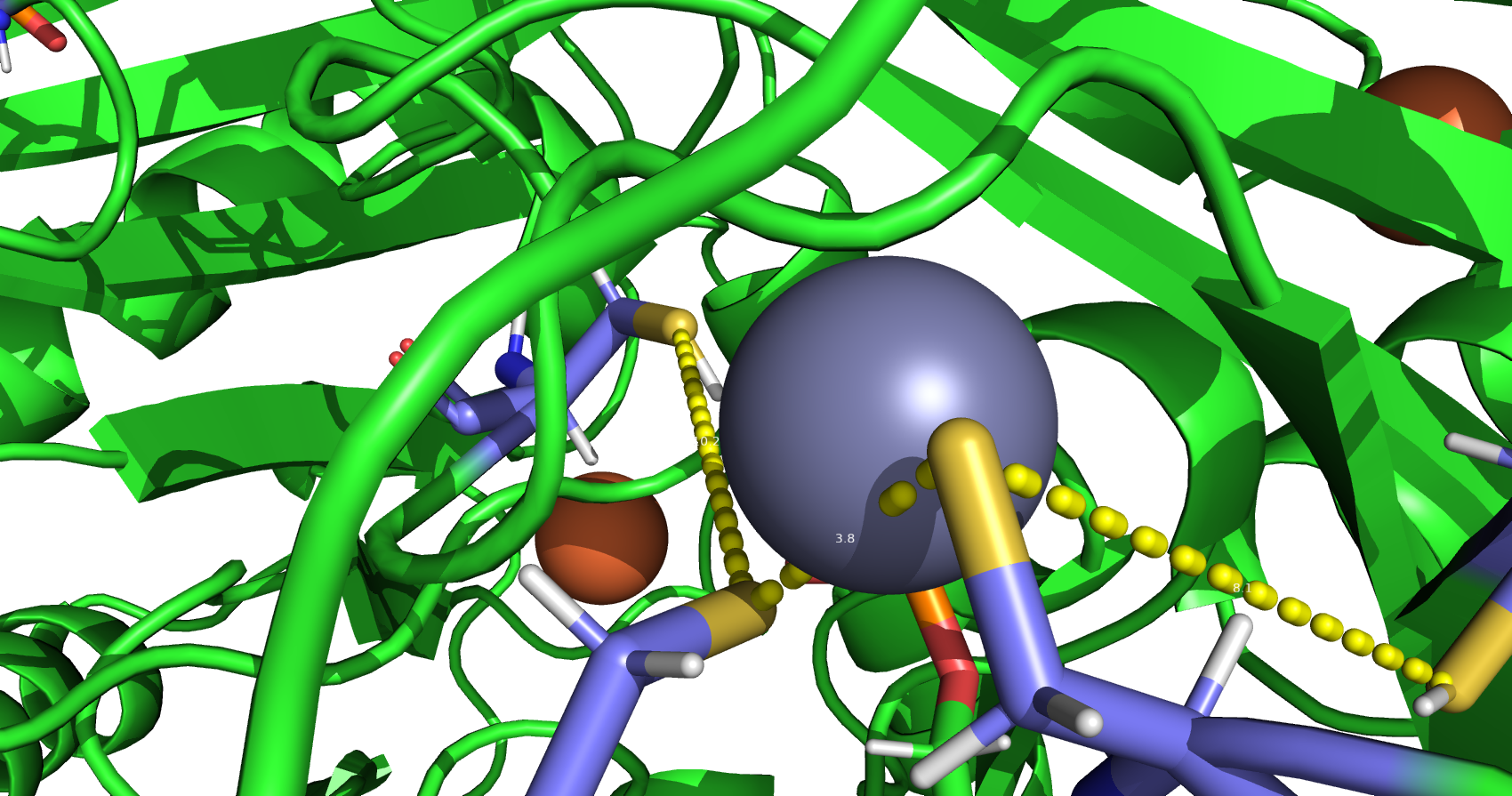
В исследуемом белке можно обнаружить множество водородных связей, затрагивающих атомы остова белка (пример на рис. 4), а также атомы боковых радикалов его аминокислот (пример на рис. 5). Кроме того, в структуре обнаруживаются солевые мостики между положительно и отрицательно заряженными аминокислотами (пример на рис. 6), а также некоторое количество стэкинг-взаимодействий между ароматическими системами радикалов гидрофобных аминокислот (пример на рис. 7). Дисульфидных связей в белке обнаружено не было (см. рис. 8), несмотря на то, что в белковых карманах каждой из цепей присутствуют группы близко расположенных цистеиновых остатков, однако, не образующих цистеиновых мостиков. Такое их расположение объясняется необходимостью координировать ионы цинка (см. рис. 9), а отсутствие дисульфидных мостиков также можно связать с внутриклеточной цитоплазматической локализацией исследуемого фермента, что предполагает его нахождение в восстановительной среде, препятствующей образованию дисульфидных связей и способствующей восстановлению цистеиновых радикалов.
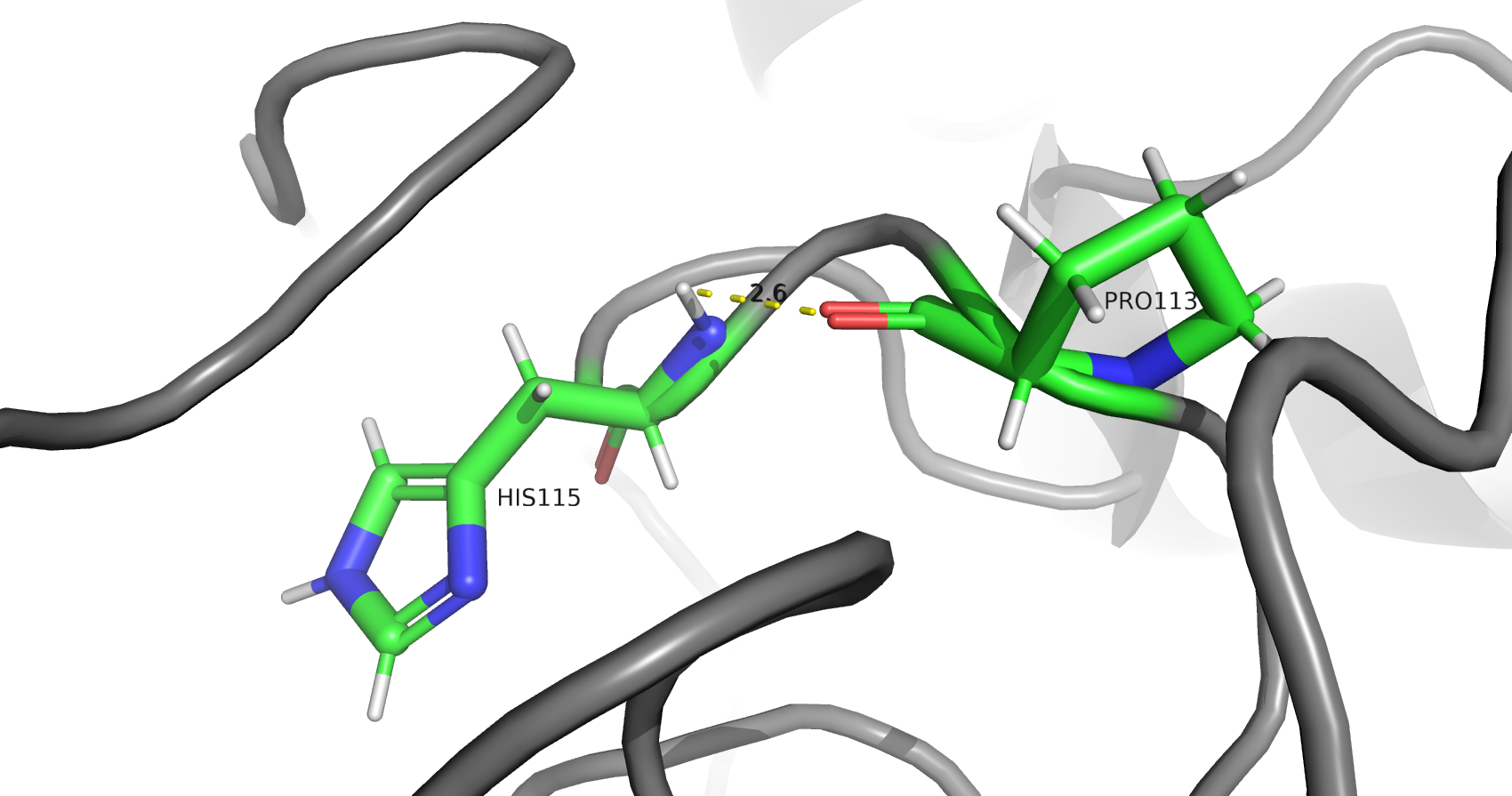
МАЛЫЕ МОЛЕКУЛЫ
В записи присутствуют такие малые молекулы, как уридин-5'-монофосфат (U5P, URIDINE-5'-MONOPHOSPHATE), ион цинка (ZN, ZINC ION) и ион железа (III) (FE, FE (III) ION), наличие которых подтверждается строками PDB-файлов для цинка, железа и уридин-5'-монофосфата.
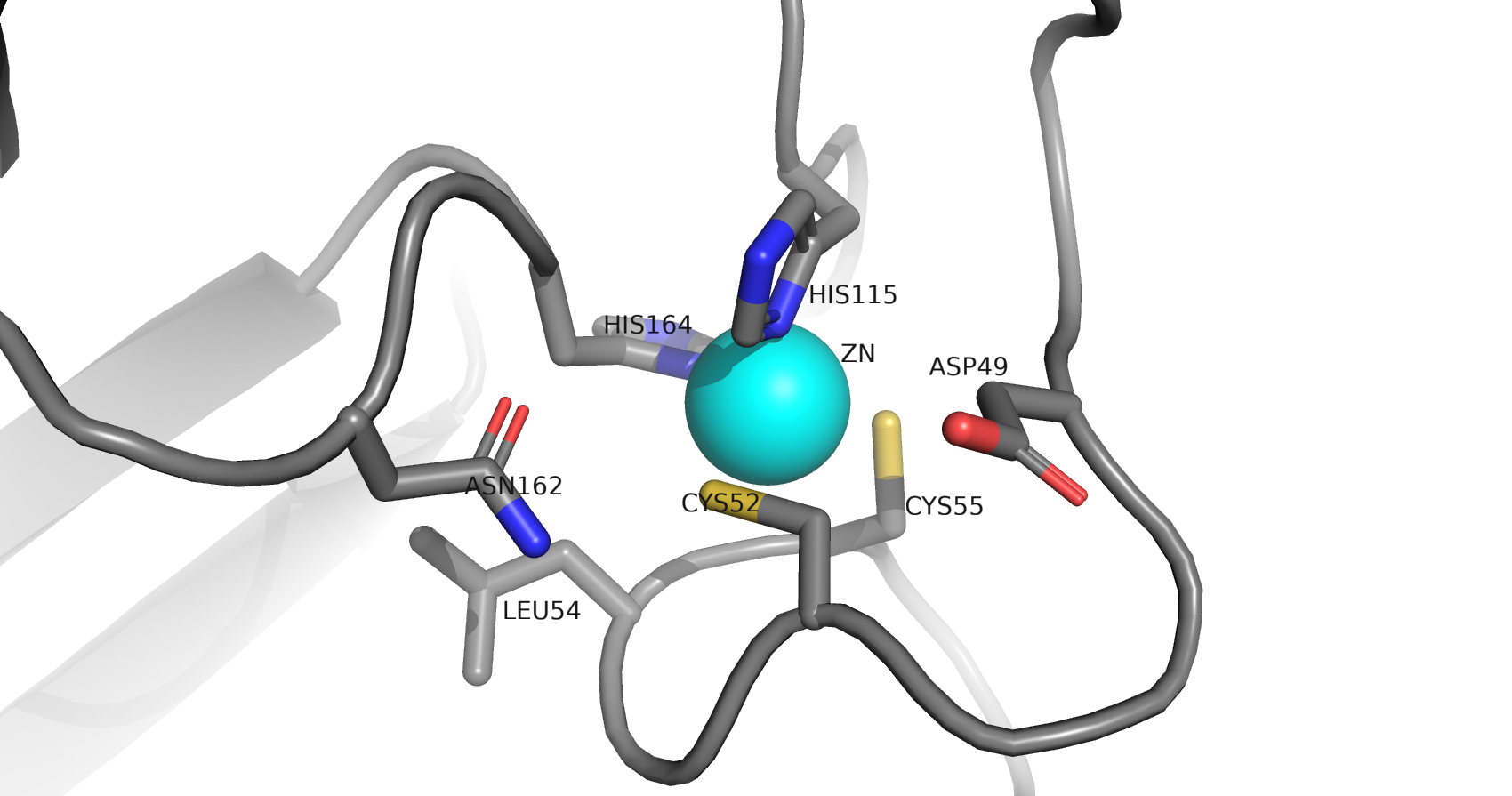
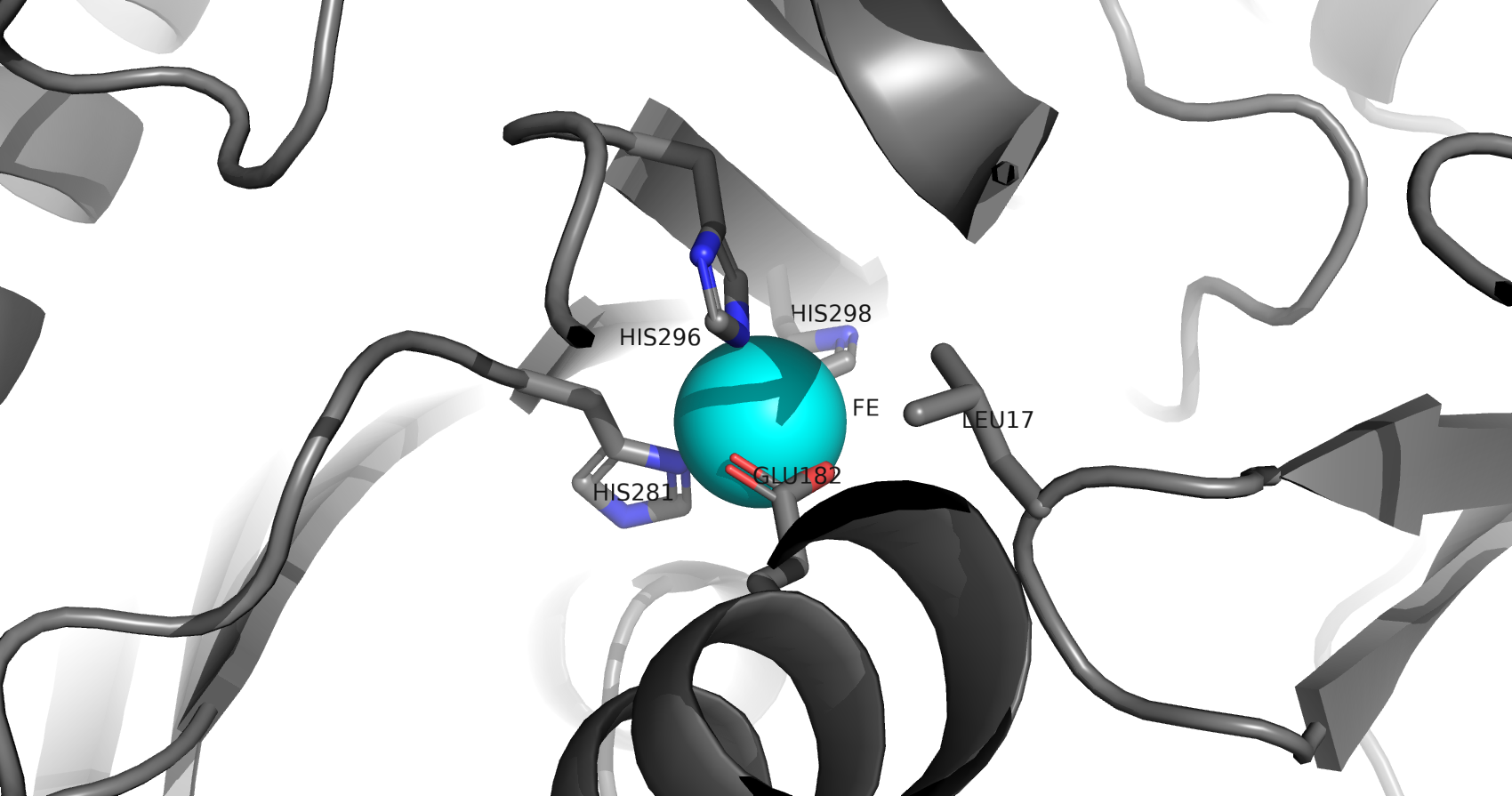
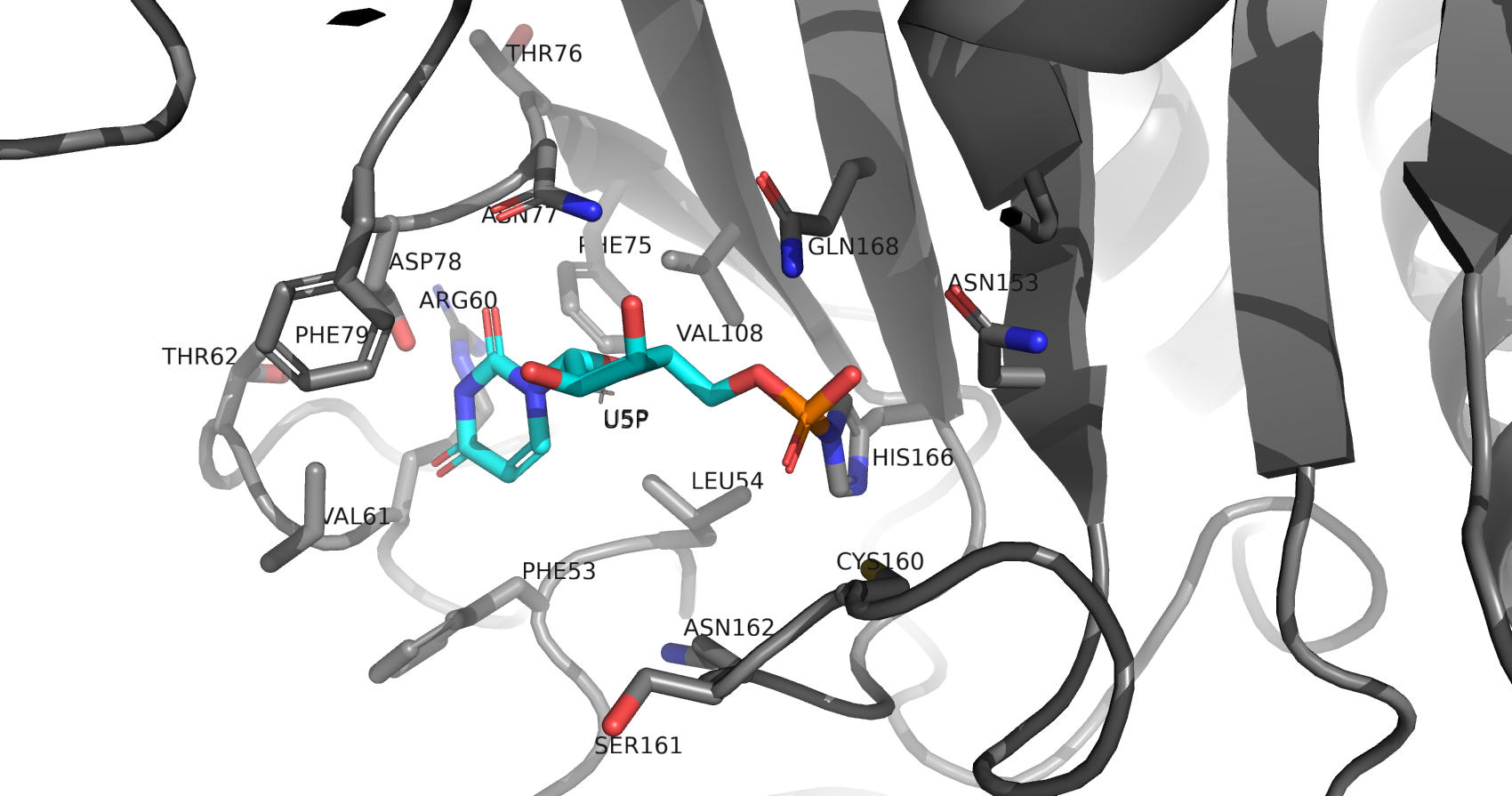
В статье, описывающей получение данной структуры, сообщается, что ион цинка присутствует в данном ферменте изначально и является "структурным", а именно координирует гистидиновый остаток в 164 позиции для корректного катализа нуклеофильной атаки остатком His-166. Ион железа же, согласно статье, также является компонентном каждой из двух субъединиц фермента, играя структурную роль. Уридин-5'-монофосфат является молекулярным фрагментом, который данный фермент переносит между указанными выше сахарами, и поэтому U5P принимает участие в образовании промежуточного соединения с белком и временно становится его частью в клетке в ходе реакции. Это объединение происходит при уридилировании нуклеофильного гистидина-166, с которым UMP формирует стабильную ковалентную нуклеотид-ферментную связь. Таким образом, ни одна из представленных в структуре малых молекул не является артефактом или не добавлена искусственно, а все они играют структурную (ионы Fe, Zn), каталитическую (Zn) роль или являются непосредственными участниками реакции, образуя интермедиат с исследуемым ферментом (U5P).