Визуализация молекулы 1OD6 (фосфопантотеинаденилтрансферазы)
В таблице представлена информация о водородных связях во вторичной структуре молекулы 1OD6.
# |
Атомы |
Длина связи (в ангстремах) |
Угол N-O-C (в градусах) |
|---|---|---|---|
Альфа-спираль | |||
| 1 | N(137ARG)-O(133LYS) | 2.91 | 151.4 |
| 2 | N(138TYR)-O(134GLU) | 3.55 | 145.1 |
| 3 | N(138TYR)-O(135ILE) | 3.23 | 113.4 |
| 4 | N(136ALA)-O(132VAL) | 2.89 | 157.7 |
| 5 | N(135ILE)-O(131MET) | 2.95 | 153.5 |
| 6 | N(134GLU)-O(130THR) | 3.04 | 153.0 |
| 7 | N(133LYS)-O(129SER) | 2.98 | 158.6 |
| 8 | N(132VAL)-O(128SER) | 3.04 | 159.0 |
Бета-складчатый слой | |||
| 9 | N(085ALA)-O(002HIS) | 3.62 | 130.8 |
| 10 | N(004VAL)-O(085ALA) | 2.98 | 156.6 |
| 11 | N(087VAL)-O(004VAL) | 2.86 | 147.2 |
Средняя длина водородной связи во вторичной структуре этого белка составляет 3.10 ангстрем, что соответствует данным компетентного источника [4] о длине водородной связи от 2.6 до 3.3 ангстрем.
Заметим, что 3 водородная связь в альфа-спирали не согласуется с формулой "i - i+4" и угол связи сильно выпадает из среднего значения, поэтому в расчетах среднего угла не будем учитывать эту связь. Средний угол связи составил 144.9 градусов в бета-структурах и 154.0 градусов в альфа-спирали, что отличается от идеального развернутого угла на 35.1 и 26 градус соответственно при максимально возможном отклонении в 45 градусов.
Биологическая роль фосфопантотеинаденилтрансферазы
Молекула относится к группе нуклеотидилтрансфераз, в данном случае фермент присоединяет к субстрату адениловую кислоту. Фермент катализирует реакцию формирования из 4'-фосфопантотеина и адениловой кислоты дефосфо-КоA:
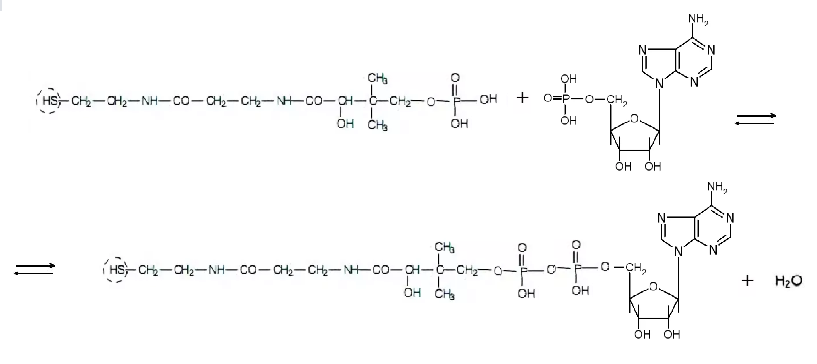
Эта реакция является предпоследней в процессе формирования кофермента A. Этот кофермент синтезируется из цистеина и пантотеновой кислоты, также известной как витамин Вз, в 5 этапов.
Показанная структура фермента встречается у модельного организма термофильной грамотрицательной бактерии T. thermophilus. Другие структуры известны у бактерий E. coli, B. subtilis, M. tuberculosis, T. maritima.
Источники:
1.Структура 1OD6 в Protein Data Bank
3.Ю. А. Овчинников "Биоорганическая химия"
4.Я. Кольман, К.Г. Рём "Наглядная биохимия"




