Общая характеристика структуры
Рассматриваемая молекула из базы данных Protein Data Bank (PDB) — белок диизопропилфторфосфатаза. Структуру данной молекулы можно увидеть на рисунке 1.
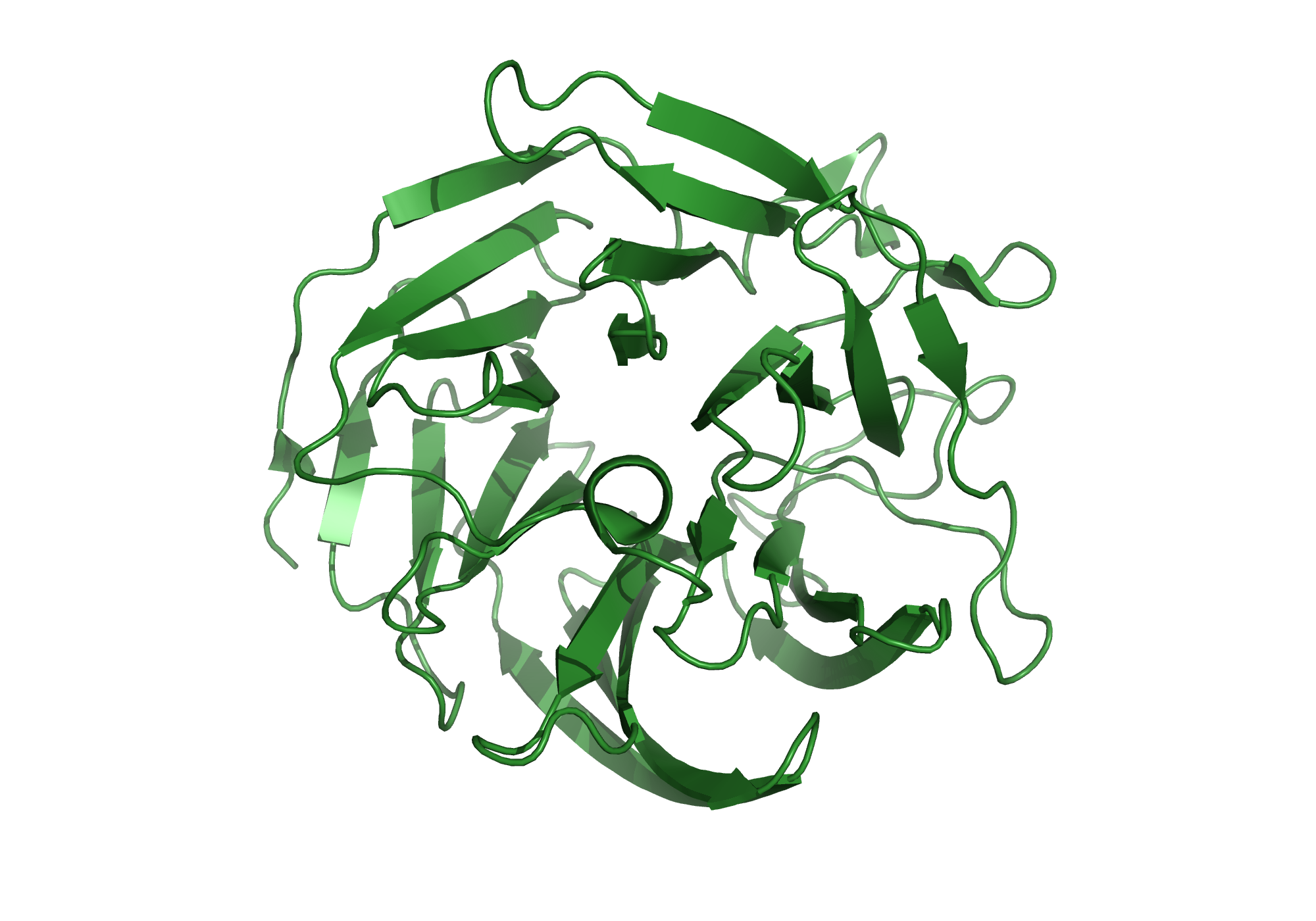
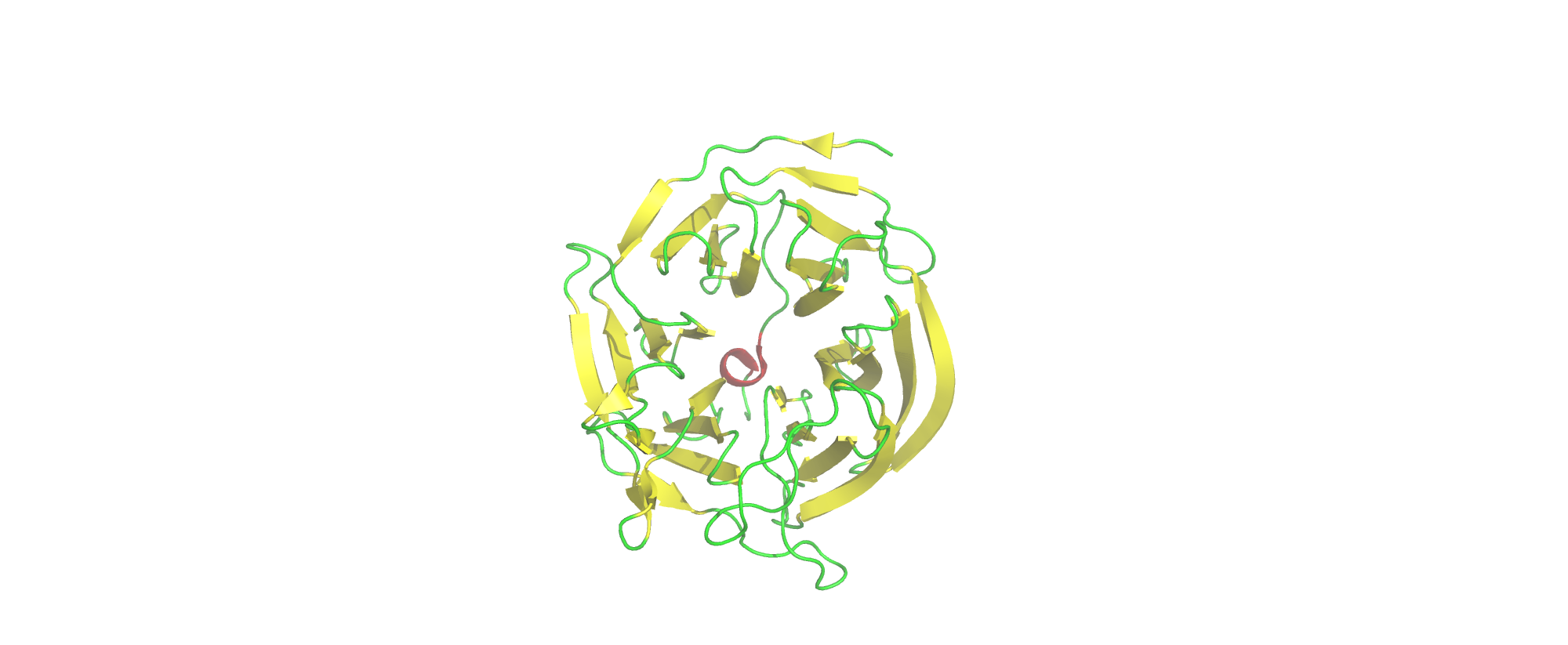
В структуре белка присутствует одна полипептидная цепь (А-цепь). В состав одной биологической единицы также входит одна А-цепь, что соответствует мономерной организации белка.
Отдельные цепи
А-цепь
Единственная А-цепь рассматриваемого белка относится к организму Loligo vulgaris. Её UniProt ID: Q7SIG4.
Согласно базе UniProt, данный белок является ферментом и катализирует гидролиз фосфорорганических соединений. Его каталитическая активность описывается следующей реакцией:
диизопропилфторфосфат + H2O → диизопропилфосфат + F- + 2H+
Мутаций относительно референсной последовательности UniProt обнаружено не было. Модифицированные аминокислотные остатки в структуре также отсутствуют.
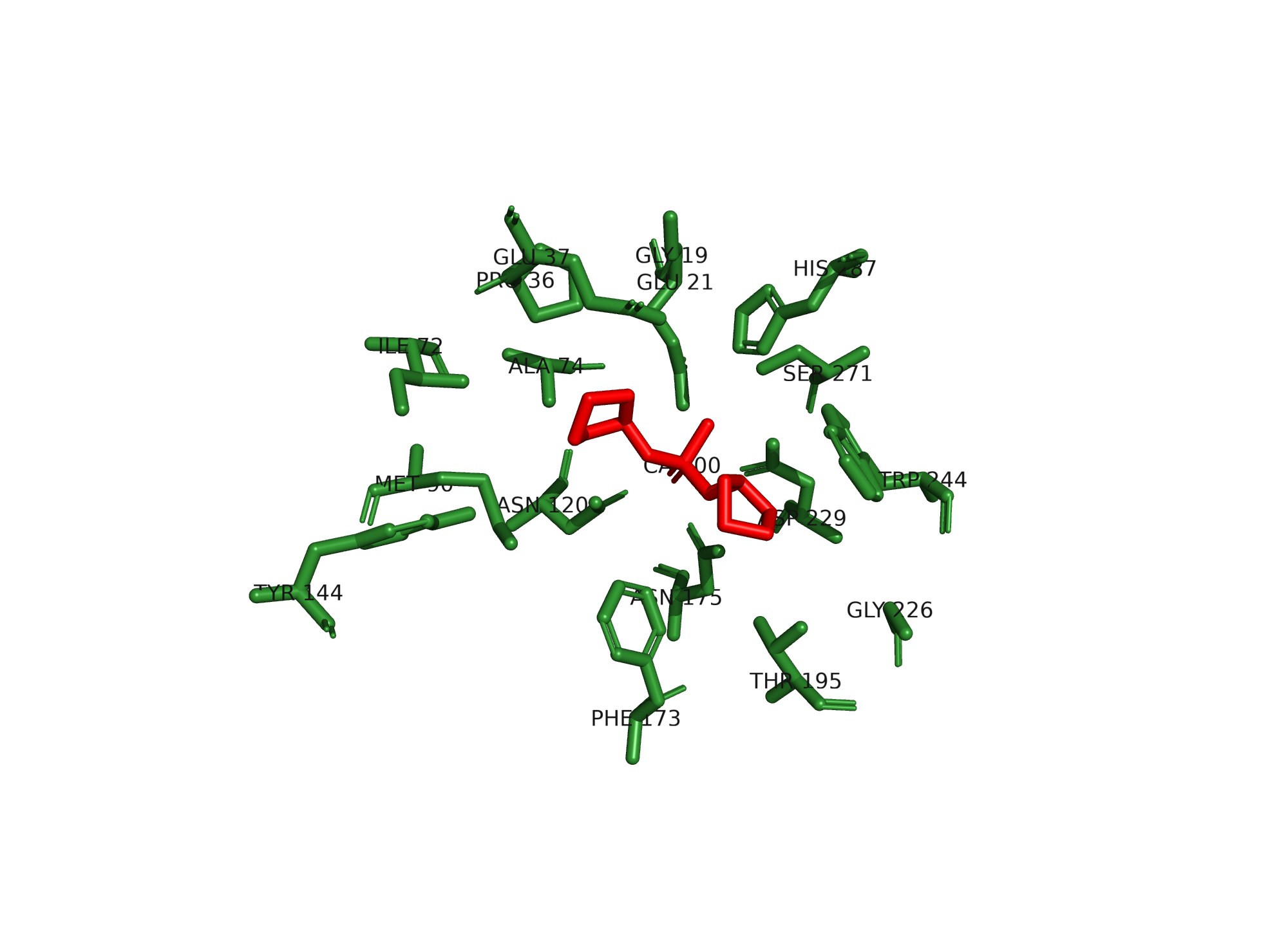
Малые молекулы
В структуре белка присутствуют следующие малые молекулы:
- DI9 — DICYCLOPENTYL PHOSPHORANIDATE
- Ca — ион кальция (CALCIUM ION)
Здесь можно найти файл со строками PDB, содержащими информацию о данных молекулах.
Согласно статье, приведённой в базе PDB, малые молекулы функционально связаны с каталитической активностью белка. Остаток D229 координирует ион кальция, который участвует в активации субстрата. В сочетании с прямой координацией ионом металла атом фосфора субстрата становится более электрофильным и уязвимым для нуклеофильной атаки молекулы воды, что приводит к образованию промежуточного фермент-субстратного комплекса.