Изучал структуры двух расшифровок белка рецептора гамма-аминомасляной кислоты (pdb_id 6YOO и 5DPT).
Особых различий между структурами, которые сразу бы бросались в глаза, замечено не было.
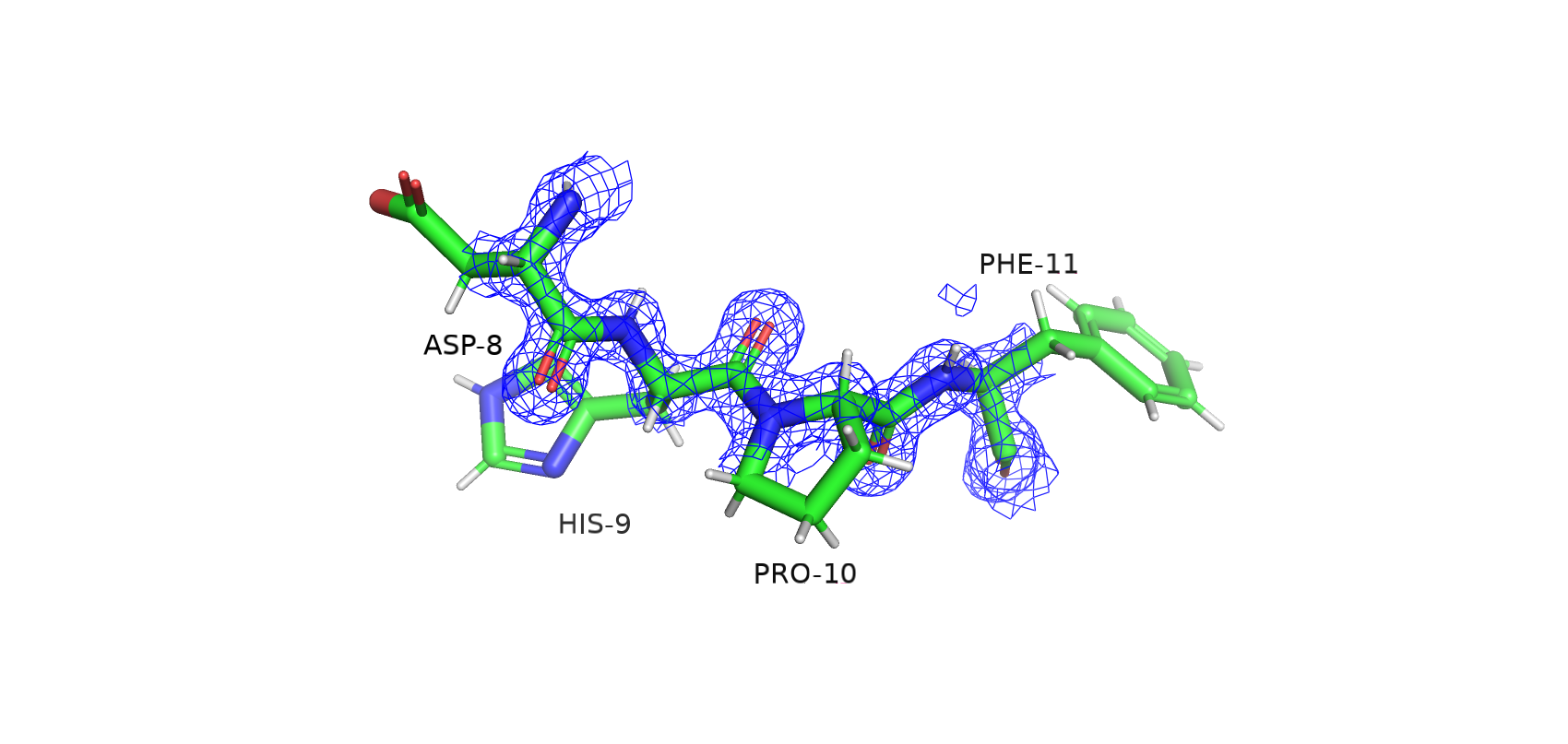
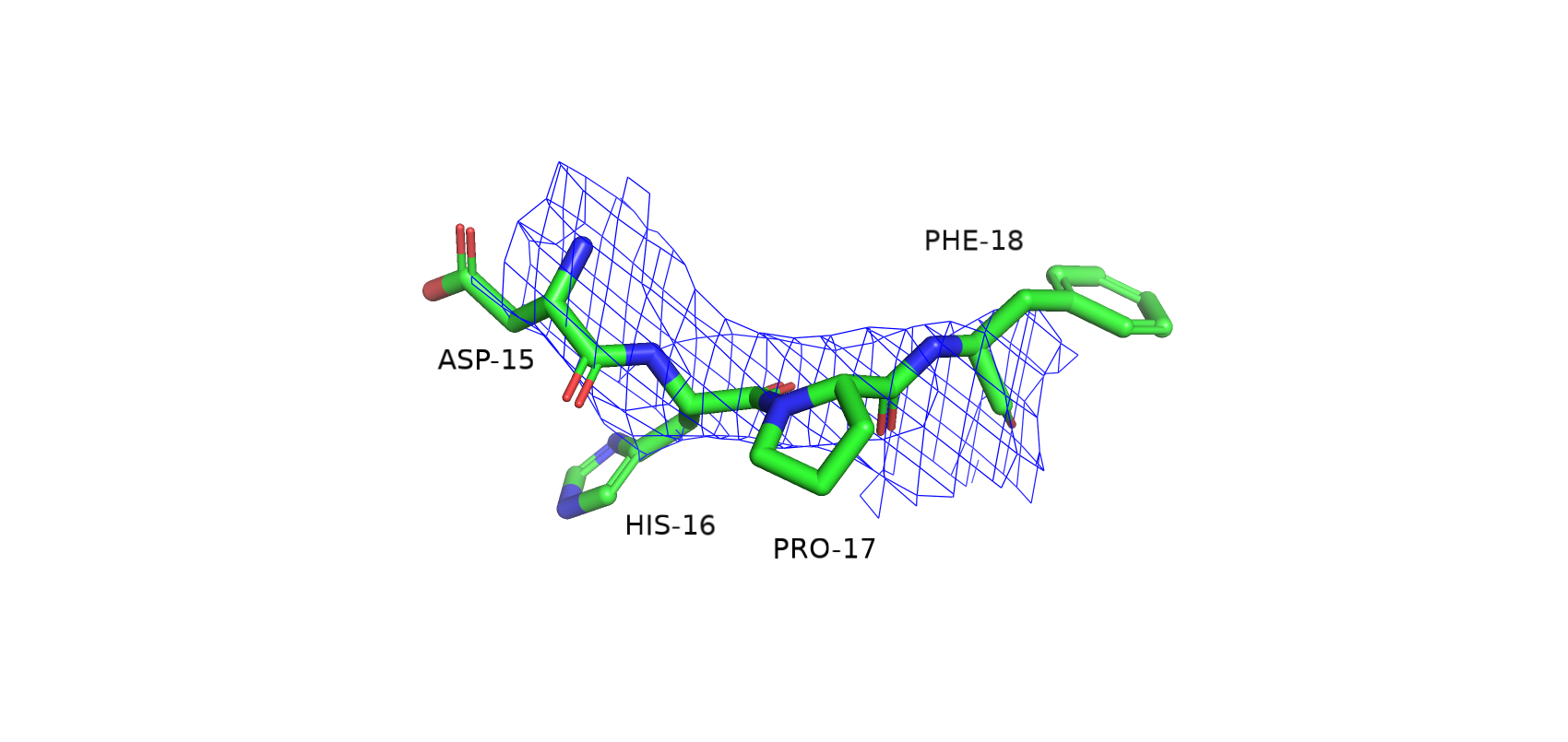
Для более подробного анализа были выбраны 2 участка (8-11 для 6YOO и 15-18 для 5DPT).


На рис.1 ЭП чётко выделяет отдельные атомы, образуя вокргу них сферы, а на рис.2 просто покрывает участок белка в общих чертах. Поэтому можно сказать, что разрешение у расшифровки 6YOO намного лучше, чем у расшифровки 5DPT.
Для подтверждения привожу значения расрешений из PDB: 6YOO - 1.06 Å, 5DPT - 2.90 Å
Для выполнения данного задания использовался один из транспортеров TRAP (pdb_id 7BCO). Ниже приведены mesh белка на уровнях подрезки 1, 2, 3, во всех случаях carve = 1.5

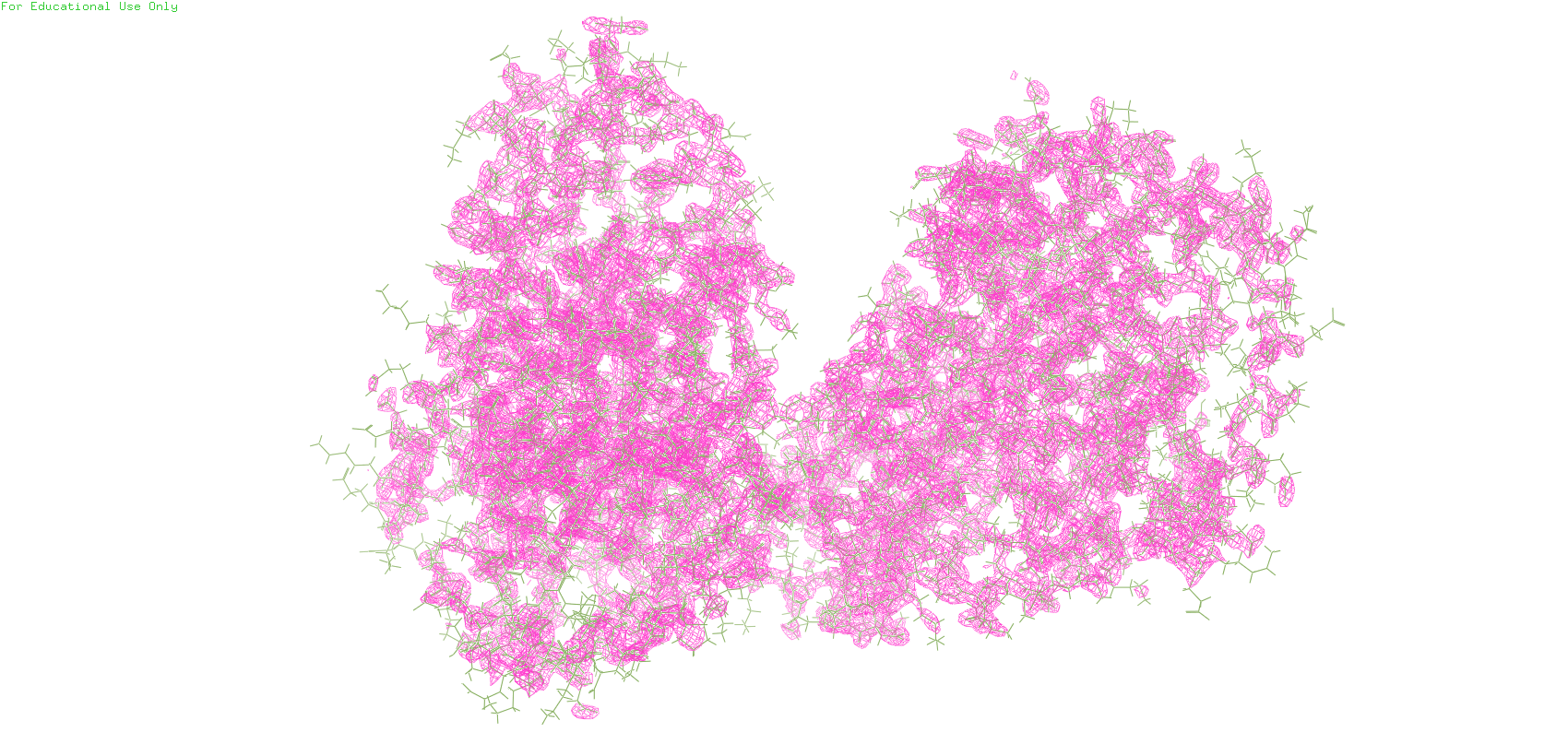
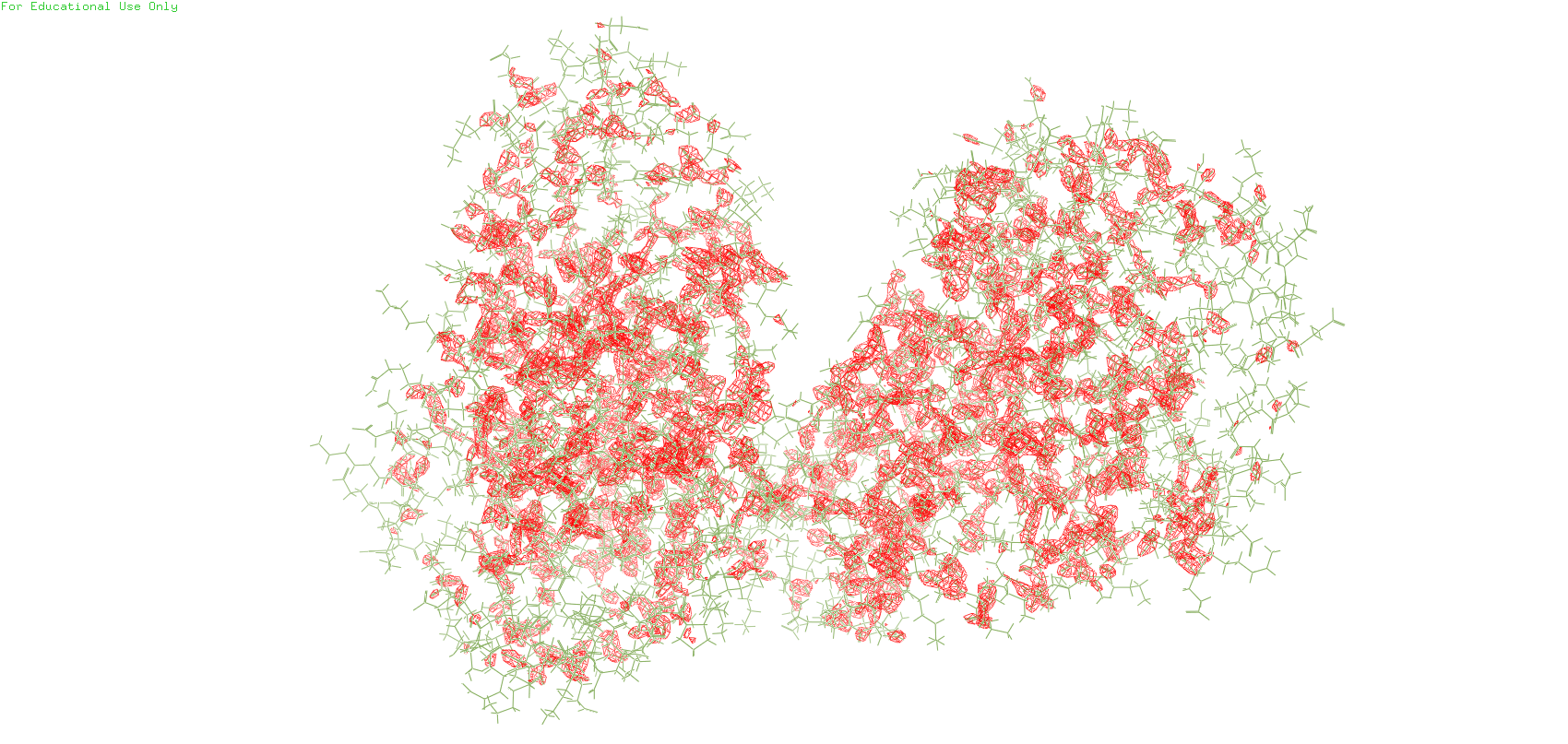
С увеличением уровня подрезки внешние атомы перестают быть покрытыми mesh'ом.
Поскольку мы описываем реконтрукцию ЭП белка, можно предположить, что на результат влияет подвижность атомов, 'размытие' ЭП. То есть если ЭП перестаёт отображаться на высоких уровнях подрезки - значит эти участки белка подвижные.
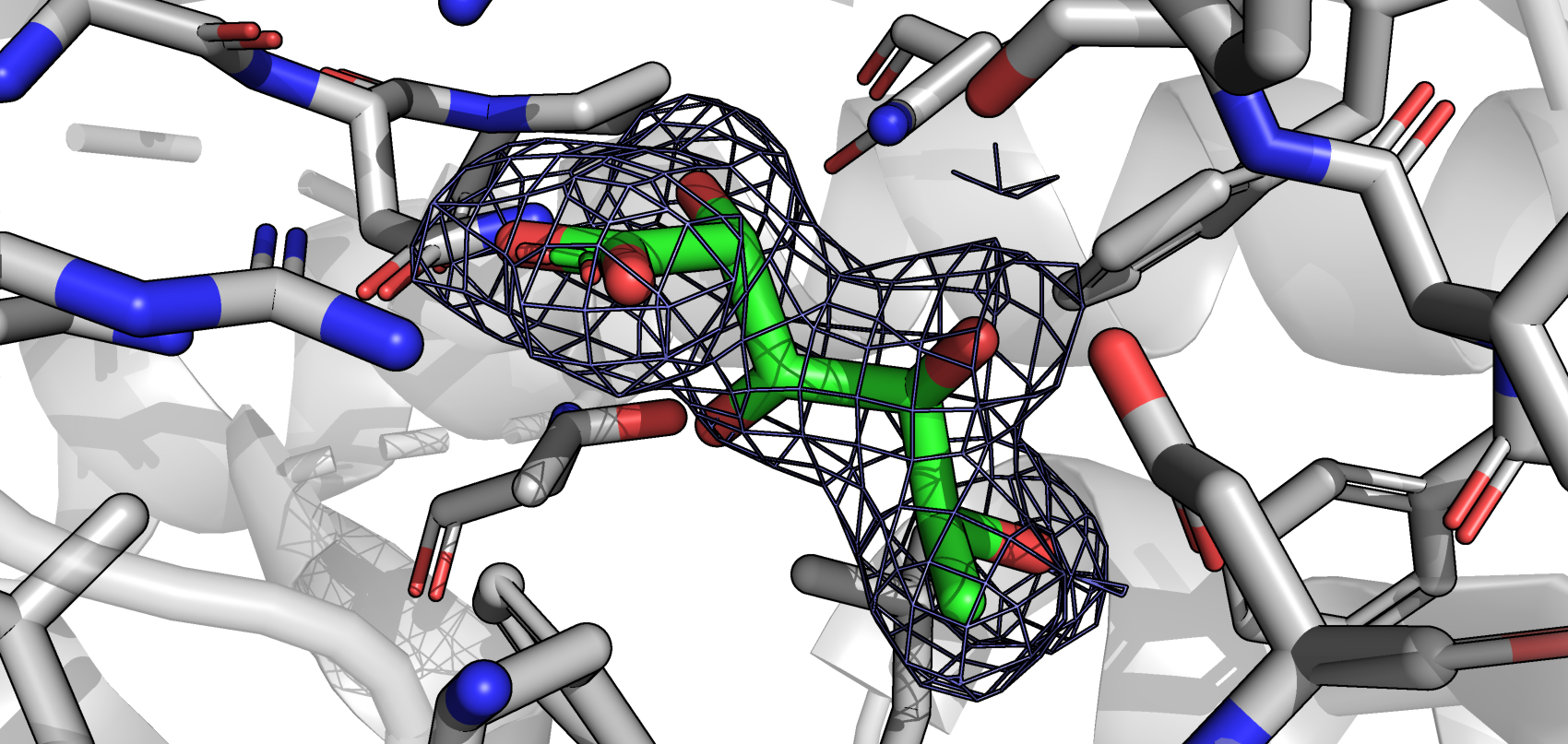
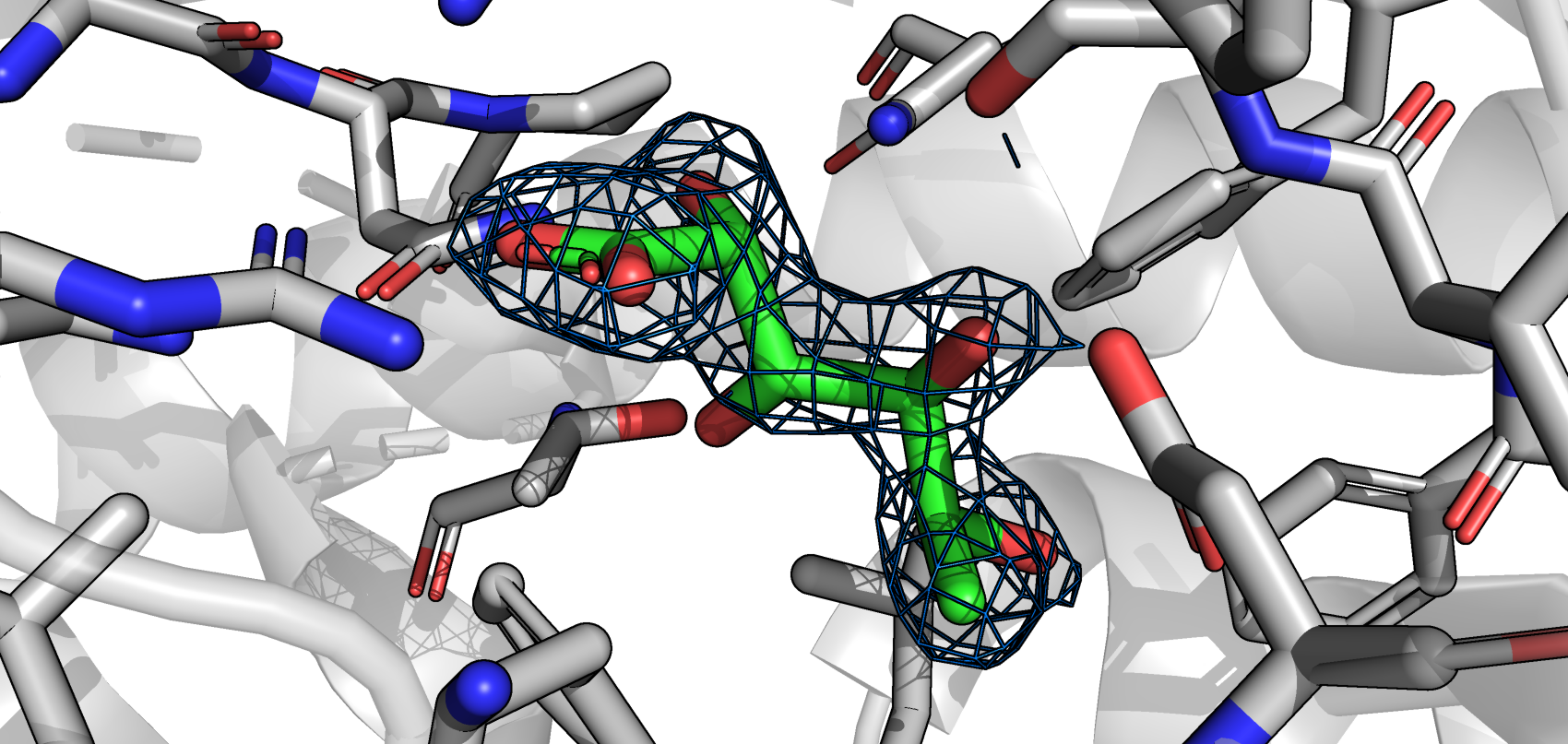
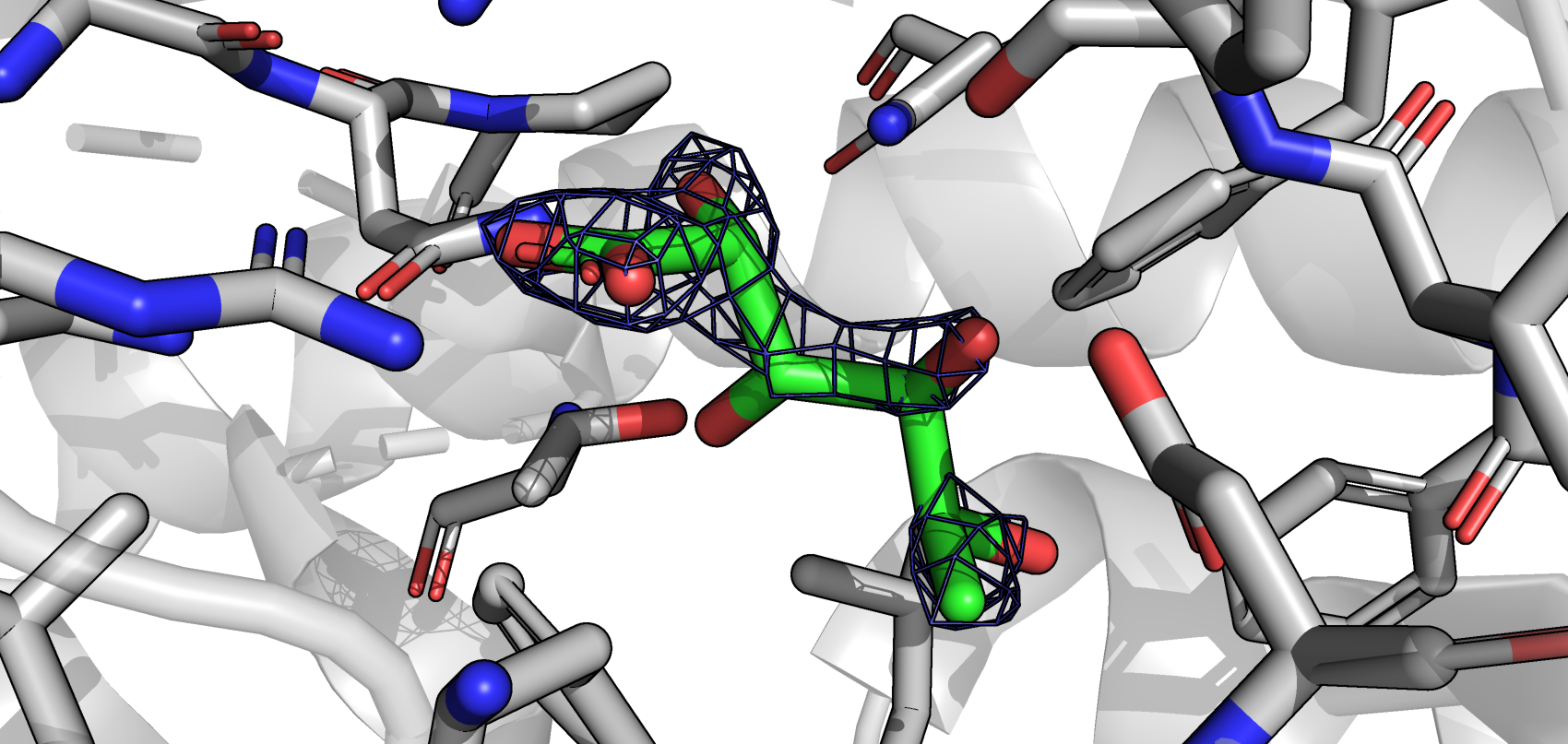
На первом уровне подрезки электронная плотность полностью покрывает молекулу. С увеличением уровня подрезки электронная плотность остаётся только в областях с кислородом, т.к. кислород оттягивает на себя электроны с углерода.
Опять же подобная реконструкция ЭП может быть связана с подвижностью - вращение вокруг С-С связей, тогда как кислороды принимают участие в водородных связях с белком и их положение не меняется.