Для работы был избран белок "PIN1 PEPTIDYL-PROLYL CIS-TRANS ISOMERASE FROM HOMO SAPIENS". Его структура разрешена методами РСА (pdb ID 1PIN) и ЯМР (pdb ID 1NMV). Разрешение РСА структуры 1.35 Å, а количество моделей в ЯМР структуре - 10. На рисунке 1 - обе структуры, наложенные друг на друга.
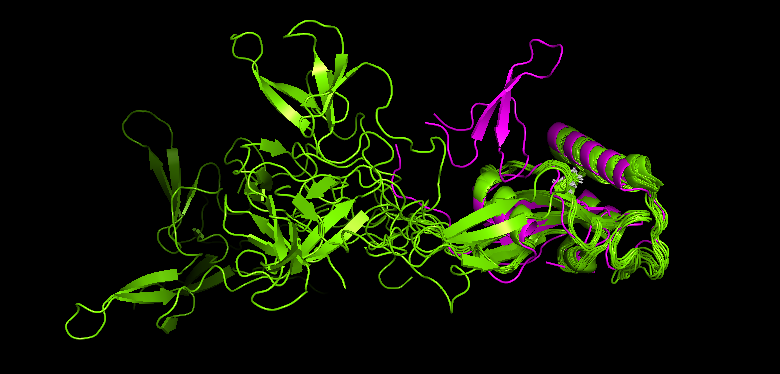
Рисунок 1. Структуры PIN1. Розовая - РСА, желтая - ЯМР (все модели).
Как можно заметить, основная часть белковой глобулы совпадает в пространстве у обеих структур, но есть и отличия: N-конец цепи в структуре РСА свернут рядом с основной частью глобулы, а в ЯМР структурах он болтается в растворе. Также видно, что в РСА структуре отсутствует часть цепи.
Рассмотрим 3 водородные связи в молекуле. Их изображения - на рисунке 2, а описание - в таблице 1. Сразу отмечу, что длины водородных связей в ЯМР структуре считались как расстояния между соответствующими тяжелыми атомами (N, O), чтобы можно было сравнивать с длинами связей в РСА структуре, так как там водородов нет.
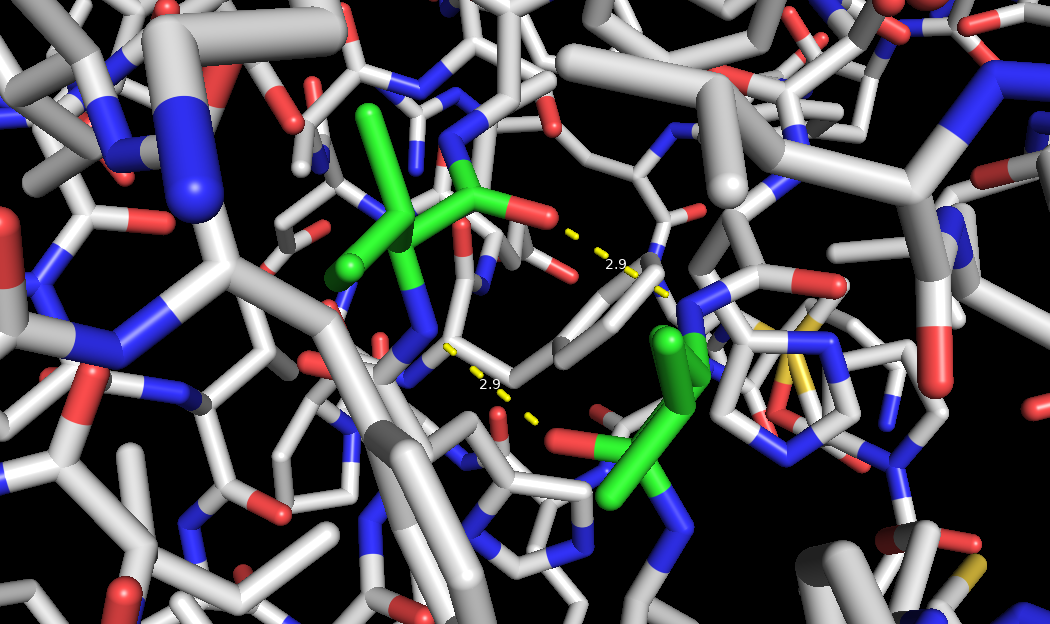
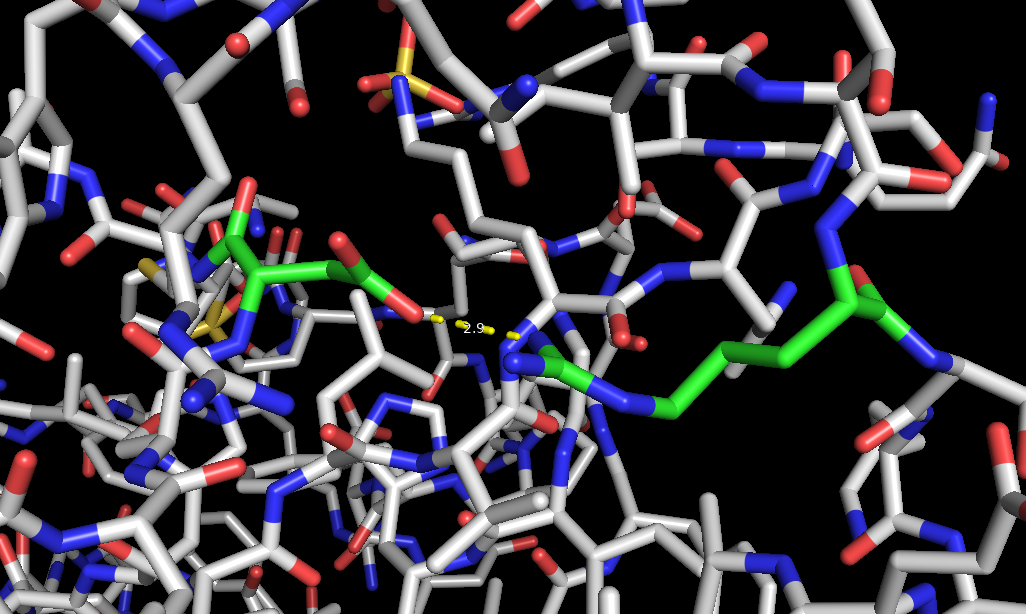
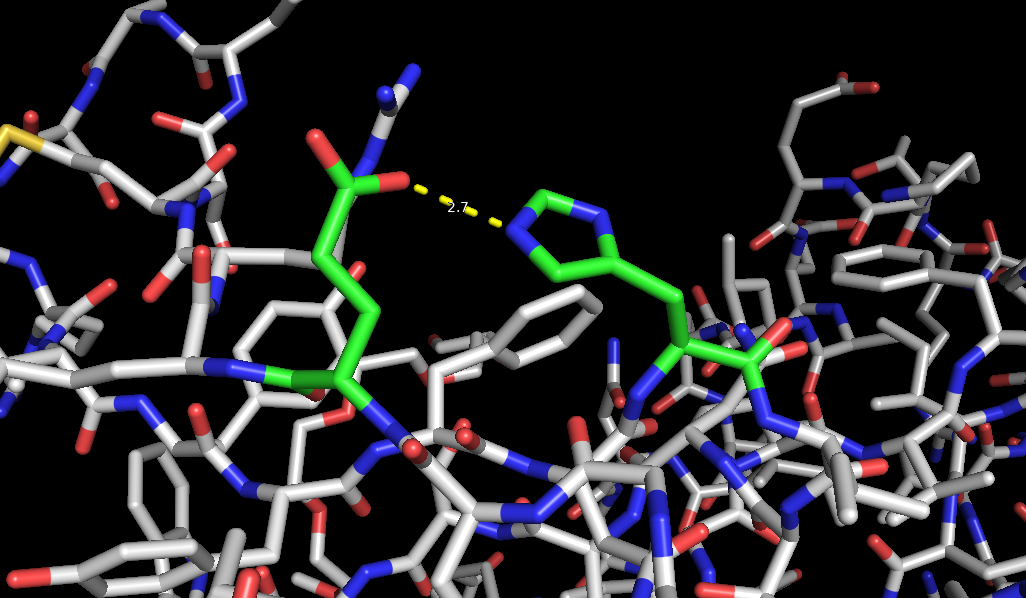
Рисунок 1. Водородные связи в молекуле PIN1. Слева - водородные связи бета-листа, в центре - водородные связи боковых цепей в ядре структуры, справа - водородные связи боковых цепей на поверхности.
| Таблица 1. Сравнение водородных связей в структурах PCA и ЯМР | ||||||
|---|---|---|---|---|---|---|
| Остатки | Описание | Длина связи, Å (РСА) |
Число моделей со связью (ЯМР) |
Min длина связи, Å (ЯМР) |
Max длина связи, Å (ЯМР) |
Median длина связи, Å (ЯМР) |
| Остовы β-листа |
2.9 | 10 | 3.0 | 3.3 | 2.9 | |
| 2.9 | 10 | 2.8 | 3.2 | 3.2 | ||
| Боковые цепи в ядре | 2.9 | 2 | 2.9 | 2.9 | 2.9 | |
| Боковые цепи на поверхности | 2.7 | 1 | 3.5 | 3.5 | 3.5 | |
Строго говоря, мне не удалось найти "чистые" водородные связи между боковыми цепями, представленные связи скорее электростатические. Как можно заметить, в бета-листе водородные связи сохранились во всех моделях ЯМР, лишь их длина варьировалась. Кстати, длина водородных связей в ЯМР в среднем больше, чем в РСА, чтоможет говорить о "набухании" структуры в растворе. С другой стороны, водородные связи боковых цепей, особенно на поверхности структуры, наблюдались лишь в немногих моделях ЯМР, что говорит об их нестабильности в растворе.