Электронная плотность в PyMol
1. Кристаллография с разным разрешением
Я изучала расшифровки с PDBID 6KAX и 6L36. Это кристаллографические расшифровки лиганд-связывающем домене (LBD) человеческого PPARα. Характеристика расшифровок:
| 6KAX | 6L36 | |
|---|---|---|
| Разрешение | 1.23 Å | 3.30 Å |
| Характеристики белка | 273 амк, 31.2 кДа | 273 амк, 64.01 кДа |
| Лиганды | Пальмитиновая кислота, глицерол | 2-[4-(4-хлорбензоил)фенокси]-2-метилпропановая кислота, 2-хлор-5-нитро-N-фенилбензамид |
Структуры белков:
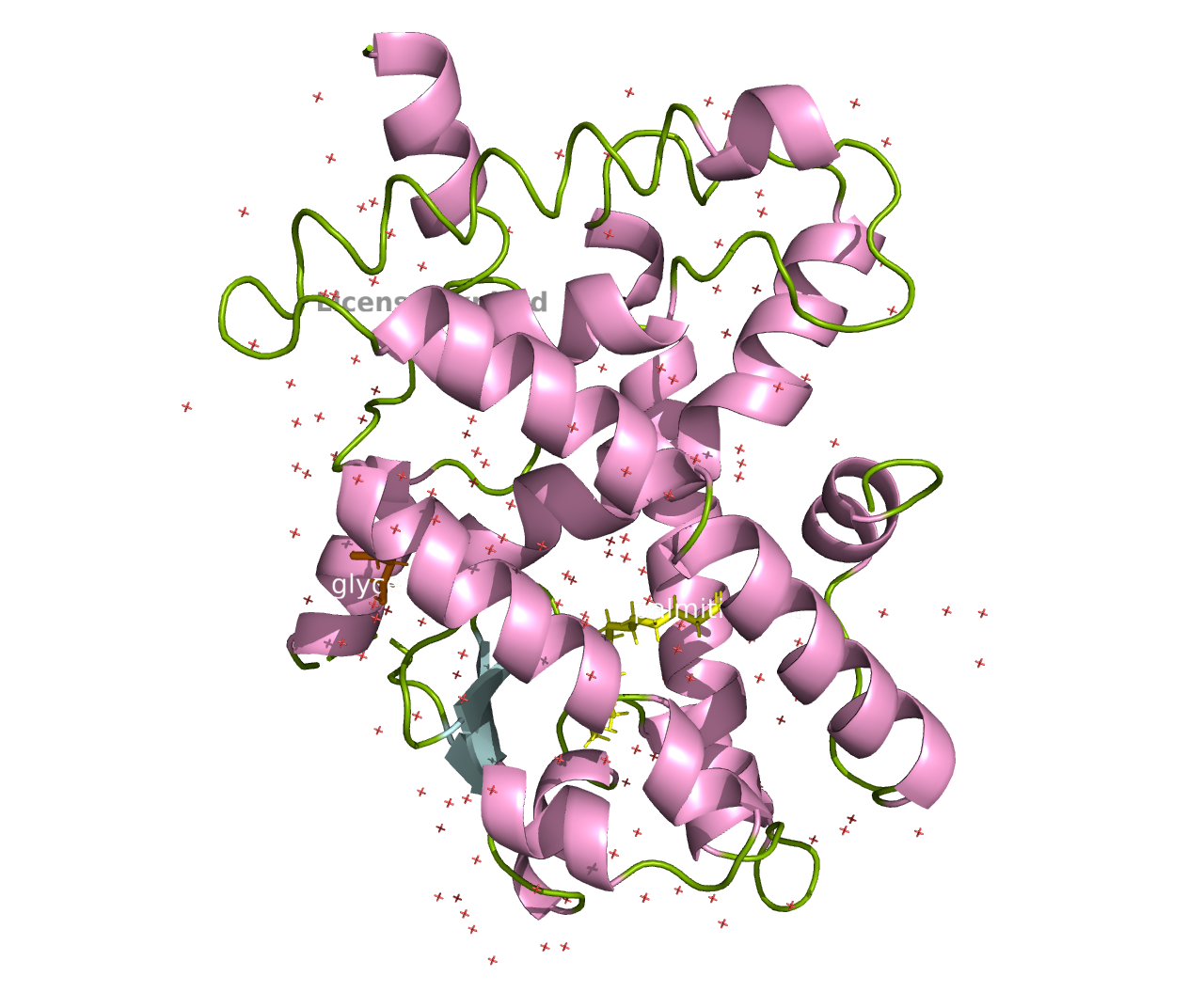
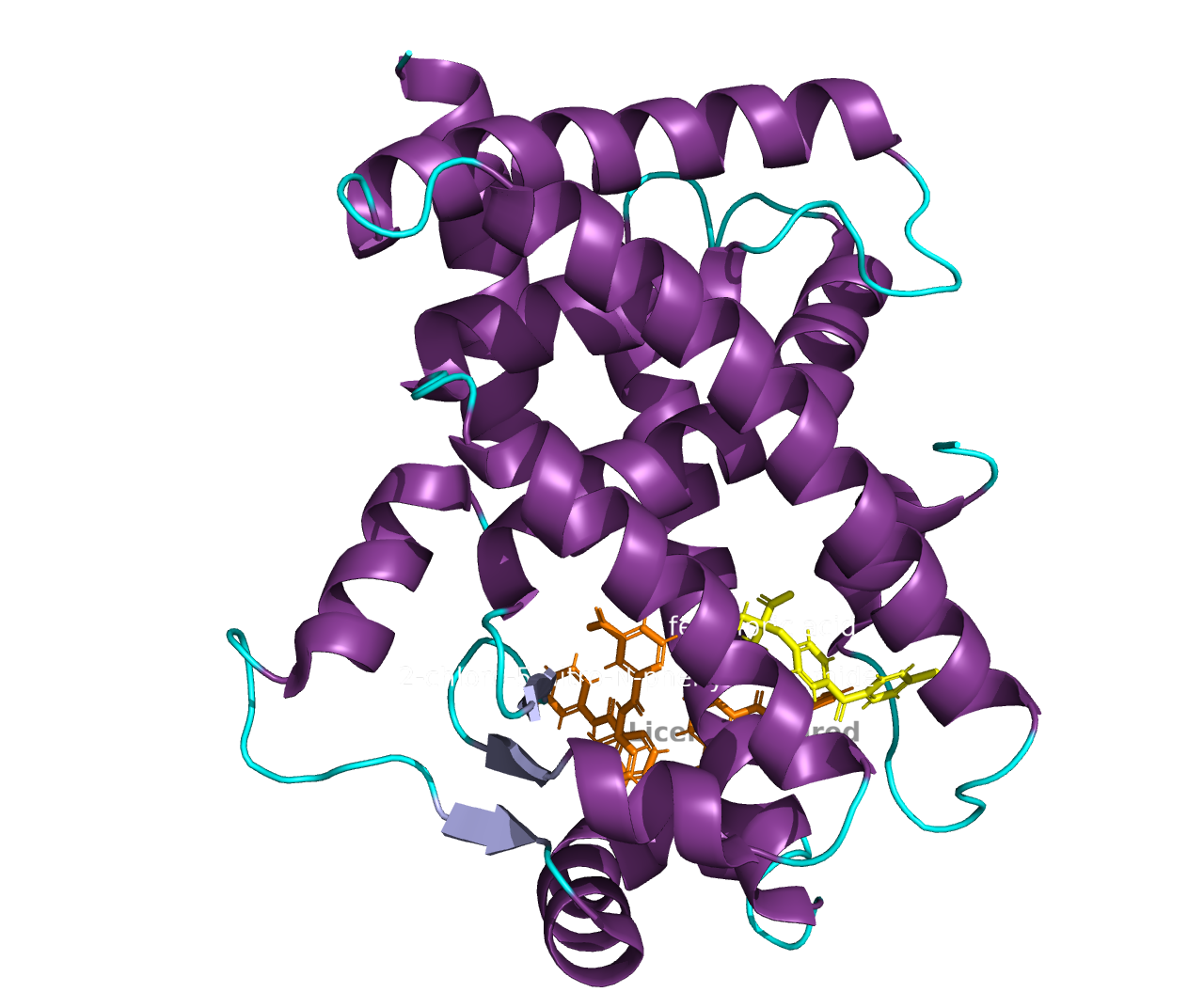
Для оценки схожести структур убрала воду, лиганды и выровняла структуры:
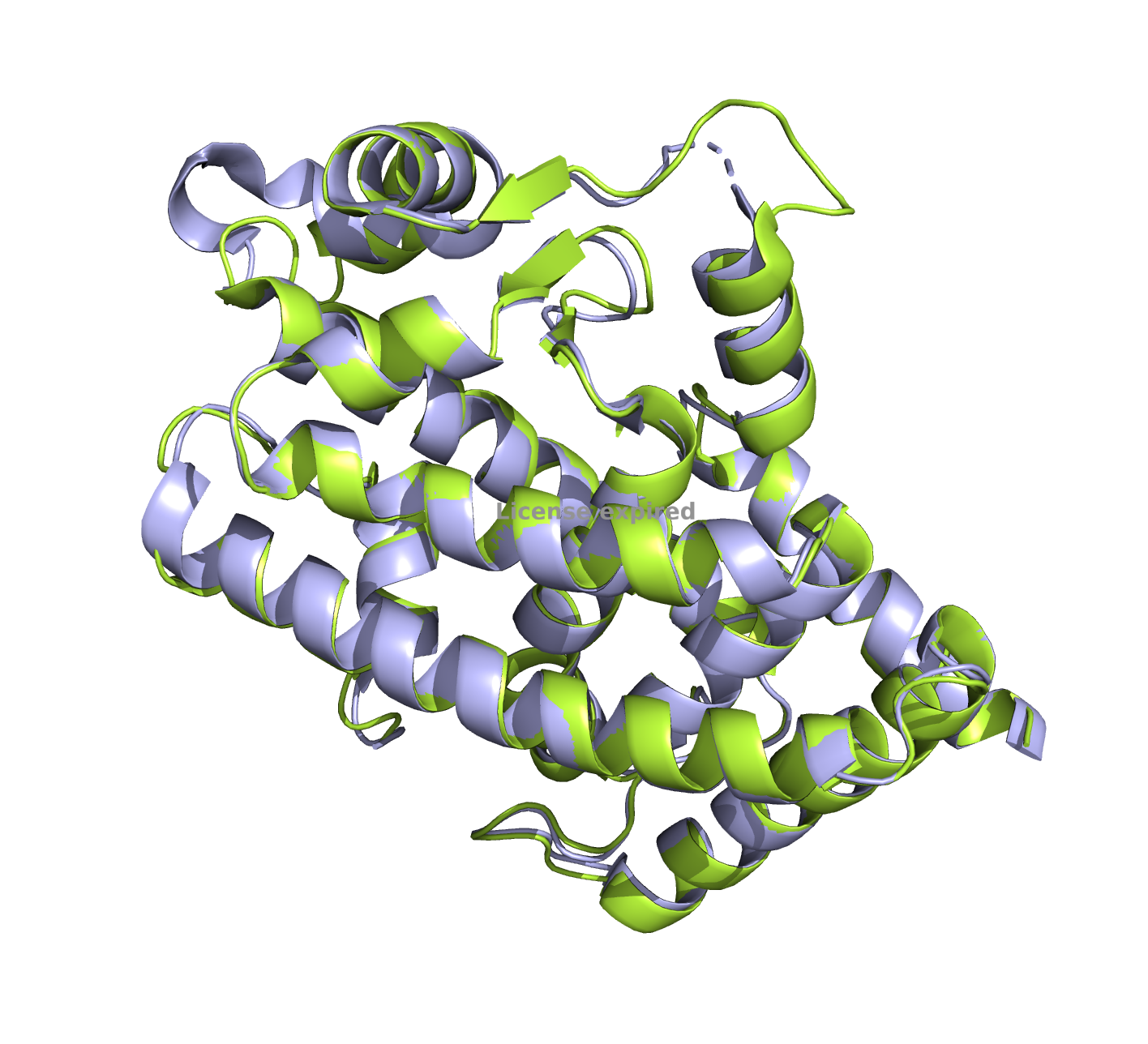
Видно, что молекулы очень похожи и можно заметить только небольшие отличия в структуре в зависимости от разрешения. В левом нижнем углу (в районе 325-326 остатков) при большем разрешении есть бета-слой, при низком разрешении его не видно. Так же при большем разрешении есть пропуск в районе 236 атома. которого нет при меньшем разрешении. Так же несколько иначе выглядит положение цепей в районе 260-267 остатков, рассмотрим поближе.

Но по большей части структуры совпадают:

Для несовпадающего региона я посмотрела жлектронную плотность на уровнях подрезки 1, 2 и 3:
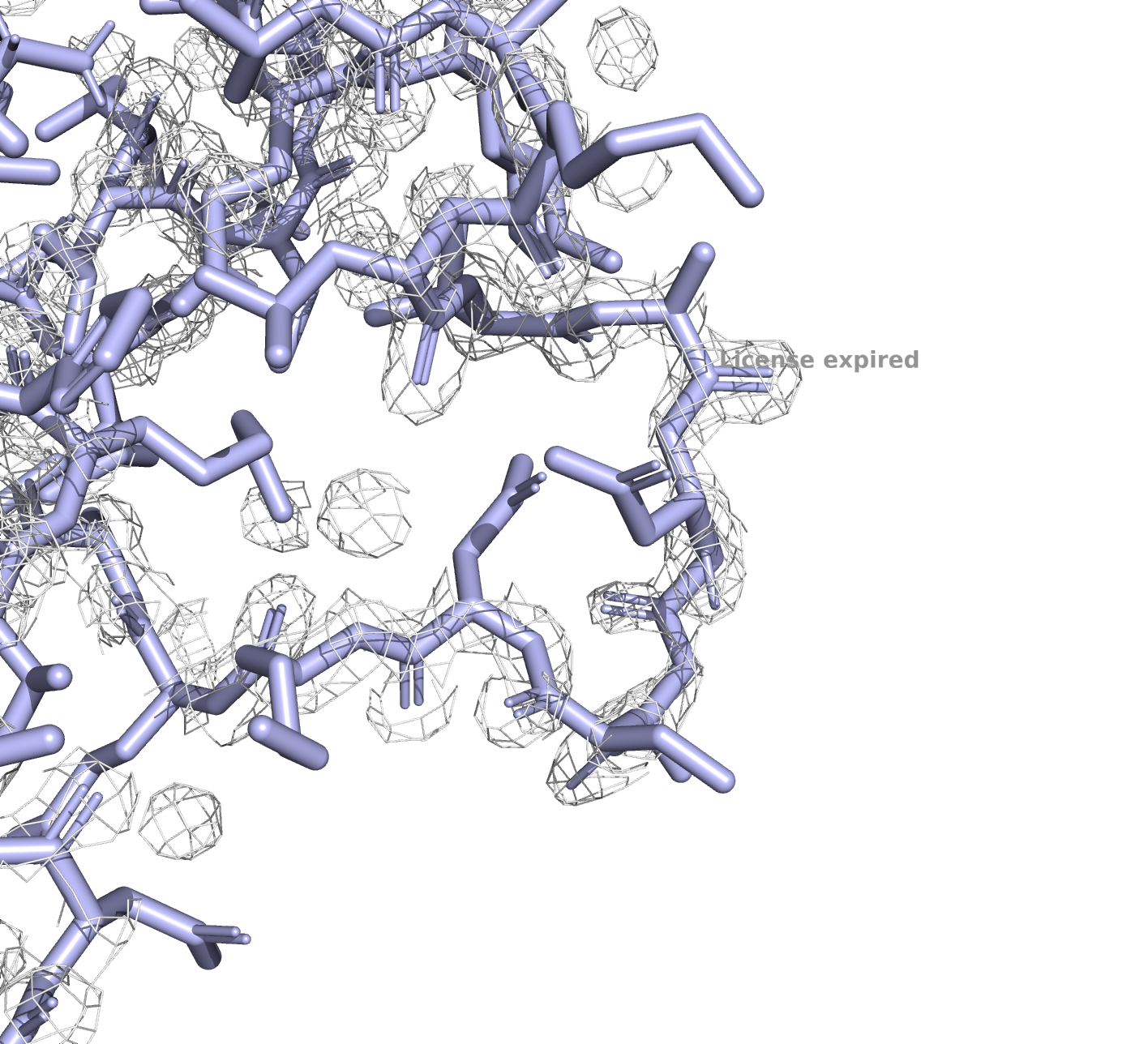
6kax, уровень подрезки 1
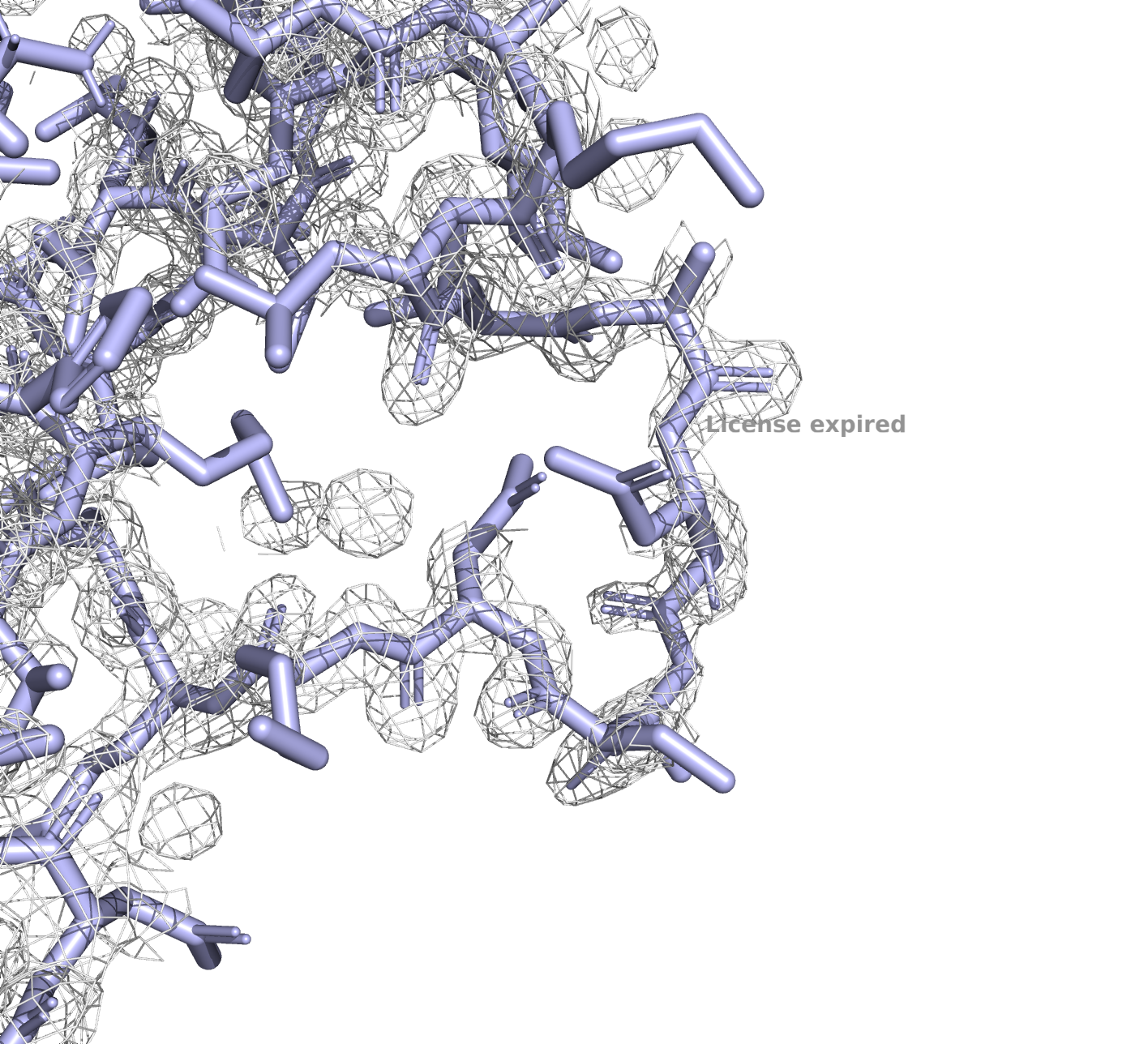
6kax, уровень подрезки 2
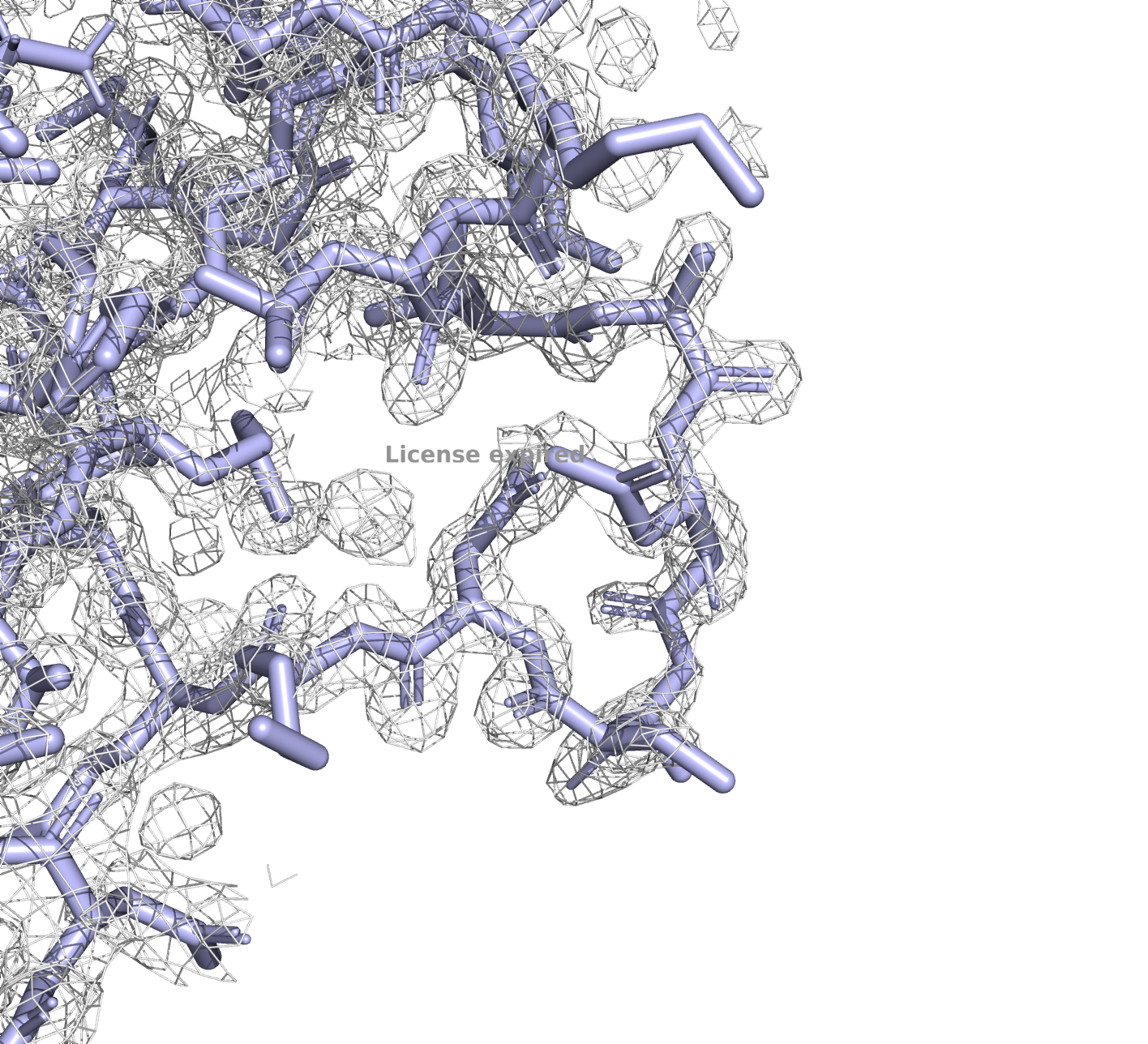
6kax, уровень подрезки 3
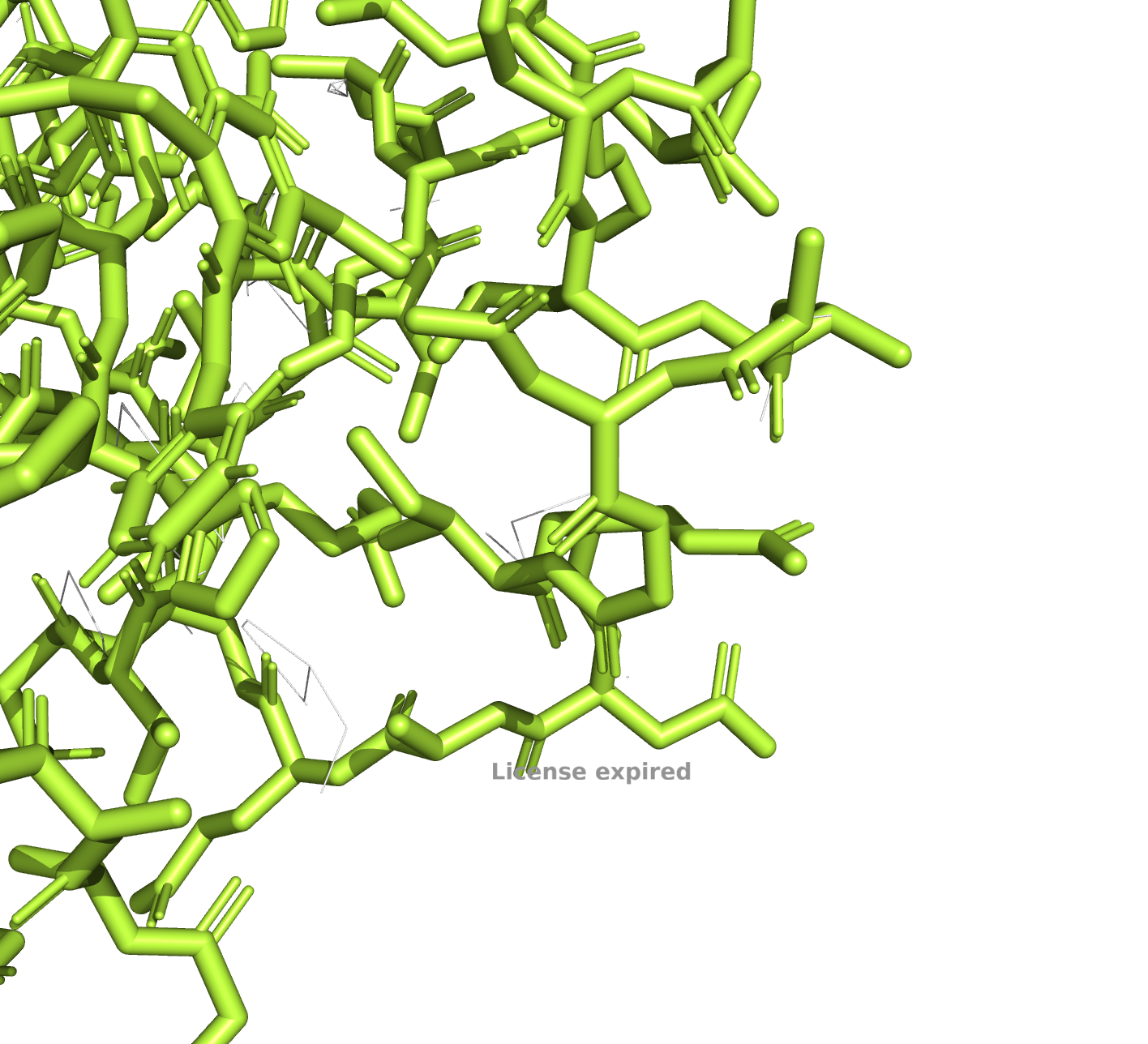
6l36, уровень подрезки 1
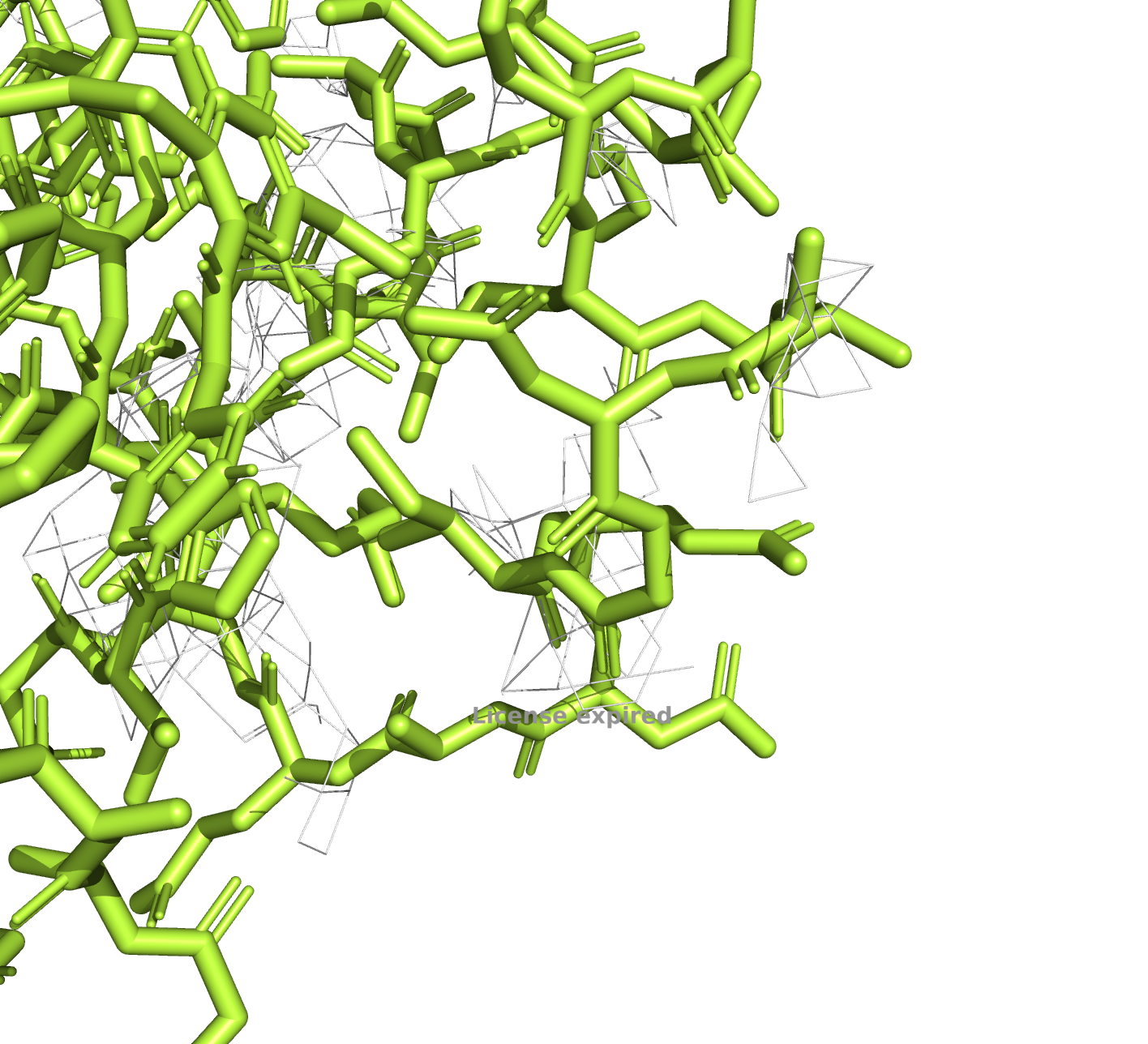
6l36, уровень подрезки 2
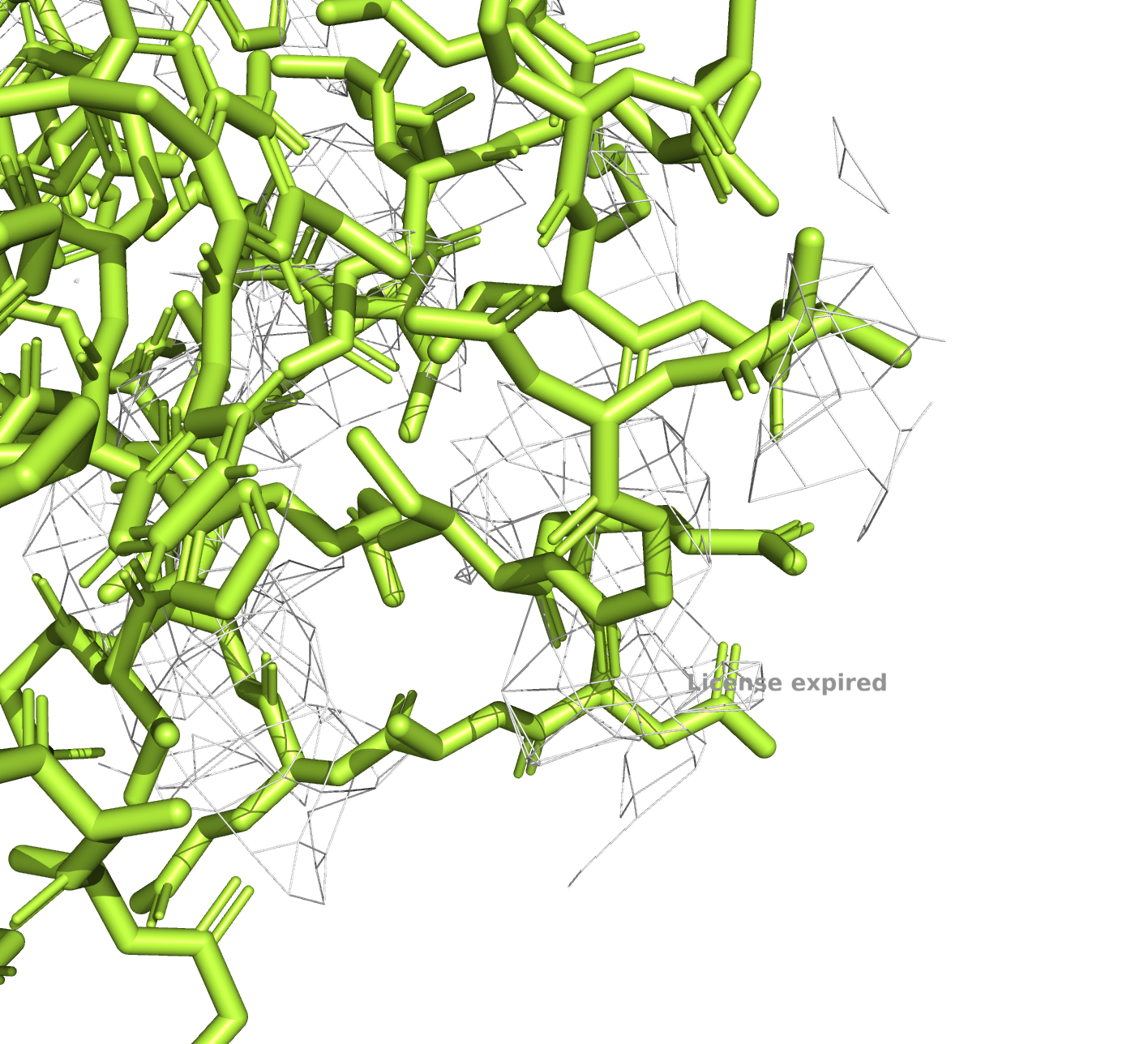
6l36, уровень подрезки 3
У PDB с разрешением в 3.3Å электронная плотность на всех уровнях подрезки гораздо хуже, чем у РDB с разрешением 1.23Å, что, впрочем, ожидаемо.
Подробнее рассмотрим несовпадающие участки (на рисунках это 250-267). По электронной плотности очевидно, что структура 6KAX надежнее.
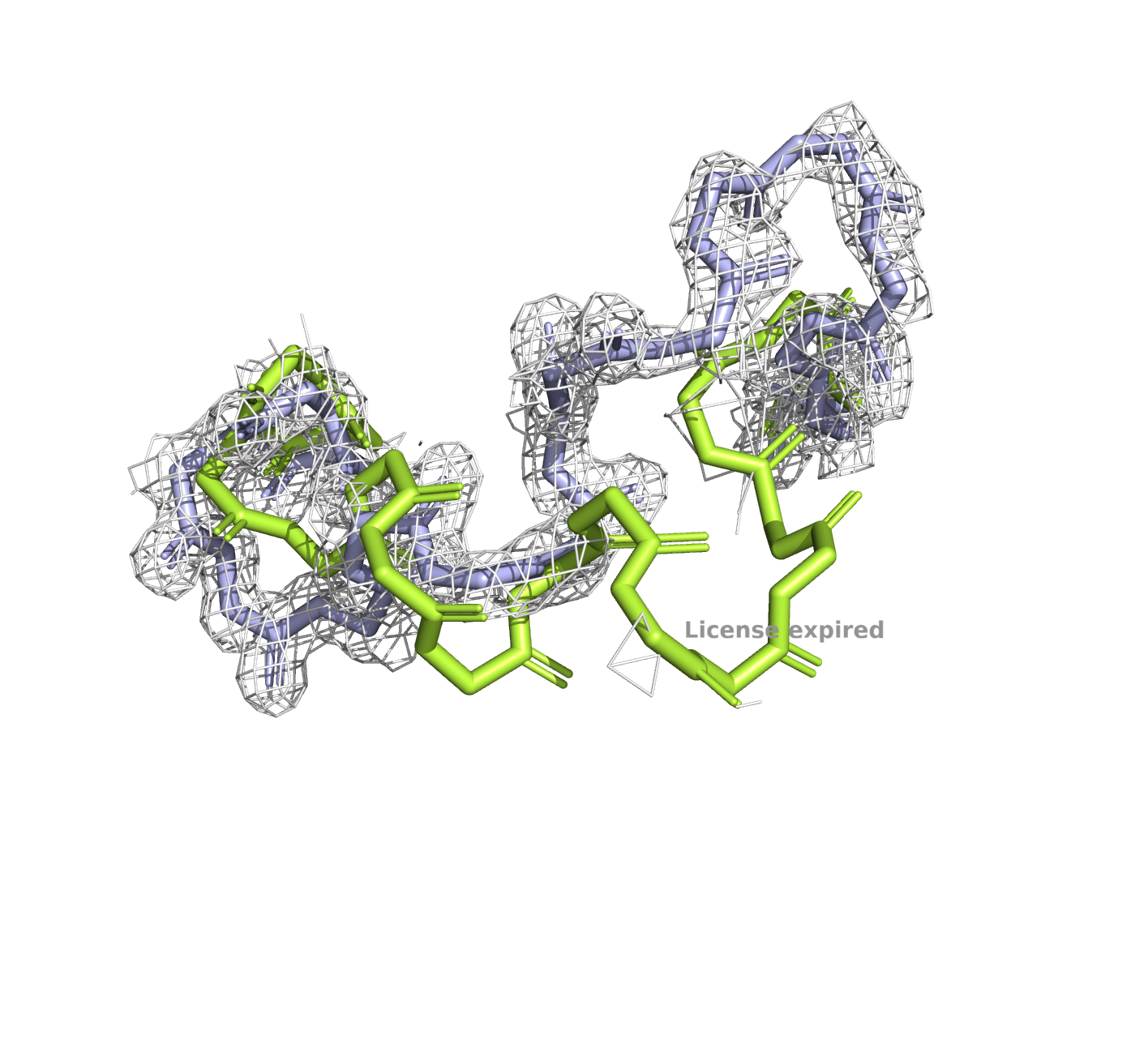
И температурный фактор (В-фактор) подвержает большую надежность структуры 6KAX: на этом участке у нее только два подвижных остатка, в то время как у 6L36 почти вся несовпадающая цепочка.
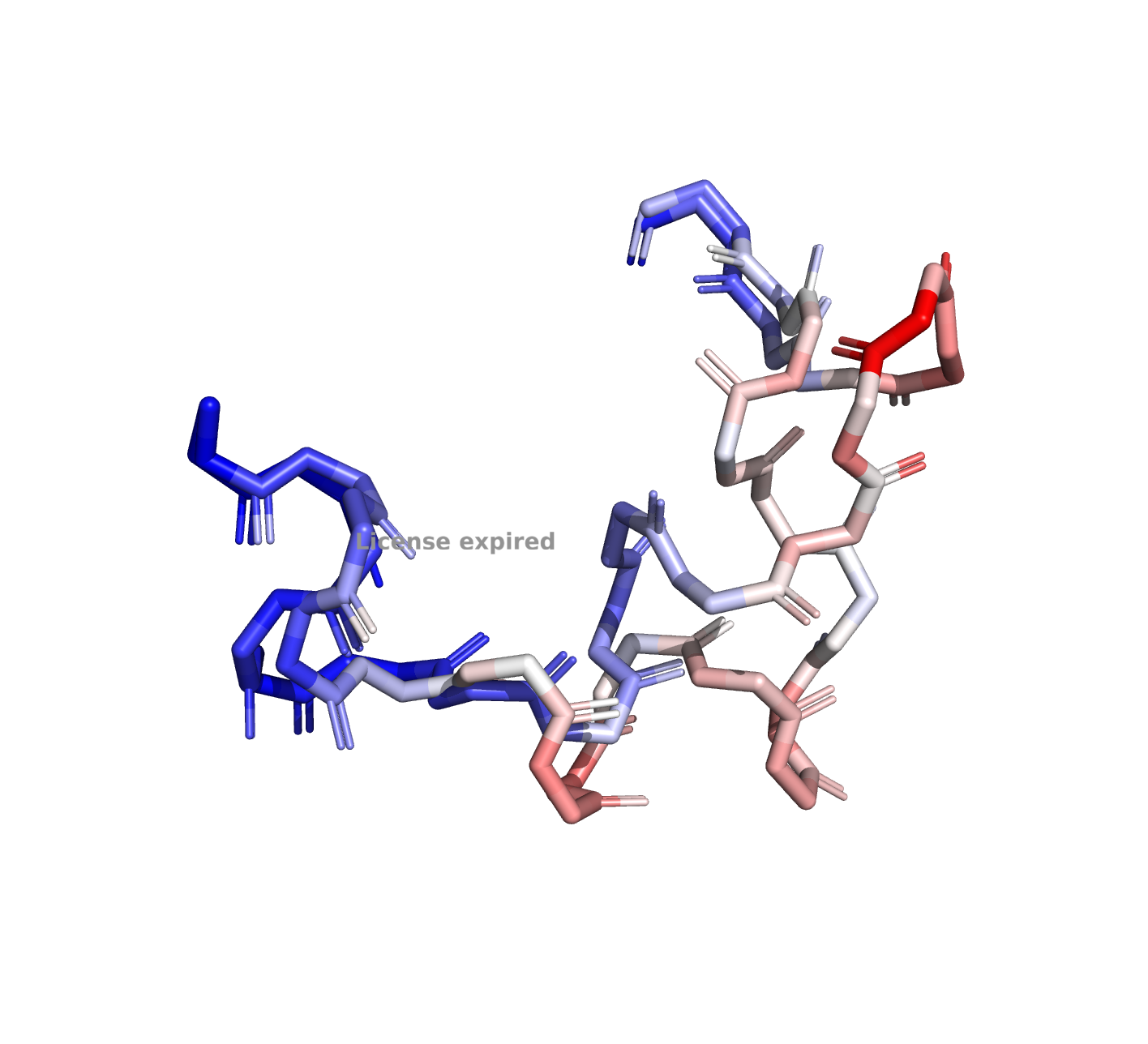
У Lys252 в 6KAX есть альт-локи, но, вероятно, они отнносятся к боковой цепи (этот остаток отмечен неподвижным в обеих цепях), на их наличие еще раз подтверждает высокое качество сборки 6KAX.
2. ЭП и положение в структуре
Я работала с белком андрогенового рецептора человека 2HVC. Это структура с разрешением 2.10 Å и связана с лигандом LDG. Структура из 250 амк.
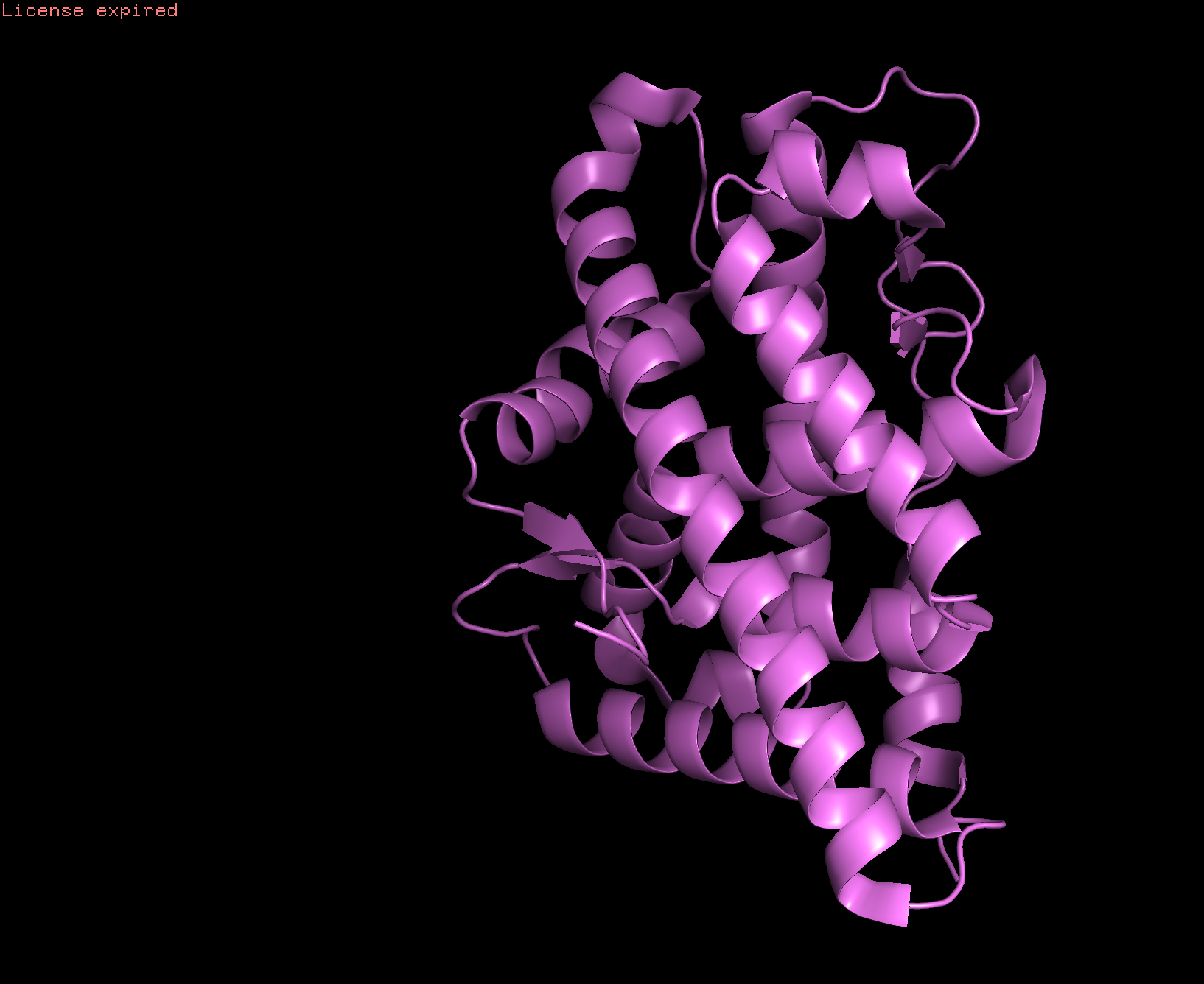
Посмотрим ЭП на уровнях подрезки 1, 2 и 3:
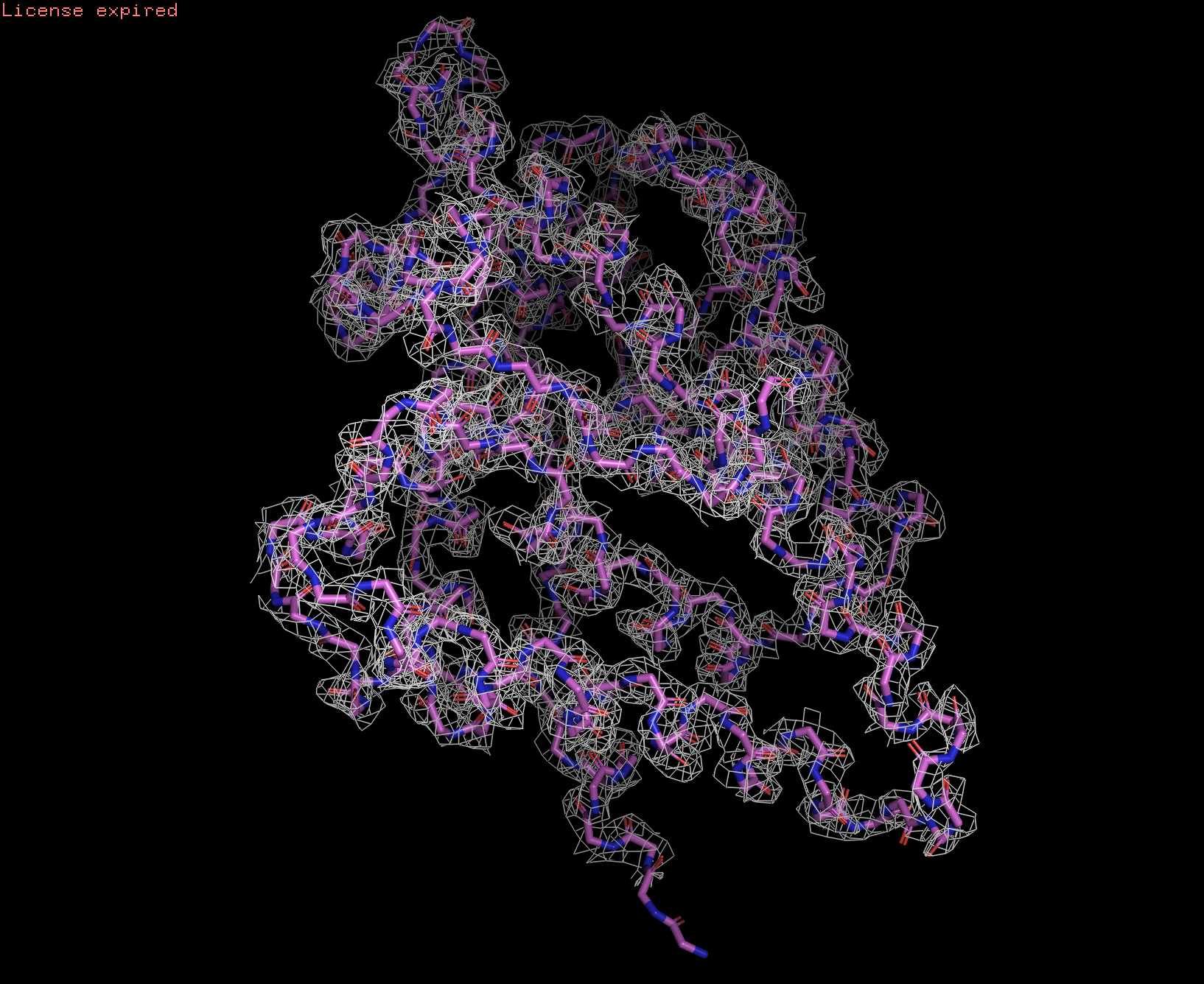
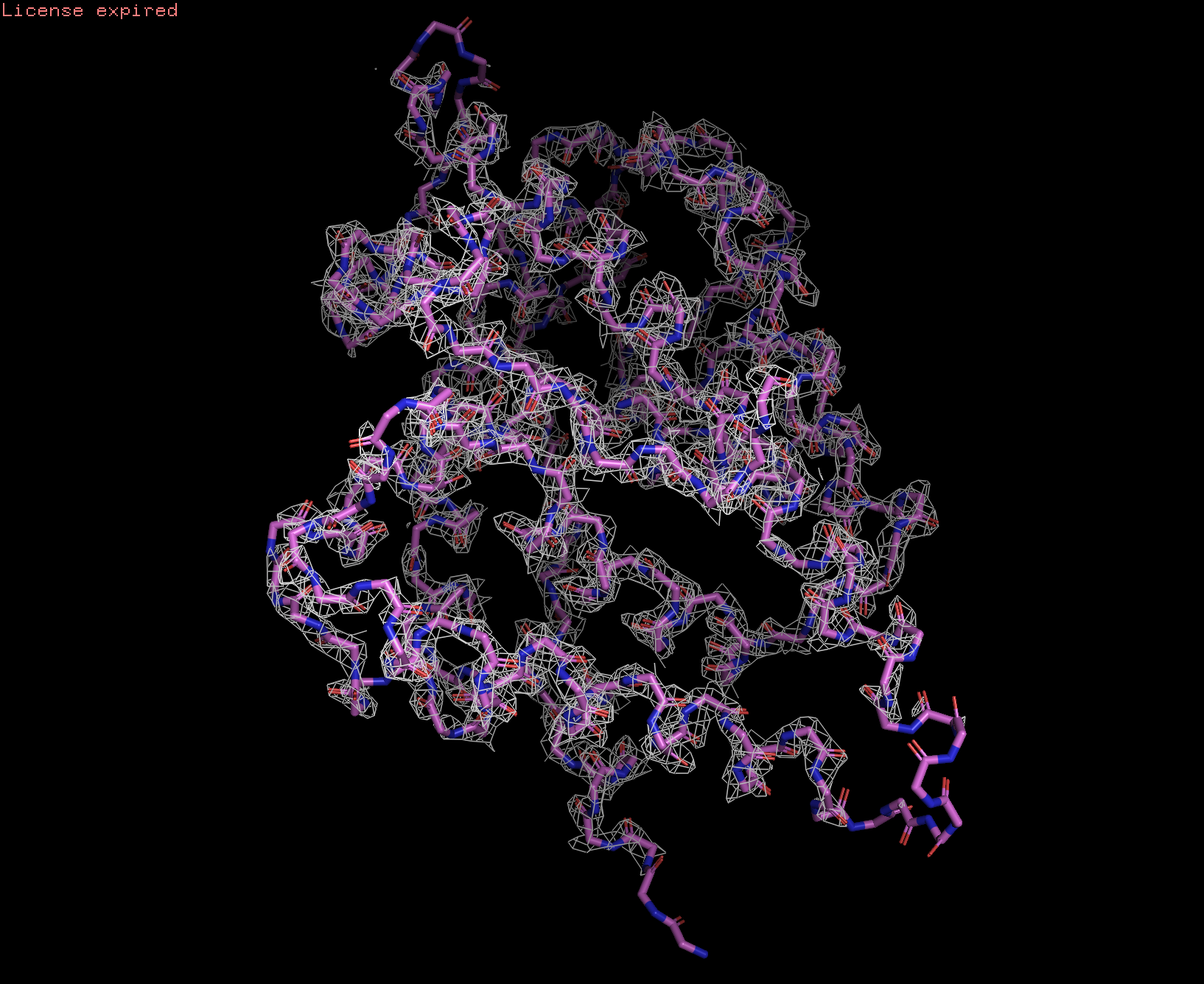
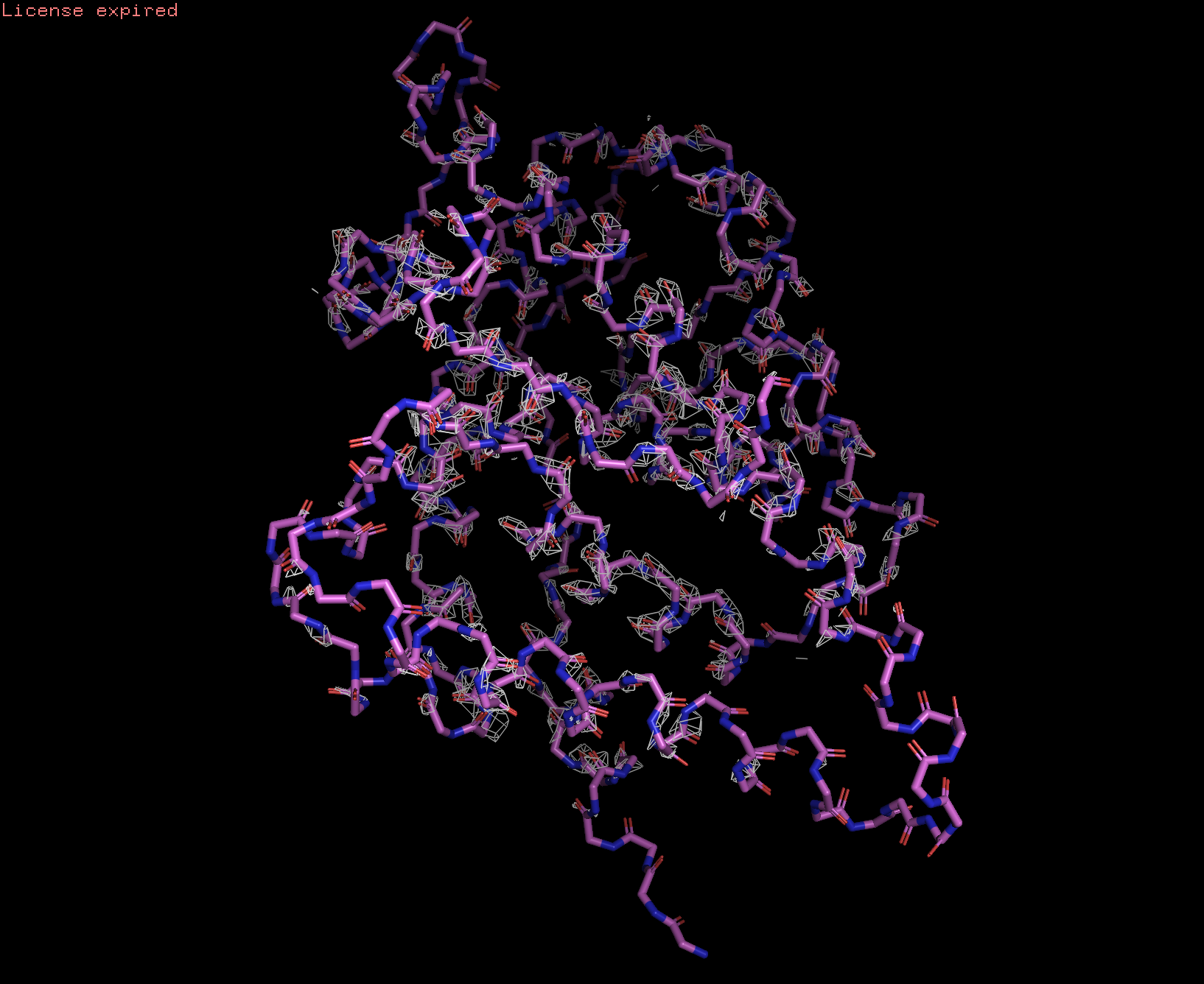
По мере увеличения уровня подрезки ЭП "уходит" со структуры. На уровне подрезки 1 ЭП покрывает почти всю структуру, а на уровне 2 ее уже нет на N-конце белка и на сгибе альфа-спирали. На уровне 3 ЭП почти исчезает и остается только на явно выделенных альфа-спиралях в центре белка. Так же можно отметить, что на уровне 3 ЭП, в основном, расположена на атомах азота и водорода и покрывает атомы углерода в меньшей степени.
3-4. Альт-локи и температурный фактор
Температурный фактор (B-фактор) показывается, насколько подвижен атом в своем положении.
Я работала со структурой 7KR0 из SARS-CoV-2. Разрешение 0.77 Å, в составе 173 амк.
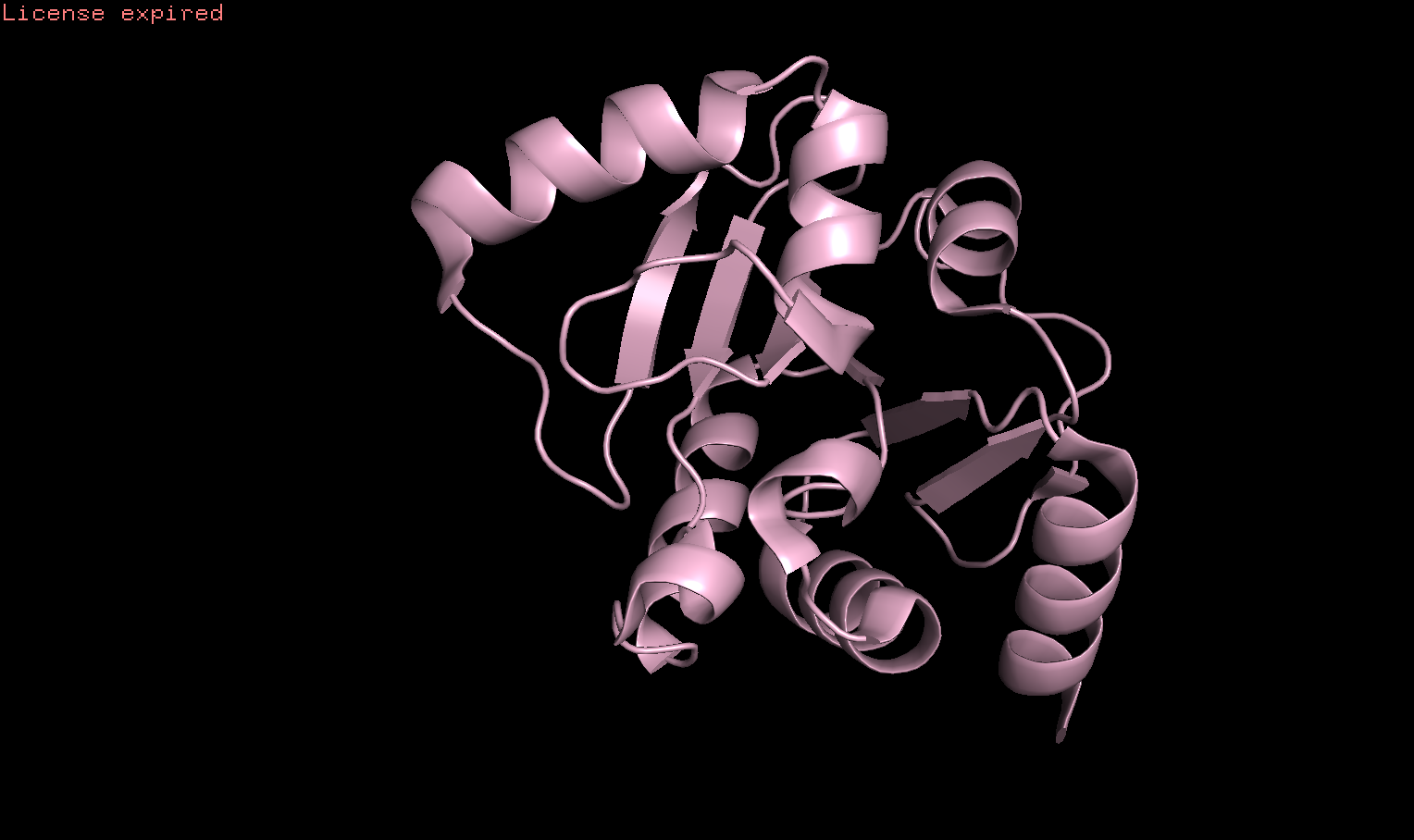
Посмотрим на "карту" температурного фактора. Но остове видно несколько красных участков- участков высокой подвижности. Они расположены на концах цепи (логично), при этом в местах узгиба петель цвет тоже довольно светлый. Альфа-спирали темные, это хорошо, они стабильны.
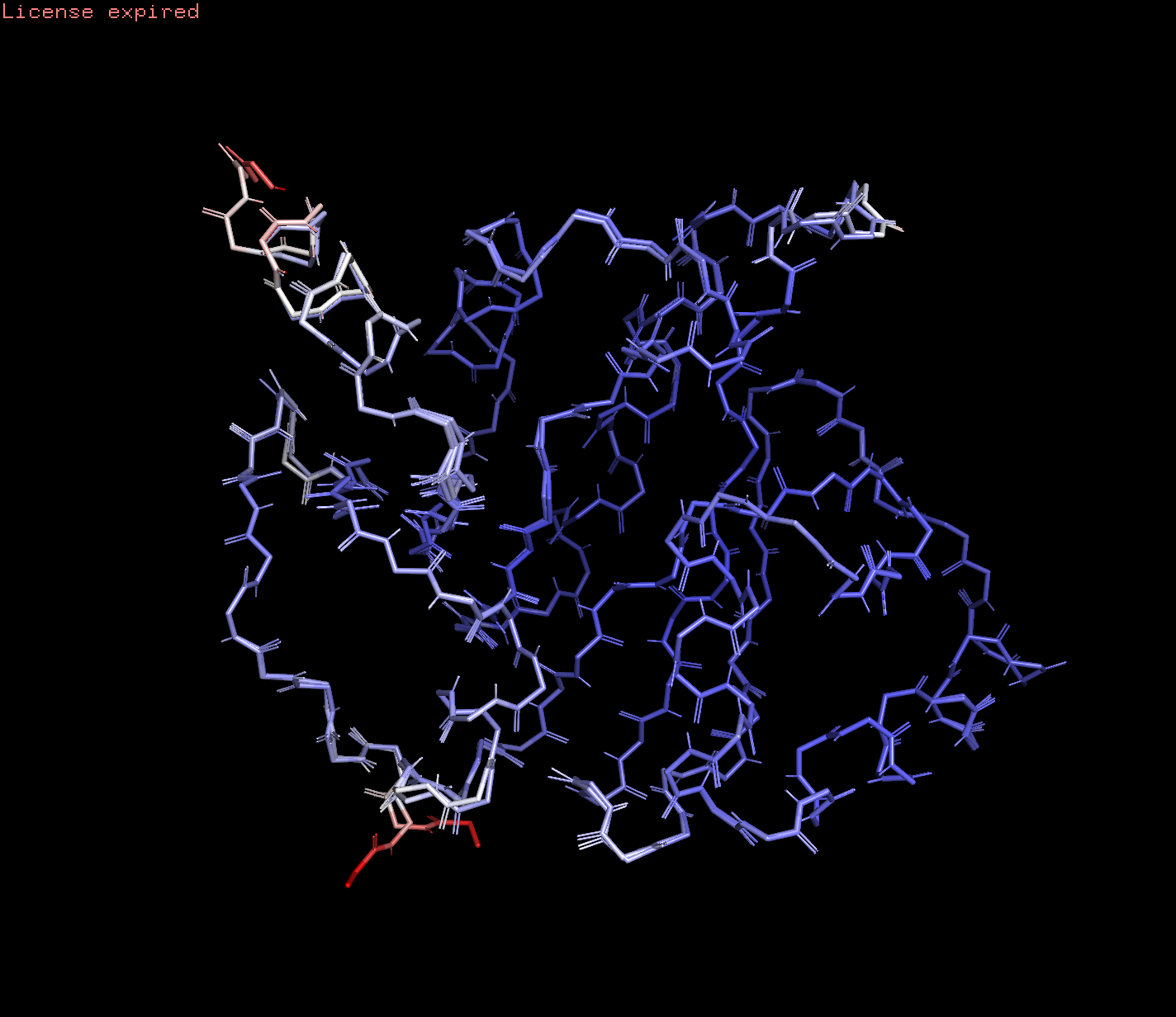

Рассмотрим 2Glu, который на остове отмечен красным. Он находится в цепи А.
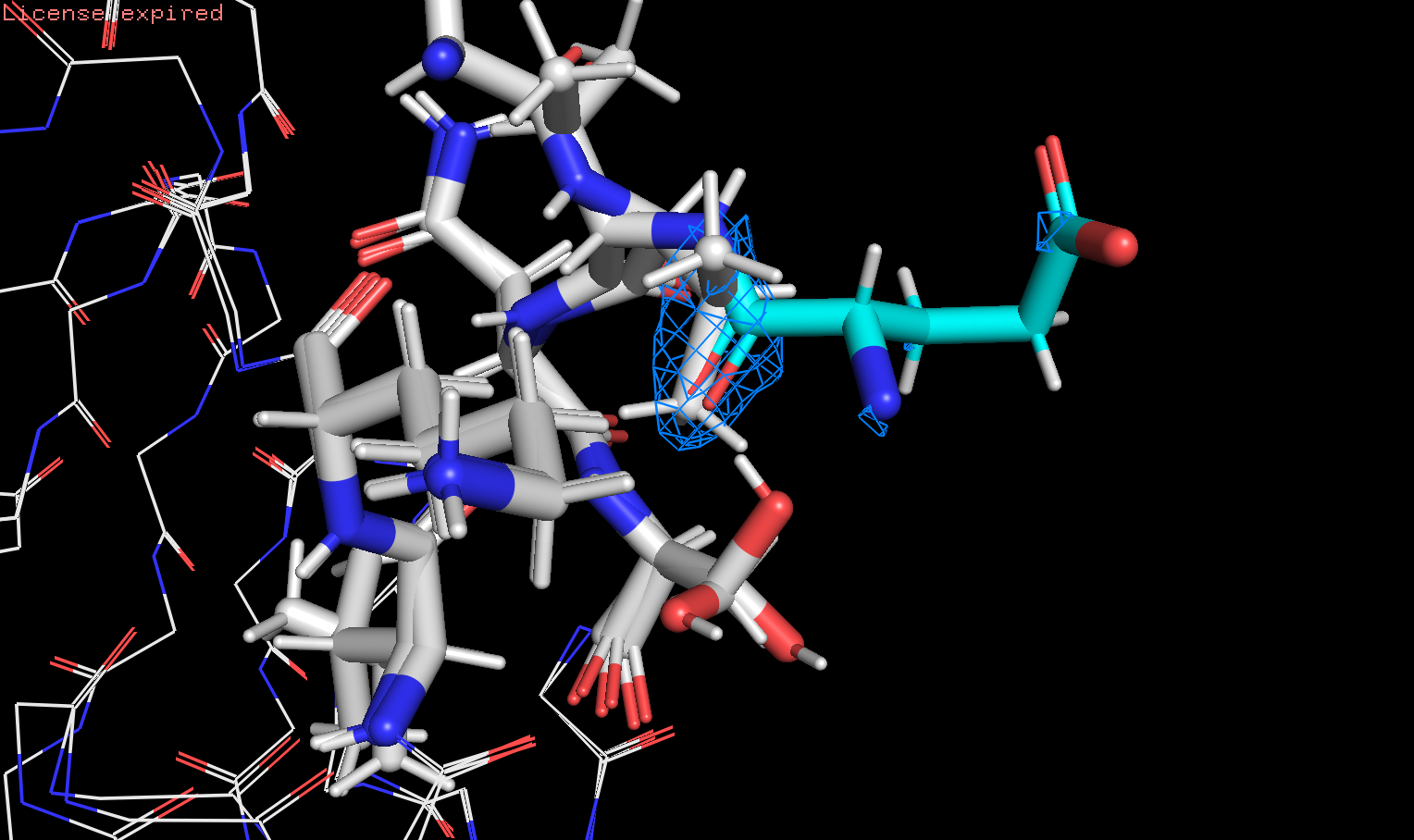
ЭП покрывает азоты и кислороды, захватывает часть амк, которая соединена со следующей.