Анализ структуры белка 3RNR
Структура в целом
Молекула белка состоит из двух полипиптидных цепей, и в биологическую единицу входят две цепи А и B, которые почти идентичны. (Теоретически — идентичны).
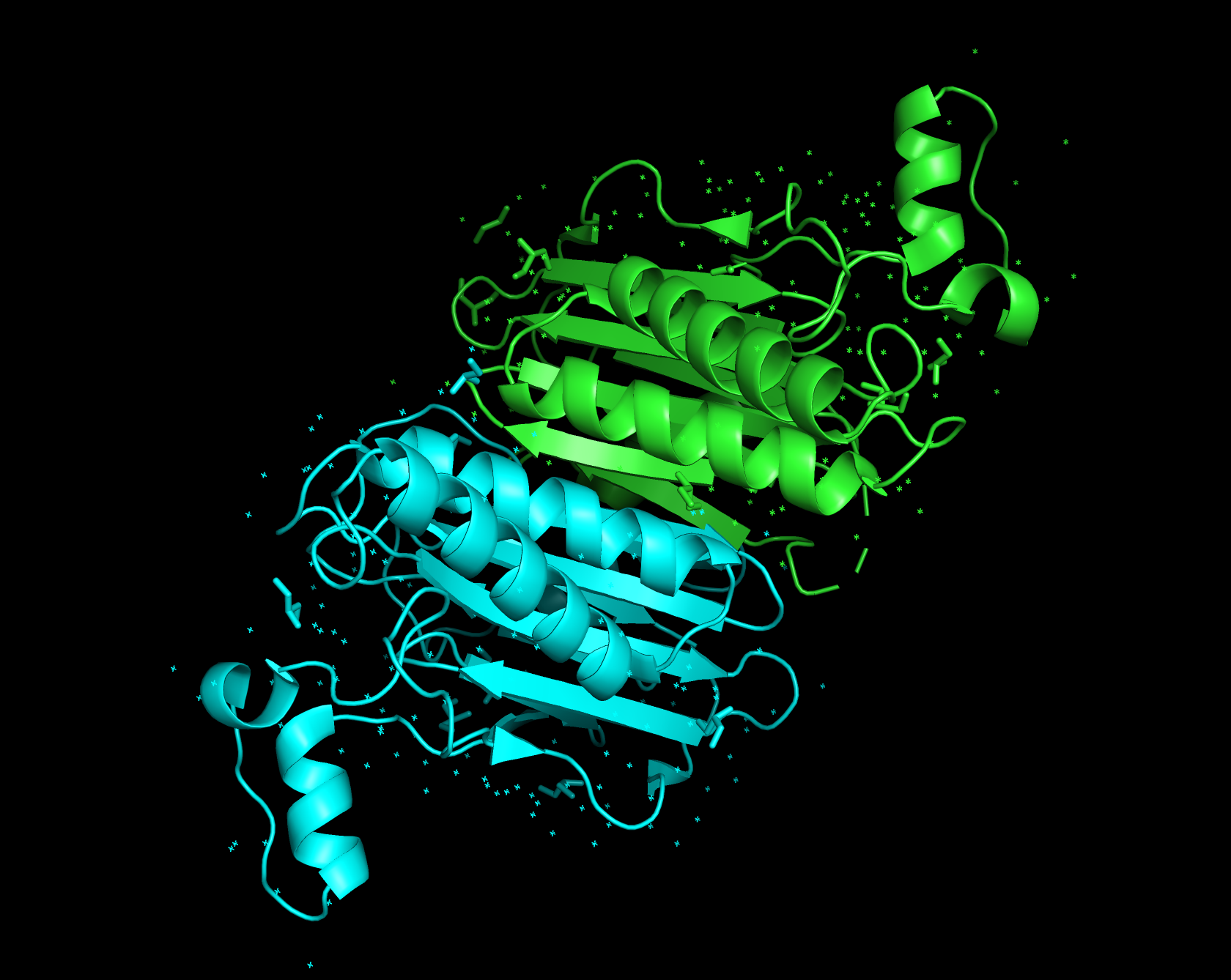
Рис 1. Белок 3RNR
Отдельные цепи
Данный белок был обнаружен в организме Thermanaerovibrio acidaminovorans DSM 6589, а экспрессировался Escherichia coli BL21.
Данные uniprot:
Uniprot_id: D1B7C2
Название: Crystal Structure of Stage II Sporulation E Family Protein from Thermanaerovibrio acidaminovorans
Функция: данные отсутствуют
Вторичная структура молекулы белка представлена 10 α-спиралями и 22 β-тяжами. Цепи, теоретически, состоят из 422 аминокислот. Однако в ходе проведения эксперимента...
Молекула не имеет мутаций по данным UniProt.
Обнаружена одна модифицированная аминокислота - селенометионин. (В файле формата .pdb перед молекулой, которая была добавлена в структуру белка стоит слово HETATM)
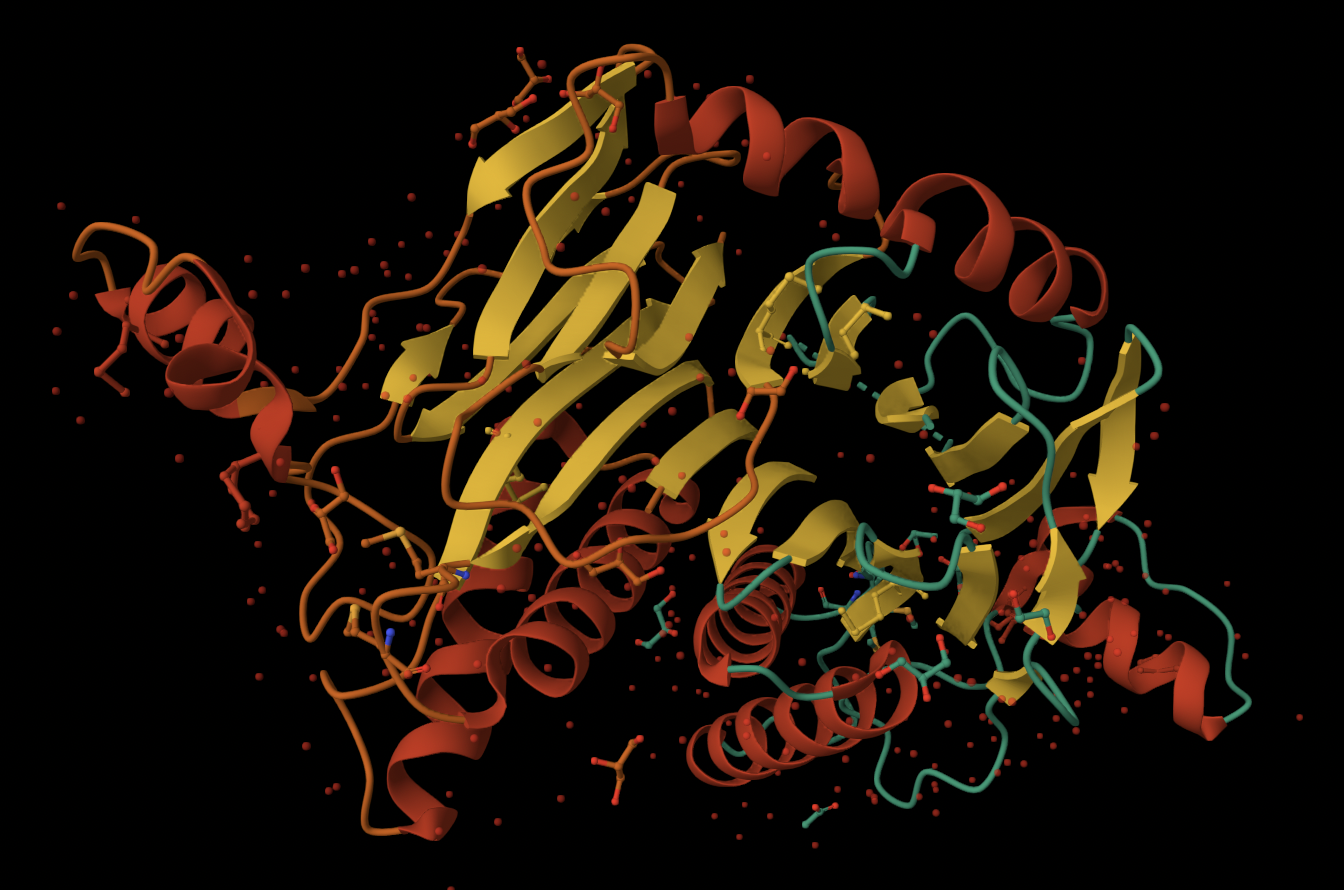
Рис 2. α-спирали (выделены красным) и β-тяжи (выделены желтым)
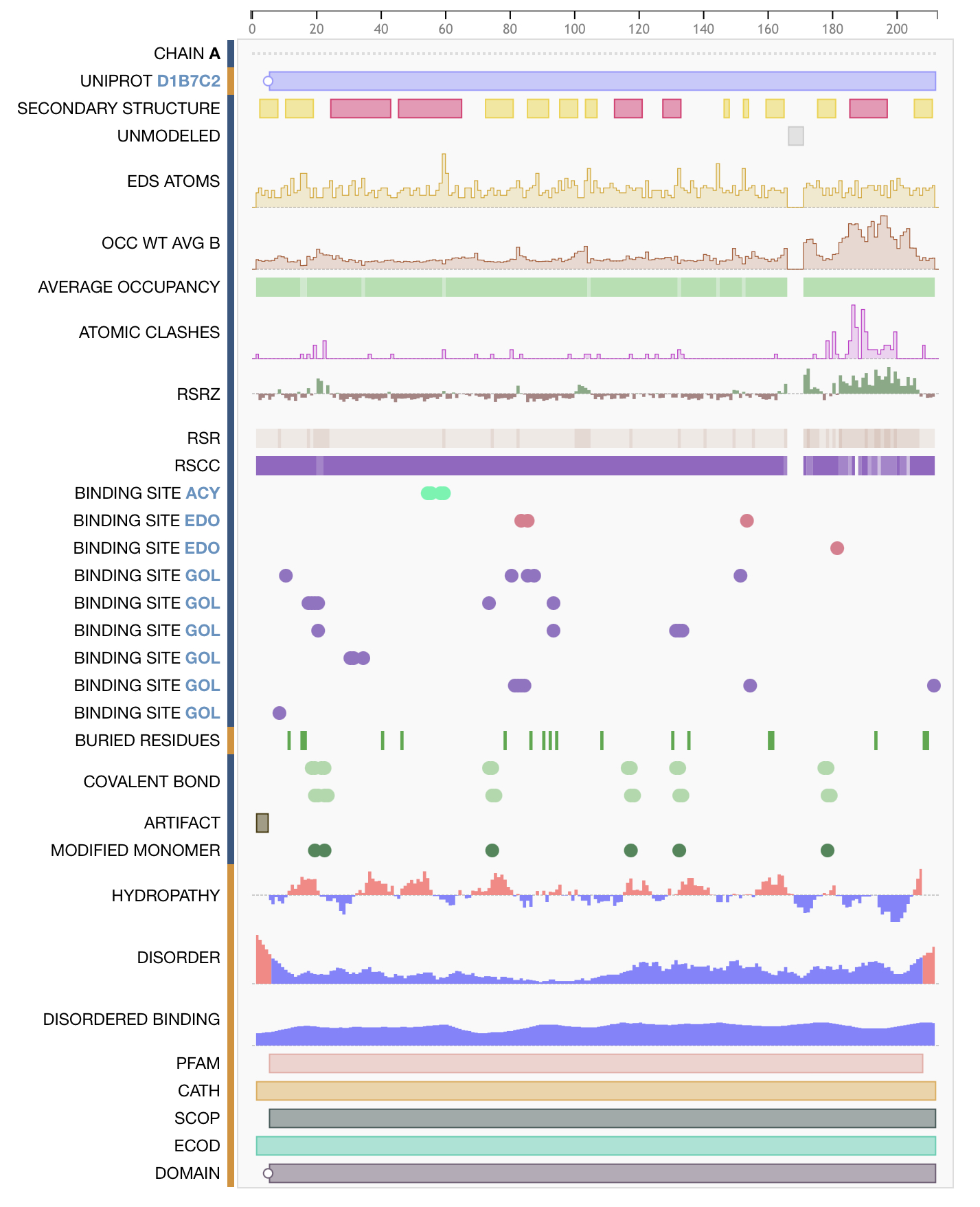
Рис 3. Данные Uniprot
Малые молекулы
В записи структуры есть три типа малых молекул:
1. GOL — GLYCEROL
Расположен в активном центре
2. EDO — 1,2-ETHANEDIOL
3. ACY — ACETIC ACID
Малые молекулы:
Исходя из данных о молекуле можно сделать вывод, что лиганды были добавлены искусственно в процессе получения структуры. (Аналогично, как и с молекулами модифицированных аминокислот).
Функции малых молекул:
Уксусная кислота: не связана с функцией белка. Могла использоваться для регуляции pH среды (буферная система).
Глицерол и 1,2 — этандиол: использовались для стабилизации структуры при низких температурах и для улучшения кристаллизации.
Исследование структуры молекулы белка
Белковое окружение лиганда
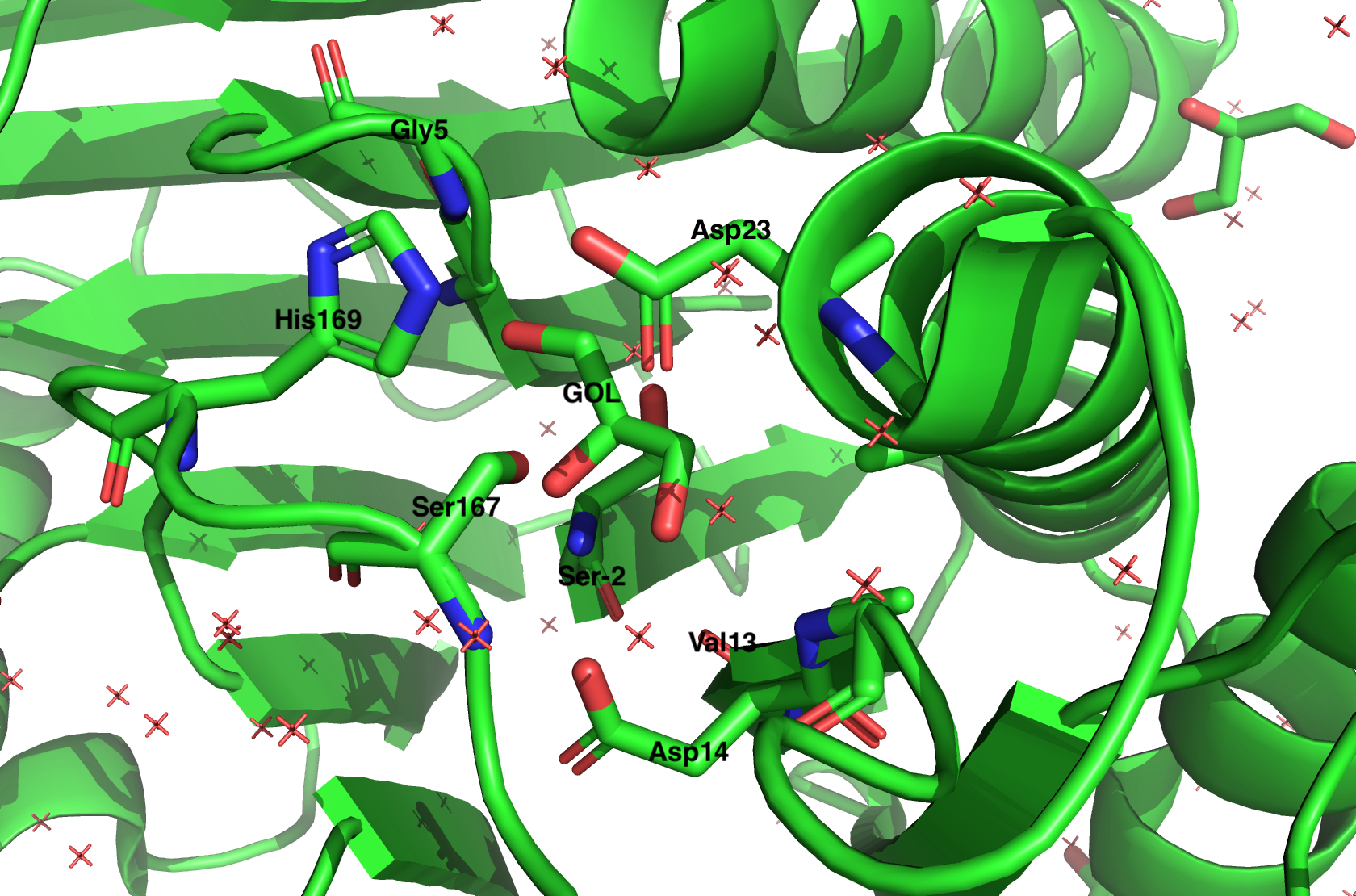
Рис 4. Белковое окружение GOL
Взаимодействия в белке 3RNR
В молекуле белка представлены различные типы взаимодействий, такие как: водородные связи, ковалентные связи, различные виды стекинг-взаимодействий.
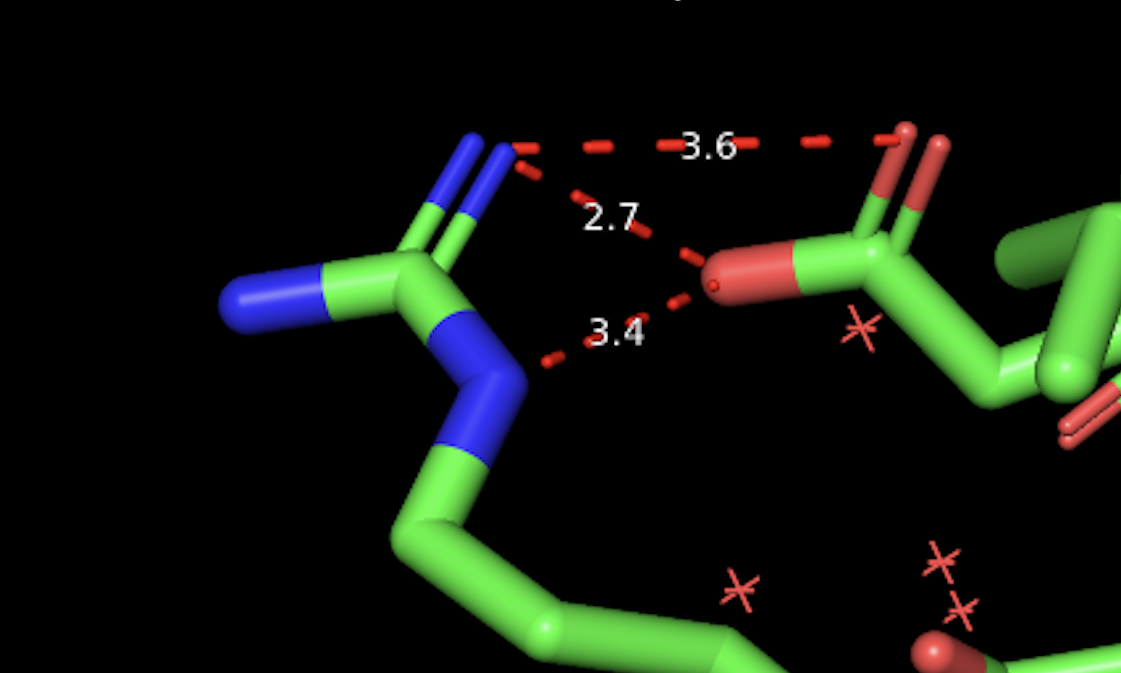
Водородные связи
Водородные связи можно рассмотреть на примере взаимодействия между аминокислотами основной цепи и лигандами.
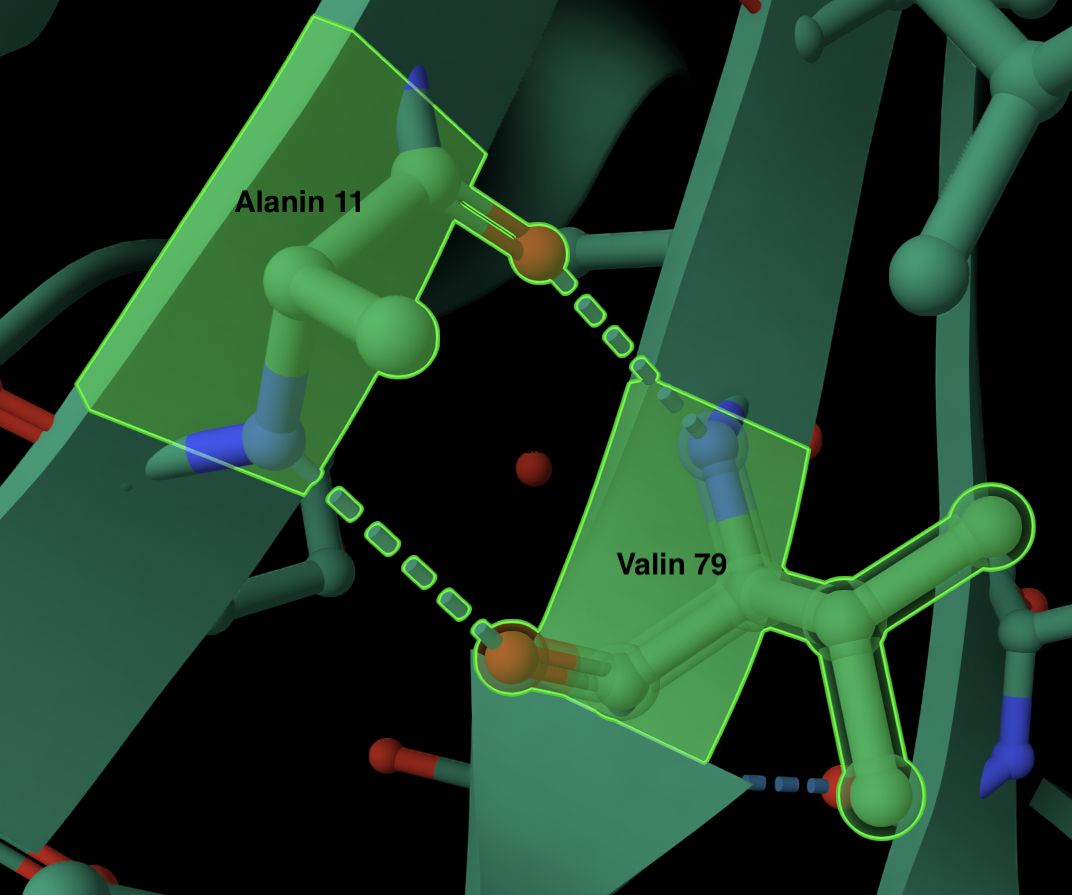
Рис 5. Водородные связи между ALA11 и VAL179
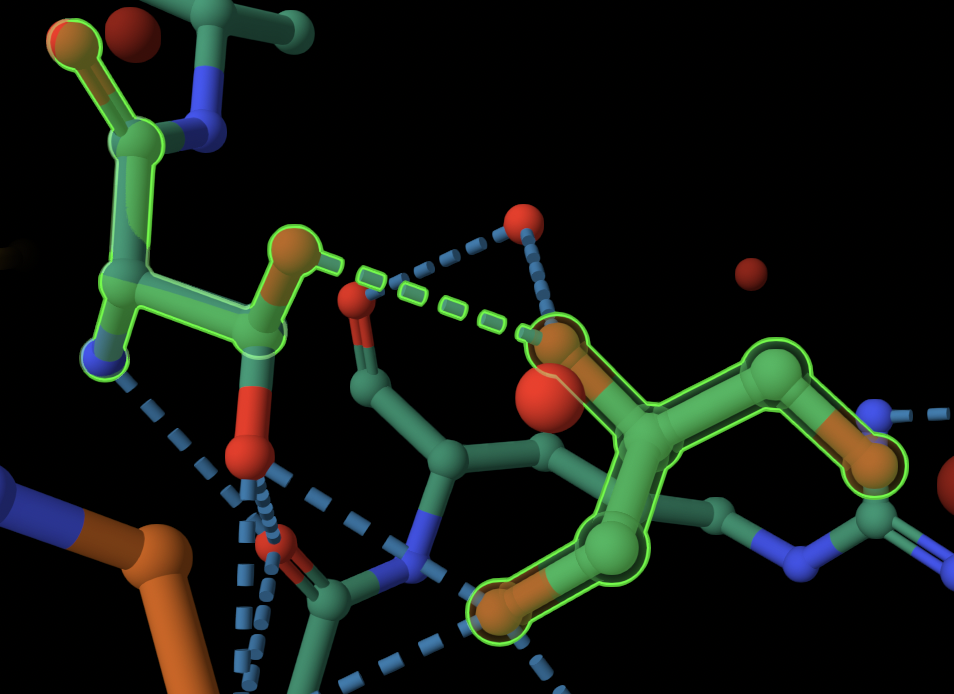
Рис 6. Водородные связи между SER34 и GOL216
Cation-π взаимодействие
Cation-π взаимодействие — тип взаимодействия, в котором задействованы положительно заряженный катион и π-электронная плотность в ароматических соединениях.
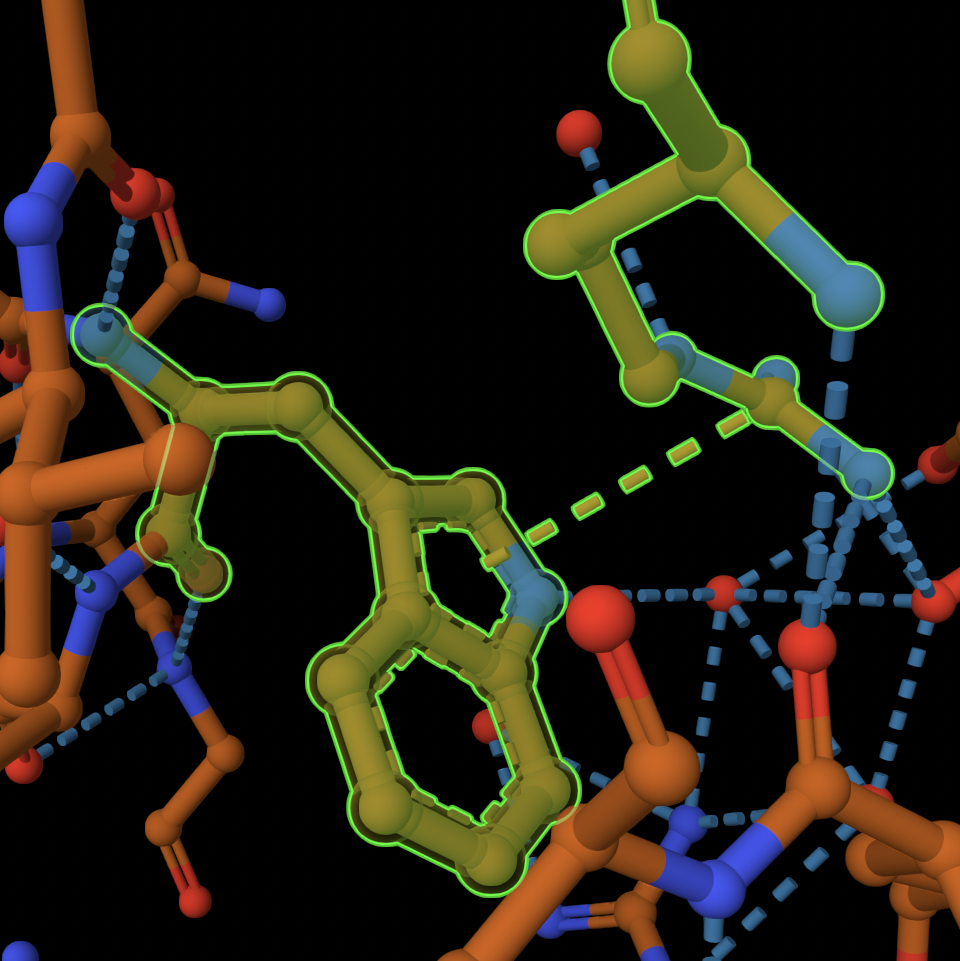
Рис 7. Cation-π взаимодействие между TRP60 и ARG31
Гидрофобные взаимодействия
Гидрофобные взаимодействия — это нековалентные взаимодействия, возникающие между неполярными или малорастворимыми в воде молекулами или группами атомов.
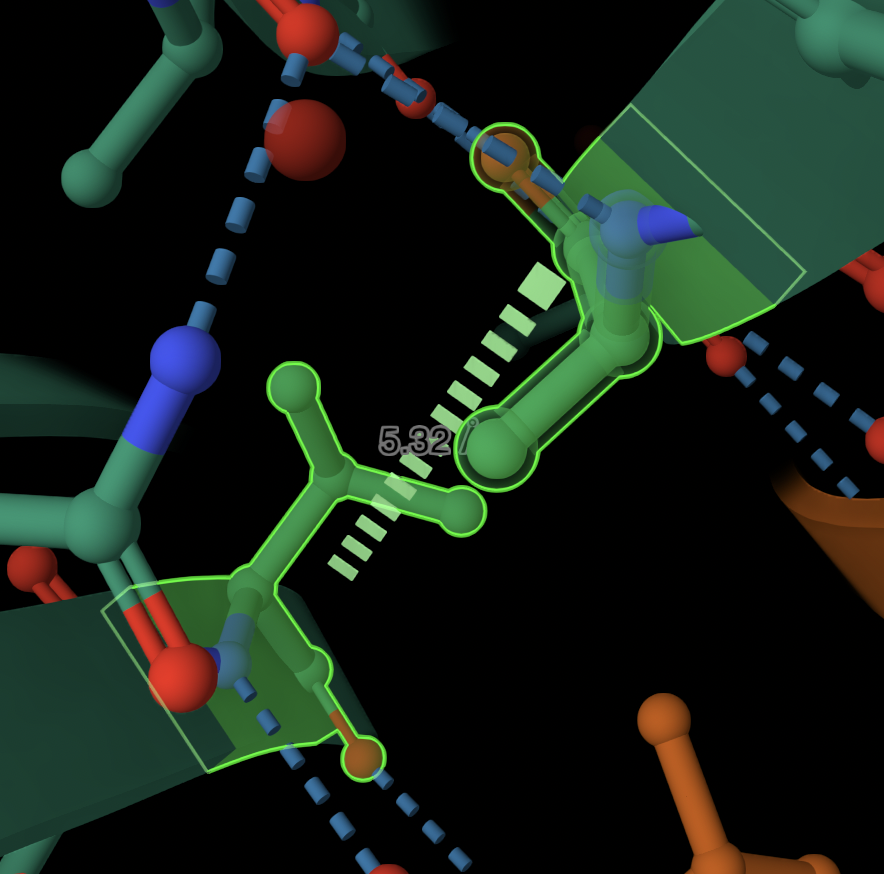
Рис 8. Гидрофобное взаимодействие между VAL4 и ALA177
Солевые мостики
Солевой мостик — это ионная связь между COO- группами аспарагиновой или глутаминовой кислоты и NH3+ группами лизина или аргинина, по длине не превышающая 3.5 Å