Практикум 3-4. PDB и PyMOL
В данном практикуме будет рассмотрена структура белка 3VO0, ковалентно связанного с 2-дезокси-2-фтор-D-глюкуроновой кислотой.
Структура в целом
Фермент 3VO0 относится к β-глюкуронидазам — группе ферментов, катализирующих гидролиз соединений, содержащих β-глюкуроновую кислоту. Поскольку эти ферменты играют важную роль в метаболизме протеогликанов, они представляют интерес с биохимической, физиологической и медицинской точек зрения. Также β-глюкуронидазы широко применяются в биологических исследованиях в качестве репортерных генов (генов, кодирующих белки, легко определяемые по флуоресценции, цвету или другим детектируемым свойствам, что позволяет отслеживать активность определенных процессов в клетке).
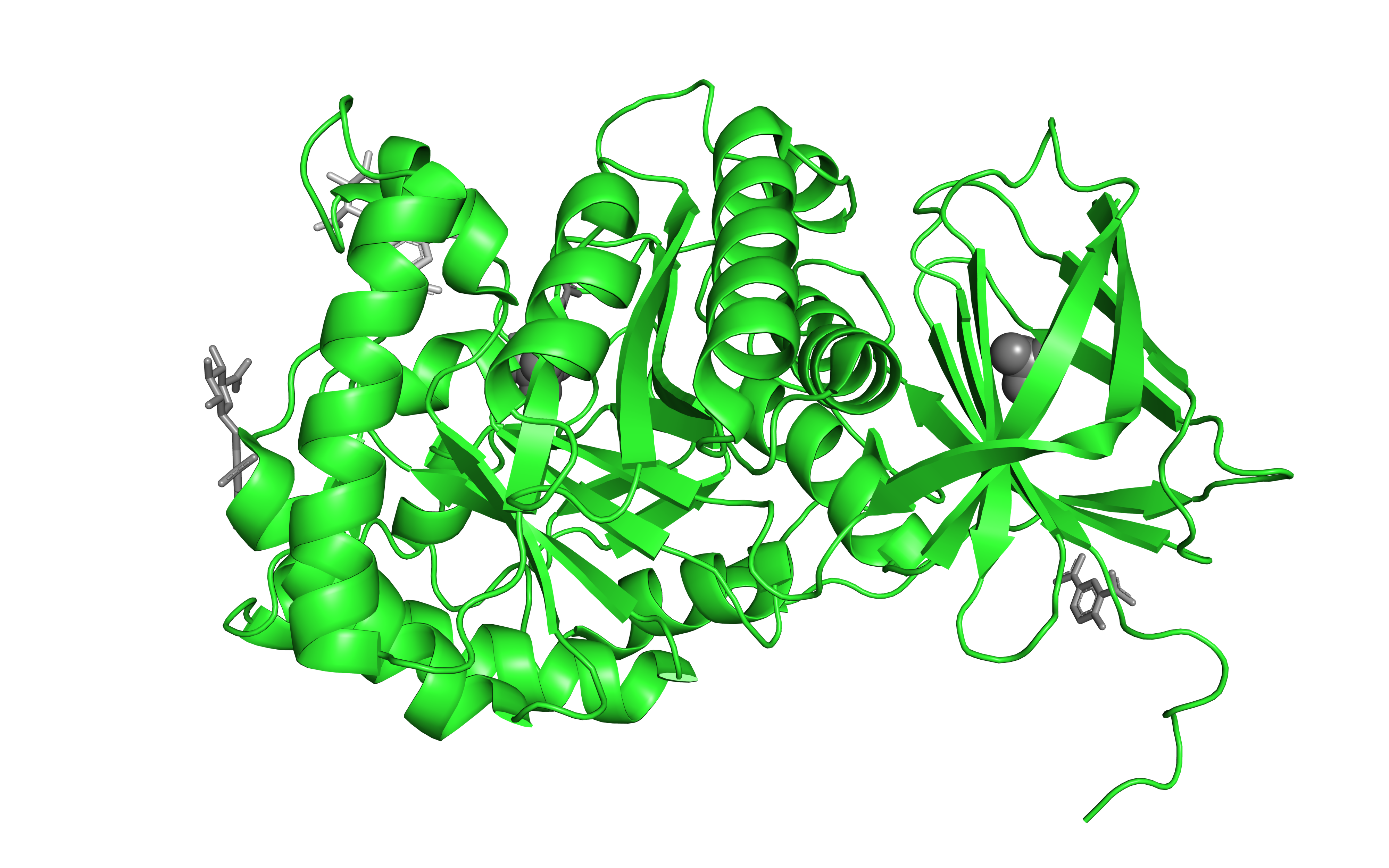
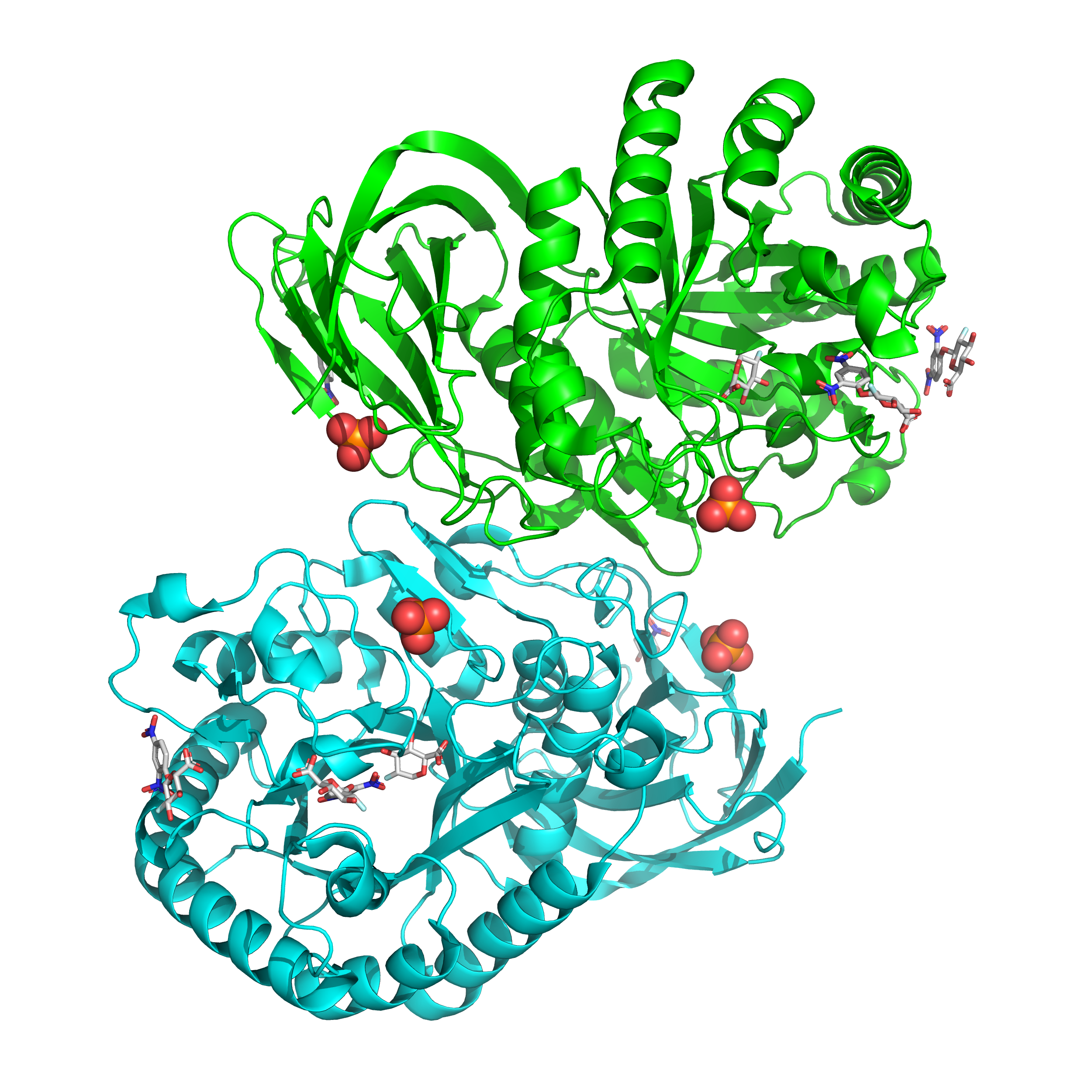
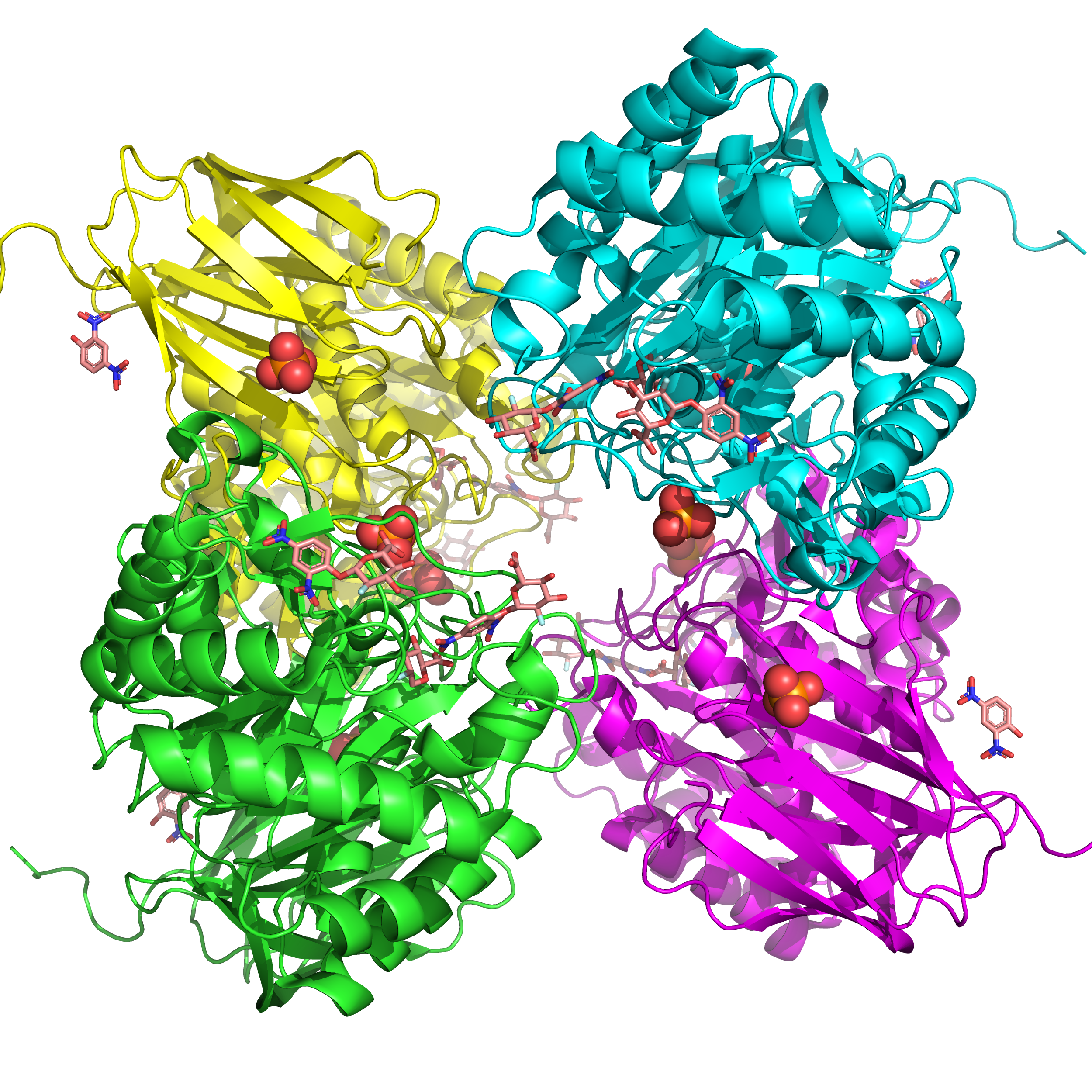
На рисунках 1, 2, 3 изображено общее строение трех биологических сборок 3VO0 (biological assembly). Ассимитрическая сборка совпадает с биологической сборкой 1. Данные о структуре исследуемого белка были взяты с сайта PDB (protein data bank) и обработаны в компьютерной программе PyMOL. Далее будет рассмотрена структура мономерной сборки белка (рис. 1).
Структура исследуемого белка представлена одной полипептидной А-цепью, состоящей из 488 аминокислотных остатков. Она и составляет биологическую единицу.
Также в программе PyMOL была обработана вторичная структура 3VO0, компоненты которой обозначены разными цветами (рис. 4). Как можно заметить, во вторичной структуре присутствуют как альфа-спирали, так и бета-слои. Они соединены петлями, которые обеспечивают гибкость и правильную ориентацию аминокислотных остатков. Согласно исходной статье по данному белку, 3VO0 состоит из (β/α)-ствола, который является каталитическим доменом (как и у многих других гликозидных гидролаз). В дополнение к основным вторичным структурам (β/α)-ствола несколько петель складываются в небольшие субструктуры и вносят вклад в формирование каталитического кармана. Также во вторичной структуре находится участок, который представлен исключительно β-листами.
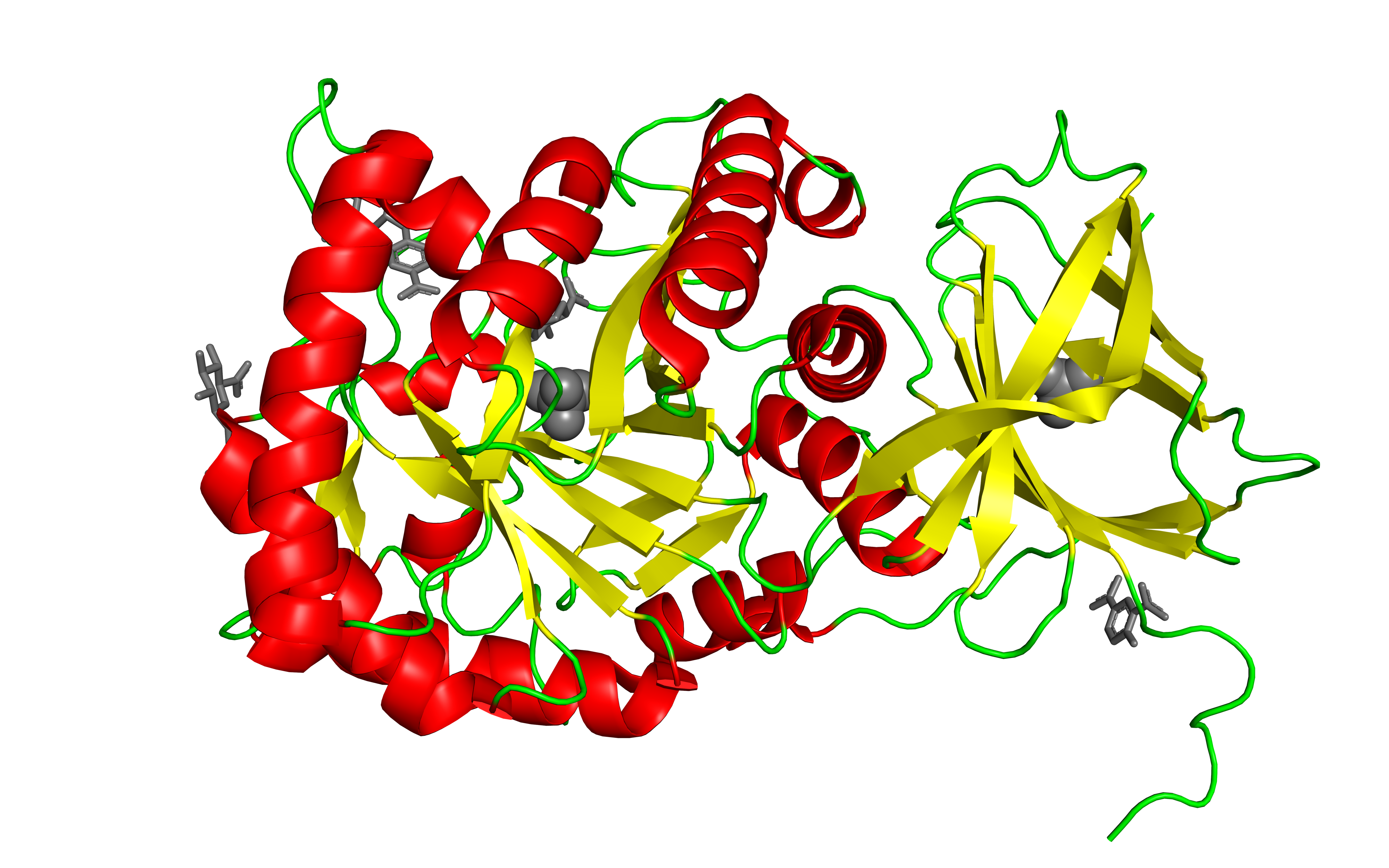
Отдельные цепи
Исследуемый белок был веделен из бактерии Acidobacterium capsulatum. Uniprot_id данного белка — C1F2K5. Мутации относительно референса из базы Uniprot отсутствуют. Модифицированные аминокислоты также не были найдены.
Малые молекулы
В структуре 3VO0 были зафиксированы следующие малые молекулы:
1. GUF (2-дезокси-2-фтор-бета-D-глюкопирануроновая кислота).
2. GUZ (2-дезокси-2-фтор-альфа-D-глюкопирануроновая кислота).
3. DNF (2,4-динитрофенол).
4. PO4 (фосфат-ион).
Также был выделен текстовый файл со строками из файла pdb, которые содержат информацию о перечисленных малых молекулах.
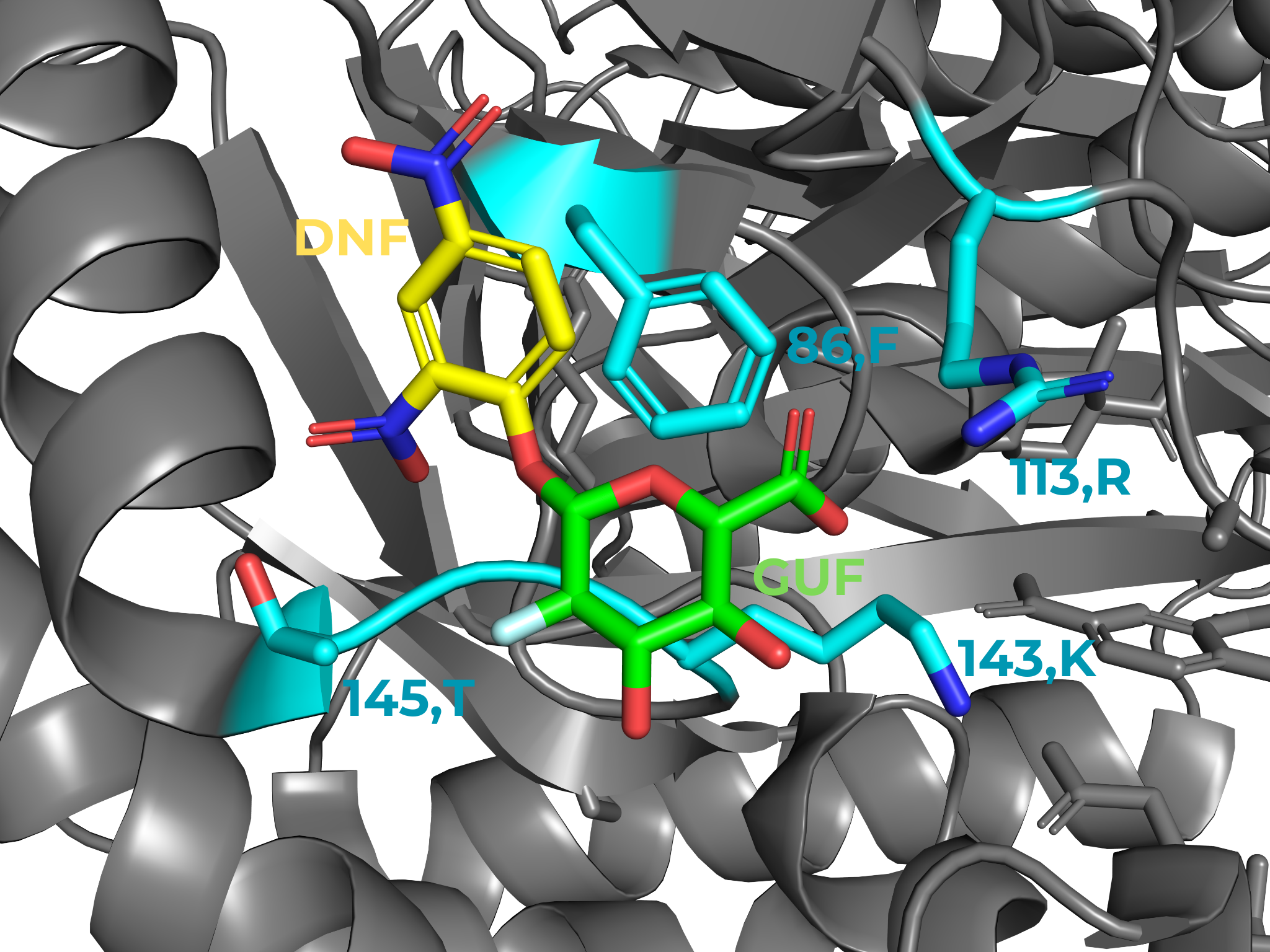
На рис. 5 изображено белковое окружение малой молекулы GUF, ковалентно связанной с DNF. Указанные аминокислотные остатки находятся на расстоянии до 5 ангстрем от молекулы лиганда GUF.