|
|
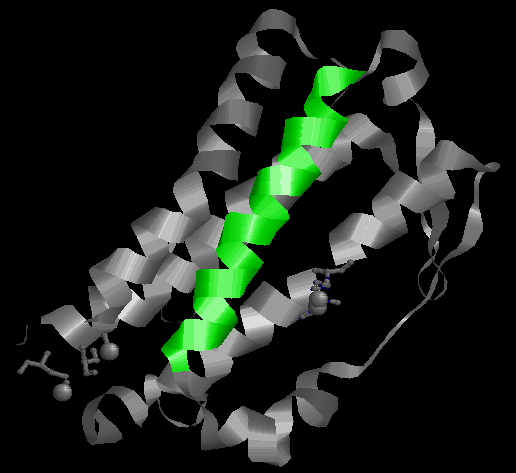
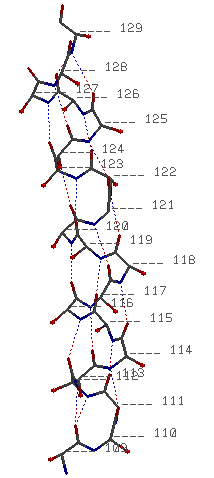
| alpha-спираль | 109-129 |
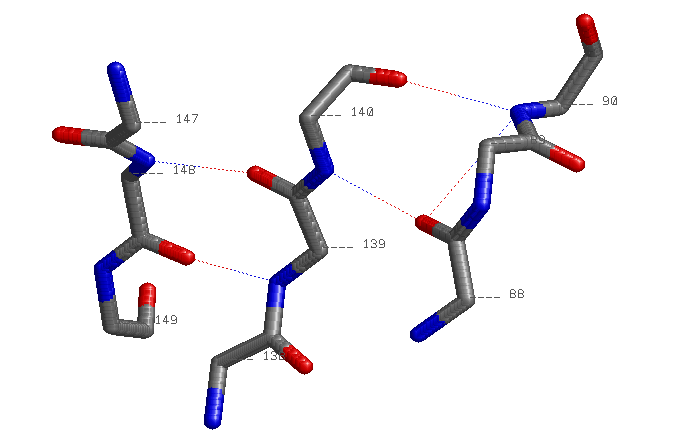
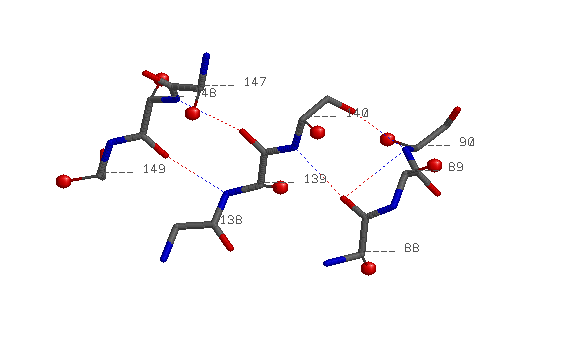
| betta-тяж | 88-90 138-140 147-149 |
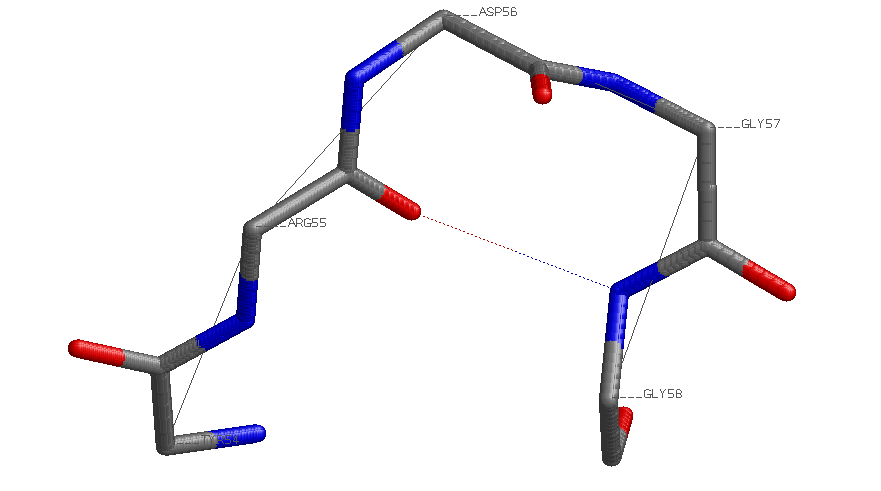
| betta-поворот | 54-58 |
|
|
|
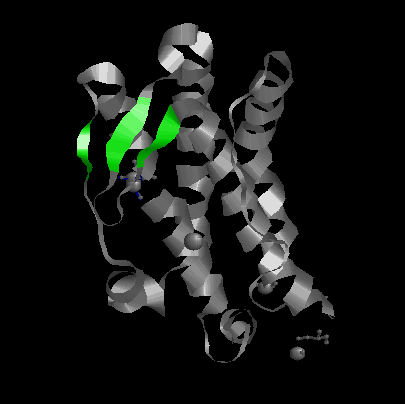
|

|
|
|
|
|
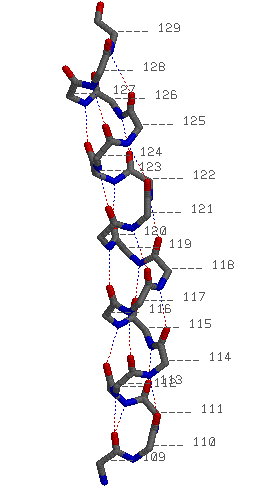
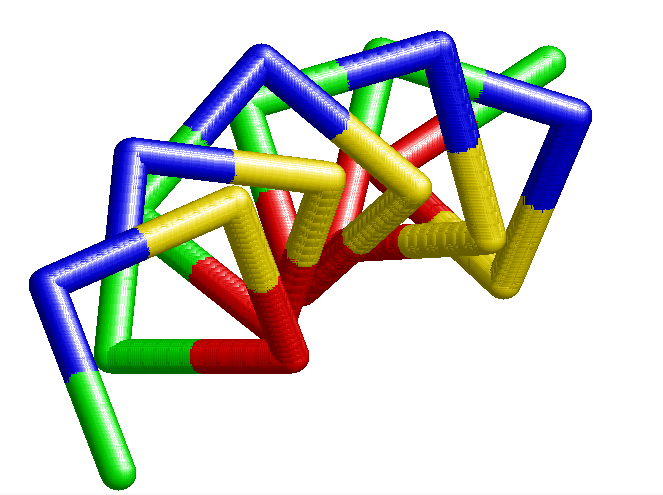
| Округляя до целых чисел, можно сказать, что на виток приходится 4 аминокислотных остатков. Спираль закручена вправо. В итоге +n=4. |
|
| Шаг спирали равен 6,13 А. Измерение проведено между 110 и 114 аминокислотными остатками. |
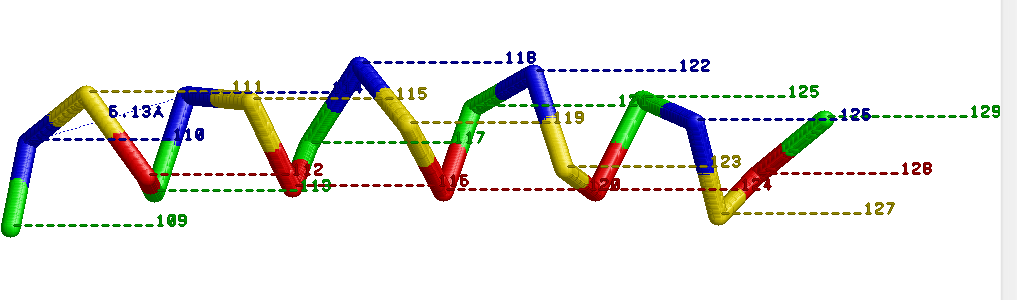
|
| Спроецировав первые четыре остатка на плоскость, можно заметить, что полученную фигуру вполне возможно экстраполировать без больших потерь до квадрата со стороной 3,83 А, что отвечает длине между соседними альфа углеродами. Тогда радиус вычисляется по формуле r=(3,83^2/2)^0,5=2,7 A. |
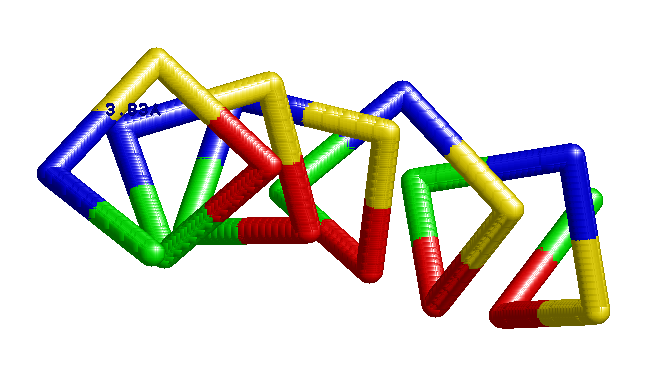
|