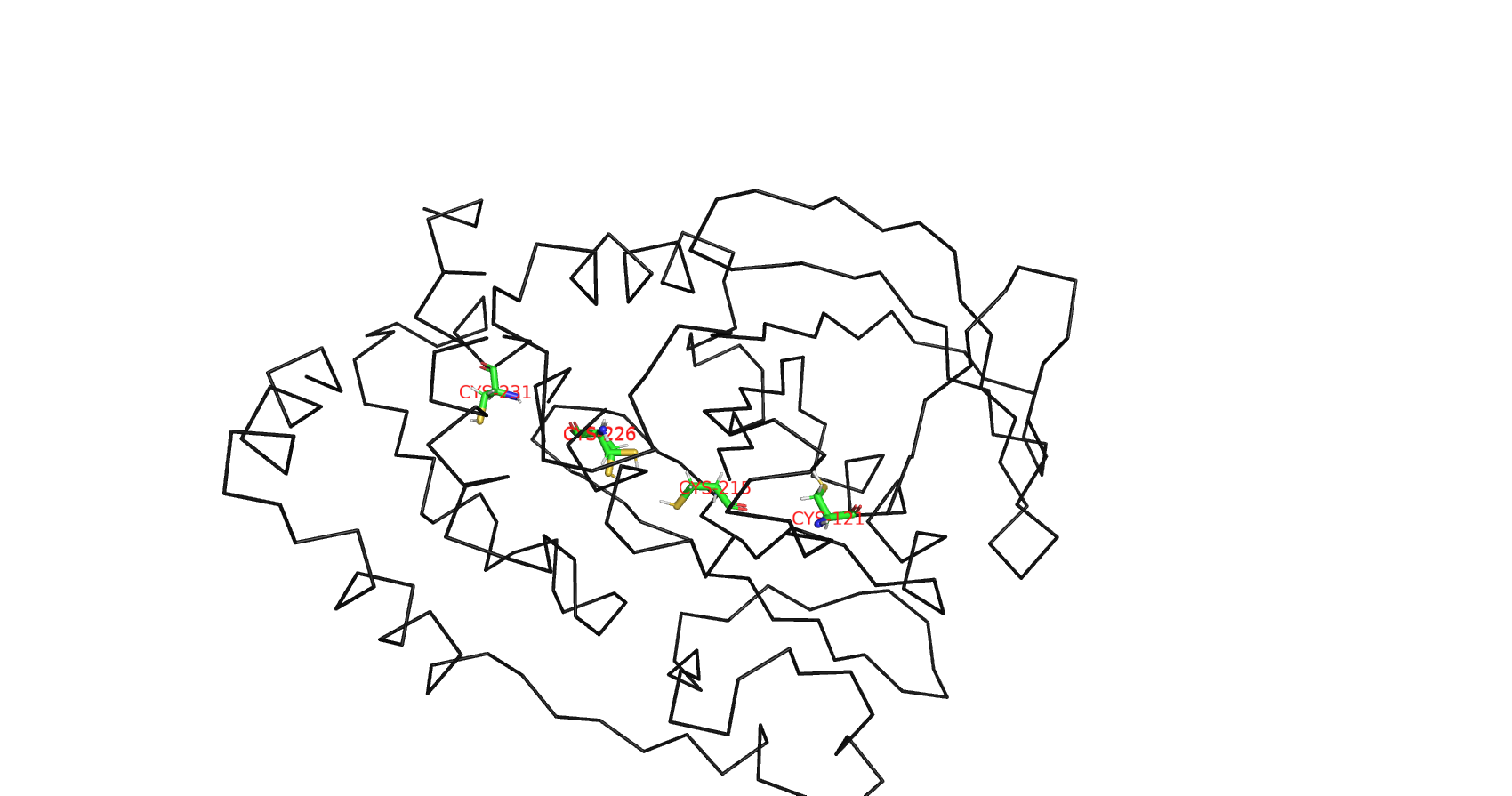
1) В данном практикуме приводится описание функций и структуры фермента, относящегося к классу гидролаз, а точнее — тирозин-протеинфосфатаз (tyrosine-protein phosphatase).
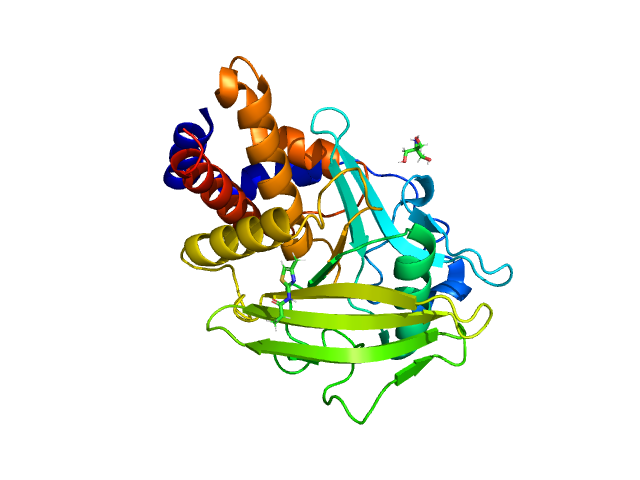
2) В структуре данного белка присутствует одна полимерная цепь A, которая представляет собой биологическую единицу.

1) Данная молекула относится к организму Homo sapiens.
2) UniProt_id — P18031, название — Tyrosine-protein phosphatase non-receptor type 1. Тирозин-протеинфосфатаза, которая действует как регулятор ответа развернутого белка эндоплазматического ретикулума. Опосредует дефосфорилирование EIF2AK3/PERK; инактивирует активность протеинкиназы EIF2AK3/PERK. Может играть важную роль в каскадах передачи сигнала, индуцированных CKII и p60c-src. Может регулировать сигнальный путь EFNA5-EPHA3, который модулирует реорганизацию и отталкивание клеток. Может также регулировать сигнальный путь рецептора фактора роста гепатоцитов через дефосфорилирование MET.
3) В данной молекуле имеется 2 мутации относительно референса в UniProt: в 32 позиции цистеин заменён на серин, а в 92 позиции цистеин заменён на валин.
4) В составе цепи модифицированных аминокислотных остатков не найдено.
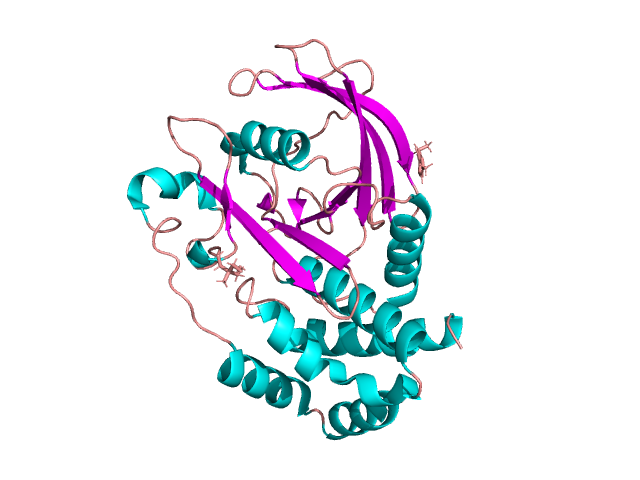
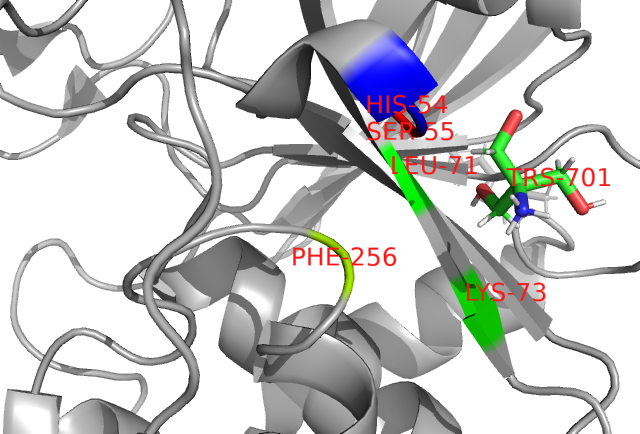
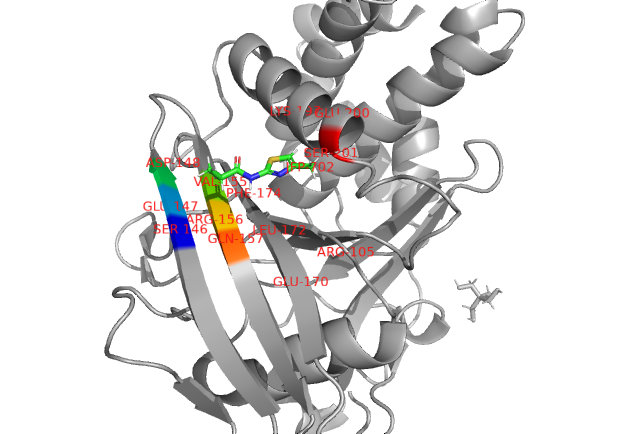
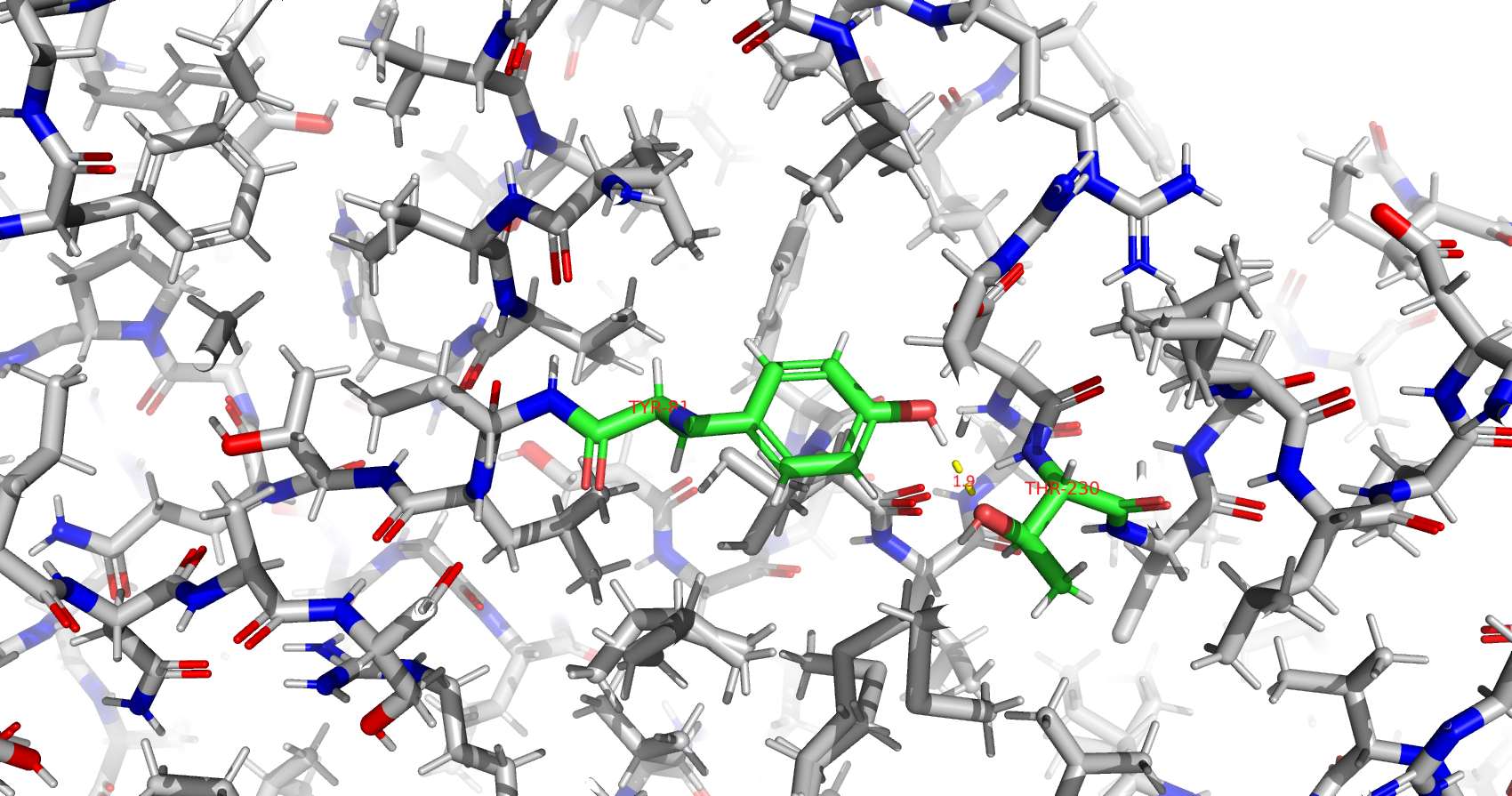
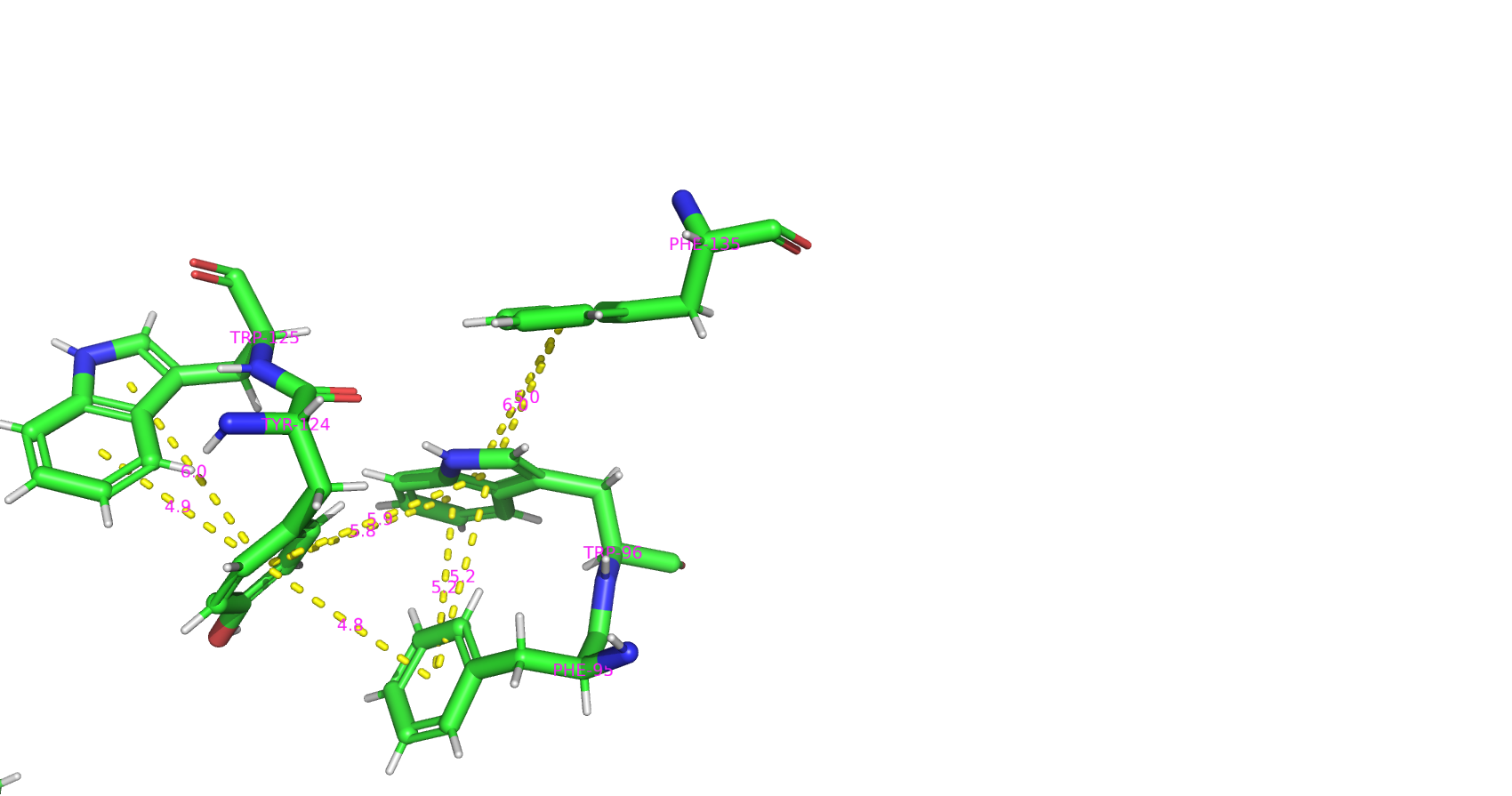
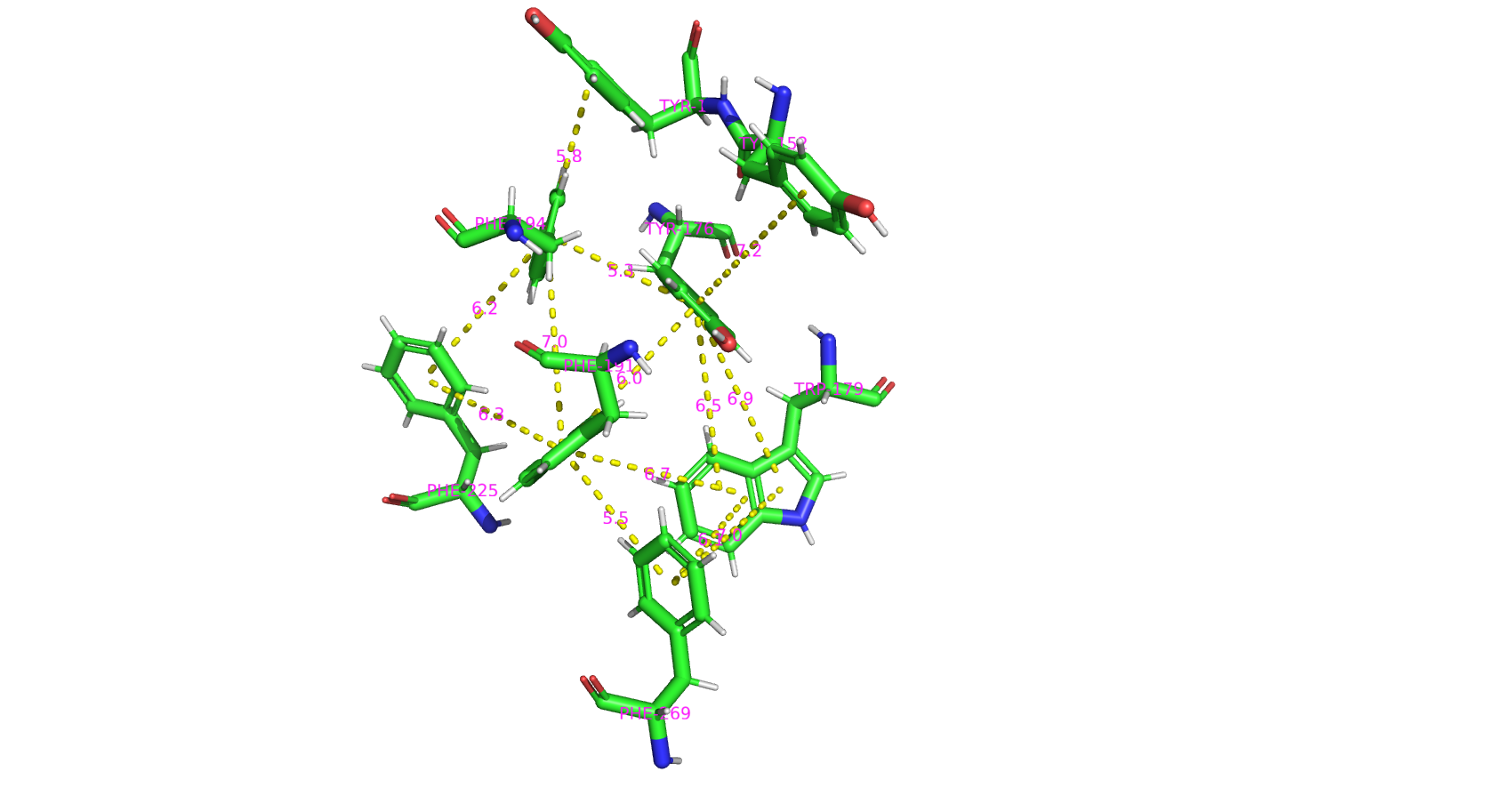
1) Помимо воды и белка, в записи также присутствуют молекулы 2-амино-2-гидроксиметил-пропан-1,3-диол (TRS) и N-(4-метил-1,3-тиазол-2-ил)пропанамид (JFP).
2) Файл с записями о малых молекулах