PyMOL.
- Введение
В данном практикуме предложено рассмотреть и проиллюстрировать возможные нековалентные взаимодействия лиганда со своим белком-рецептором. Я изучал такие взаимодействия на структуре PDB 4YMB (1).
Данная структура была получена методом рентгеноструктурного анализа на разрешении 1.93 А. Структура включает в себя две белковые молекулы лиганд-связывающего домена ионотропного глутаматного рецептора GluK1 (2) крысы в составе одной ассиметрической единицы. Каждая белковая молекула связывает антагонист данного рецептора CNG10111.
Глутамат - основной возбуждающий нейромедиатор в центральной нервной системе позвоночных. Глутаматэргическая система вовлечена во такие процессы высшей нервной деятельности, как память и мышление. Однако с воздействием глутамата связывают развитие психических и нейродегенеративных заболеваний (3), в связи с чем может быть оправдан поиск эффективных антагонистов глутаматных рецепторов.
Данный эксперимент по получению структуры был проведен как часть работы (4) по поиску антагонистов таких рецепторов. Для антагониста метаботропных и ионотропных глутаматных рецепторов широкого спектра были предложены модификации за счет присоединения боковых групп; эти молекулы были синтезированы и была изучена аффинность их связывания с рецептором. Молекулы, показавшие наибольшую аффинность, были кристаллизованы с соответствующими рецепторами и была определена трехмерная структура такого комплекса. - Взаимодействия лиганда с рецептором
На Рисунке 1 отмечены взаимодействия, которые могут играть роль в удержании лиганда рецептором. Желтым отмечены водородные связи, голубым - соляные мостики между карбоксильной группой лиганда и ARG95 и азотом лиганда и карбоксильной группой GLU190, фиолетовым - возможный пи-катионный стекинг между атомом азота пирролидинового кольца и бензольным кольцом TYR61. Я посчитал важным вклад водородных связей, которые атомы кислорода лиганда, выступая акцепторами, могут образовывать с молекулами воды. Они, в свою очередь, могут принять водородные связи от SER173 и SER193 в одном случае, и от азота SER141 - в другом. Также мне показалось, что возможная водородная связь между карбоксильным кислородом GLU13 и кислородом TYR61 способствует поддержанию формы данного кармана связывания и аккомодации лиганда.
На Рисунке 2 приведено изображение поверхности кармана с помощью функции mesh. Видно, что карбоксильные группы и n-пропил лиганда хорошо ложатся в полости данного сайта связывания. Авторами работы отмечается, что присоединение именно n-пропила на 4 позицию пирролидина дало существенное увеличение аффинности связывания с рецептором по сравнению с другими рассмотренными модификациями.
Лиганд, заякоренный в глобуле другой белковой цепи, расположен схожим образом, и я не увидел каких-то иных возможных взаимодействий.
Паймол-сессия.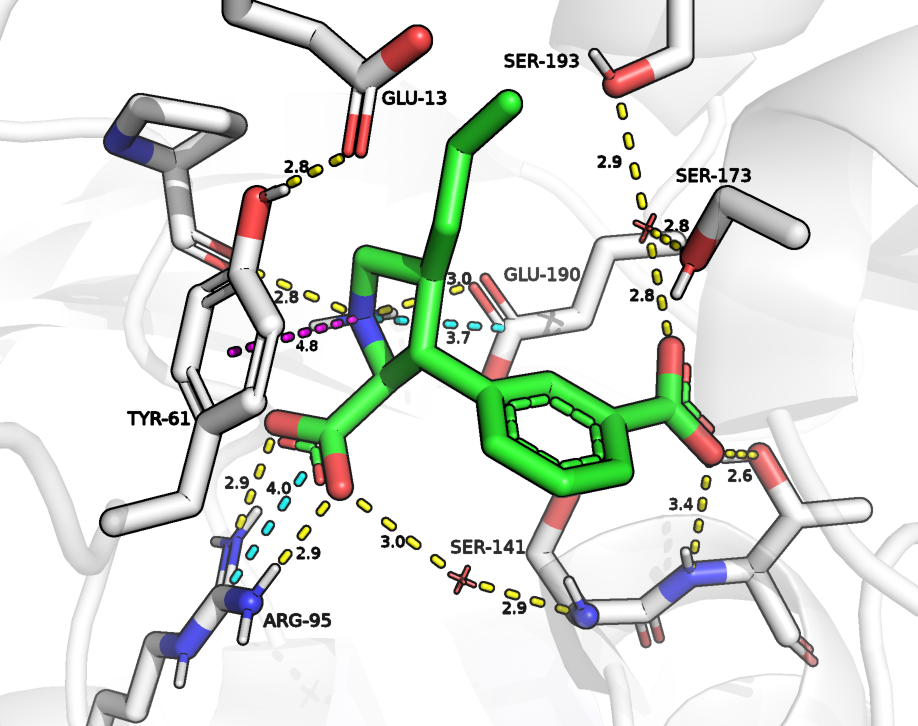
Рисунок 1. Взаимодействия лиганда (зеленым) с окружающими остатками (серым).
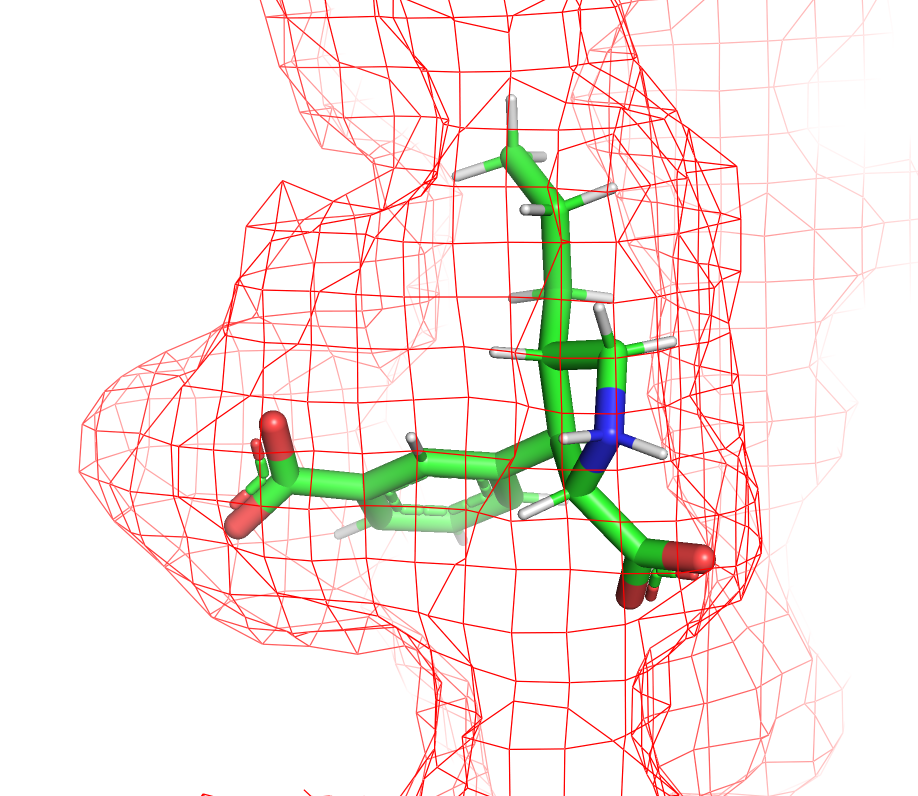
Рисунок 2. Карман связывания лиганда.
Источники:
1. R. P. D. Bank, 4YMB, (available at https://www.rcsb.org/structure/4YMB)
2.UniProtKB - P22756 (GRIK1_RAT)
3. Brian S. Meldrum, Glutamate as a Neurotransmitter in the Brain: Review of Physiology and Pathology, The Journal of Nutrition, Volume 130, Issue 4, April 2000, Pages 1007S–1015S,
4. N. Krogsgaard-Larsen, M. Storgaard, C. Møller, C. S. Demmer, J. Hansen, L. Han, R. N. Monrad, B. Nielsen, D. Tapken, D. S. Pickering, J. S. Kastrup, K. Frydenvang, L. Bunch, Structure-Activity Relationship Study of Ionotropic Glutamate Receptor Antagonist (2S,3R)-3-(3-Carboxyphenyl)pyrrolidine-2-carboxylic Acid. J. Med. Chem. 58, 6131–6150 (2015)