Электронная плотность.
- Введение
В данном практикуме изучается модель электронной плотности, построенной по результатам рентгеноструктурного анализа молекул белков. Я использовал структуры 7DF5, 2NMN, 7BCP.
- Задание 1
В этом задании требуется сравнить две структурные модели карбогидрат-узнающего домена белка галектина-3 - 7DF5 и 2NMN. Обе структуры получены методом ренгеноструктурного анализа, однако параметры данных экспериментов отличаются. Эксперимент для 7DF5 проведен в 2017 году, и получена структура с разрешением 1.08 Å на основании 53291 измеренных рефлексов со 100% покрытием интервала разрешений набора рефлексов. 2NMN была получена в 2006 году с разрешением 2.45 Å; получено 5400 рефлексов с полнотой 98.4%. Длина волны падающего излучения в первом случае составила 0.969 Å, во втором - 1.5418 Å.
На Рисунке 1 показаны белковые цепи структур, выравненных командой super (RMSD 0.284). Нектороые боковые цепи аминокислот не совсем точно накладываются друг на друга, а другие, как остатки глутаминовой кислоты 193 (покрашены фиолетовым), развернуты в противоположных направлениях. Это может быть объяснено движением остатков, находящихся на поверхности (и не только) глобулы белка в процессе кристаллизации. Паймол сессия.
Далее я взял участок белковой цепи с LYS233 по GLY238, входящий в β-лист, и отобразил электронную плотность остова с помощью функции isomesh для обеих структур на уровне подрезки 2. На Рисунке 2 видно, что полученная для структуры 7DF5 электронная плотность хорошо соответсвует вписанным в нее атомам, формируя вокруг них сферическую поверхность, что соответствует теоретическим представлениям о распределении ЭП. Электронная плотность на этом же участке 2NMN имеет угловатую форму, не очерчивая отдельные атомы остова. Кажется, что структура 2NMN имеет худшее разрешение, что согласуется с информацией из записей PDB. Это может говорить о том, что рефлексов, полученных во втором эксперименте, недостаточно для более детальной аппроксимации электронной плотности. Возможно, такая разница в разрешениях объясняется точностью приборов, использованных в экспериментах, а также длиной волны падающего излучения - для модели 7DF5 она меньше. Также возможной причиной высокого разрешения в случае 7DF5 мне кажется температура проведения эксперимента - 100 K, в то время как другой проводился при 295 K, что могло усилить тепловое движение атомов белка и в каждой конкретной ячейке кристалла одинаковые атомы заняли немного отличающиеся позиции.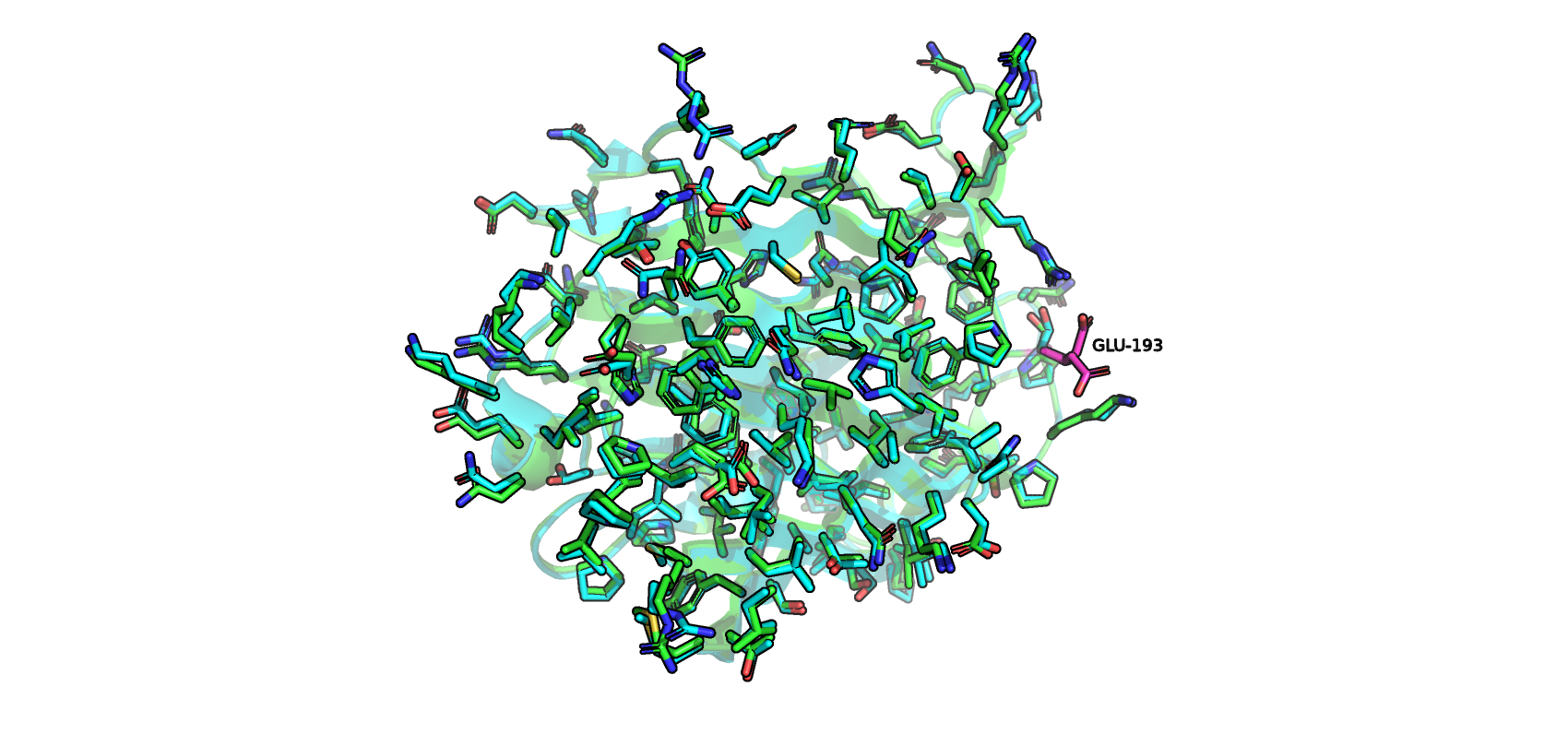
Рисунок 1. Отличающееся положение остатков.
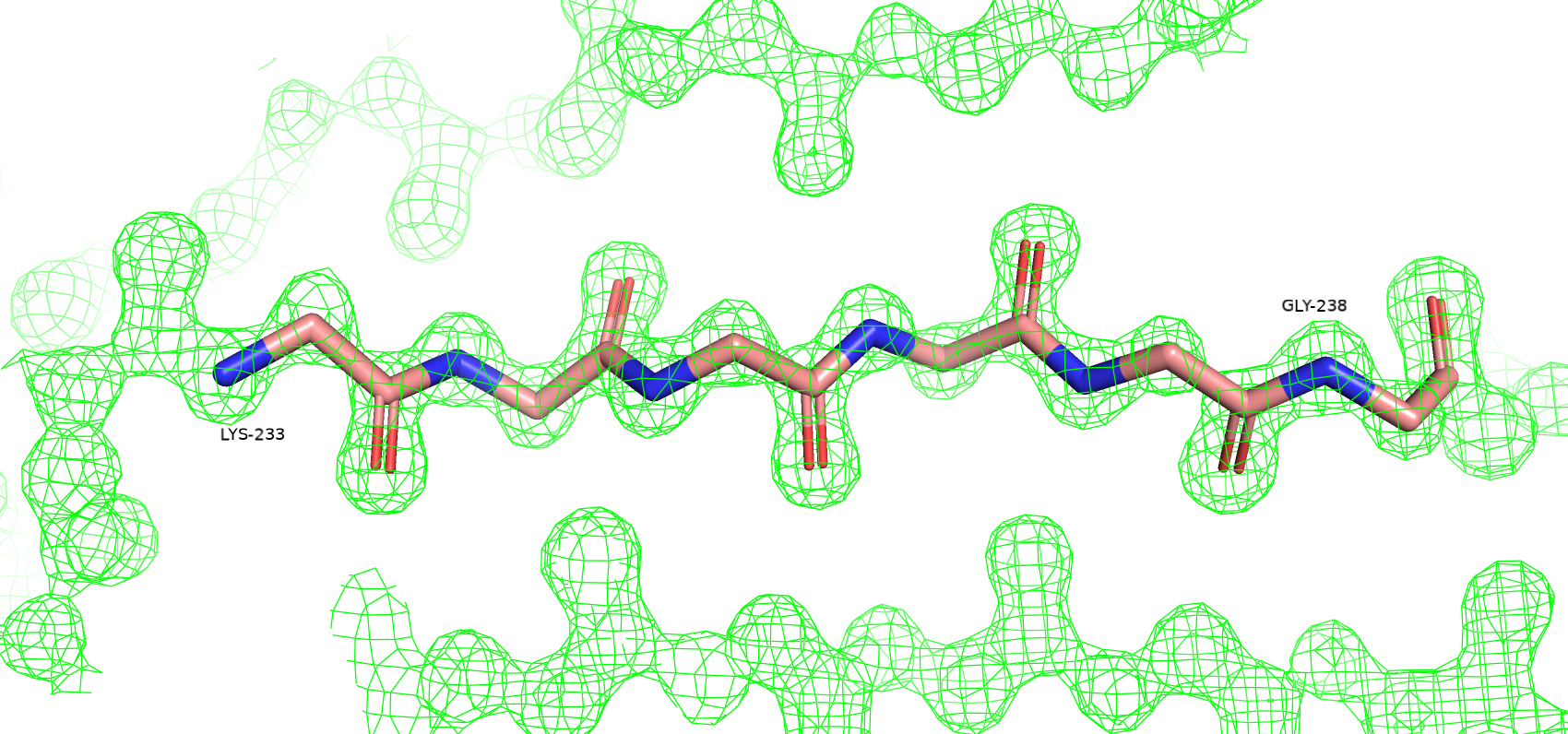
Рисунок 2. Электроннная плотность фрагмента 7DF5 на уровне подрезки 2, carve = 1.1.
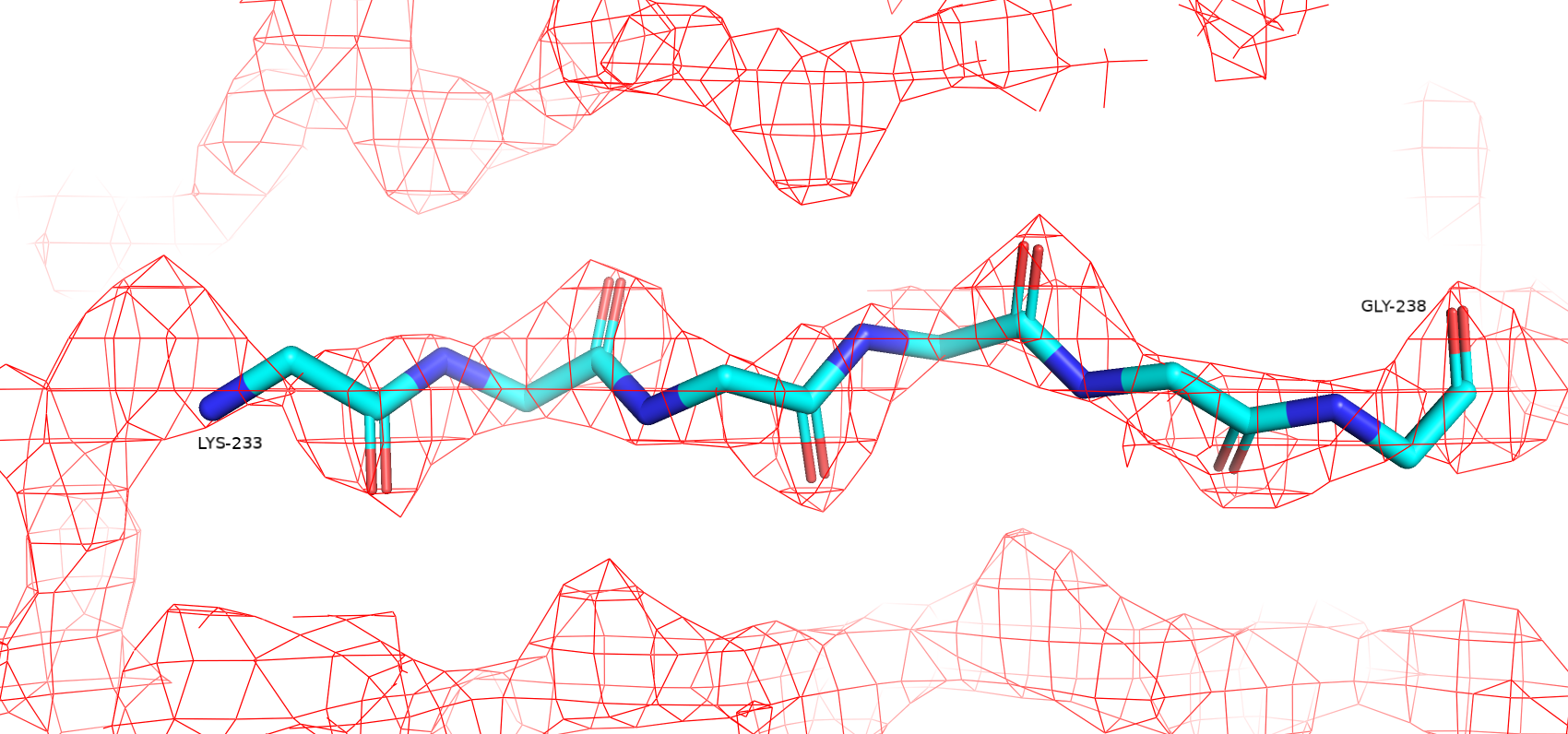
Рисунок 3. Электронная плотность фрагмента 2NMN на уровне подрезки 2, carve = 1.8.
- Задание 2
Для визуализации электронной плотности на разных уровнях подрезки я использовал структуру 7BCP. В ней приведена модель белка, связывающего глюконовую ксилоту, с разрешением 2.00 Å, полученную методом ренгеноструктурного анализа. Электронная плотность отображена только для остова белка, белок покрашен по В-фактору, где синему цвету соответсвуют меньшие значения фактора, а желтым - большие. B-фактор - мера отклонения позиции атома от его среднего положения по всем ячейкам кристалла.
На рисунках 4, 5, 6 показана ЭП остова белка на разных уровнях подрезки. Видно, что с увеличением уровня для некоторых участков остова плотность не отображается: эти участки располагаются ближе к поверхности белка и имеют большую свободу колебаний в растворе или кристалле. Части остова, образующего β-листы и α-спирали, покрашены в синий цвет, на них отображается ЭП даже на уровне подрезки 3. Исключением является α-спираль, расположенная в верхней части рисунка, - для нее значения B-фактора выше, и ее ЭП почти не отображена на уровне 3. Также N-конец, не вовлеченный в образование вторичной структуры, окрашен в зеленый, и лишь для отдельных его участков отображается ЭП на высоких уровнях подрезки.
Можно предположить, что из-за тепловых колебаний атомов белка внутри кристалла "размывается" электронная плотность, вычисляемая в ходе эксперимента, так как такие подвижные атомы обнаруживаются в большем объеме пространства. Таким образом, высокая ЭП соответствует менее подвижным участкам белка, а низкая ЭП подвижных участков перестает отображаться на высоких уровнях подрезки, так как не достигает таких значений в данных точках пространства.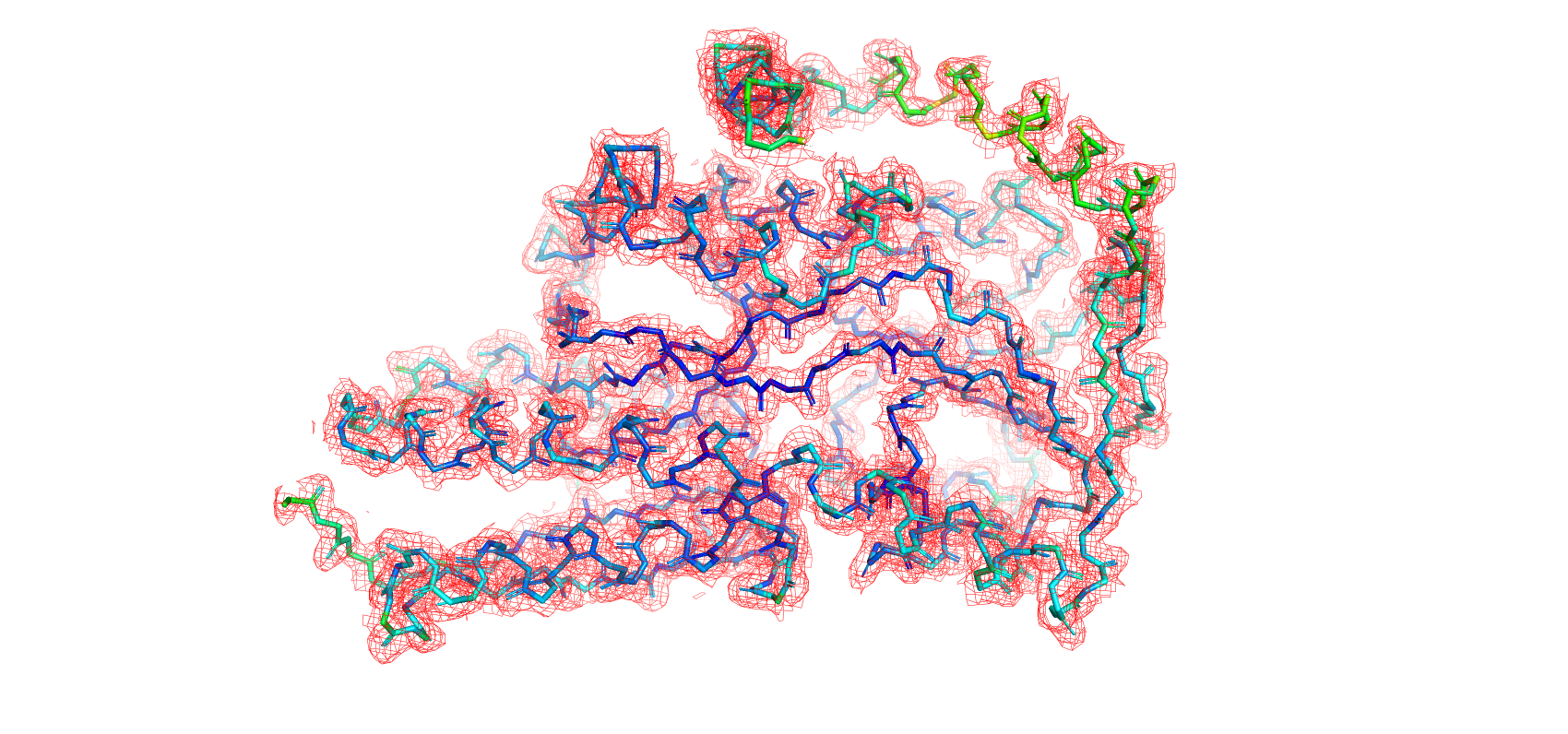
Рисунок 4. ЭП остова белка на уровне подрезки 1.
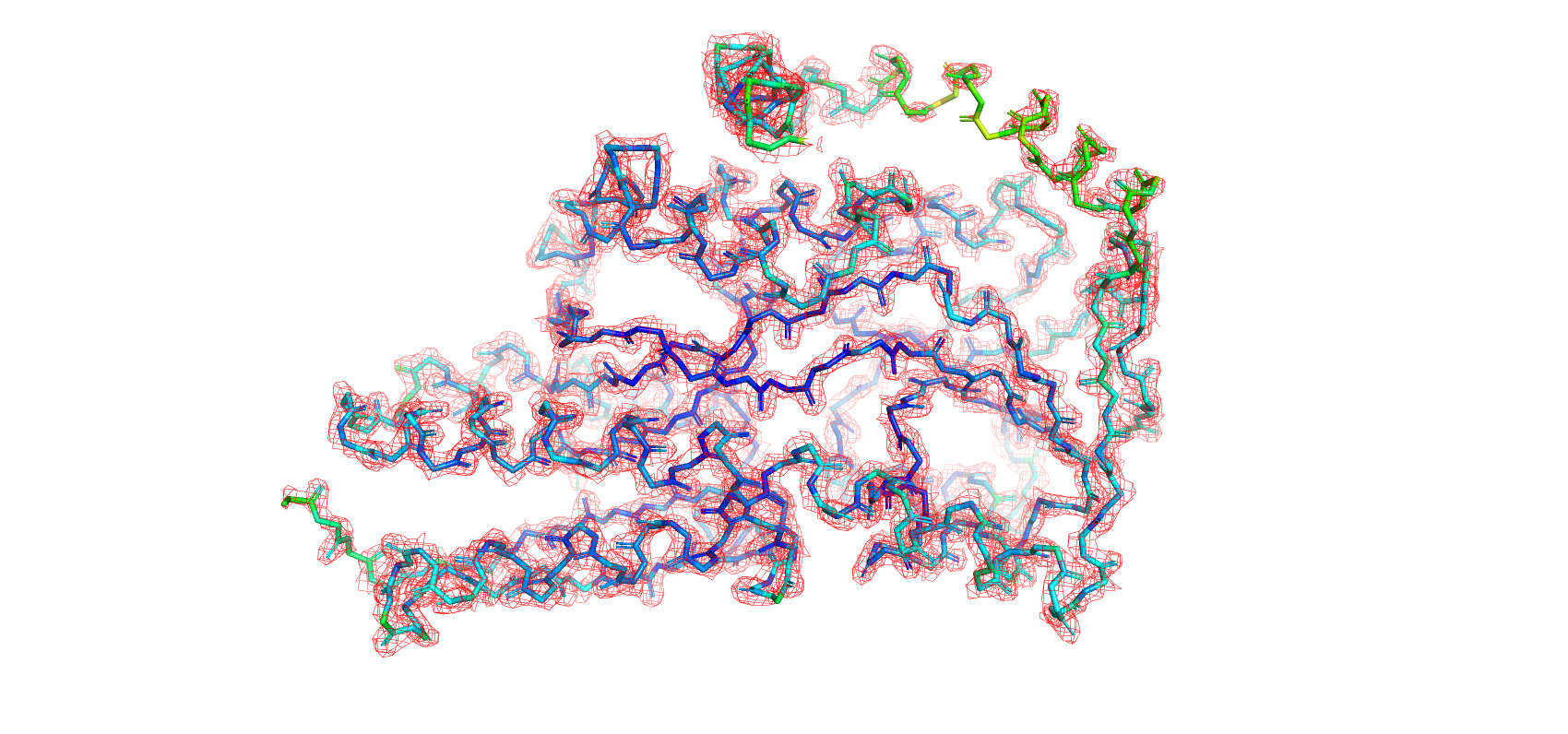
Рисунок 5. ЭП остова белка на уровне подрезки 2.
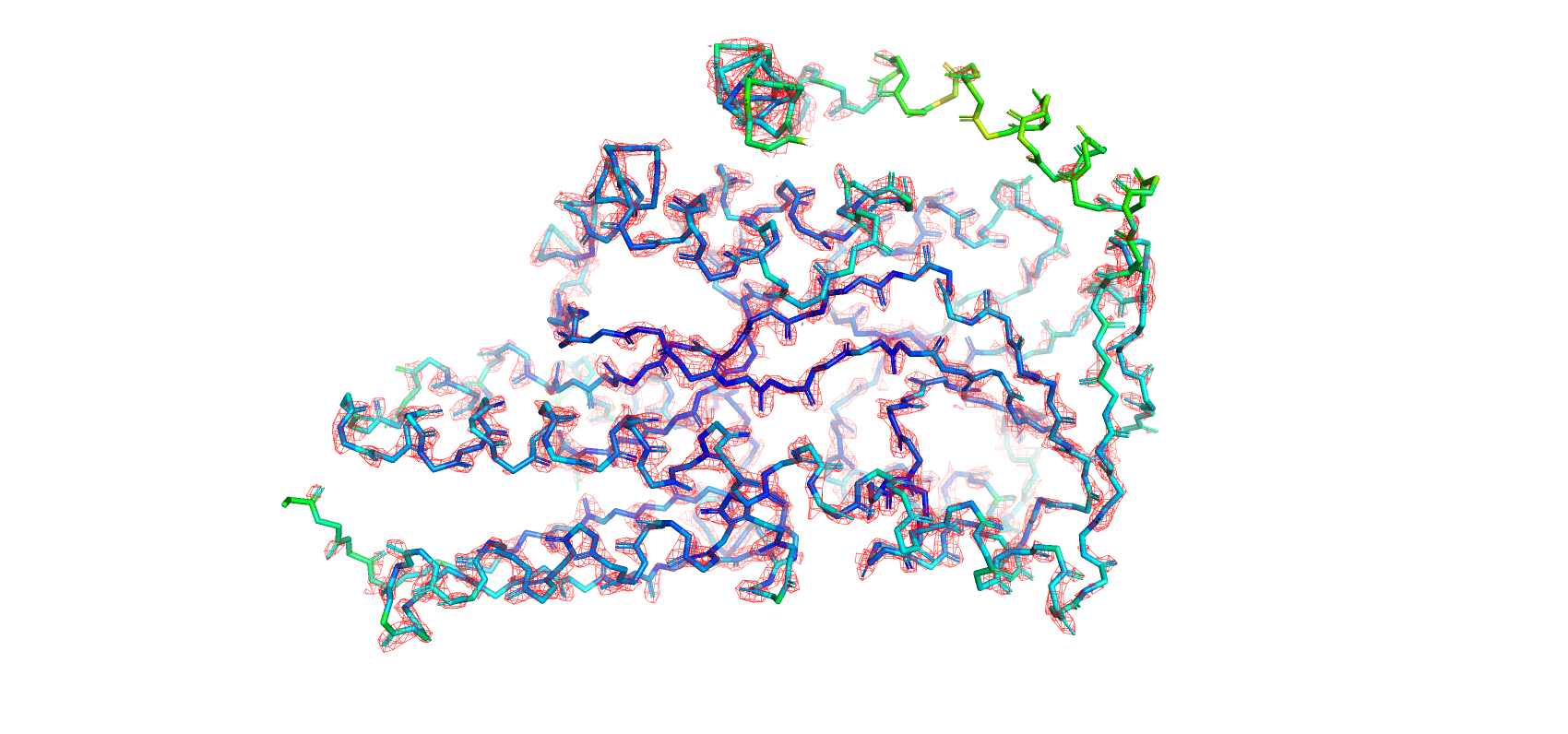
Рисунок 6. ЭП остова белка на уровне подрезки 3.
- Задание 3
На рисунках 7, 8, 9 показана ЭП лиганда - глюконовой кислоты - на разных уровнях подрезки. На уровнях 1 и 2 ЭП отображается вокруг всех атомов лиганда, но на уровне 3 остается в основном вокруг атомов кислорода. На рисунке 9 показаны возможные нековалентные взаимодействия между лигандом и рецептором. Показаны только полярные водороды. Карбоксильная группа образует солевой мостик с отсатком аргинина-177, а водород у атома O6 может образовывать π-катионную связь с бензольным кольцом фенилаланина-96.
Я вижу два возможных объяснения тому, что расчитанное значение ЭП не достигает уровня в 3 сигмы вокруг углеродов, а вокруг кислородов - достигает. Во-первых, кислород находится правее углерода в своем периоде, атом O меньше в диаметре, чем атом С, также кислород частично оттягивает на себя электроны углерода и водорода, что дает большую электронную плотность таким атомам. Во-вторых, именно кислороды выступают донорами или акцепторами связей лиганда с белком, что фиксирует их, но не запрещает колебания углеродного скелета и вращения вокруг C-C и C-O связей. Однако B-факторы, указанные в записи PDB для атомов углерода и кислорода глюконовой кислоты в этой структуре разнятся не сильно и принимают достаточно низкие значения порядка 20 Å2.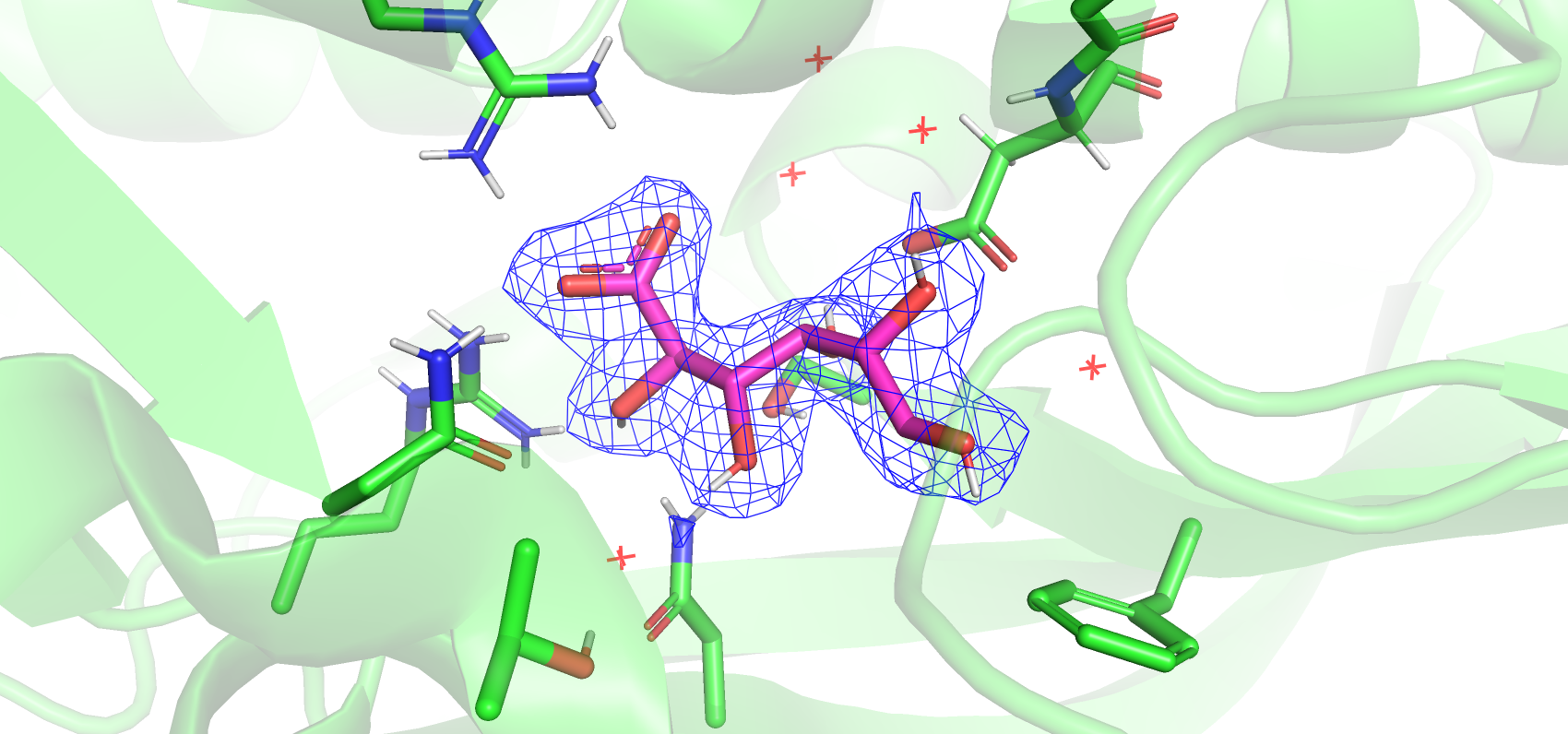
Рисунок 7. ЭП вокруг лиганда на уровне подрезки 1.
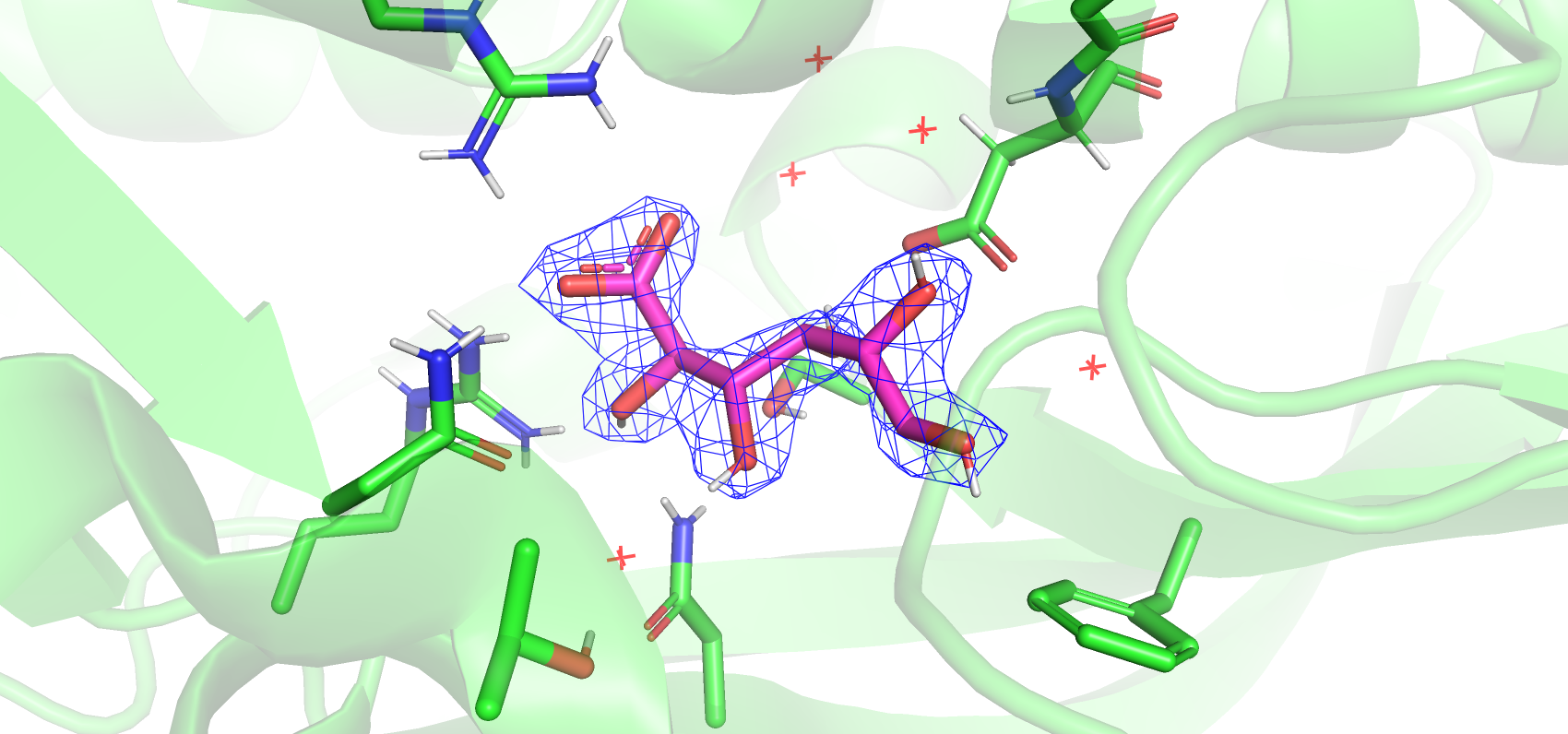
Рисунок 8. ЭП вокруг лиганда на уровне подрезки 2.
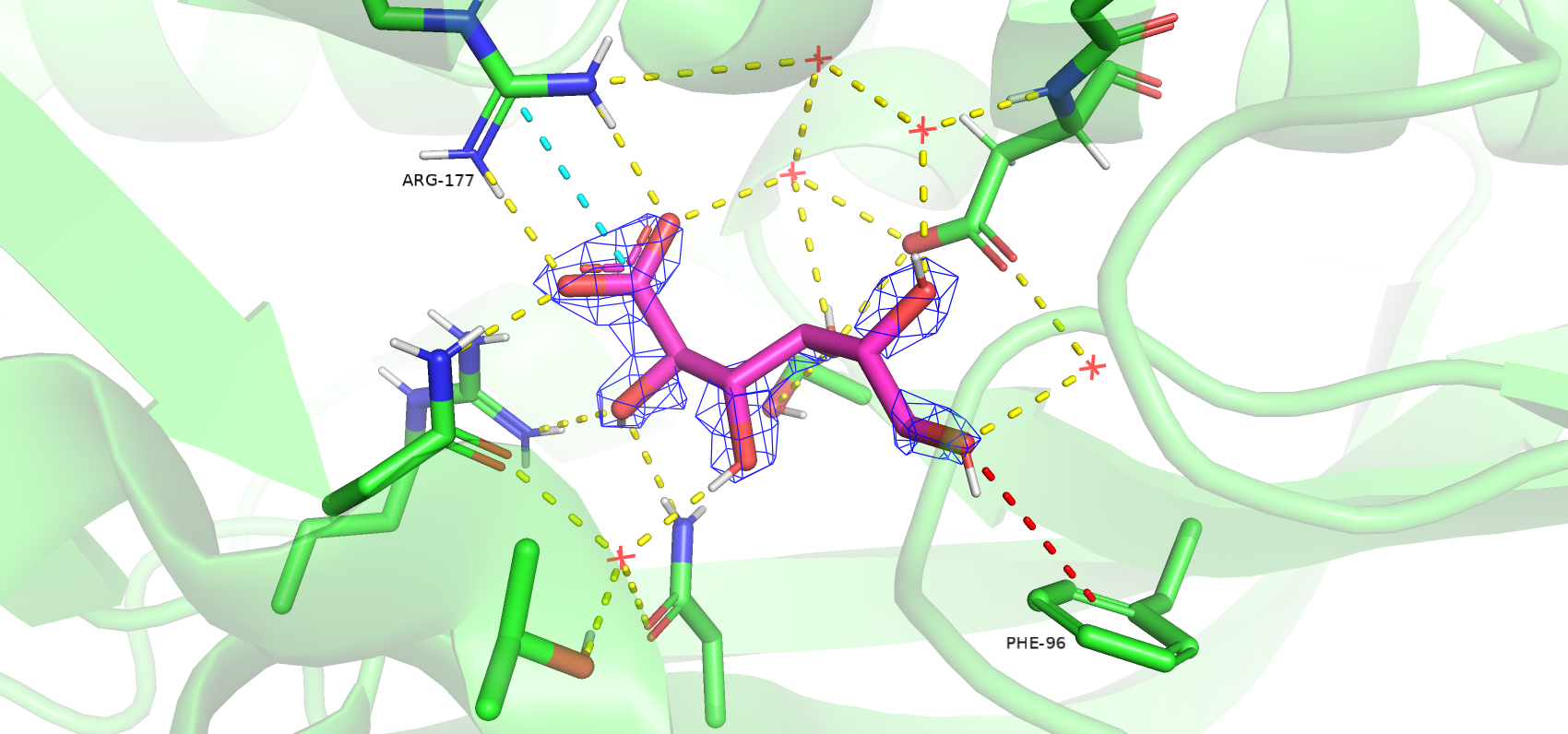
Рисунок 9. ЭП вокруг лиганда на уровне подрезки 3 с отмеченными взаимодействиями. Желтым показаны водородные связи, голубым - соляной мостик, красным - пи-водородная связь.