-

-
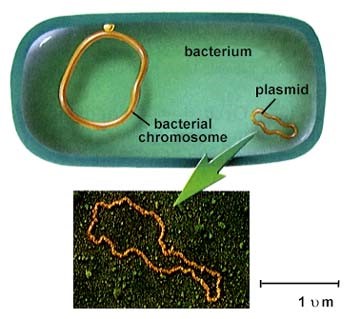
Общие сведения о плазмидах
Плазмида (plasmid) - способный к автономной (независимой от основной хромосомы) репликации внехромосомный генетический элемент, существующий у многих видов бактерий, обычно дающий преимущество клетке-хозяину (например, устойчивость к антибиотикам, тяжелым металлам и т.п.). Это линейные или кольцевые ковалентно замкнутые молекулы ДНК, содержащие от 1500 до 40000 пар нуклеотидов. Для них характерно стабильное существование и наследование в бактериях в ряду клеточных поколений. Используются в качестве векторов для клонированияя. Размеры плазмид варьируют от нескольких тысяч до сотен тысяч пар оснований, а число копий на клетку - от одной до нескольких сотен .
Хотя многие плазмиды дают клеткам-хозяевам ощутимые селективные преимущества, большинство из них являются криптическими, т.е. не проявляющимися в фенотипе клеток. Область начала репликации небольшой плазмиды ColE1 , несущей гены устойчивости к колицинам, традиционно используется в генной инженерии при конструировании векторных молекул ДНК, которые находят применение для клонирования и экспрессии в клетках E. coli коротких последовательностей нуклеотидов. Плазмиды обнаружены у многих бактерий, принадлежащих к разным таксономическим группам. Количество плазмидной ДНК в клетке составляет обычно не более нескольких процентов от клеточного генома, а число плазмид колеблется от 1 до 38. Большинство плазмид состоит из трех групп генов: участка ДНК, ответственного за автономную репликацию плазмиды в клетке; системы генов, обеспечивающих возможность переноса плазмид из одной клетки в другую; генов, определяющих свойства, полезные для клетки-хозяина. Отличительная особенность плазмид - способность к автономной репликации, поэтому минимальное количество ДНК, которое может быть названо плазмидой, - это фрагмент, обеспечивающий автономную репликацию плазмидной ДНК в клетке как единого целого. Обычно о присутствии плазмид в бактериальной клетке судят по проявлению определенных признаков, к которым относится устойчивость к отдельным лекарственным препаратам, способность к переносу генов при конъюгации , синтез веществ антибиотической природы, способность использовать некоторые сахара или обеспечивать деградацию ряда веществ.
Генетический аппарат бактерии[5]
Из перечисленного выше видно, что плазмиды делают возможным существование организмов в более широком диапазоне условий внешней среды, т.е. действуют как факторы адаптации. Большую группу составляют плазмиды с нерасшифрованными функциями; такие плазмиды выявляют с использованием физико-химических методов. Большинство бактериальных плазмид имеет фактор несовместимости и фактор переноса. Они несут множество специальных, детерминируемых каждой отдельной плазмидой маркеров, таких как устойчивость к антибиотикам, тяжелым металлам, ультрафиолетовому облучению, способность к биосинтезу токсинов.Наиболее распространенным методом генной инженерии является метод получения рекомбинантных, т. е. содержащих чужеродный ген, плазмид. Каждая бактерия помимо основной, не покидающей клетку молекулы ДНК (5-6 млн. пар нуклеотидов), может содержать, как уже было сказано, несколько различных плазмид, которыми она обменивается с другими бактериями. Плазмиды реплицируются в бактериальной клетке не в то же время, что основная молекула ДНК. Хотя на долю плазмид приходится лишь небольшая часть клеточной ДНК, именно они несут такие жизненно важные для бактерии гены, как гены лекарственной устойчивости. Разные плазмиды содержат разные гены устойчивости к антибактериальным препаратам. Большая часть таких препаратов - антибиотиков используется в качестве лекарств при лечении ряда заболеваний человека и домашних животных. Бактерия, имеющая разные плазмиды, приобретает устойчивость к различным антибиотикам, к солям тяжелых металлов. При действии определенного антибиотика на бактериальные клетки плазмиды, придающие устойчивость к нему, быстро распространяются среди бактерий, сохраняя им жизнь. Простота устройства плазмид и легкость, с которой они входят и выходят из бактерий, используются генными инженерами для введения в клетки бактерий генов высших организмов.
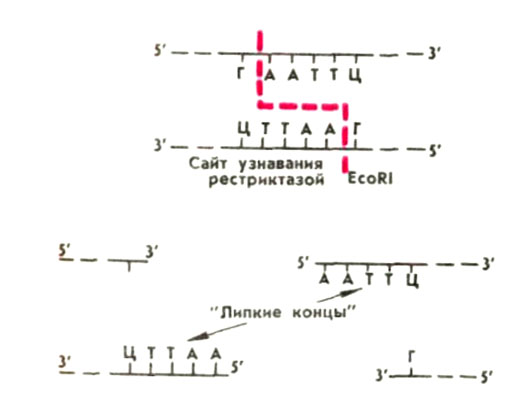
Мощным инструментом генной инженерии являются открытые в 1974 г. ферменты - рестрикционные эндонуклеазы, или рестриктазы. Рестрикция буквально означает ограничение. Бактериальные клетки вырабатывают рестриктазы для разрушения инородной, в первую очередь фаговой ДНК, что необходимо для ограничения вирусной инфекции. Рестриктазы узнают определенные последовательности нуклеотидов (так называемые сайты - участки узнавания) и вносят симметричные, расположенные наискось друг от друга, разрывы в цепях ДНК на равных расстояниях от центра сайта узнавания. В результате на концах каждого фрагмента рестриктированной ДНК образуются короткие одноцепочечные "хвосты", называемые липкими концами. Из разных видов бактерий выделено около 200 различных рестриктаз, для которых описаны сайты рестрикции.В 60-70 годы прошлого века накопилось множество фактов, свидетельствующих о роли плазмид, преимущественно крупных, в процессе быстрого распространения в клинике устойчивых штаммов бактерий. И тогда закономерно встал вопрос о происхождении этих плазмид: присутствовали ли они в клетках патогенных бактерий изначально (до применения антибиотиков), а затем просто произошло увеличение их численности, или же они сформировались в условиях интенсивного использования различных антибиотиков. Для ответа на этот вопрос повторно исследовали штаммы энтеробактерий из коллекции Муррея, выделенные в годы, предшествующие открытию и применению антибиотиков. Оказалось, что большинство исследованных штаммов содержат конъюгативные плазмиды, причем тех же групп несовместимости, что и современные штаммы, но, в отличие от последних, гены антибиотикоустойчивости в них отсутствуют [ Hughes, 1983 , Datta, 1983 ]. Поэтому был сделан однозначный вывод, что начало процесса возникновения плазмид с генами лекарственной устойчивости следует приурочить к первым годам использования антибиотиков в медицинской практике.
Многочисленные исследования, выполненные в лабораториях различных стран в последующие годы, показали, что формирование плазмид, несущих гены множественной лекарственной устойчивости, происходило путем внедрения в их ДНК различных мобильных элементов, преимущественно транспозонов и интегронов . В ряде случаев удалось проследить этапы этого процесса во времени. Так, в результате ретроспективного анализа структуры конъюгативных плазмид Salmonella enterica Typhimurium было установлено, что формирование и повсеместное распространение штаммов салмонелл, характеризующихся множественной лекарственной устойчивостью, произошло в результате нескольких последовательных актов встраивания интегронов, несущих различные наборы генов устойчивости, в геном этих плазмид [ Carattoli, 2001 ]. В дальнейшем неоднократно наблюдалось, как по мере внедрения в медицинскую практику новых антибиотиков неизменно появлялись плазмиды, содержащие интегроны с генами, обеспечивающими устойчивость бактерий к этим антибиотикам. В плазмидах "современных" штаммов бактерий обычно обнаруживают интегроны, содержащие длинные цепочки генов устойчивости, иногда - до 9 генов [ Naas, 2001 ]. В настоящее время, благодаря использованию современных методов молекулярной биологии, удалось полностью расшифровать молекулярно- генетическую структуру многих сложных плазмид, обнаруженных в устойчивых штаммах бактерий. Типичными примерами плазмид, демонстрирующих сложную мозаичную структуру и выделенных из различных источников сравнительно недавно, являются плазмида pTP10 и плазмида pRSB107[3].
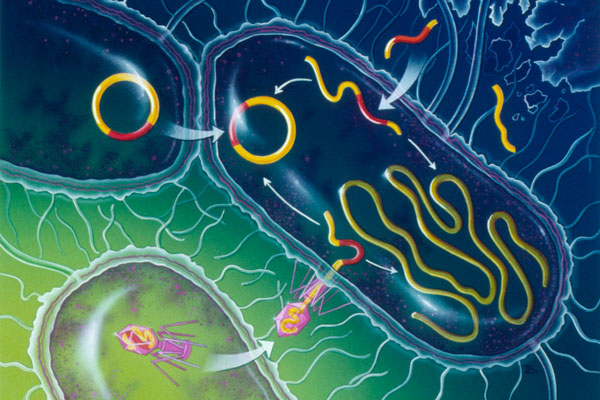
Два типа горизонтального переноса генов у бактерий - трансформация (с помощью плазмид) и трансдукция (осуществляют вирусы)[4]Сведения о плазмидах Lactobacillus plantarum ZJ316
Для начала работы необходимо скопировать текстовый документ plasmids.txt[1] в таблицу "Еxcel", где сразу же программа сформирует соотсветствующие столбцы и строки. Обратим внимание, что между видивым названием и родовым символ пробела - используем его как символ раздела строк, таким образом получая список родов. Скопируем для удобства полученный столбец в таблицу на новом листе. Нетрудно заметить, что число плазмид можно определить по тому, сколько раз в списке написано родовое/видовое название. Поэтому воспользуемся функцией подсчета (СЧЁТЕСЛИ) одинаковых ячеек и выдадим значение в следующем столбце. Теперь изменим формулы на числа (можно F9) в полученном столбце. Затем просто удалим одинаковые ячейки и получим неоходимую сводную таблицу.
По данным, взятым из документа plasmids.txt, представленныых даллее, можно сделать следующие выводы:
Lactobacillus plantarum ZJ316 Bacteria Firmicutes Bacilli pLP-ZJ101 NC_021903.1 CP006247 15.167 40.1727 13 - - - 15 2 1 Lactobacillus plantarum ZJ316 Bacteria Firmicutes Bacilli pLP-ZJ103 NC_021912.1 CP006249 41.508 39.4984 33 - - - 37 4 1 Lactobacillus plantarum ZJ316 Bacteria Firmicutes Bacilli pLP-ZJ102 NC_021904.1 CP006248 39.116 38.6926 33 - - - 38 5 1
1.В роде Lactobacillus представлена 231 плазмида (число плазмид можно определить по тому, сколько раз в списке написано родовое/видовое название).
2.В штамме Lactobacillus plantarum ZJ316 представлено 3 плазмиды, самая длинная из которых - 41.508Kb, самая короткая - 15.167Kb.
3.Учитывая полученные данные, рассчитаем среднюю длину плДНК у данной бактерии и обозначим медиану длин. Очевидно, что медиана ряда длинн - плазмида pLP-ZJ102 (39.116Kb). Средняя длина составила 31.930Kb.
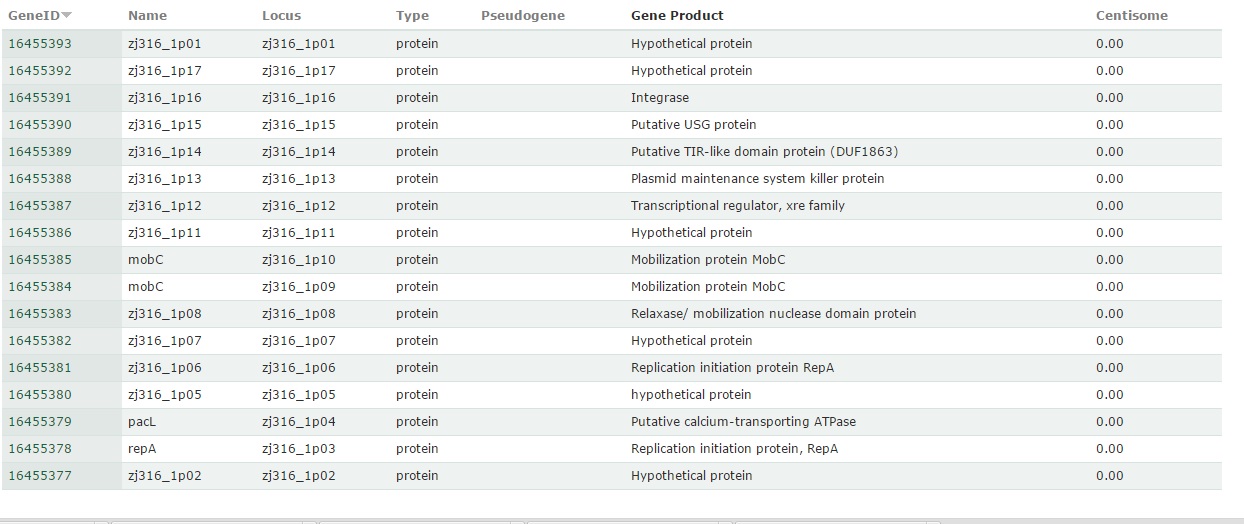
Белки, закодированные в плазмиде pLP-ZJ101[2]
Источники:
[1] NCBI [Электронный ресурс]
[2] EcoGene-RefSeq [Электронный ресурс] // URL: http://www.ecogene.org/refseq/refseq/NC_021903/searchtool///protein///all?sort=desc&order=GeneID
[3] Биология и медицина [Электронный ресурс] // URL: http://medbiol.ru/medbiol/antib_rez/0001d400.htm
© Yuliia Preobrazhenskaya, 2015