Практикум №5
Задание №1: Протонирование.
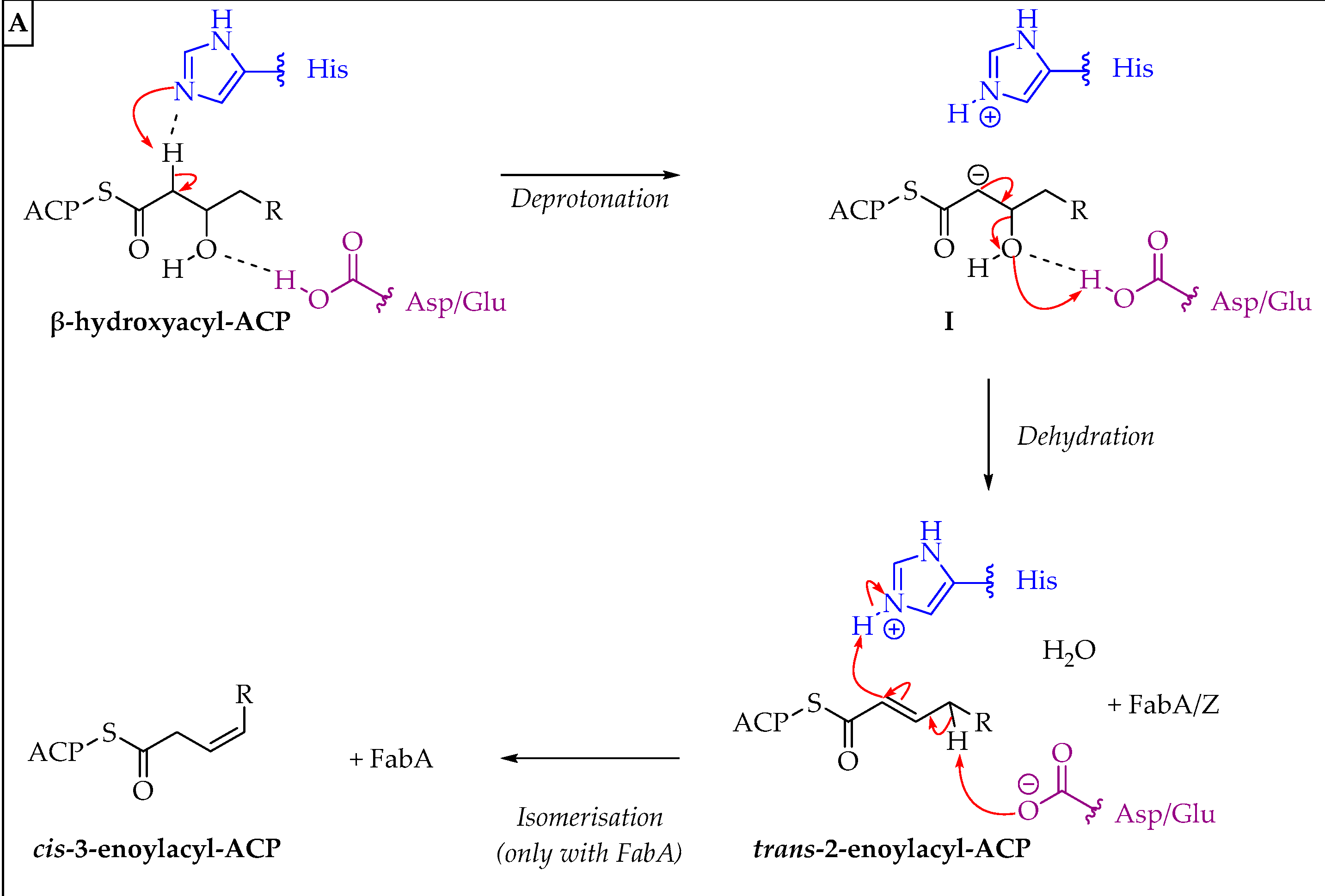
В этом практикуме я буду работать со структурой 7SVT, полученной методом рентгеноструктурного анализа при pH = 3.5 с разрешением 2.40 Å. Это структура 3-гидрокси-ACP-дегидратазы HadAB, составляющей комплекс HadAB/AC Mycobacterium tuberculosis, принимающий участие в синтезе миколовых кислот, в связи с ингибитором. Основную роль в катализе принимают участки B-D36 и B-H41 (каталитическая диада). В составе асимметрической единицы представлено 4 комплекса HadAB (в пространственной группе P212121): 4 пары гетеродимеров - A/B, H/I, O/P, V/W.
С использованием сервиса PDB2PQR алгоритмом PROPKA с указанием pH (3.5) были получены следующие файлы: ptgtghas82.log, ptgtghas82.pqr.
Среди всех остатков (370), включающих в себя ASP (83), GLU (83), HIS (24), было найдено несколько представителей с наибольшим значением pKa, превышающим к тому же значение pH кристаллизации (3.5):
1. ASP-36, W, 7.12 (каталитический аспарагин)
2. GLU-21, O, 12.44
3. HIS-11, A, 6.98
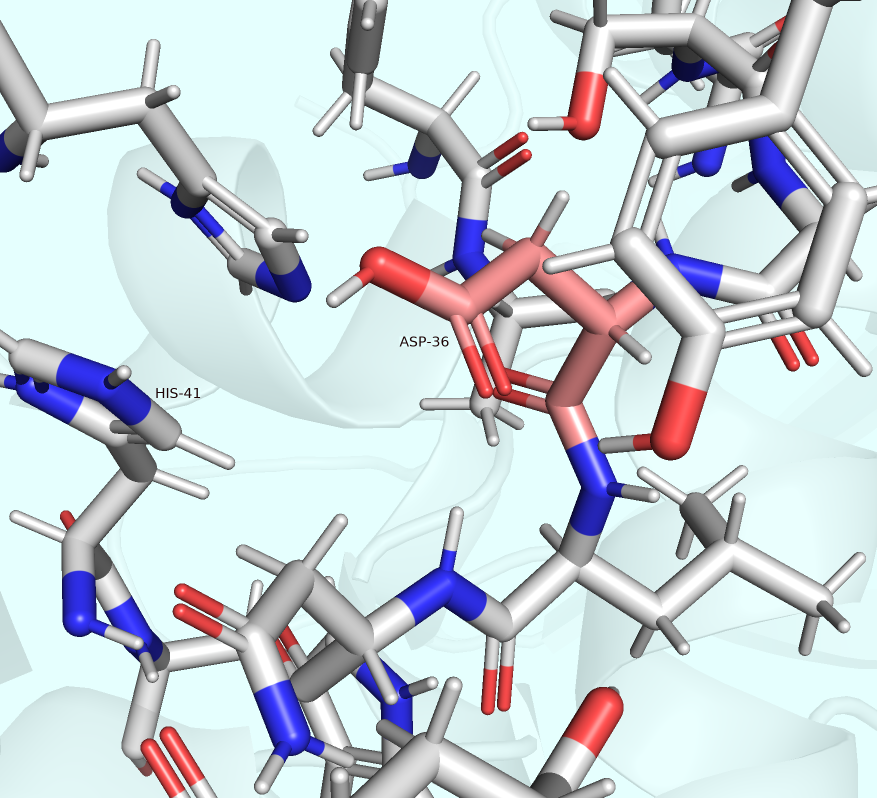
К сожалению, рассмотрение окружения ASP-36 не привело к удовлетворительным результатам. Я не нашёл в структуре ничего, что способствовало бы стабилизации именно протонированной формы этого остатка (Рис. 1).
Нельзя сказать, что он находится в гидрофобном окружении (которое бы повышало потенциальную энергию структуры, будь аспартат депротонирован и, соответствено, заряжен). Точно так же нет никаких водородных связей, в которых участвует этот водород. Нет и отрицательно заряженных остатков поблизости, которые бы конфликтовали с ASP-36 в противном случае (если бы он не был протонирован).
Тем не менее оказывается, что в нативном виде ASP-36 большую часть времени присутствует не иначе как в протонированном виде, поскольку именно эта форма является важным составляющим катализа ферментов 3-гидрокси-ACP-дегидратаз.
Но ристалле данная структура содержится при низких pH и в отсутствие субстрата, что ставит под сомнение этот аргумент. Быть может, в стабилизацию вовлечён ингибитор, структура которого создаёт эффект оксианионного центра [1].
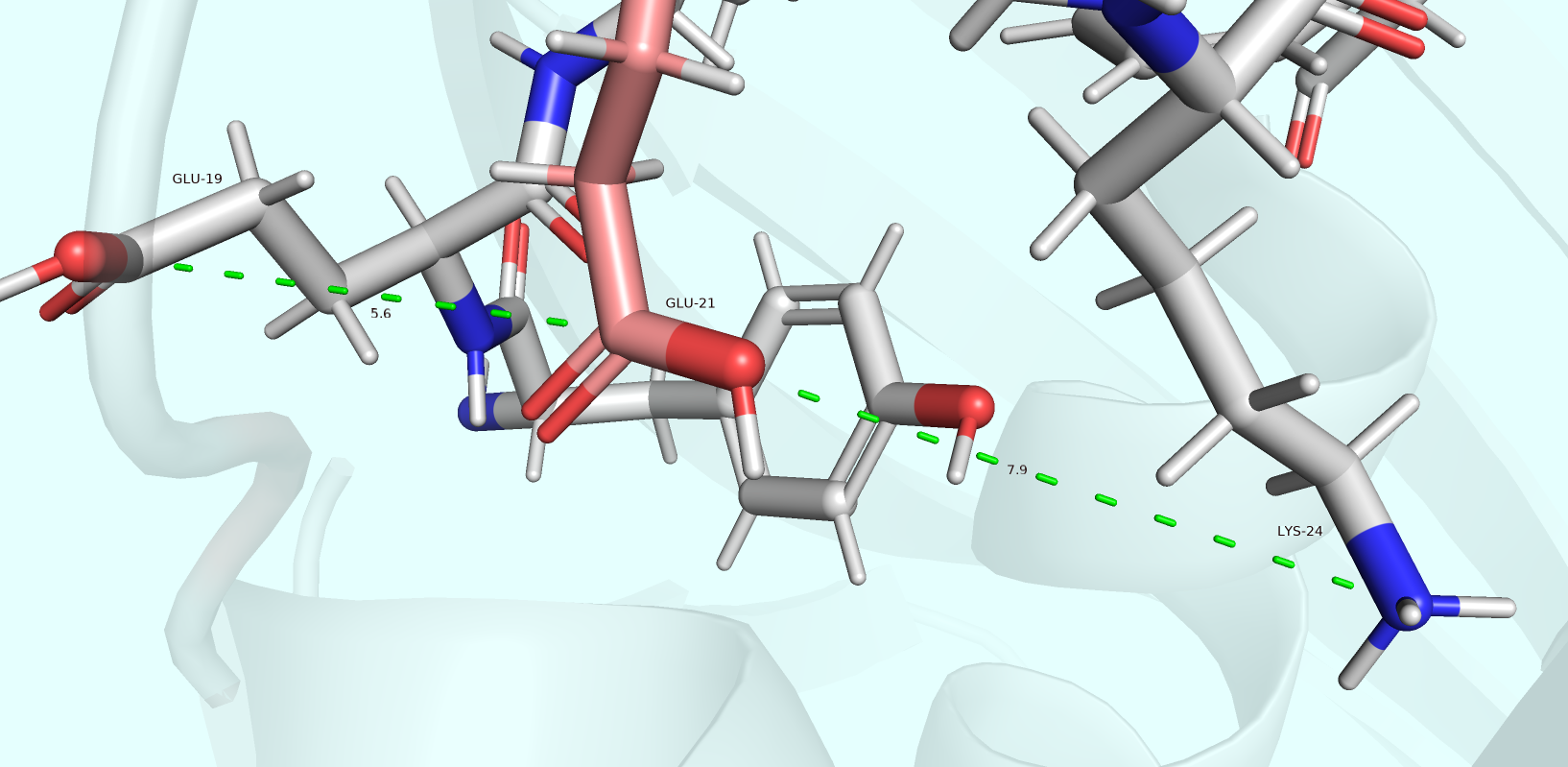
Рассмотрим теперь окружение GLU-21 (Рис. 3). Здесь ситуация оказывается ещё более непростой: остаток располагается на поверхности белка, имея возможность к контакту с растворителем. Поэтому в целом было бы логичнее оказаться депротонированным (для контакта с водой, поскольку рядом нет гидрофобного окружения). Притом, что pH окружения равен 3.5, а в норме у глутамата pKa около 4.5.
Мне совершенно неясно, откуда PROBKA взяла цифру в 12.44. Возникает подозрение, что, поскольку изначальный PDB файл содержит асимметрическую единицу с 4-мя структурами, PROBKA думает, что это всё есть единая макромолекула (с большим количеством цепей), и для неё этот глутамат - не наружный глутамат (как должно быть), а находящийся в контакте с соседями по асимметрической единице.
Таким образом, оказывается совсем сложным пытаться предсказывать качество работы пробки для остатков, находящийхся не вглуби фермента...
Посмотрим теперь, наконец, на остаток HIS-11 в цепи A.
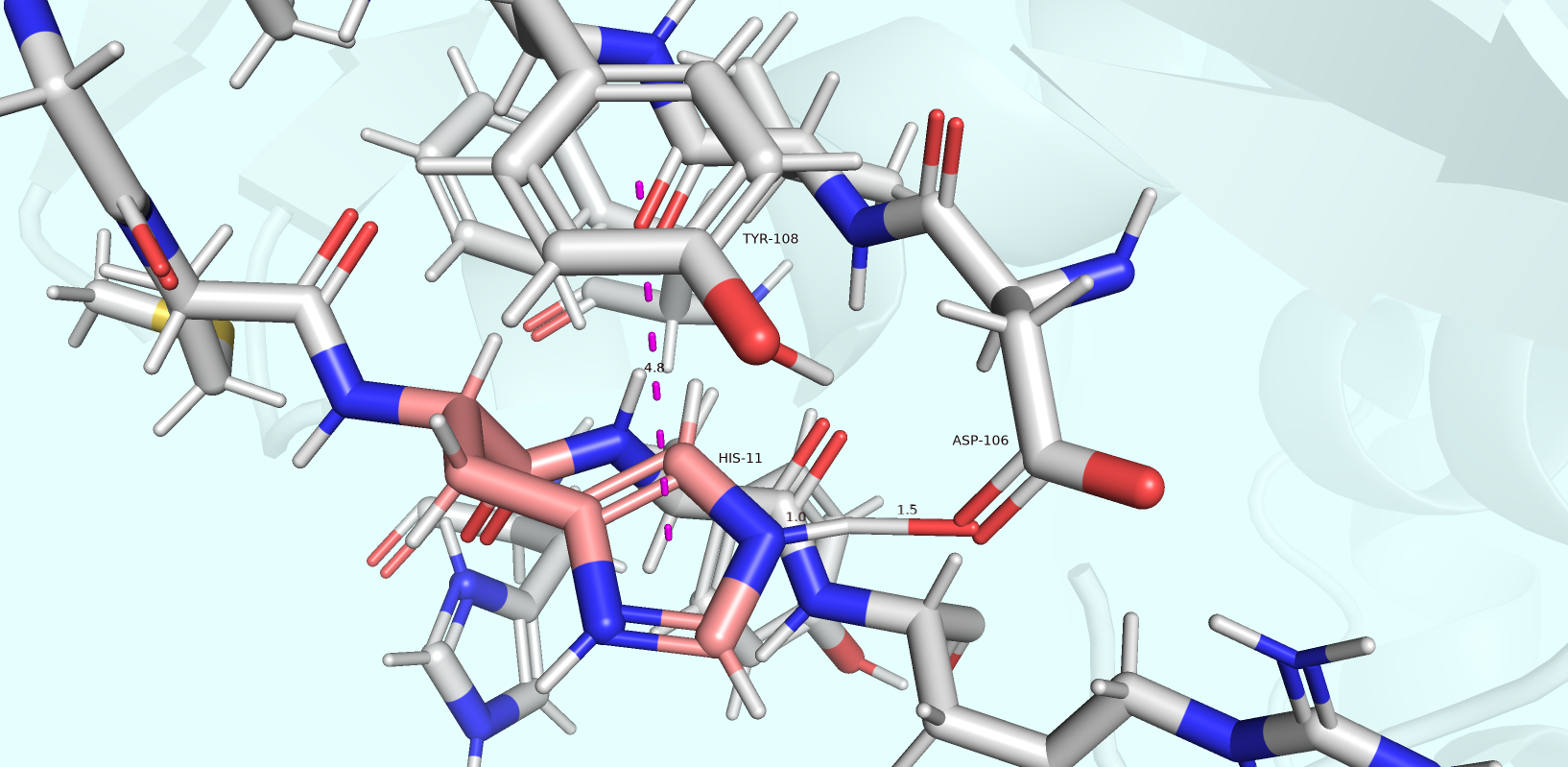
Здесь всё интереснее. Привлекает внимание сразу специфическая водородная связь, в рамках которой водород принадлежит и HIS-11, и ASP-106. Это так называемая low-barrier HB, более устойчивая водородная связь, которая имеет место в предположении, что ASP-106 и HIS-11 протонированы. Но здесь вроде бы как и нет никаких противодействий протонированному положительно заряженному гистидину. Формируется параллельно сдвинутый стекинг, образуется прочная водородная связь (в этом отношении достаточно было ε-гистидина, но и по δ-положению ничего не мешает протонированию). Таким образом, в данном случае я верю тому, как PROBKA отобразила водороды (несмотря на тяготы визуализации PyMOL, рисующего двухвалентные водроды...)
Кирилл Кузенков, студент четвёртого курса ФББ