Практикум №7
Задание №1: Реализация алгоритма DOMAK
В заготовленном Colab notebook был реализован алгоритм DOMAK, используемый для разбиения структуры на домены. Представлялось необходимым продемонстрировать его работу на выданной структуре 1EUT фермента нейраминидазы массы 68 kDa из Micromonospora viridifaciens.
Эта бактерия экспрессирует две формы нейраминидазы - 41 kDa и 68 kDa. Первая (малая) форма представляет из себя классическую укладку β-пропеллера нейраминидазы, в то время как вторая (большая) имеет два дополнительных домена: первый имеет иммуноглобулинподобную укладку и служит связующим звеном для второго домена, который гомологичен галактозосвязывающему домену грибковой галактозидазы. Таким образом, 68 kDa сиалидаза Micromonospora viridifaciens представляет из себя комбинацию из углевод-связываюего и расщепляющего доменов, между которыми находится третий, связующий их домен [1].
На полученном в результате работы алгоритма графике (Рис. 1) очевидным образом обособляются два пика, соответствующие 401-ому и 501-ому остаткам белка (Здесь и далее приводится авторская нумерация остатков).
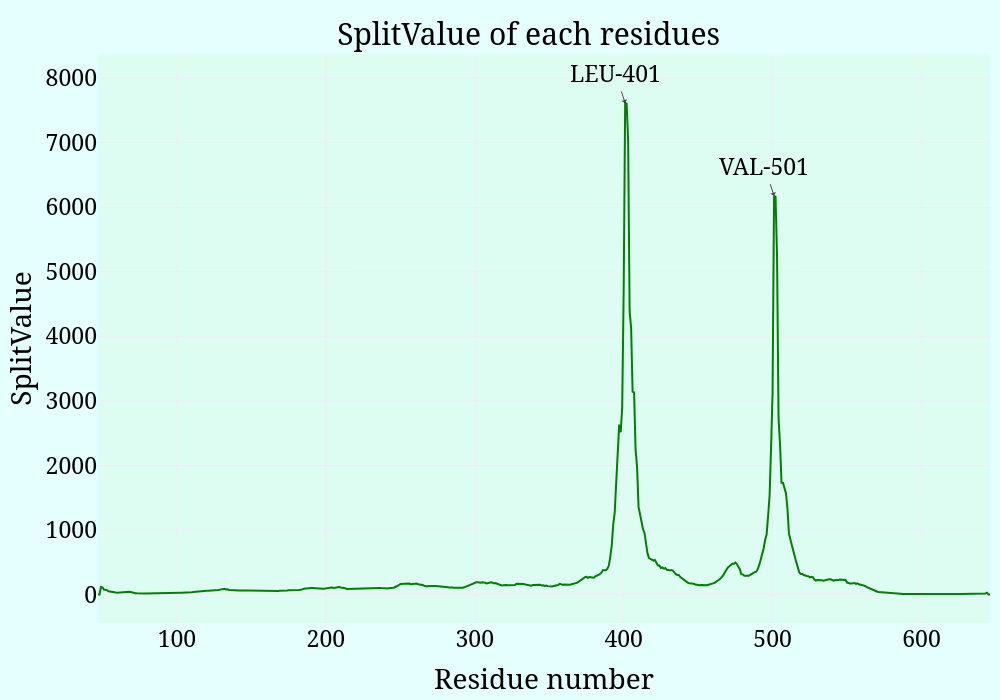
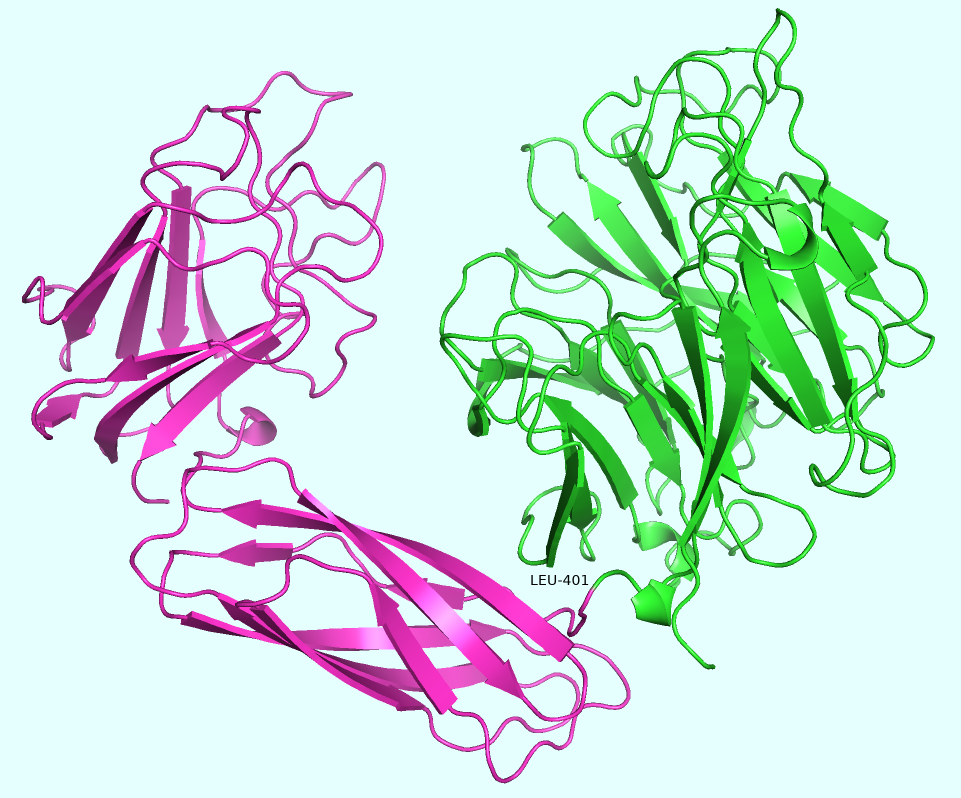
Далее в PyMOL были получены изображения, на которых продемонстрированы соответствующие разбиения (Рис. 2).
Кажется, что разбиения, которые выявил DOMAK, довольно хорошо соотносятся с визуальным отображением структур: в белке действительно выделяется три явственных домена, разделённых небольшими петлями.
Задание №2: SCOP и CATH
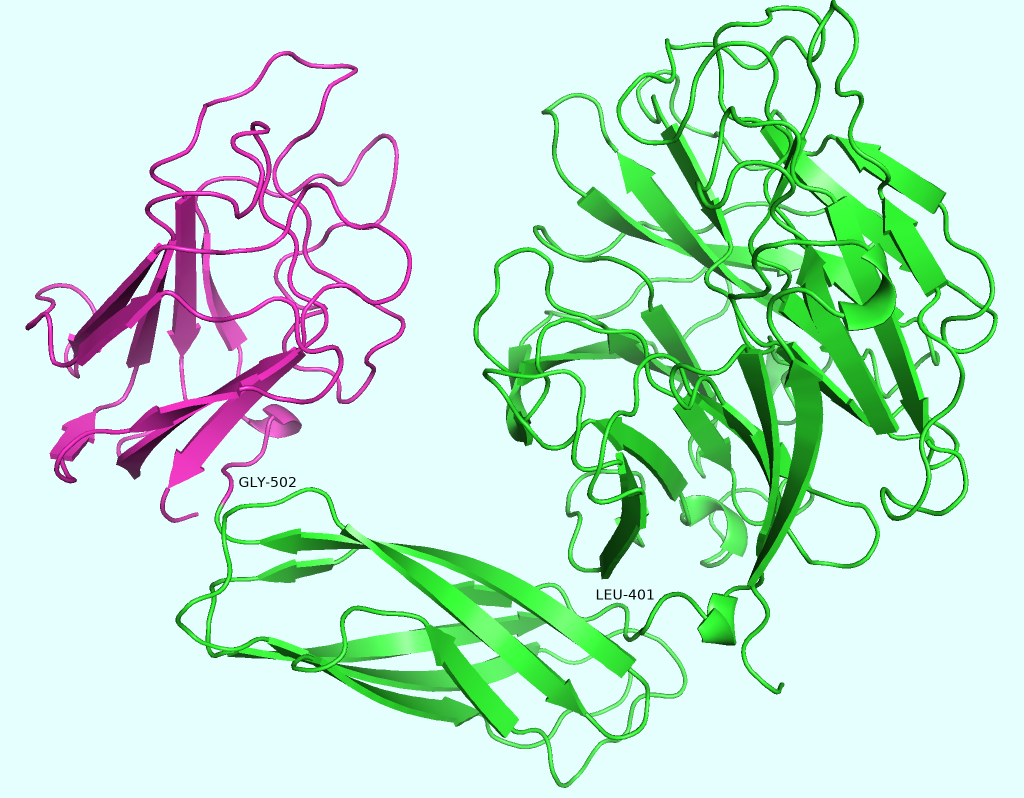
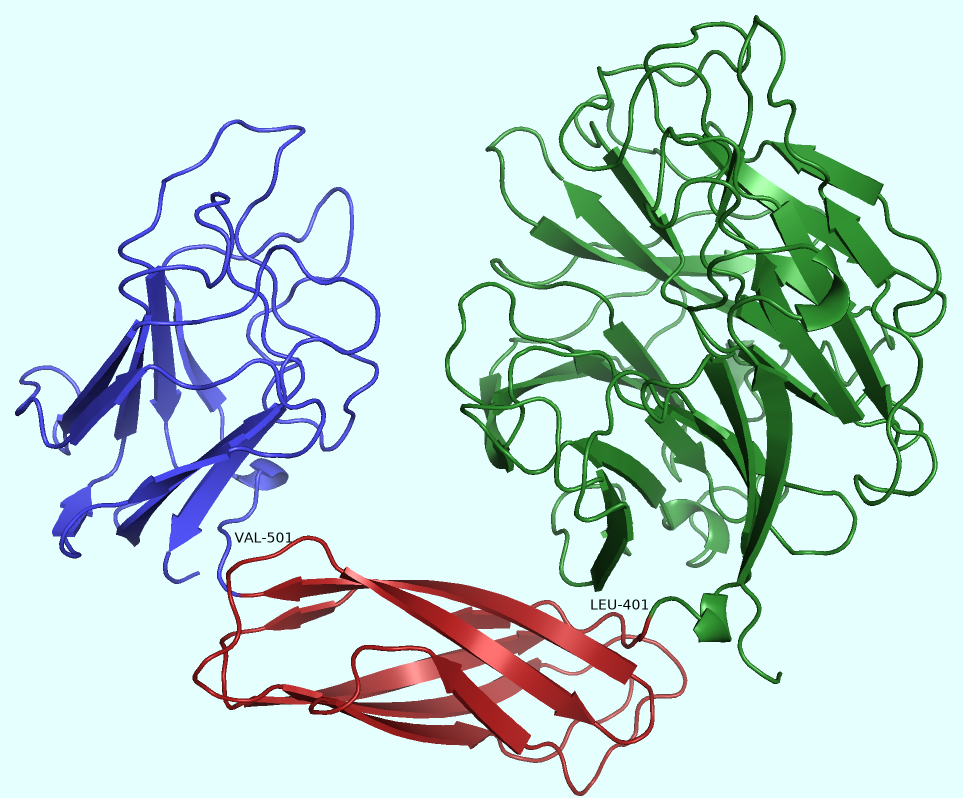
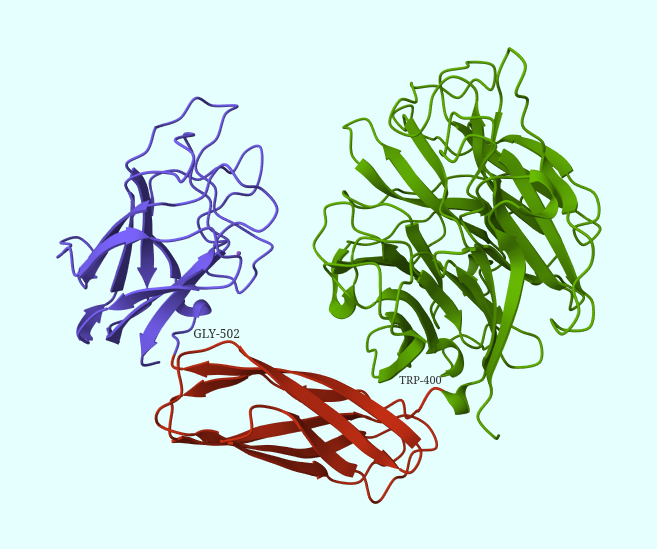
Далее предлагалось сравнить полученное разбиение с теми, что предлагаются в базах данных SCOP и CATH (Рис. 3).
Как и предпологалось, разбиения на структурные домены в рамках баз данных SCOP и CATH сходны с тем, что предсказал DOMAK на основе данных попарных взаимодействий.
Есть ряд отличий на границах, но общий вид остаётся сходным.
Приведём список граничных остатков (граничный остаток включается в предыдущий домен подобно тому, как при разделении в ходе работы алгоритма DOMAK на части A и B остаток, сооветствующий split_position, включается в часть A: [≤ split_position]):
1) DOMAK: LEU-401, VAL-501,
2) SCOP: GLY-402, ASP-505,
3) CATH: TRP-400, GLY-502,
Несмотря на присутствие отличий в граничных остатках, есть основания полагать, что в рамках такого большого белка (около 600 АО) отличия в 2-3 остатка могут быть признаны несущественными. Поэтому, можно сказать, что DOMAK отлично справился с разделением белка на домены, и полученное разбиение совпадает с "общепринятыми" разбиениями, представленными в базах данных структурных доменов SCOP и CATH.
При этом можно заметить, что и SCOP, и CATH определяют функциональную роль этих доменов следующим образом: 1) Зелёным (В цветовой схеме, представленной на рисунке 3) обозначен сиалидазный (нейраминидазный) домен, 2) Красным - иммуноглобулинподобный, 3) Синим - галактозо-связывающий.
Задание №3: InterPro
В ходе третьего задания с помощью сервиса "InterPro" в соответствующей базе данных необходимо было провести поиск эволюционных доменов, подавая на вход последовательность выданного белка.
Сервисом было определено семейство (Sialidase family) и разбиение на эволюционные домены (Рис. 4).

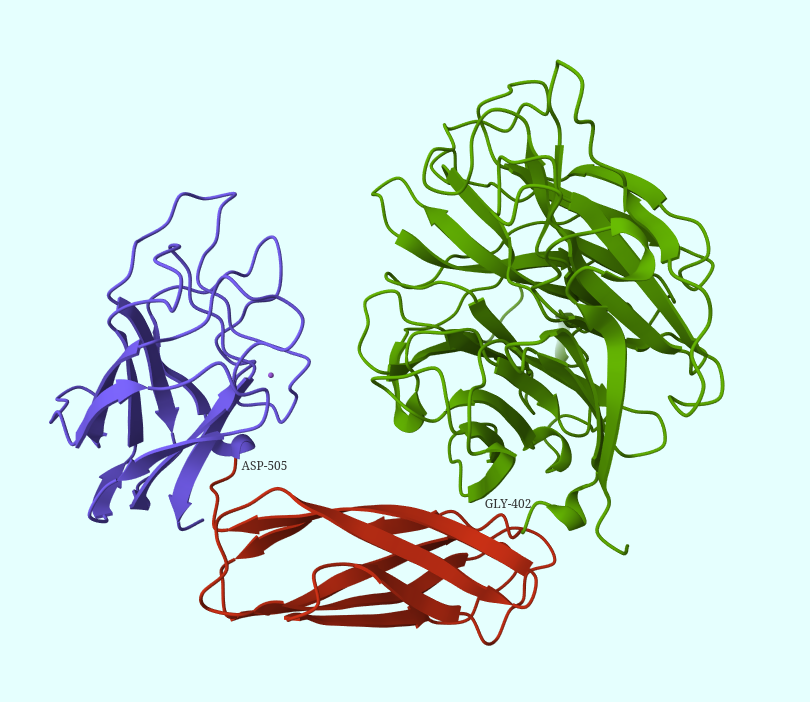
В PyMol было получено изображение этого разбиения в той же цветовой нотации, что и в рамках рисунка 3 (Рис. 5).
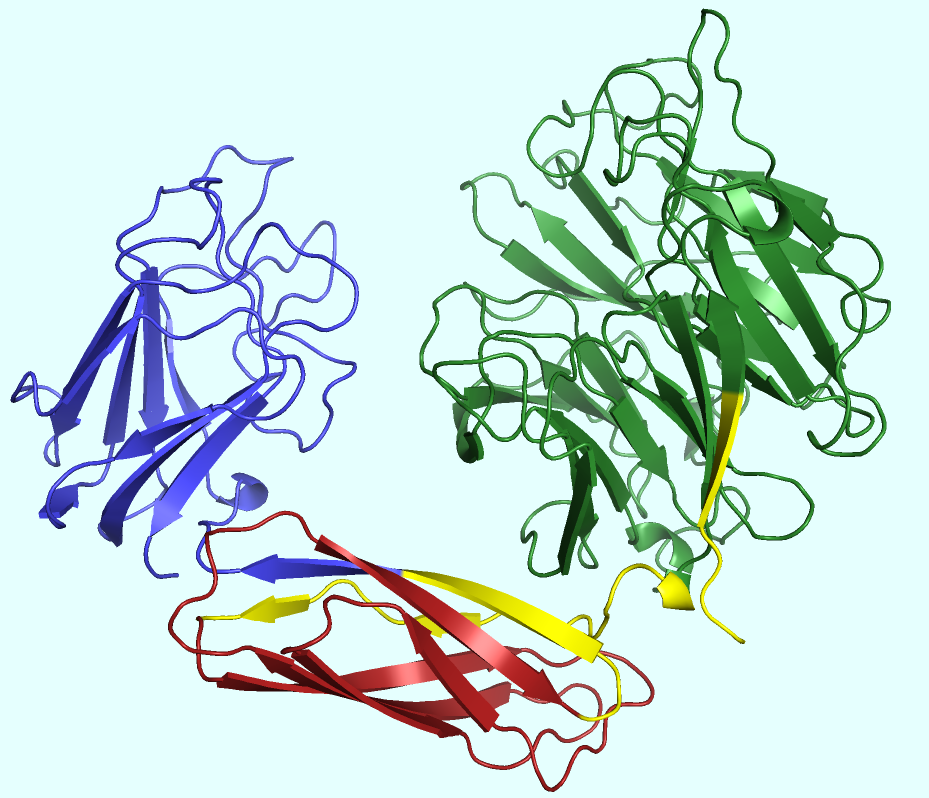
Видно, что InterPro более или менее верно определил границы доменов (урезав значимую часть от обозначеного красным цветом домена). Однако же функциональная роль, определённая базой данных, отличается от приведённой ранее из литературы и баз данных SCOP и CATH: InterPro верно определил функцию первого (c N-конца) домена (сиалидазная активность), но с последующими возникли сомнения.
Второй домен, определённый InterPro как "NPCBM-associated, NEW3 domain of alpha-galactosidase" (обнаруживается в бактериальных галактозидазах. Функция, по-видимому, в силу малой изученности, не выяснена [2]), на деле является иммуноглобулинподобным доменом, который играет роль только лишь связующего звена в ферменте.
Третий домен идентифицируется как "Coagulation factors 5/8 type C domain (FA58C) profile", содержащийся на C-конце факторов свёртывания крови V и VIII и проявляющий структурное сходство с галактозосвязывающим доменом грибковой галактозооксидазы. Однако же он исполняет в соответствующих факторах свёртывания крови несколько иную функцию (связывания анионных фосфолипидов на поверхности тромбоцитов и эндотелиальных клеток) [3].
Таким образом, с наиболее "непонятными" функциями у InterPro возникли "проблемы", но в целом границы выбраны правильно, поэтому будем считать, что он справился со своей задачей.
Ссылка на сессию pymol: 7pr.pse
Кирилл Кузенков, студент четвёртого курса ФББ