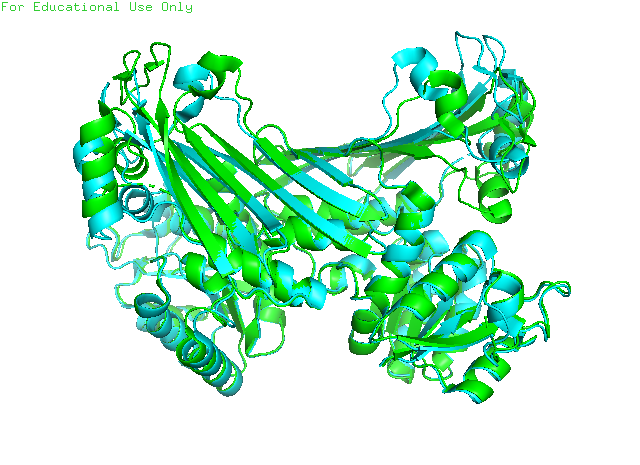
В это задании рассматриваем открытую и закрытую форму аминдегидрогеназы Petrotoga mobilis. Изначально мне были даны PDB с id 6G1M и 6G1H, но для 6G1H biologacal assembly был представлен мономером, а для 6G1M гомодимером. А так же я заметил, что для 6G1M есть два biological assembly (открытая и закрытая форма), поэтому для выполнения задания сравнивал их.

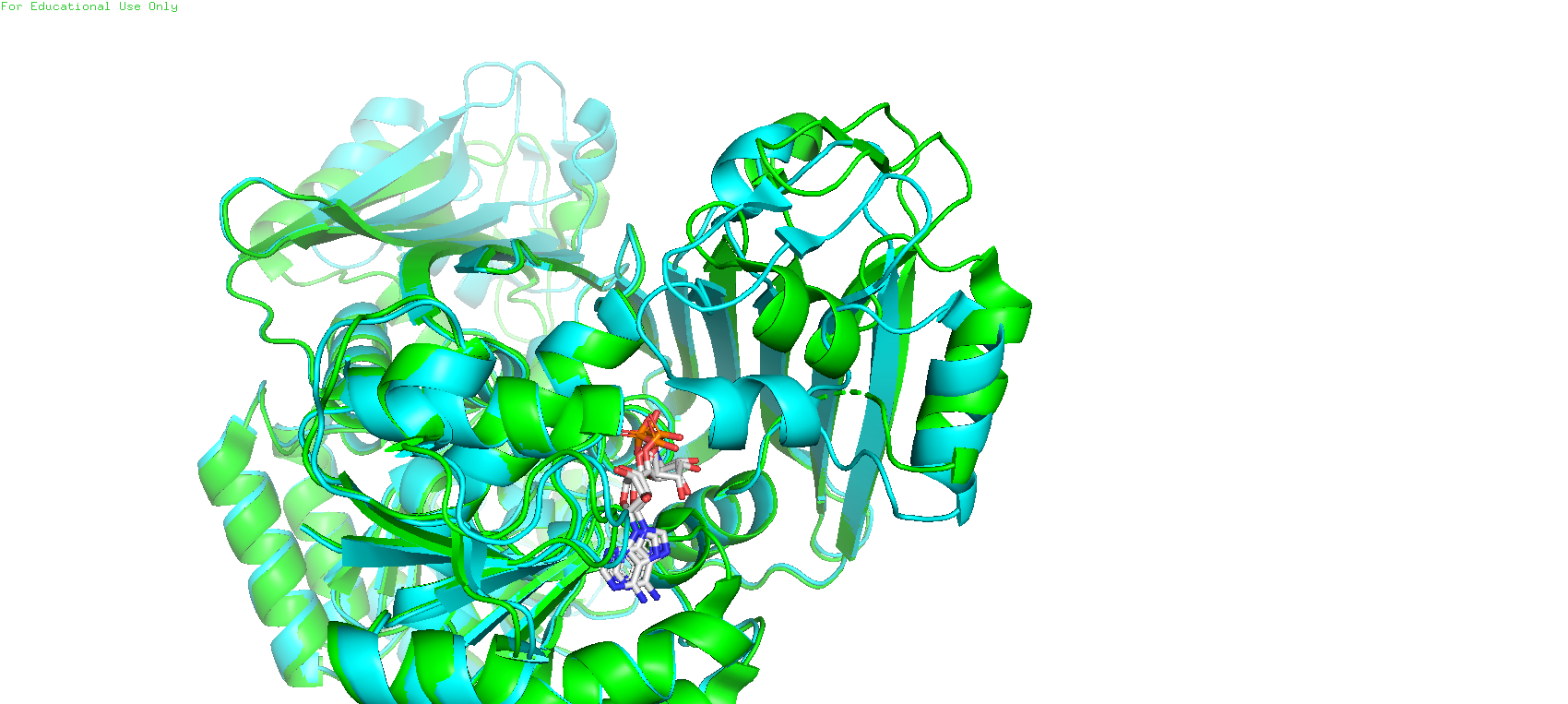
На Рис.2 видим сильное смещение альфа-спирали, которое отвечает за связывание кофермента - NAD.
| MS, Ангстремы квадратные | SAS, Ангстремы квадратные | |
| Open | 63545.141 | 25359.777 |
| Close | 64147.016 | 25611.127 |
Из полученных площадей можно сделать вывод, что площадь молекулярной поверхности и площадь, доступная растворителю у закрытой формы немного больше. Для подсчёта площадей выделил из двух biological assembly только белковую часть.
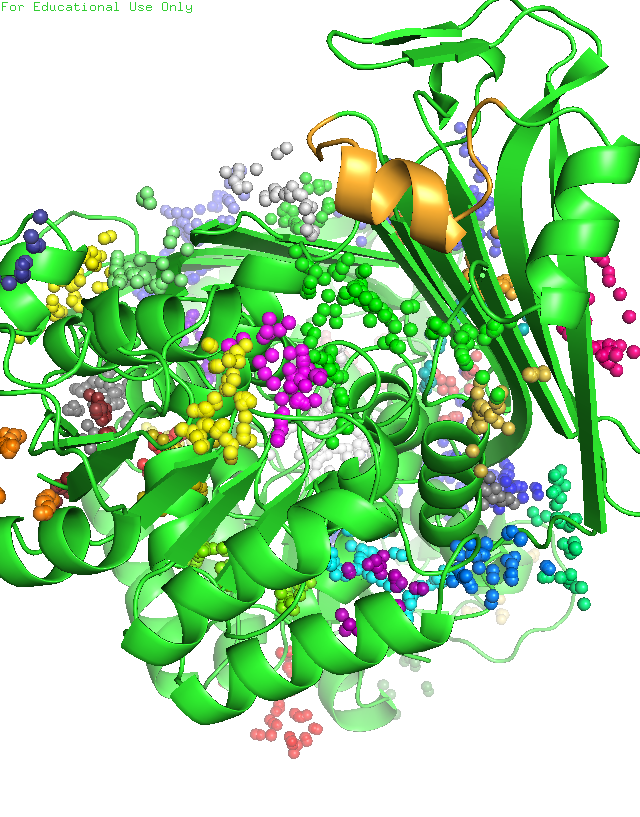
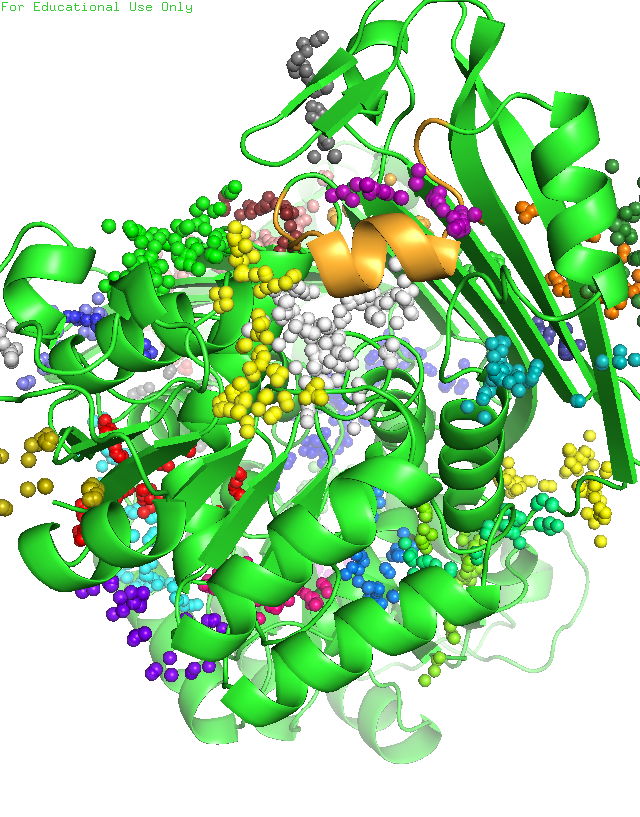
С помощью сервиса fpocket нашли карманы у белков. Ниже показаны карманы связывания двух белков. Видно, что у открытой формы есть 3 полости (зелёная, маджента и желтая), а у закрытой формы их уже 2 (желтая и белая). У открытой формы NAD связывается в зелёной полости, а у закрытой в белой. Сравнив эти полости можем заметить, что объём белой полости (2391.98 A^3) меньше объёма зелёной полости (3623.66 A^3). Это логично, потому что происходит связывание NAD.
В данном задании было необходимо сопоставить экспонированность остатков закрытой и открытой конформаций и выбрать остаток с её наибольшим изменением. Изменение экспонированности нельзя трактовать как-то однозначно, например, какой-то остаток в одной конформации мог быть целиком погруженным в глобулу, а потом оказаться снаружи. Поэтому я решил оценивать абсолютное изменение экспонированности.
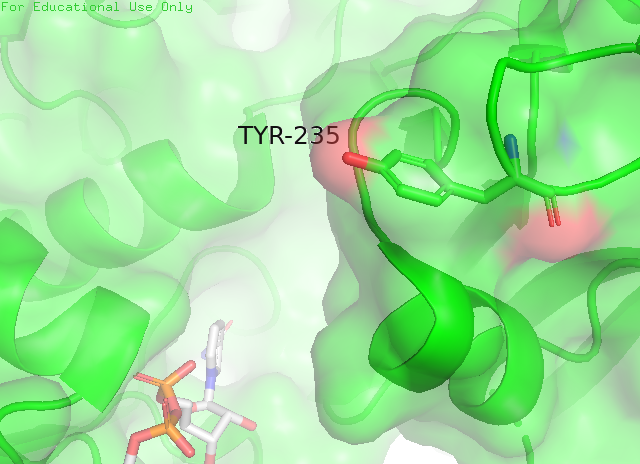
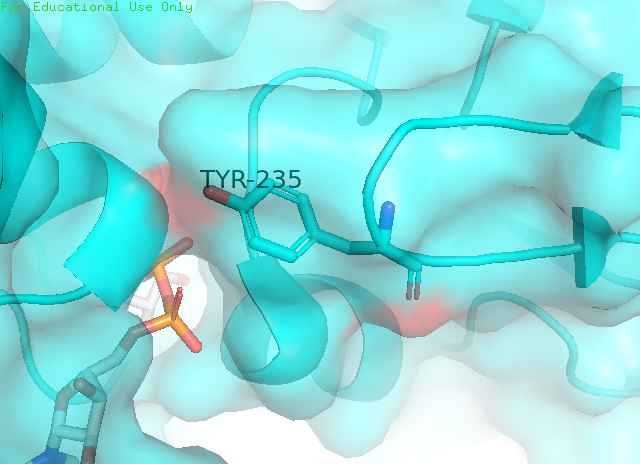
Экспонированности остатков были рассчитаны командой mkdssp. Остатком с наибольшим изменением экспонированности оказался TYR-235 (открытая форма - 141, закрытая форма - 71, разница - 70).