Мини-обзор генома бактерии Aliivibrio fischeri ES114
город Москва, территория Ленинские горы, 1с73
Данный обзор посвящен краткому анализу генома симбиотической бактерии Aliivibrio fischeri ES114, выделенного из органа свечения Euprymna scolopes.
Введение
Объектом данного исследования является бактерия Aliivibrio (ранее Vibrio) fischeri ES114, грамотрицательная, морская бактерия из филума Pseudomonadota (Таблица 1). A. fischeri может вступать в симбиоз с Euprymna scolopes, в котором осуществляет биолюминесценцию в органе свечения в мантии головоногого [1].
| Domain | Bacteria |
|---|---|
| Kingdom | Pseudomonadati |
| Phylum | Pseudomonadota |
| Class | Gammaproteobacteria |
| Order | Vibrionales |
| Family | Vibrionaceae |
| Genus | Aliivibrio |
| Species | Aliivibrio fischeri |
| Strain | Aliivibrio fischeri ES114 |
Бактерия встречается как в свободной форме, так и в симбиозе с морскими организмами. Однако люминесценция встречается, когда бактерия колонизирует орган симбионта, а не в свободной форме [3]. При этом симбиотическая форма утрачивает полярные жгутики и теряет способность к движению [4]. A. fischeri используется в экотоксикологии для оценки уровня загрязнения по ингибированию люминесценции [5]. A. fischeri является модельным объектом для изучения чувства кворума в бактериальных популяциях. Бактерия имеет 2 системы чувства кворума, которые играют роль в колонизации симбионта [6]. Несмотря на то, что род Aliivibrio и родственная группа Vibrio содержат патогенных представителей (например, A. salmonicida, V. cholerae, V. vulnificus) для A. fischeri не была показана патогенность [7]. Поэтому бактерию используют в сравнительной геномике для выявления особенностей генома, отличающих A. fischeri от патогенных бактерий рода Vibrio и Aliivibrio [8]. Таким образом, данная бактерия имеет большое значение для практических исследований. Согласно анализу времени дивергенции, бактерия произошла в Девоне (385 млн. лет назад), этот период сопутствовал активной дивергенции головоногих моллюсков и лучеперых рыб [9].
Методы
Данные о геноме Aliivibrio fischeri, Vibrio cholerae, Vibrio natriegens и Vibrio harveyi были взяты с сайта Национального Центра Биотехнологической информации (NCBI). Для анализа последовательности использовались электронные таблицы, командная оболочка BASH, скрипты, написанные на языке Python.
Скрипт, написанный на языке Python, использовался для подсчета длины репликонов, длины и доли кодирующей последовательности, нуклеотидного состава репликона и GC-skew (S1 в сопроводительных материалах).
Электронные таблицы использовались для подсчета типов генов на каждом репликоне (S2 в сопроводительных материалах), построения гистограммы длин белков, распределения GC-состава по CDS и дальнейшая статистическая обработка этих гистограмм (S3 в сопроводительных материалах).
Результаты
1. Основные данные о геноме A. fischeri
Геном бактерии представлен тремя репликонами: две хромосомы и плазмида pES100. Первая хромосома содержит многие важные гены, при этом ее размер в семействе сохраняется относительно постоянным [10]. Также этой хромосоме в семействе Vibrionaceae свойственна низкая частота внутрихромосомных перестроек [11]. При этом для второй хромосомы характерна вариабельность в размере в семействе. Согласно одной из гипотез, хромосома 2 произошла от мегаплазмиды у предка Vibrionaceae, т.к. все представители семейства имеют 2 хромосомы. Эта плазмида стабилизировалась из-за переноса на нее некоторых важных генов [10, 12]. Видимо, это приобретение произошло достаточно давно, потому что GC составы этих репликонов примерно равны (Табл. 2).
| Репликон | Длина, п.н. | GC-состав, % |
|---|---|---|
| Хромосома I | 2897536 | 38.95 |
| Хромосома II | 1330333 | 37.02 |
| Плазмида pES100 | 45849 | 38.42 |
Лимитирующим фактором в размножении бактерии зачастую становится скорость репликации, поэтому в геноме не должно быть лишних элементов. Поэтому в их геноме поддерживается высокая доля кодирующей последовательности (в среднем около 88%) [13]. Геном A. fischeri тоже содержит низкую долю некодирующих последовательностей (Табл. 3).
| Репликон | Длина кодирующей последовательности, п.н. | %CDS |
|---|---|---|
| Хромосома I | 2518102 | 86.90 |
| Хромосома II | 1165932 | 87.64 |
| Плазмида pES100 | 40176 | 87.63 |
Также было определено количество различных типов генов в репликонах бактерии. При этом можно заметить, что количество рРНК и тРНК относительно общего количества генов в репликоне значительно меньше для второй хромосомы (Табл. 4), что снова подтверждает гипотезу о приобретении хромосомы II через мегаплазмиду (жизненно необходимые гены, такие как гены рРНК, концентрируются на хромосоме I и еще не успели перенестись на хромосому II). При этом существует гипотеза о том, что при изменении условий среды при делении бактерии могут производить так называемые "дроновые клетки", которые несут только хромосому II и не способны реплицироваться, при этом на хромосоме II есть гены метаболизма и образования биопленок, экспрессия которых в теории должна помочь общей популяции пережить эти неблагоприятные условия [12].
На хромосоме I находятся гены некоторых минорных РНК, таких как ген РНК субъединицы РНКазы P. Рибонуклеаза P участвует в процессинге 5'-конца тРНК. При этом РНК субъединица показывает рибозимную активность также в отсутствии белковой субъединицы [14]. Также хромосома I несет ген SRP РНК. Эта молекула РНК входит в рибонуклеотидный комплекс, который участвует в ко- и посттрансляционном транспорте белков к внутренней мембране [15]. На хромосоме I можно найти тмРНК. Транспортно-матричные РНК имеют структурные особенности как транспортных, так и матричных РНК, при этом тмРНК участвует в механизме транс-трансляции, который позволяет рибосоме освободиться от дефектной мРНК без стоп-кодона [16].
| Тип гена | Хромосома I | Хромосома II | pES100 |
|---|---|---|---|
| protein_coding | 2541 | 1151 | 56 |
| pseudogene | 33 | 12 | 0 |
| ncRNA | 1 | 0 | 0 |
| RNase_P_RNA | 1 | 0 | 0 |
| rRNA | 34 | 3 | 0 |
| SRP_RNA | 1 | 0 | 0 |
| tRNA | 108 | 11 | 0 |
| tmRNA | 1 | 0 | 0 |
Второе правило Чаргаффа гласит, что процентный состав комплементарных нуклеотидов на одной цепи ДНК примерно равны [17]. Соответственно, данные по нуклеотидному составу репликонов согласуются с этим правилом (Табл. 5). При этом для плазмиды из-за небольшой длины цепи содержание комплементарных нуклеотидов отличается больше чем у хромосом.
| Репликон | A, % | T, % | G, % | C, % |
|---|---|---|---|---|
| Хромосома I | 30.47 | 30.58 | 19.51 | 19.45 |
| Хромосома II | 31.80 | 31.17 | 18.60 | 18.42 |
| pES100 | 33.39 | 28.19 | 20.20 | 18.22 |
2. Распределение длин белков A. fischeri
Для протеома A. fischeri было определено распределение числа белков в зависимости от количества аминокислотных остатков (Рис. 1). Больше всего белков в области 200-300 аминокислотных остатков. Для этого распределения были определены некоторые статистические показатели (Таблица 6).
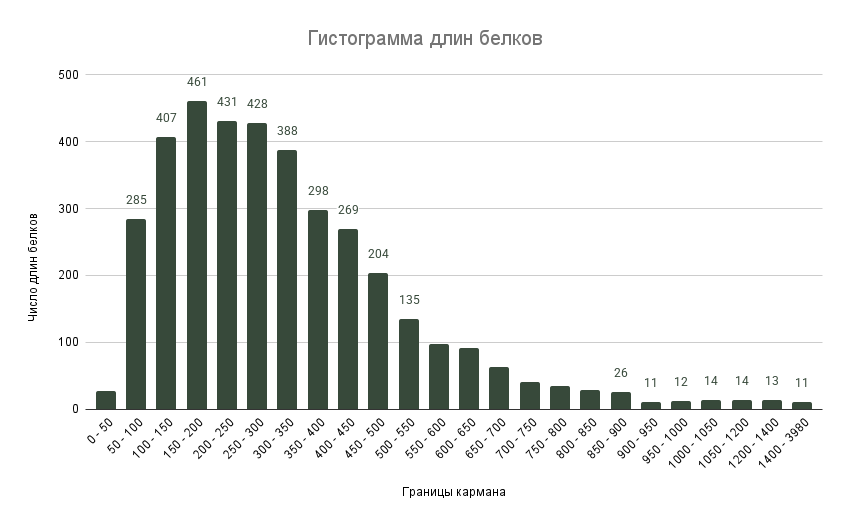
| Медиана | 285 |
|---|---|
| Среднее значение | 326.49 |
| Стандартное отклонение | 232.41 |
| Максимальная длина | 3971 |
| Минимальная длина | 29 |
Белок с максимальным количеством аминокислотных остатков — это RtxA1 (кальций-связывающий цитотоксин), для которого была показана токсичность у патогенных видов рода Vibrio (например, патоген человека V. vulnificus) [18]. Но у A. fischeri наличие этого белка не было доказано, его предсказали по соответствующей последовательности в геноме [19].
Белок из семейства YnhF мембранных белков имеет наименьшее количество аминокислотных остатков в протеоме. У Escherichia coli этот белок является добавочной субъединицей цитохрома bd-I. Эта субъединица найдена только у представителей клады протеобактерий и занимает предполагаемое место входа кислорода в bd-оксидазе [20].
3. Распределение CDS по GC-составу
Была построена столбчатая диаграмма, отражающая распределение CDS по GC-составу у A. fischeri (Рис. 2), также для данных по распределению были вычислены некоторые статистические параметры (Таблица 7).
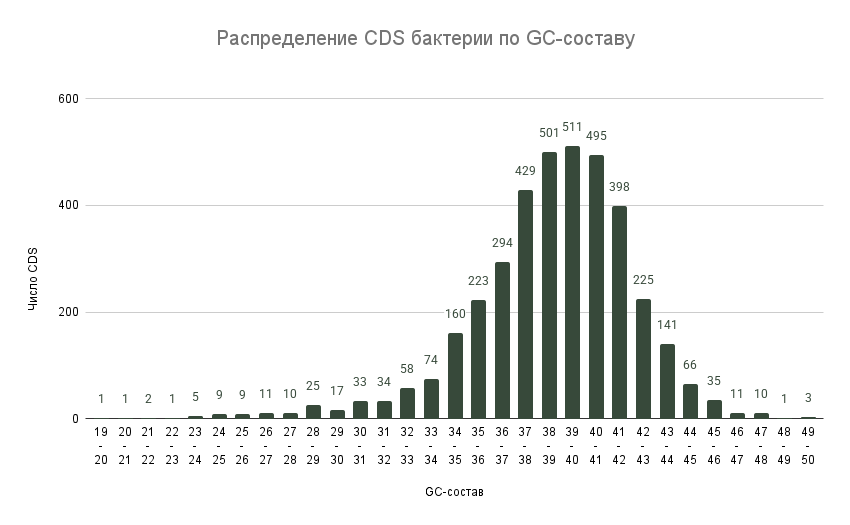
| Медиана | 38.99 |
|---|---|
| Среднее значение | 38.645 |
| Стандартное отклонение | 3.47 |
| Максимальный GC% | 49.74 |
| Минимальный GC% | 19.05 |
A. fischeri имеет самый низкий средний GC-состав в геноме среди всех видов родов Aliivibrio и Vibrio [19].
4. GC-skew
Для двух хромосом были посчитаны значения GC-skew и кумулятивного GC-skew (Рис. 3). GC-skew показывает представленность гуанина в участке ДНК (оценивает неравномерность распределения нуклеотидов).
GC-skew = (G-C)/(G+C)
Кумулятивный GC-skew показывает сумму значений GC-skew на участке от начала до искомой позиции. Известно, что максимальное значение кумулятивного параметра отвечает за точку терминации, а минимальное значение — за точку начала репликации [21]. Таким образом для хромосом I и II были посчитаны oriC и ter: для I: 2894103 нуклеотид и 1454294 нуклеотид, соответственно; для II: 1328670 нуклеотид и 657020 нуклеотид соответственно.
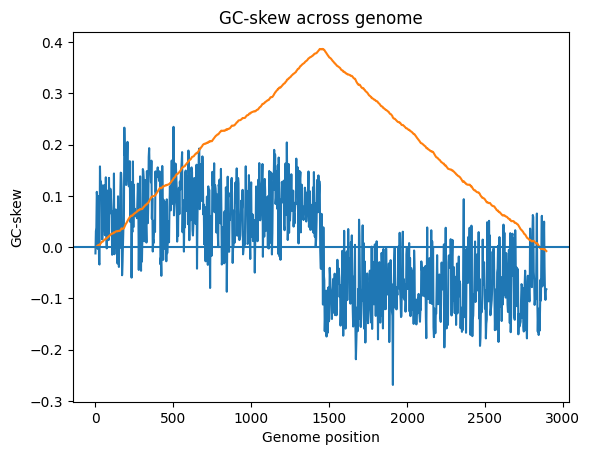
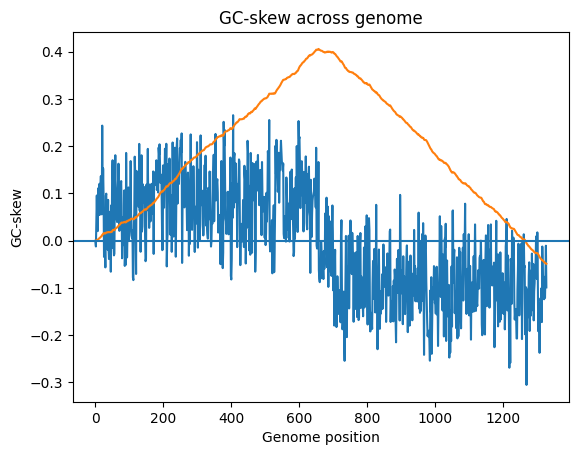
5. Сравнение GC в семействе Vibrionaceae
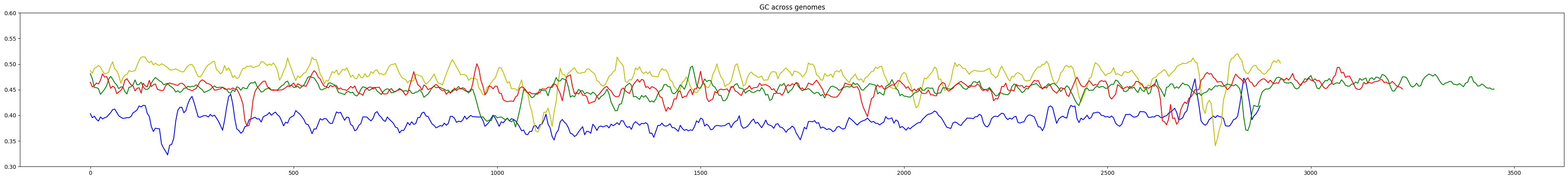
Был проанализирован GC-состав хромосом I у нескольких видов семейства Vibrionaceae (Aliivibrio fischeri, Vibrio cholerae (Vc), Vibrio natriegens (Vn), Vibrio harveyi (Vh)) по всей длине. На основе графика (Рис. 4) можно выдвинуть гипотезу о том, что, возможно, некоторые участки передавались горизонтальным переносом от Aliivibrio fischeri и поэтому эти регионы у Vc, Vn, Vh имеют GC-состав ниже, чем в среднем по геномам этих бактерий.
В дальнейшем можно проанализировать геномы Vibrionaceae для выявления конкретных участков, которые имеют близкий GC-состав к Aliivibrio fischeri, и наличие в них каких-либо маркеров горизонтального переноса. На основе этих данных можно будет построить новые эволюционные гипотезы. Также анализ различий близкородственных видов, которые являются патогенами и симбионтами, поможет уточнить механизмы патогенности.
Сопроводительные материалы
S1 Genome_Aliivibrio.ipynb (Google Colab)
S2 Genomic features of Aliivibrio fischeri ES114 (Google Sheets)
S3 CDS from genome of Aliivibrio fischeri ES114 (Google Sheets)
Список литературы
- Aizawa, Shin-Ichi. The flagellar world: electron microscopic images of bacterial flagella and related surface structures. Elsevier, 2013. 16-17.
- Schoch CL, et al. NCBI Taxonomy: a comprehensive update on curation, resources and tools. Database (Oxford). 2020: baaa062. PubMed: 32761142; PMC: PMC7408187. [NCBI Taxonomy]
- RUBY, Edward G., and Kenneth H. NEALSON. "Symbiotic association of Photobacterium fischeri with the marine luminous fish Monocentris japonica: a model of symbiosis based on bacterial studies." The Biological Bulletin 151.3 (1976): 574-586.
- Ruby, E. G., and L. M. Asato. "Growth and flagellation of Vibrio fischeri during initiation of the sepiolid squid light organ symbiosis." Archives of microbiology 159.2 (1993): 160-167.
- Froehner, K., T. Backhaus, and L. H. Grimme. "Bioassays with Vibrio fischeri for the assessment of delayed toxicity." Chemosphere 40.8 (2000): 821-828.
- Lupp, Claudia, and Edward G. Ruby. "Vibrio fischeri uses two quorum-sensing systems for the regulation of early and late colonization factors." Journal of bacteriology 187.11 (2005): 3620-3629.
- Christensen, David G., and Karen L. Visick. "Vibrio fischeri: laboratory cultivation, storage, and common phenotypic assays." Current protocols in microbiology 57.1 (2020): e103.
- Lilburn, Timothy G., et al. "Comparative genomics of the family Vibrionaceae reveals the wide distribution of genes encoding virulence-associated proteins." BMC genomics 11.1 (2010): 369.
- Lin, Heyu, et al. "Comparative genomic analysis reveals the evolution and environmental adaptation strategies of vibrios." BMC genomics 19.1 (2018): 135.
- Okada, Kazuhisa, et al. "Vibrios commonly possess two chromosomes." Journal of bacteriology 187.2 (2005): 752-757.
- Makino, Kozo, et al. "Genome sequence of Vibrio parahaemolyticus: a pathogenic mechanism distinct from that of V. cholerae." The Lancet 361.9359 (2003): 743-749.
- Heidelberg, John F., et al. "DNA sequence of both chromosomes of the cholera pathogen Vibrio cholerae." Nature 406.6795 (2000): 477-483.
- Kirchberger, Paul C., Marian L. Schmidt, and Howard Ochman. "The ingenuity of bacterial genomes." Annual Review of Microbiology 74.1 (2020): 815-834.
- Evans, Donald, Steven M. Marquez, and Norman R. Pace. "RNase P: interface of the RNA and protein worlds." Trends in biochemical sciences 31.6 (2006): 333-341.
- Rosenblad, Magnus Alm, et al. "Kinship in the SRP RNA family." RNA biology 6.5 (2009): 508-516.
- Muto, Akira, Chisato Ushida, and Hyouta Himeno. "A bacterial RNA that functions as both a tRNA and an mRNA." Trends in biochemical sciences 23.1 (1998): 25-29.
- Rudner, Rivka, John D. Karkas, and Erwin Chargaff. "Separation of B. subtilis DNA into complementary strands. 3. Direct analysis." Proceedings of the National Academy of Sciences 60.3 (1968): 921-922.
- Satchell, Karla JF. "Multifunctional-autoprocessing repeats-in-toxin (MARTX) Toxins of Vibrios." Microbiology spectrum 3.3 (2015): 10-1128.
- Ruby, Edward G., et al. "Complete genome sequence of Vibrio fischeri: a symbiotic bacterium with pathogenic congeners." Proceedings of the National Academy of Sciences 102.8 (2005): 3004-3009.
- Safarian, Schara, et al. "Active site rearrangement and structural divergence in prokaryotic respiratory oxidases." Science 366.6461 (2019): 100-104.
- Grigoriev, Andrei. "Analyzing genomes with cumulative skew diagrams." Nucleic acids research 26.10 (1998): 2286-2290.