Обзор связей в структуре 3GBR
Водородные связи остова
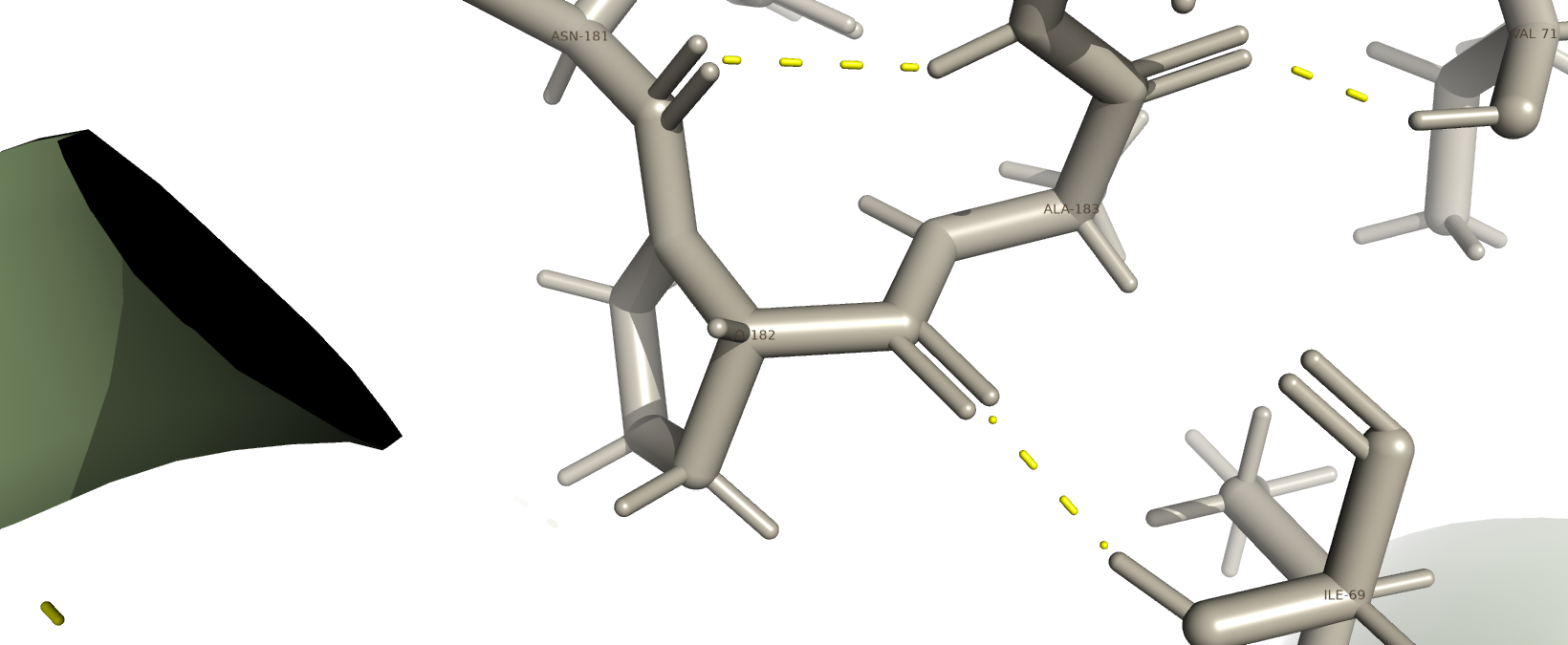
Водородные связи между атомами остова белка являются основным фактором стабилизации вторичной структуры фермента. Такие взаимодействия формируются между карбонильным кислородом одной пептидной связи и амидным водородом другой (Рис. 1), что приводит к образованию регулярной сети водородных связей в α-спиралях и β-слоях.
Водородные связи боковых радикалов
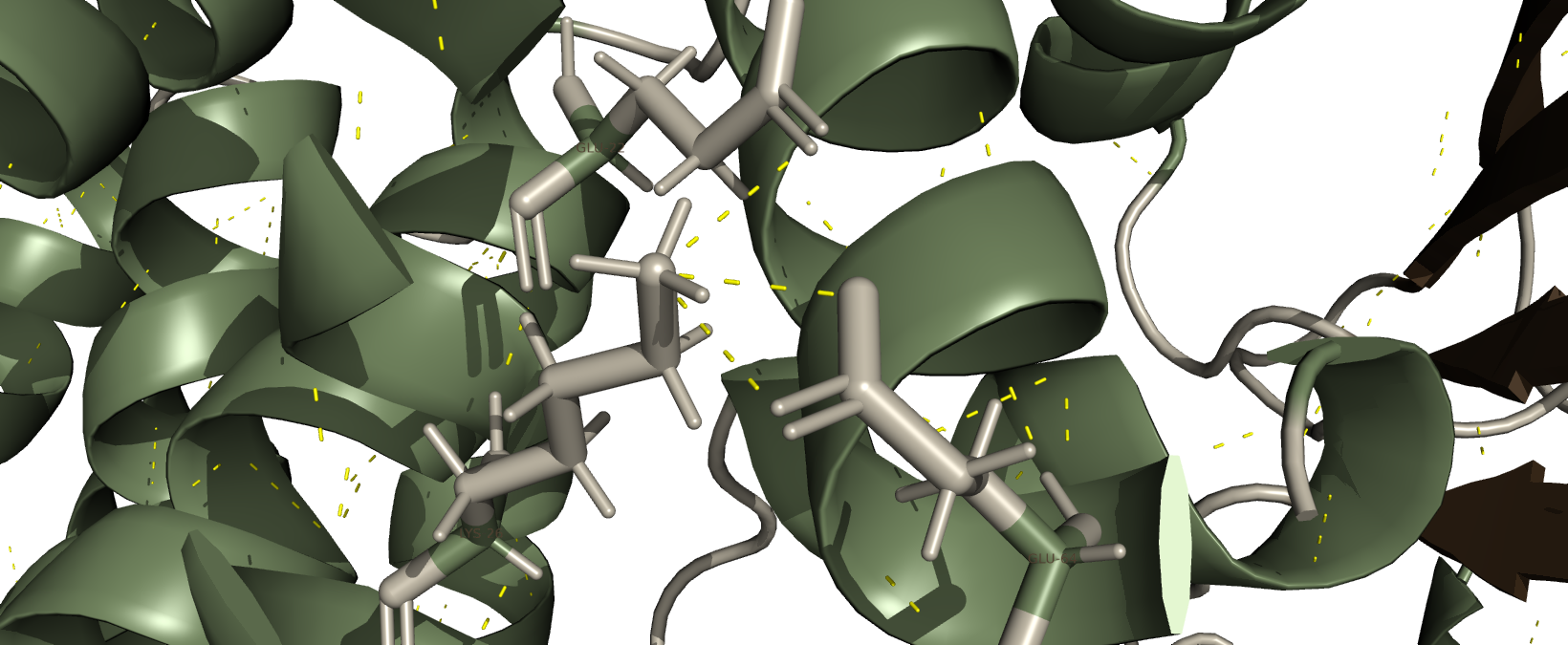
Водородные связи между боковыми радикалами аминокислот (Рис. 2) играют важную роль в стабилизации третичной структуры белка и формировании локальных взаимодействий между элементами вторичной структуры. Эти взаимодействия также могут участвовать в формировании активного центра фермента.
Солевые мостики
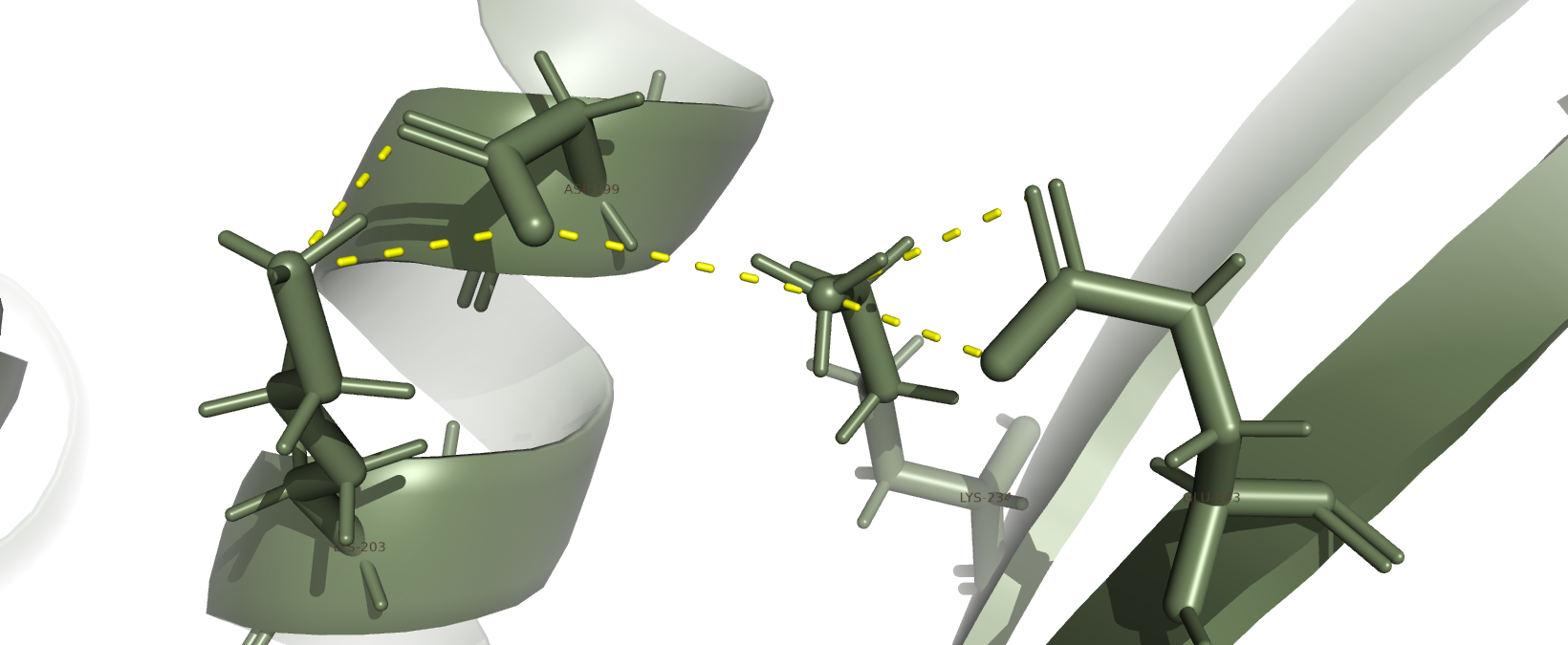
Солевые мостики представляют собой электростатические взаимодействия (Рис. 3) между противоположно заряженными боковыми цепями аминокислот, например между остатками Asp или Glu и Lys, Arg или His. Такие контакты значительно усиливают стабильность третичной структуры белка и могут участвовать в стабилизации интерфейсов между доменами или субъединицами.
Дисульфидные связи
Белок антранилат фосфорибозилтрансфераза является цитоплазматическим, поэтому дисульфидные моситики не эффективны в поддержании структуры(подвержены восстановительным агентам цитоплазмы). В последовательности фермента нет цистеинов, поэтому дисульфидные мостики не могут быть образованы.
Стекинг
В белке не наблюдаются стекинг взаимодействия ароматических аминокислот (Рис. 4)