Обзор структуры 3GBR
Введение
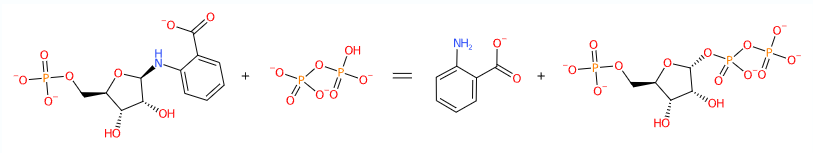
Под идентификатором 3GBR в базе данных PDB расположен белковый комплекс антранилат фосфорибозилтрансфераза (Anthranilate phosphoribosyltransferase), который является ферментом группы гликозилтрансфераз. Этот фермент был выделен из гипертермофильной археи Sulfolobus solfataricus (Табл. 1). Фермент катализирует реакцию переноса фосфорибозильной группы с 5-фосфорубозибозо-1-пирофостфата (PRPP) на антранилат с получением N-(5'-фосфорибозил)-антранилата (PRA) (Рис. 1) , предшествующей синтезу триптофана, в специализированном пути синтеза бензоидных ароматических соединений (Шикиматный путь). Антранилат фосфорибозилтрансфераза является высоко термостабильным белком, но при этом работает с низкой скоростью при температуре 37°C [1].
| Domain | Archaea |
|---|---|
| Kingdom | Thermoproteati |
| Phylum | Thermoproteota |
| Class | Thermoprotei |
| Order | Sulfolobaceae |
| Family | Sulfolobaceae |
| Genus | Saccharolobus |
| Species | Saccharolobus solfataricus |
Структура
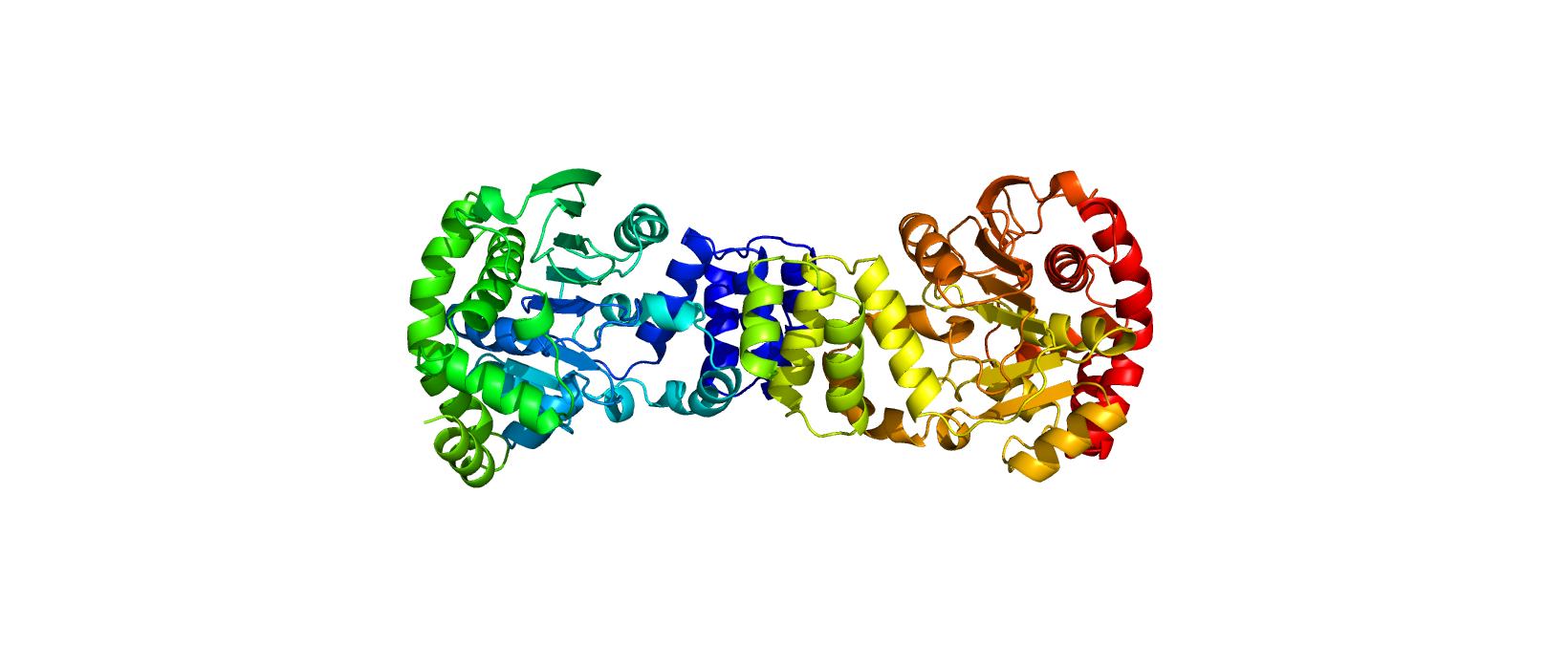
Биологическая еденица представлена гомодимером. Белок состоит из идентичных цепей А и B длиной 345 а.о. Асимметрическая единица совподает с биологической единицей (Рис. 2). В цепях наблюдаются две инженерные мутации, отличающие их от референса из базы данных Uniprot (ID P50384)
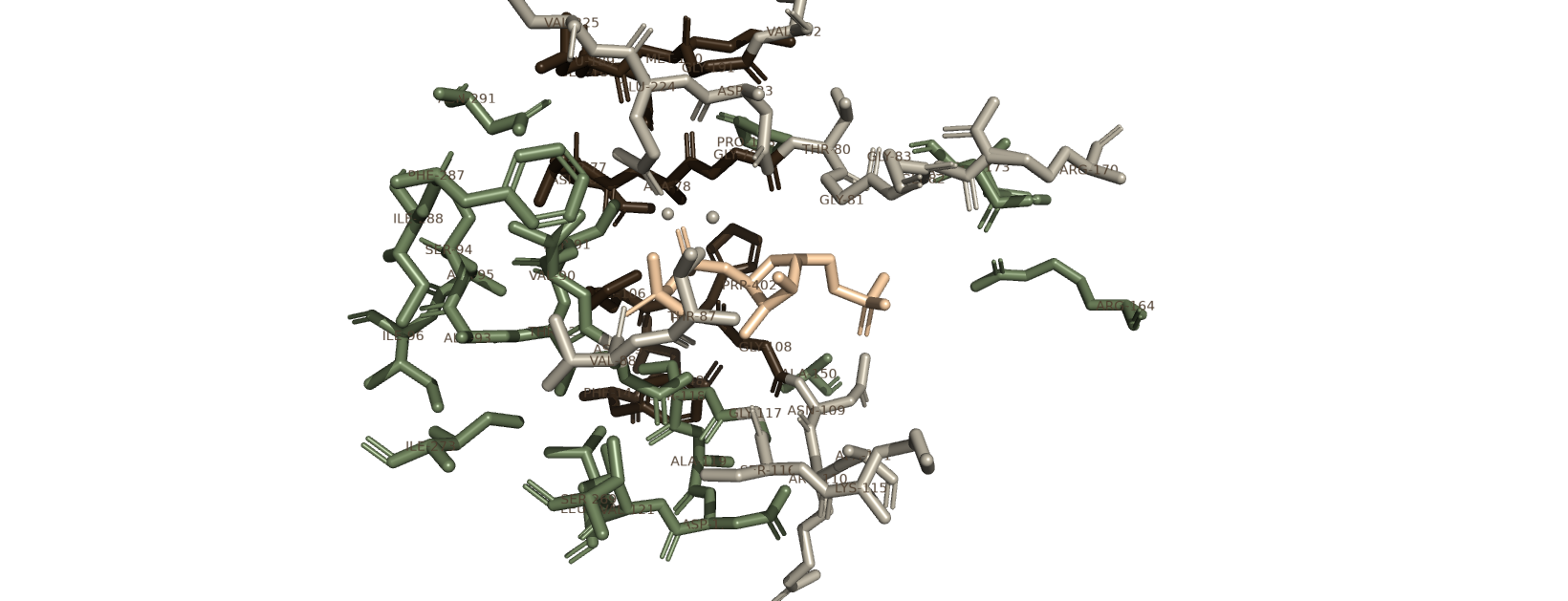
Мутация D83G была произведена, потому что аспартат в позиции 83 участвует в координации Mg2+, который ингибирует катализ. При удалении карбоксильной группы происходит снижение ингибирования. Так же была произведена мутация F149S, которая позволила убрать гидрофобный фенилаланин из кормана, участвующего в связывании антранилата, поэтому продукт реакции стал легче высвобождаться [1] .
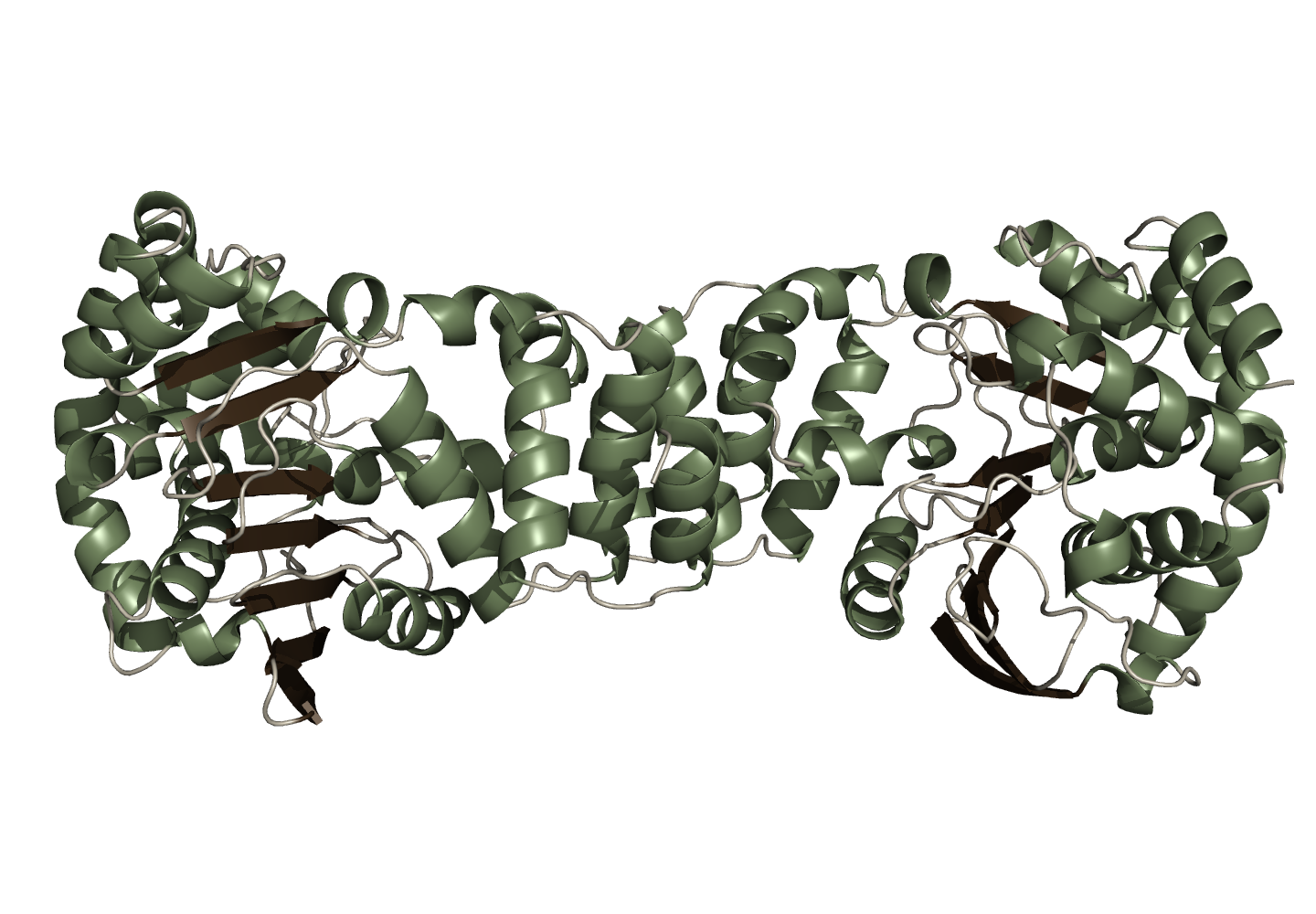
Для вторичной структуры антранилат фосфорбибозилтрансферазы характерно наличие как бета-листов, так и альфа-спиралей (Рис. 3). При этом альфа-спирали находятся во внешней чати гомодимера и окружают бета-листы.
Малые молекулы
В кристаллической структуре фермента присутствуют несколько типов малых молекул (Табл. 1). 5-фосфорубозибозо-1-пирофостфат (1-O-pyrophosphono-5-O-phosphono-alpha-D-ribofuranose, PRP, S1) является одним из субстратов фермента, связан с каталитическим центром и необходим для визуализации структуры взаимодействий внутри активного центра (Рис. 4). Также среди малых молекул есть ион магния(MN, Manganese (II) ion, S1), который координирует субстрат в активном центре и необходим для катализа. Кроме функционально значимых малых молекул в записи присутсвуют молекулы воды (HOH, Water, S1), которые участвуют в образовании водородных связей. Для кристаллизации белка добавлялись диэтиленгликоль (PEG, Di(hydroxyethyl)ether, S1) и глицерин (GOL, Glycerol, S1) в качестве криопротектора и резолюции структуры.
| Код | Полное название | Количество |
|---|---|---|
| PRP | 1-O-пирофосфоно-5-O-фосфоно-альфа-D-рибофураноза | 2 |
| MN | Ион магния | 4 |
| GOL | Глицерин | 2 |
| PEG | Диэтиленгликоль | 2 |
| HOH | Вода | 254 |
Сопроводительные материалы
Список литературы
- Schlee, Sandra, et al. "Activation of anthranilate phosphoribosyltransferase from Sulfolobus solfataricus by removal of magnesium inhibition and acceleration of product release." Biochemistry 48.23 (2009): 5199-5209.
- Schoch CL, et al. NCBI Taxonomy: a comprehensive update on curation, resources and tools. Database (Oxford). 2020: baaa062. PubMed: 32761142; PMC: PMC7408187. [NCBI Taxonomy]