Общая характеристика структуры
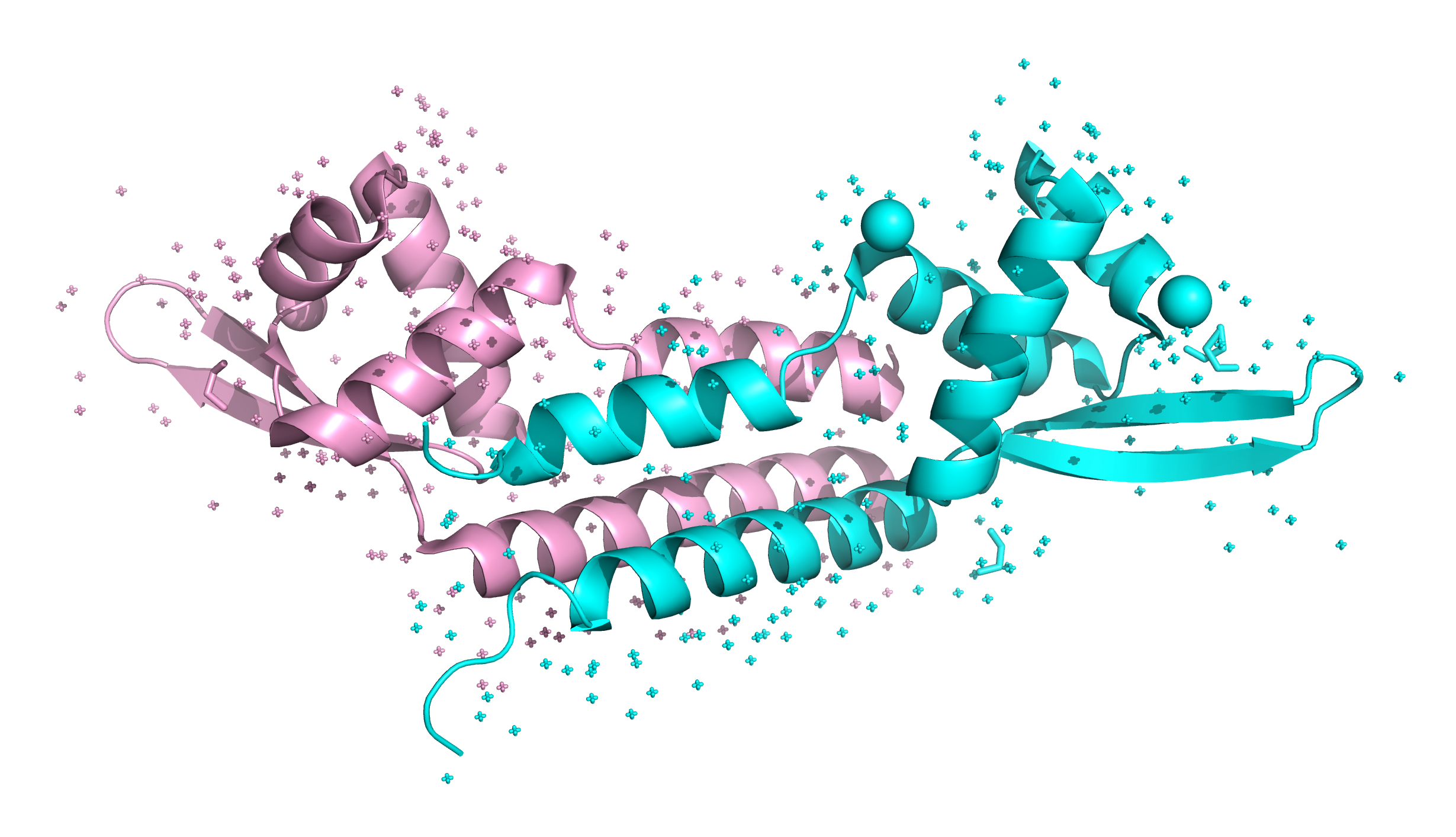
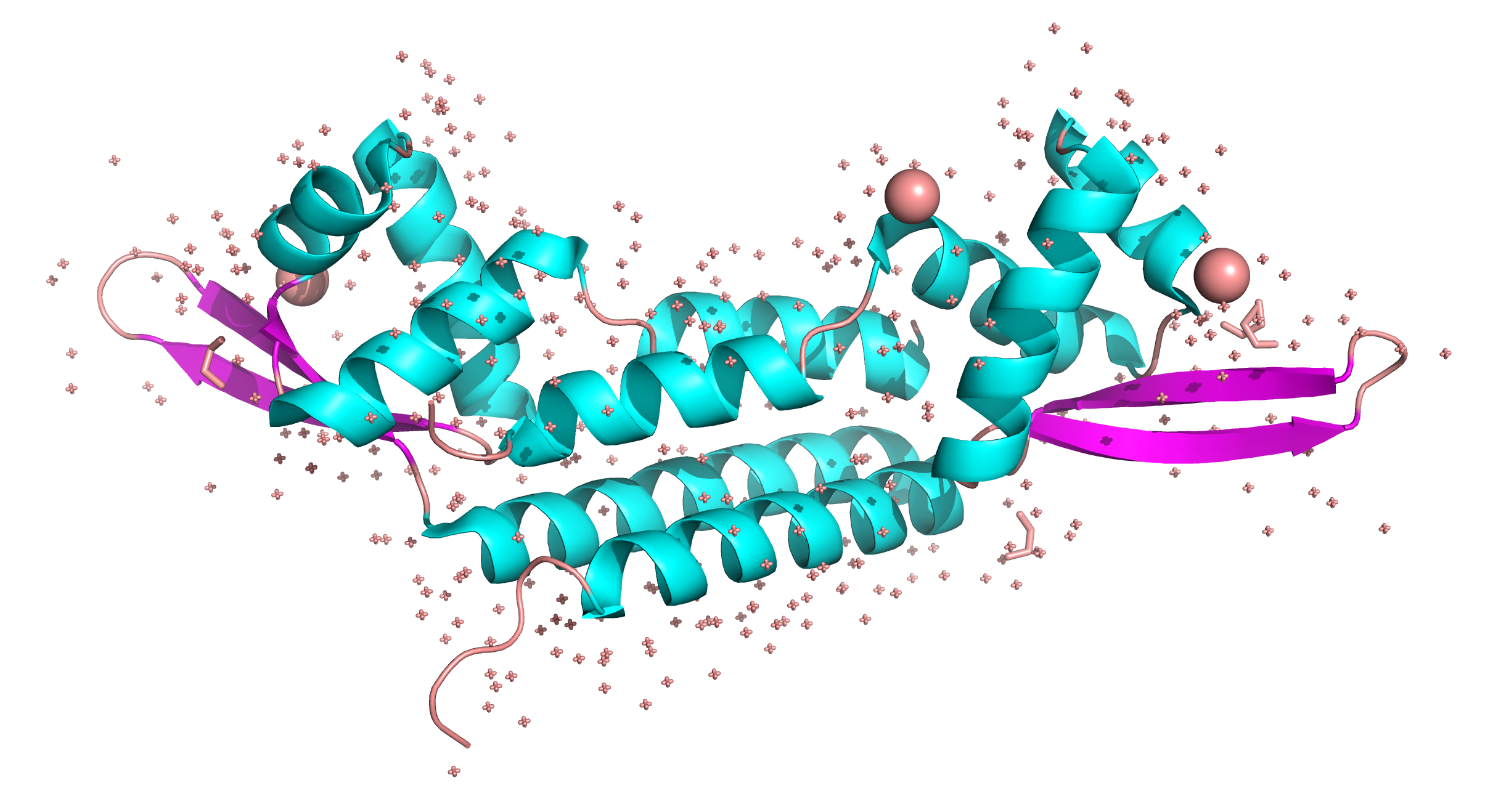
Объектом исследования является белок, пространственная структура которого определена методом рентгеновской кристаллографии. Биологическая единица - гомодимер, образованный двумя идентичными полипептидными цепями (A и B). Асимметрическая единица совпадает с биологической.
Характеристика отдельных цепей
Цепи A и B полностью идентичны, что позволяет провести их совместное описание.
• UniProt ID: O28271
• Организм: Archaeoglobus fulgidus
• Рекомендуемое название: Transcription regulator TrmB N-terminal domain-containing protein.
• Предполагаемая функция: регулятор транскрипции, содержащий ДНК-связывающий домен типа «спираль-поворот-спираль» (HTH).
• Мутации: мутаций относительно референсной UniProt-последовательности нет. Все отличия — либо модифицированные остатки (MSE), либо добавленные клонированные остатки (Cloning artifacts).
| Позиция в PDB | Остаток в PDB | Остаток в UniProt | Комментарий |
|---|---|---|---|
| 0 | HIS | — | Cloning artifact (N-концевой His-тег) |
| 1 | MSE | MET | Модифицированный остаток (селенометионин) |
| 34 | MSE | MET | Модифицированный остаток (селенометионин) |
| 103 | MSE | MET | Модифицированный остаток (селенометионин) |
| 107 | GLY | — | Cloning artifact (вставка для кристаллизации) |
| 108 | SER | — | Cloning artifact (вставка для кристаллизации) |
Вторичная структура
Анализ вторичной структуры показал, что в белке преобладают α-спирали.
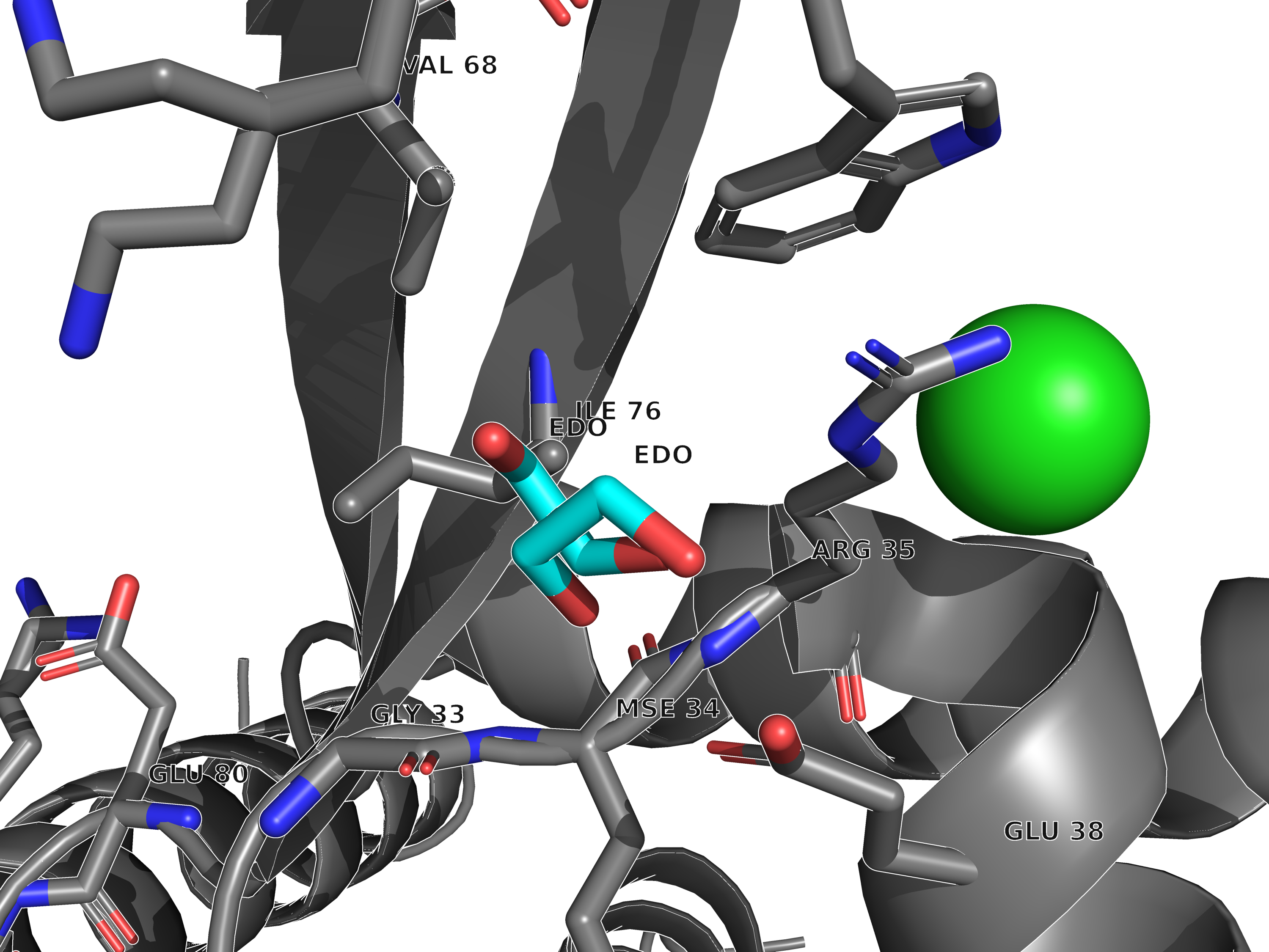
Малые молекулы
В записи структуры присутствуют такие малые молекулы, как:
• Ионы хлора (CL, Chloride ion)
• Этиленгликоль (EDO, 1,2-Ethanediol)
• Вода (HOH, Water)
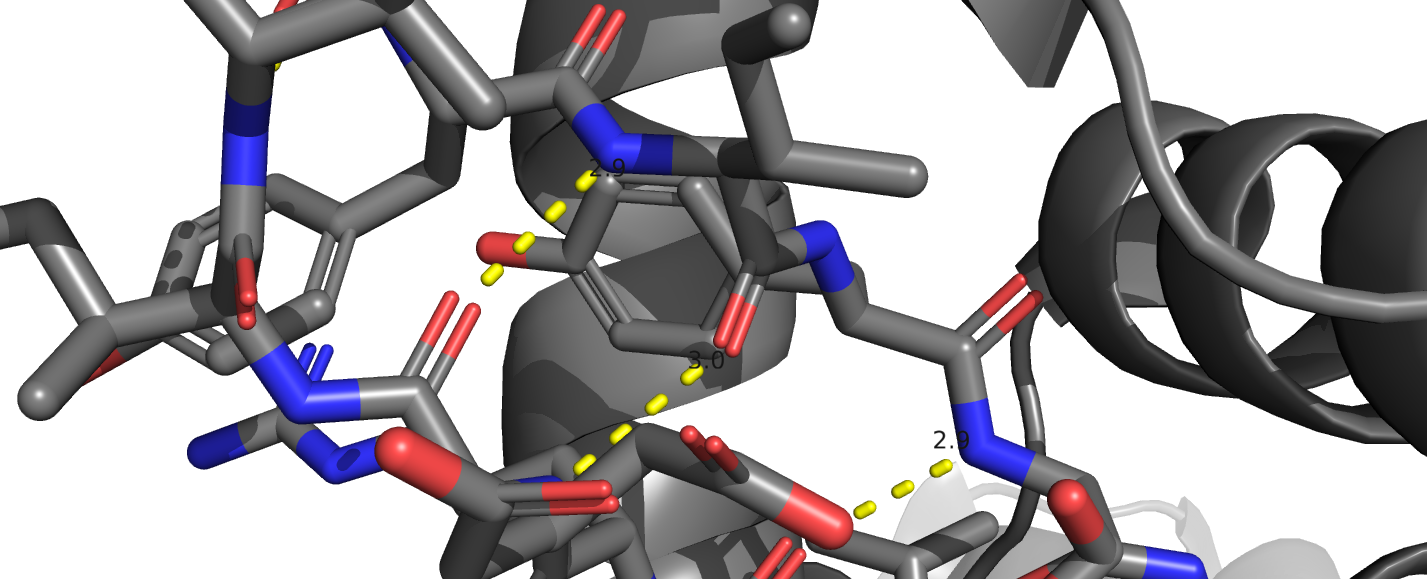
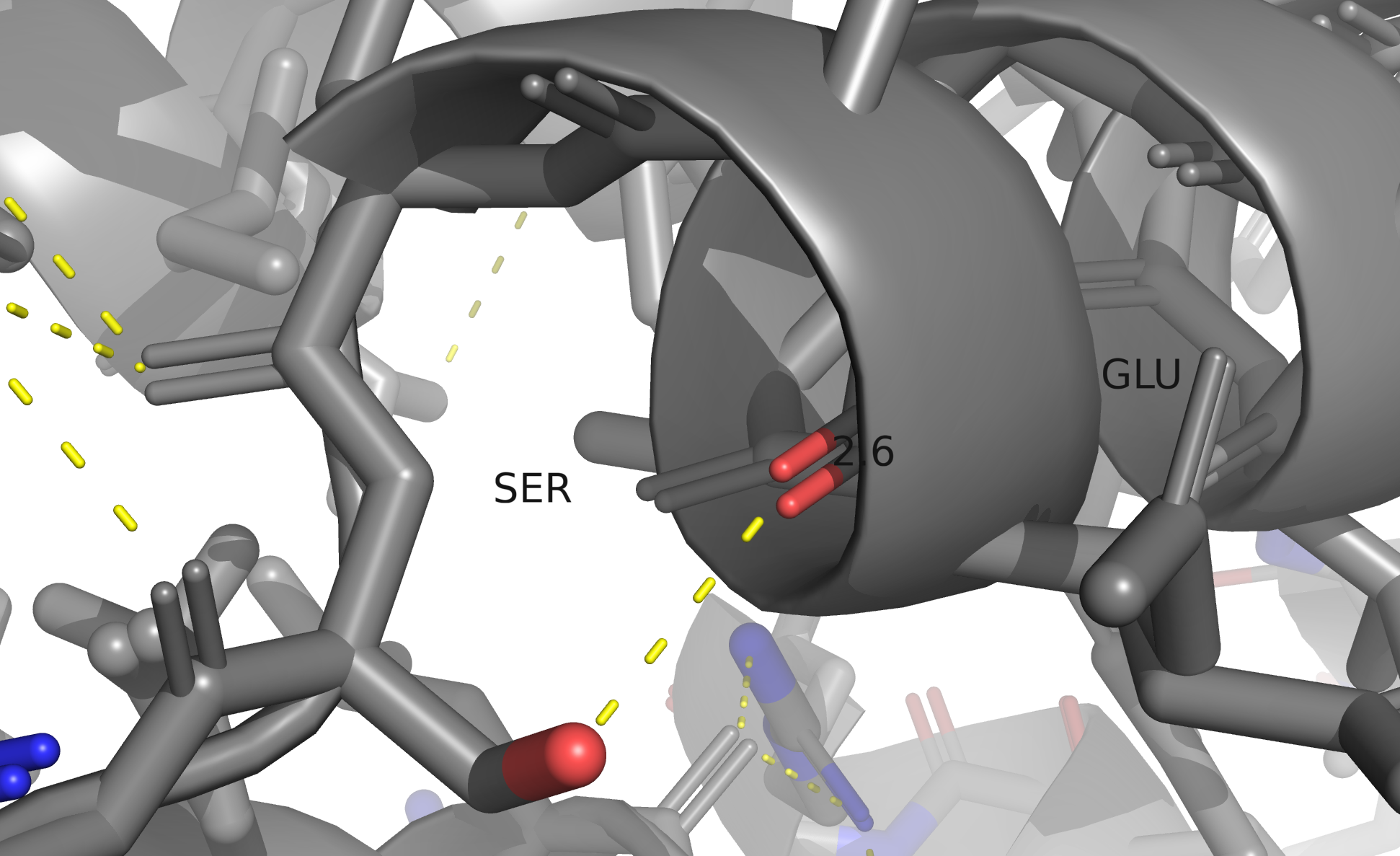
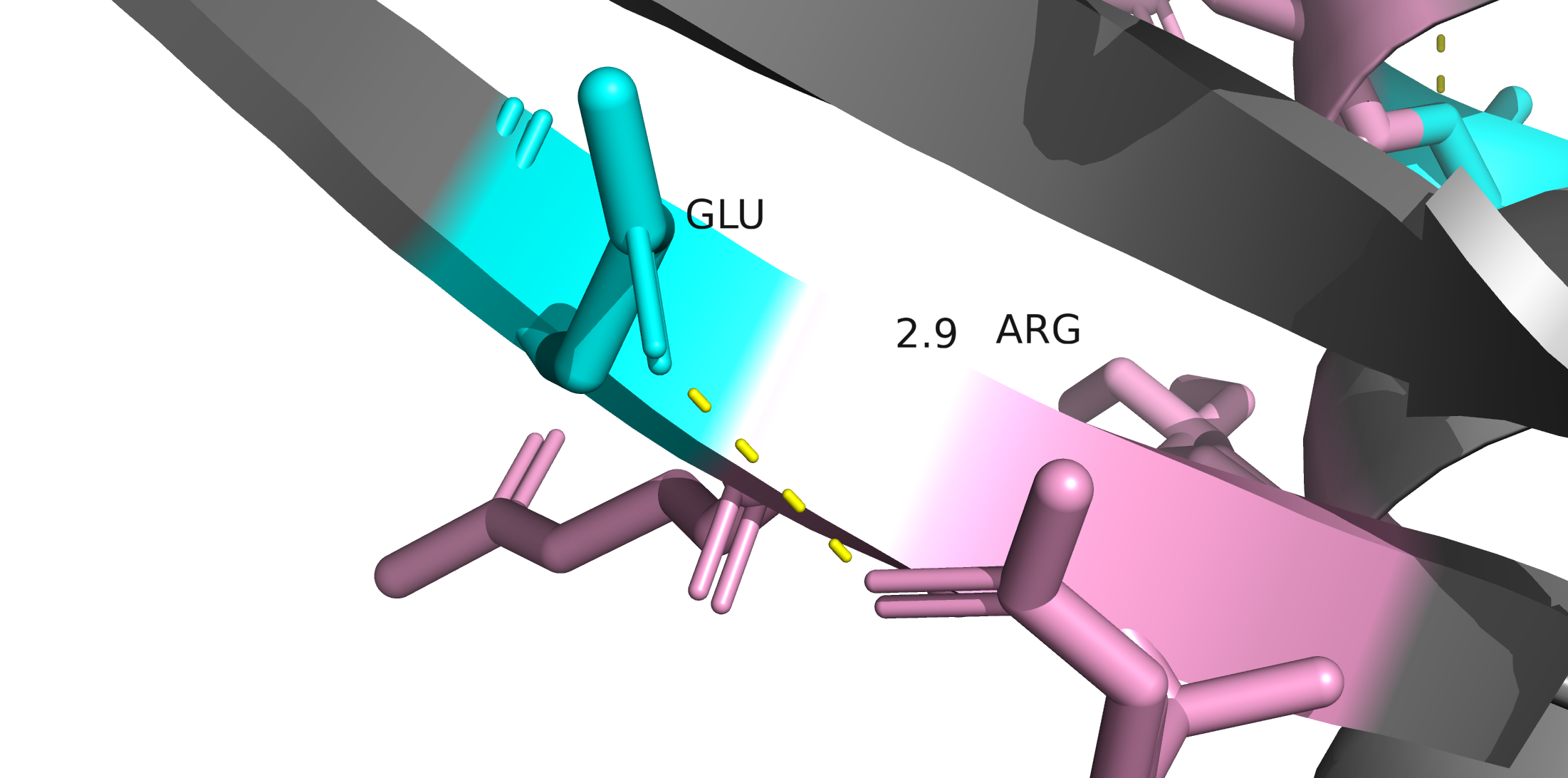
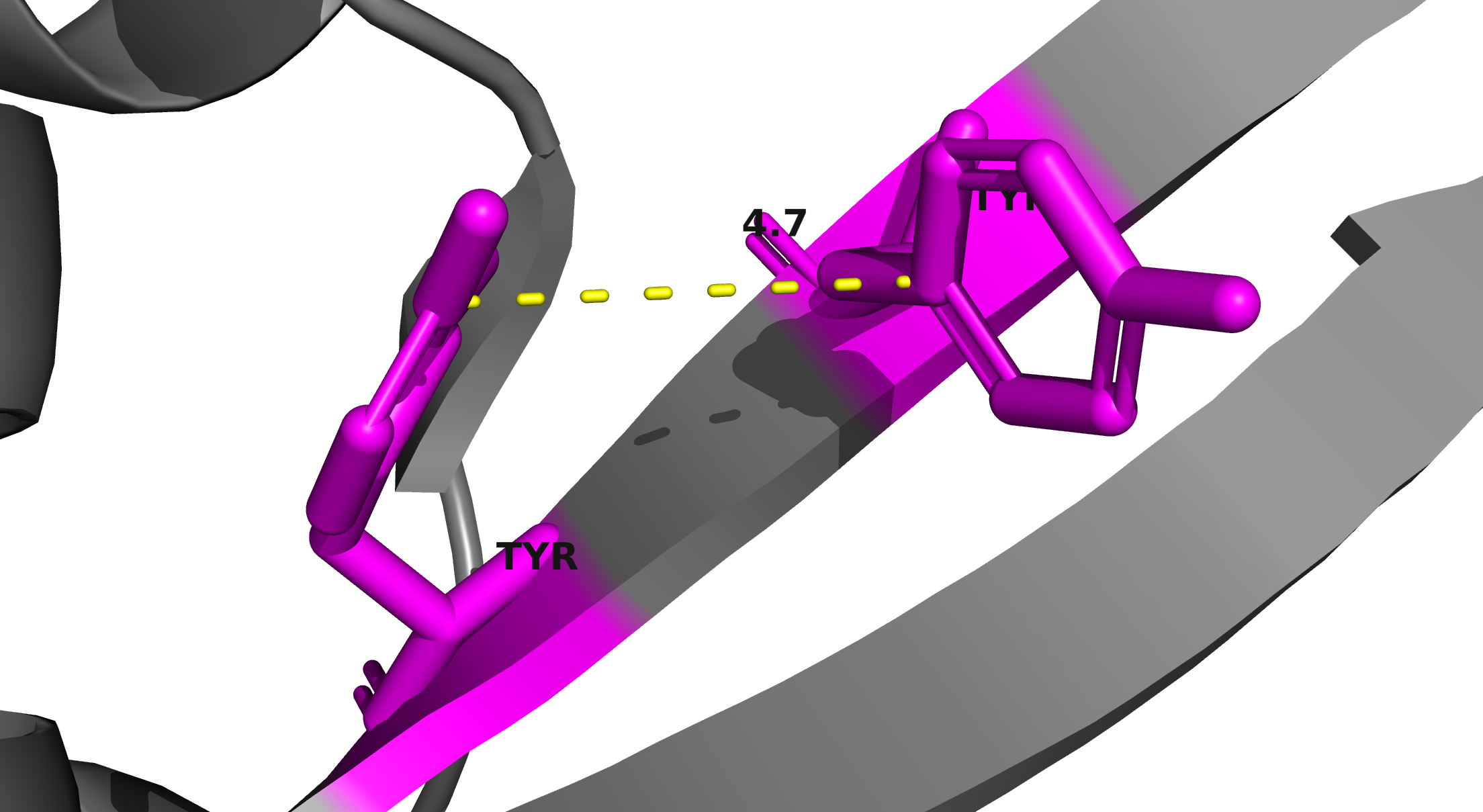
Взаимодействия в структуре белка
Структура данной молекулы поддерживается водородными связями, солевыми мостиками и стекинг-взаимодействиями. Дисульфидных мостиков обнаужено не было, так как в белке отсутствуют остатки цистеина.