Практикум 3. PDB
Общая информация
PDB_id: 1D3Y [1]
Название: Субъединица A топоизомеразы 6
Семейство: Топоизомеразы 2 типа
Организм: Methanocaldococcus jannaschii
Молекулярная масса: 68,32 kDa
Количество аминокислотных остатков: Каждая полипептидная цепь состоит из 369 аминокислотных остатков (в дальнейшем, ак), однако после частичного протеолиза остается фрагмент длиной 301 ак, устойчивый к протеолизу, именно он и описан в PDB и в приложенной статье на PubMed [2].
Функция: Расслабляет как положительные, так и отрицательные сверхвитки и проявляет сильную декатеназную активность.
Структура в целом
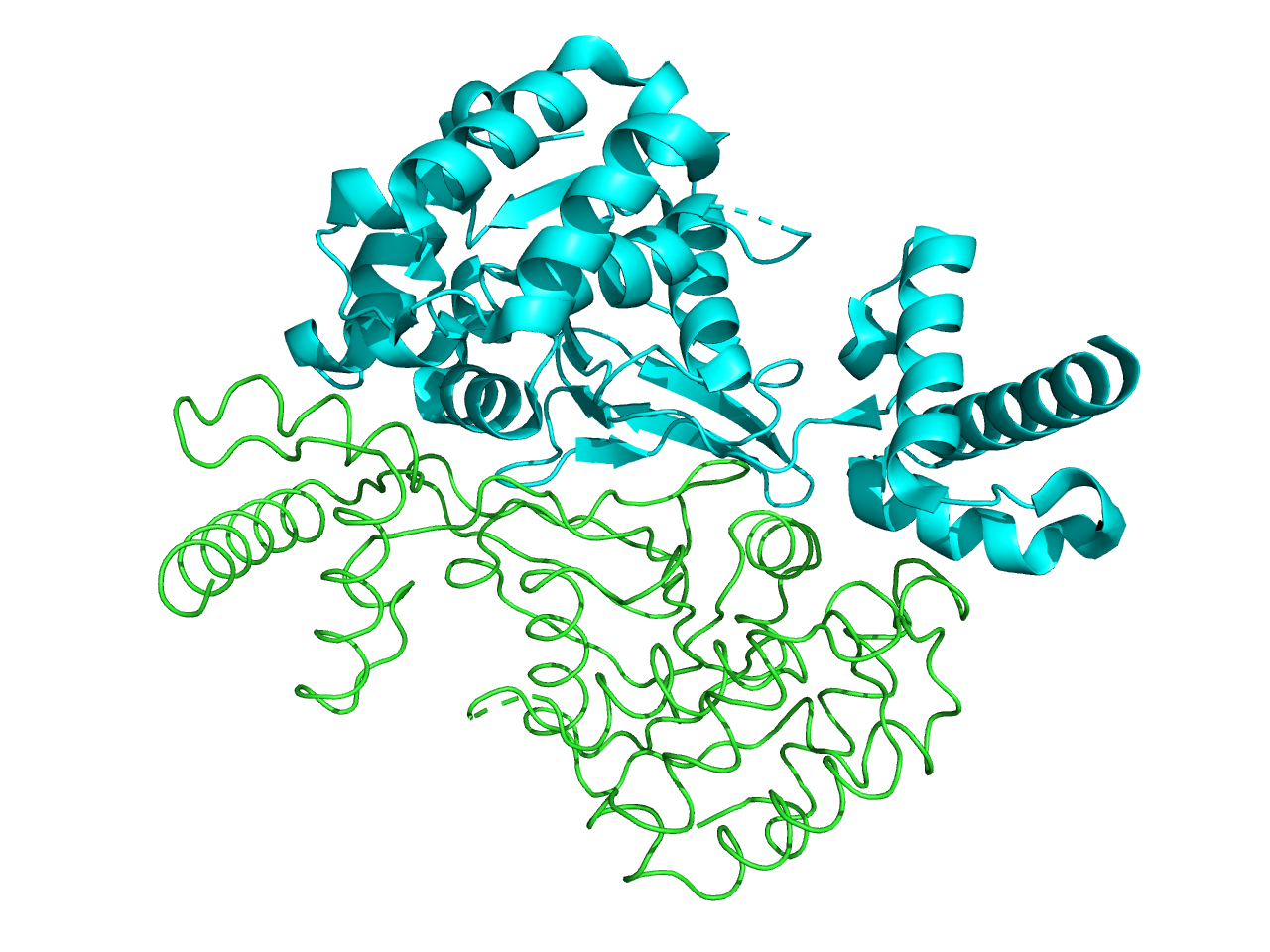
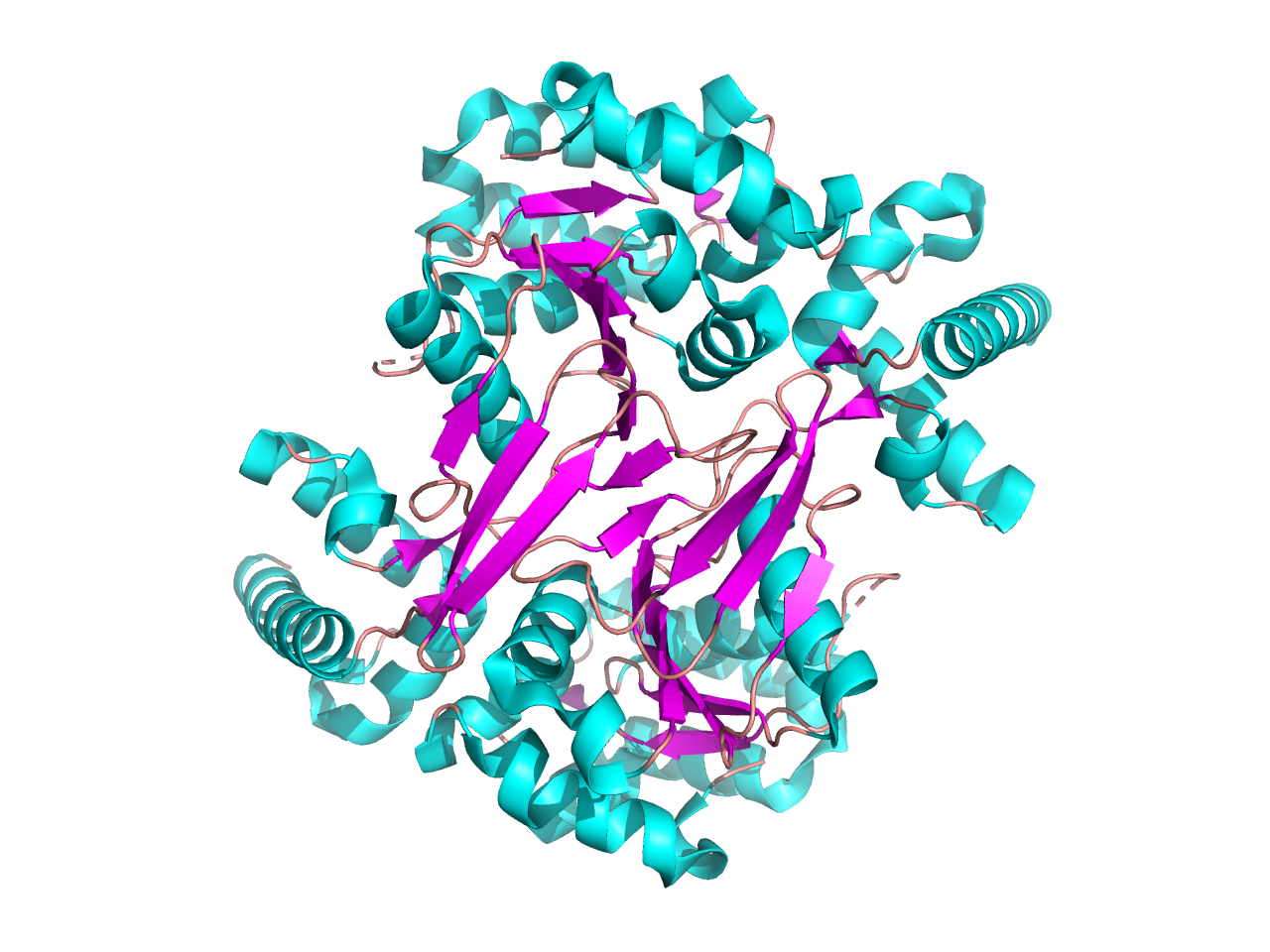
Субъединица A является гомодимером и состоит из двух идентичных цепей A и B (Рис.1, Рис.2.). Целостный фермент топоизомераза 6 явлется гетеротетрамером, состоящим из субъединиц A и B (не путать с полипептидными цепями). Мономер состоит из двух доменов: N-концевого (ак 69–140) и C-концевого (ак 147–369), соединенных коротким линкером (ак 141–146). Поиск по базе структурных данных DALI не выявил близких аналогов для всей молекулы, что подтверждает уникальность третичной структуры субъединицы А топоизомеразы 6 (Рис.3.) Тем не менее, два региона проявляют сходство с небольшими доменами или укладками, характерными для других белков [2].
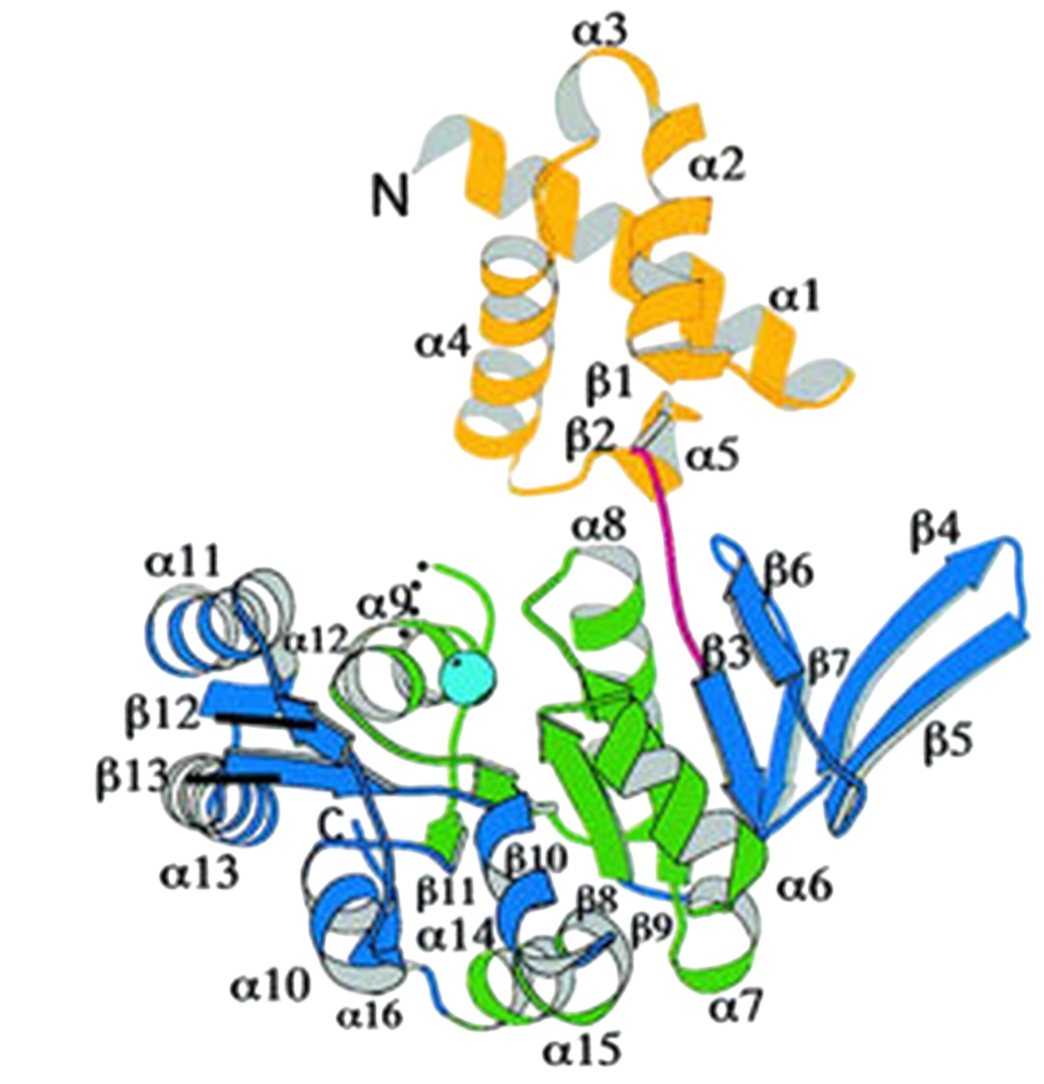
Отдельные цепи
Цепи идентичные, поэтому у них одинаковый UniprotID - Q57815 [3]. Они принадлежат организму Methanocaldococcus jannaschii (strain ATCC 43067). Каждая цепь релаксирует положительные и отрицательные супервитки, проявляя выраженную декатеназную активность. Осуществляет АТФ-зависимый разрыв, проведение и воссоединение цепей двухцепочечной ДНК. В файле 1D3Y.pdb присутствуют следующие строки: "COMPND 6 ENGINEERED: YES;", "COMPND 7 MUTATION: YES" (см. Сопроводительные материалы/1). Что говорит о том, что в последовательности есть мутации. Однако детальное их описание в файле отсутствует. Сравнение последовательностей из UniProt и PDB различий не выявило. Возможно, данные теги приведены вследствие того, что исследуемый фрагмент был получен в результате частичного протеолиза. Модифицированные аминокислотные остатки также не обнаружены.
Малые молекулы
В петлях складки типа Россмана обнаружен выраженный пик электронной плотности (>3.5σ). Октаэдрическая геометрия, межатомные расстояния 2.1–2.2 Å и наличие MgCl2 в условиях кристаллизации указывают на присутствие иона Mg2+. Ион координируется консервативными остатками: Glu197 (соединение β8/α6), Asp249 и Asp251 (петля β10–α9). Взаимодействие происходит напрямую через Glu197 и Asp249, тогда как Asp251 связывается через две молекулы воды. Еще две молекулы воды дополняют координацию до полной октаэдрической. Двухвалентные катионы, в частности ион Mg2+, часто являются кофакторами топоизомераз. Mg2+ участвует в присоединении фермента к ДНК, также сообщается о его участии в механизме разрезания цепей ДНК. Все вышеперечисленное характерно для обеих цепей A и B. Что интересно, в PDB файле также обнаружен несвязанный с белком ион Mg2+, координированный чисто молекулами воды. Это, по всей видимости, артефакт кристаллизации (см. Сопроводительные материалы/2).
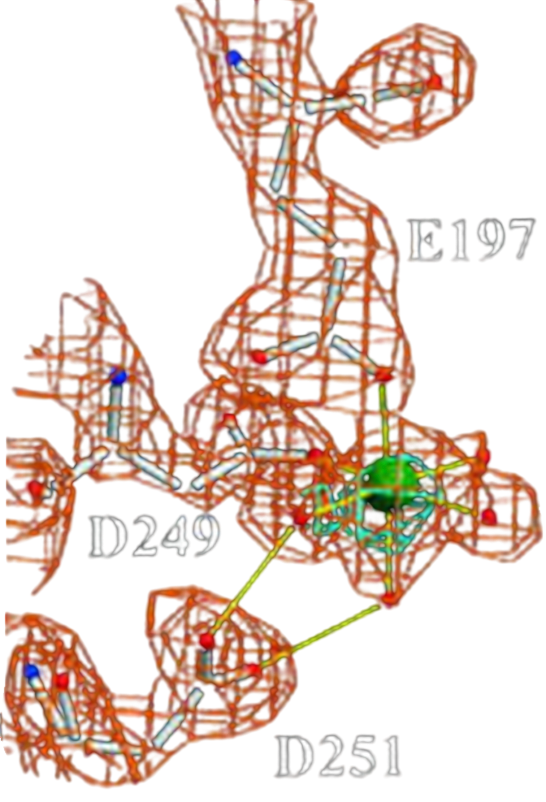
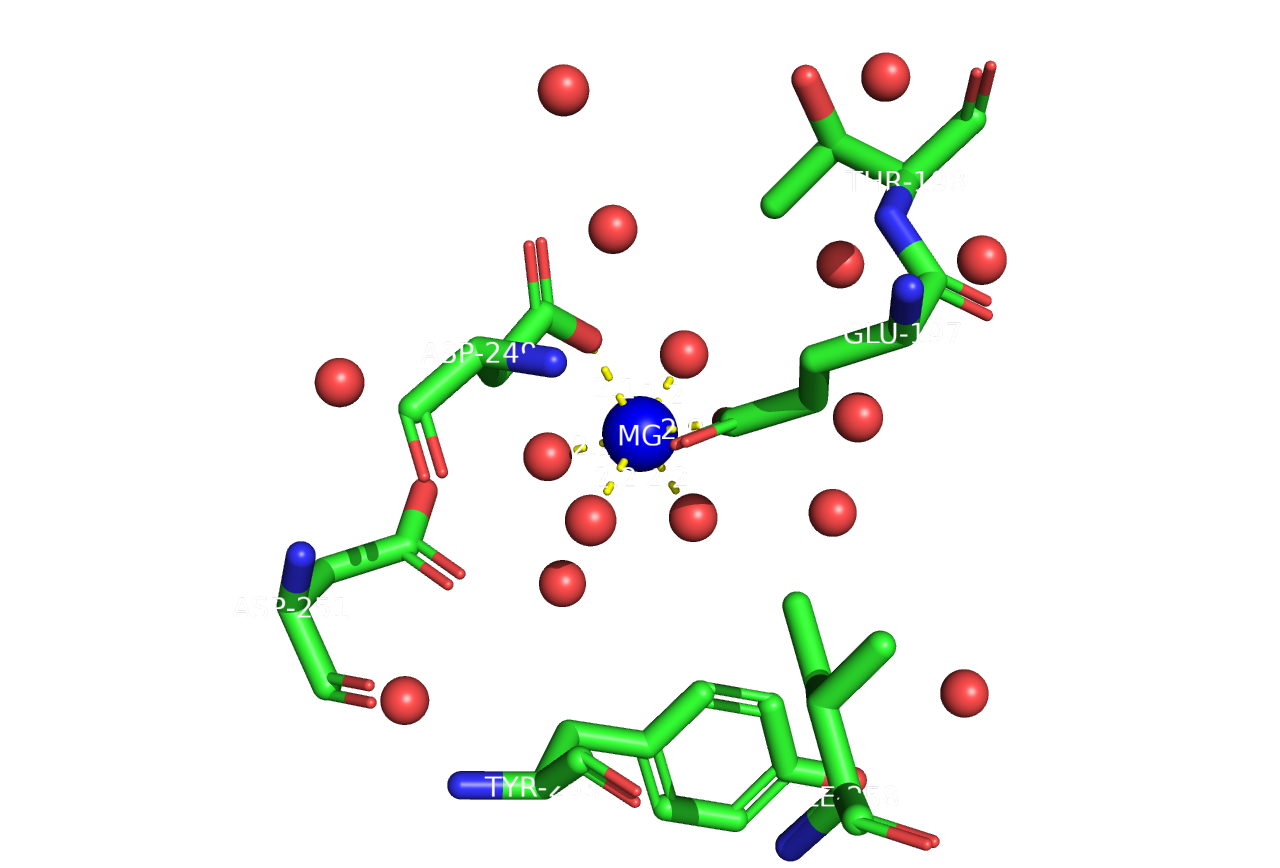
В PDB файле в контексте малых молекул также упоминается Na+, однако, судя по всему, он не является частью нативной структуры белка. В методике кристаллизации использовалось множество реагентов, содержащих соли Na (например, NaCl), поэтому логично предположить, что наличие иона Na+ - артефакт кристаллизации.
Описание взаимодействий между аминокислотными остатками
В субъединице А топоизомеразы 6 можно найти много различных типов взаимодействий между аминокислотами. Эти взаимодействия необходимы для поддержания нативной вторичной, третичной, а так же четвертичной структуры.
Водородные взаимодействия играют исключительную роль в поддержании вторичной структуры белка. На рисунках ниже изображены водородные связи: между элементами остова белка (Рис.5), между боковыми радикалами (Рис.6).
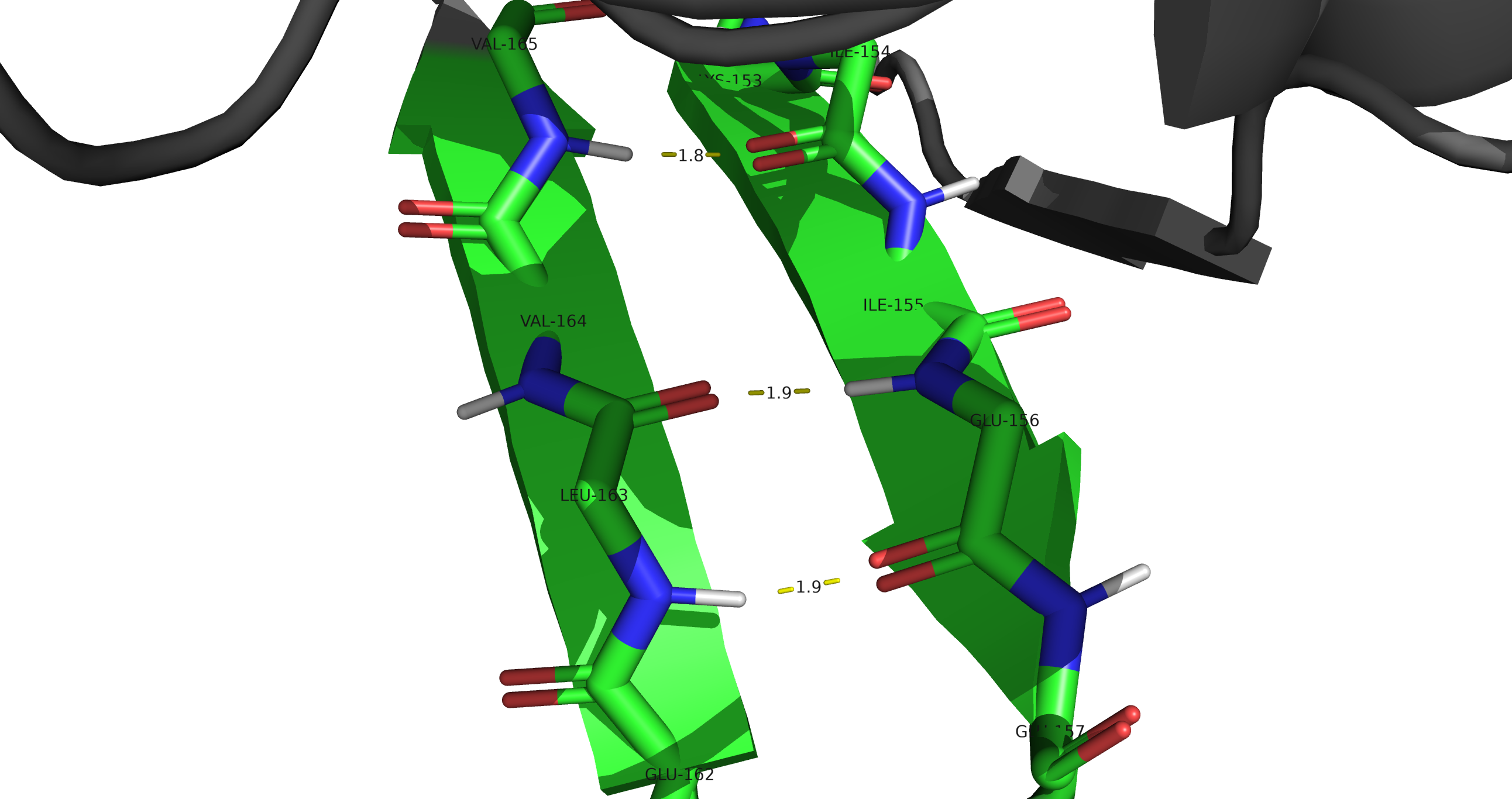
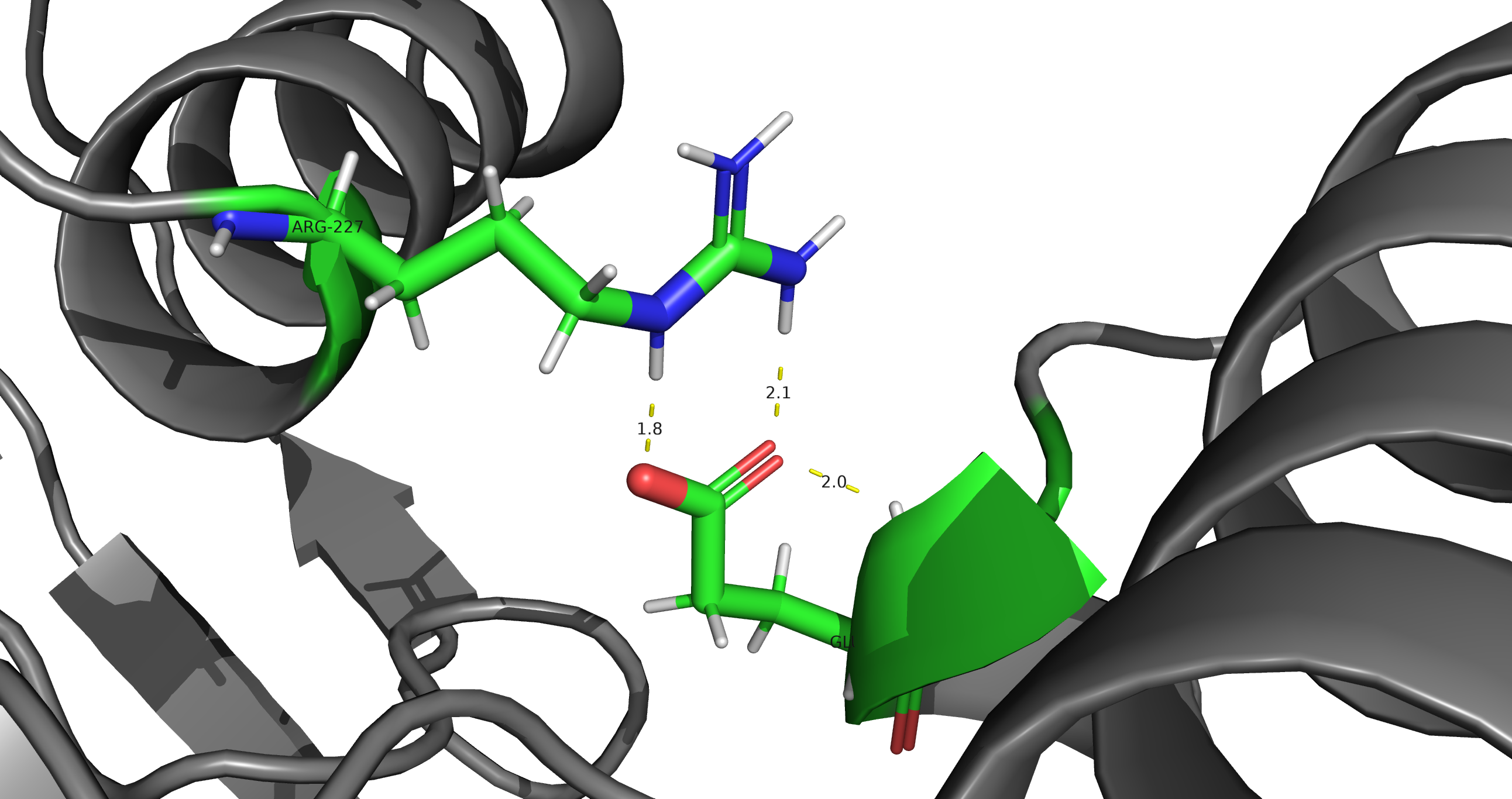
Солевые мостики возникают между положительно заряженными и отрицательно заряженными боковыми радикалами аминокислот. Ниже изображен солевой мостик между Asp114 и Lys74 (Рис.7).
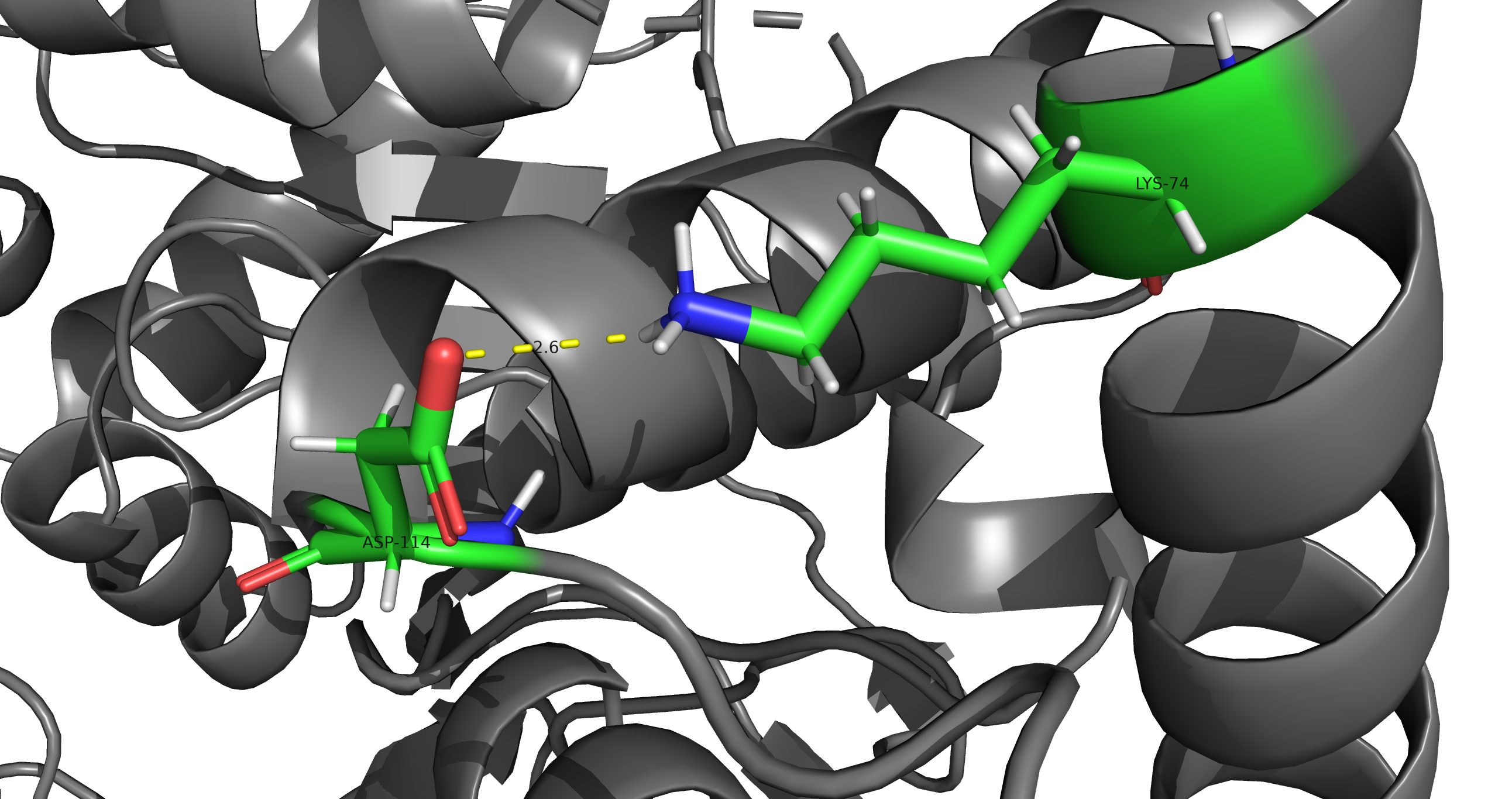
Дисульфидные мостики в данном белке не обнаружены. Снизу приведено изображение всех остатков цистеина в белке (Рис.8).
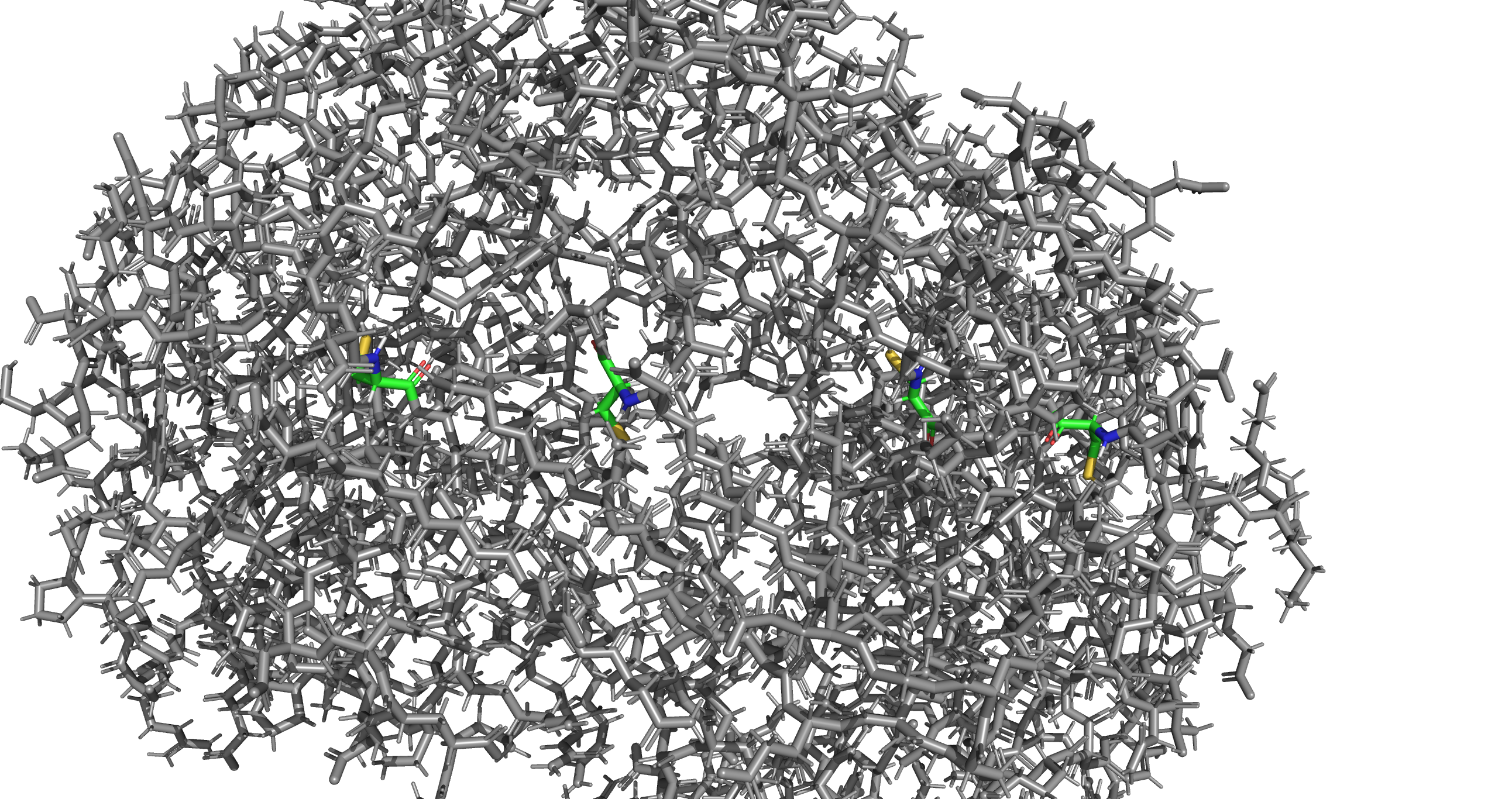
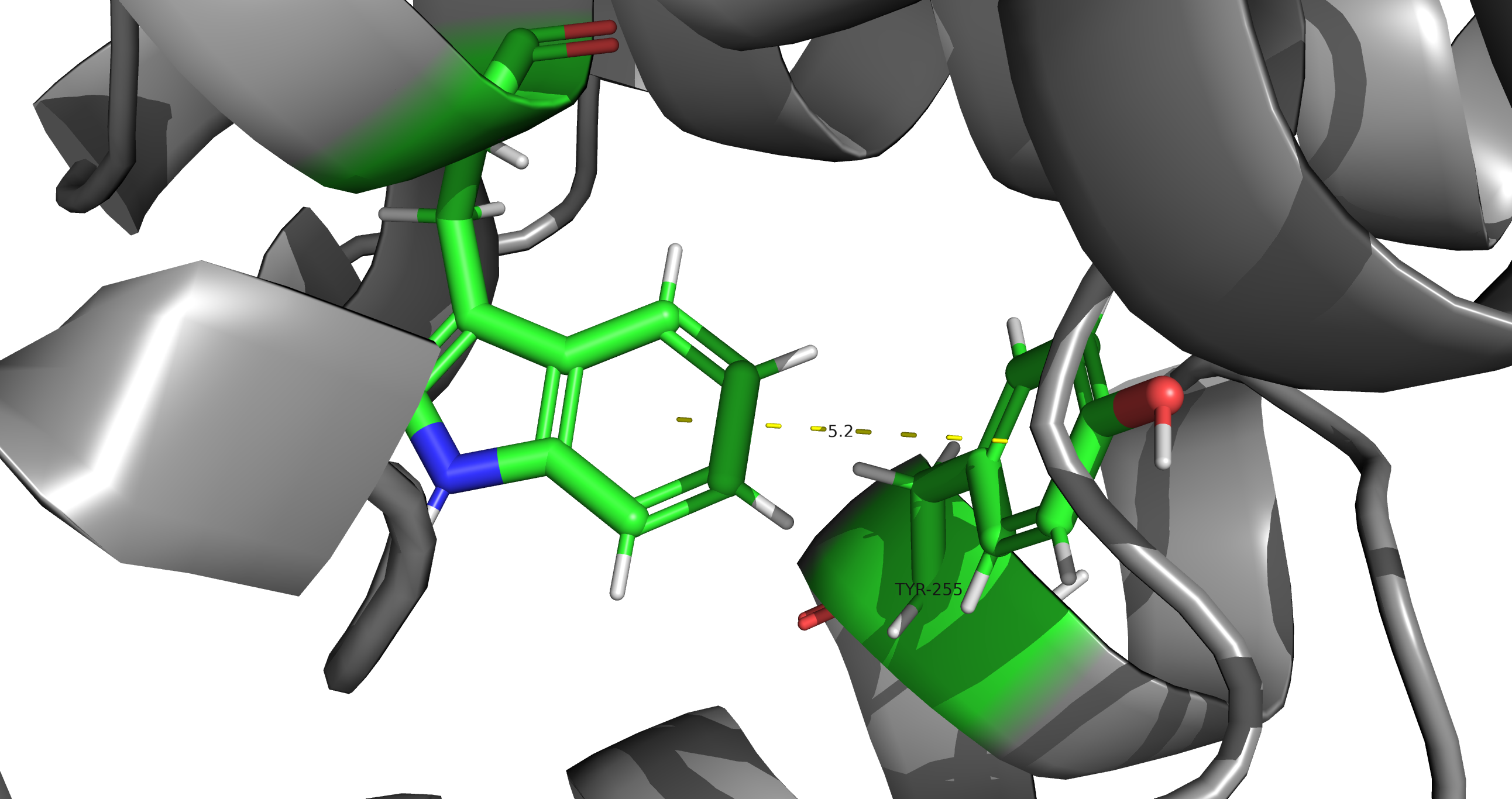
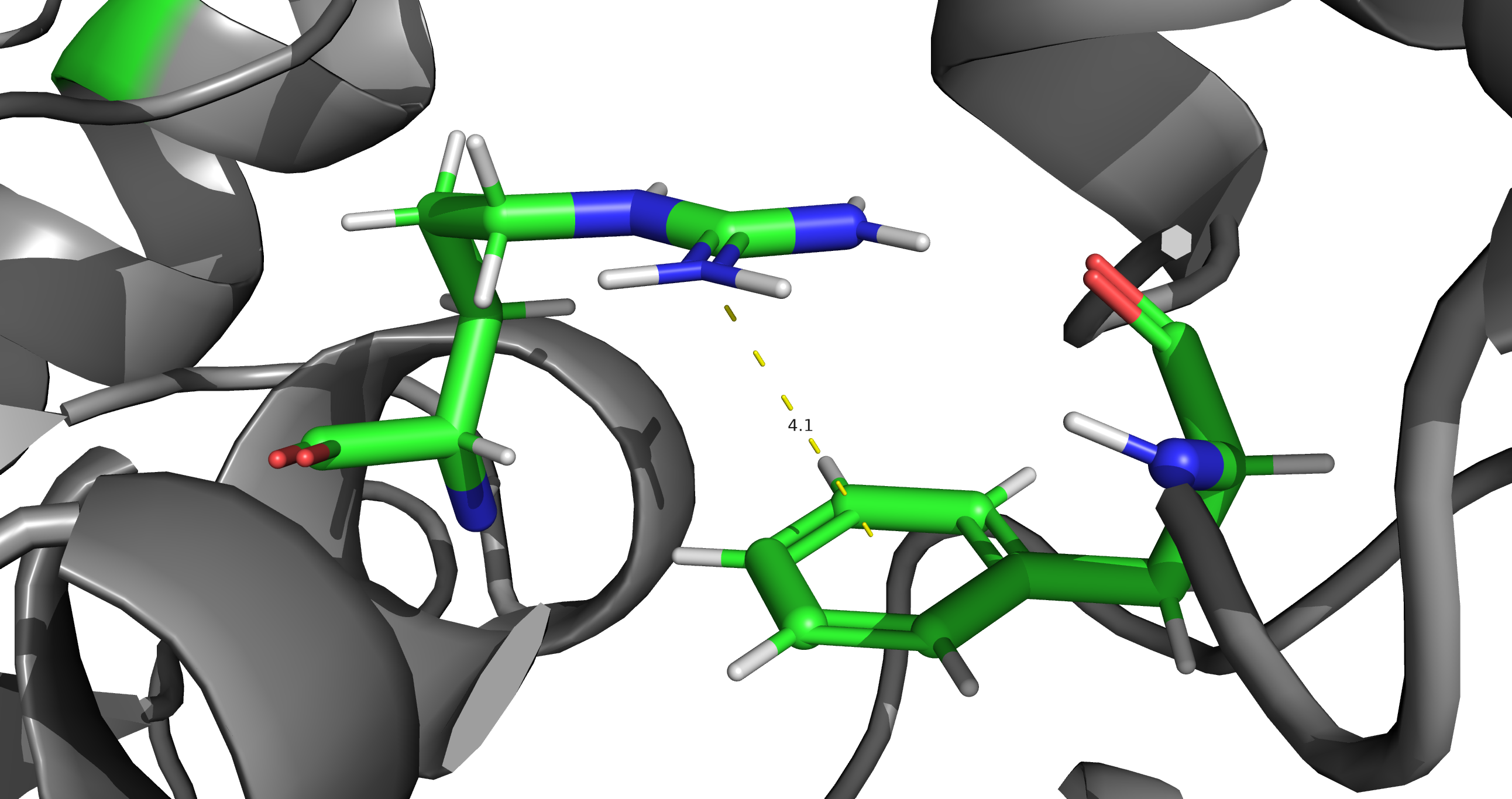
Стекинг взаимодействия участвуют в стабилизации третичной структуры белка. Различают параллельно сдвинутый стекинг (ароматические кольца расположены параллельно), Т-стекинг (ароматические кольца расположены перпендикулярно) и Пи-катионный стекинг (взаимодействие между катионом и ароматическим кольцом). Ниже приведены примеры T-стекинга (Рис.9) и Пи-катионного стекинга (Рис.10) в субъединице А топоизомеразы 6.
Сопроводительные материалы
1.Файл с описанием тегов COMPND
2.Файл с описанием малых молекул
Список литературы и иных источников
2.Matthew D. Nichols, Kristen DeAngelis, James L. Keck & James M. Berger. Structure and function of an archaeal topoisomerase VI subunit with homology to the meiotic recombination factor Spo11. The EMBO Journal. 1999;18:6177–6188
https://link.springer.com/article/10.1093/emboj/18.21.6177#Sec7