Для анализа была выбрана последовательность μ-кристаллина человека (GenBank AC: AAB94938.1). В описании записи последовательности присутствует указание, что данный белок является орнитин-циклодеаминазой (превращение орнитина в пролин с выходом аммиака). В тоже время было показано, что mu-кристаллин млекопитающих обладает кетиминредуктазной активностью (NAD(P)H-зависимое восстановление иминной связи). Поиск через psi-blast может помочь определить дальние гомологи этого белка.
При поиске с помощью psi-blast по базе данных Swiss-Prot с порогом E-value: 0.001 (в остальном параметры дефолтные) на первой итерации находятся 50 последовательностей. Среди них - μ-кристаллины - кетимин редуктазы (соответствующая ферментативная функция указана в описании этих записей) западного серого кенгуру, домашнего быка, домашней мыши и серой крысы. Также среди результатов оказались бактериальные дельта-пирролин-2-карбоксилат редуктазы, являющиеся кетимин-редуктазами, специфичными к пролину, бактериальные орнитин-циклодеаминазы и различные дегидрогеназы.
На следующей итерации число найденных последовательностей выросло до 351. Все новые последовательности - глутамил-тРНК редуктазы. Катализируемая этим ферментом реакция NADPH зависима, что сближает её с реакцией, катализируемой кетимин редуктазой.
На третьей итерации находок стало 500 (их число достигло лимита). В списке появились новые глутамил-тРНК редуктазы, а также шикимат редуктазы и цитокин-подобный ядерный фактор N-PAC. С ранее описанными ферментами их сближает способность связывать NADPH.
На четвёртой итерации в списке появились новые глутамил-тРНК редуктазы.
Пятая итерация стала последней - при попытке проводить дальнейшие итерации в списке находок лишь появляются всё новые и новые глутамил-тРНК редуктазы.
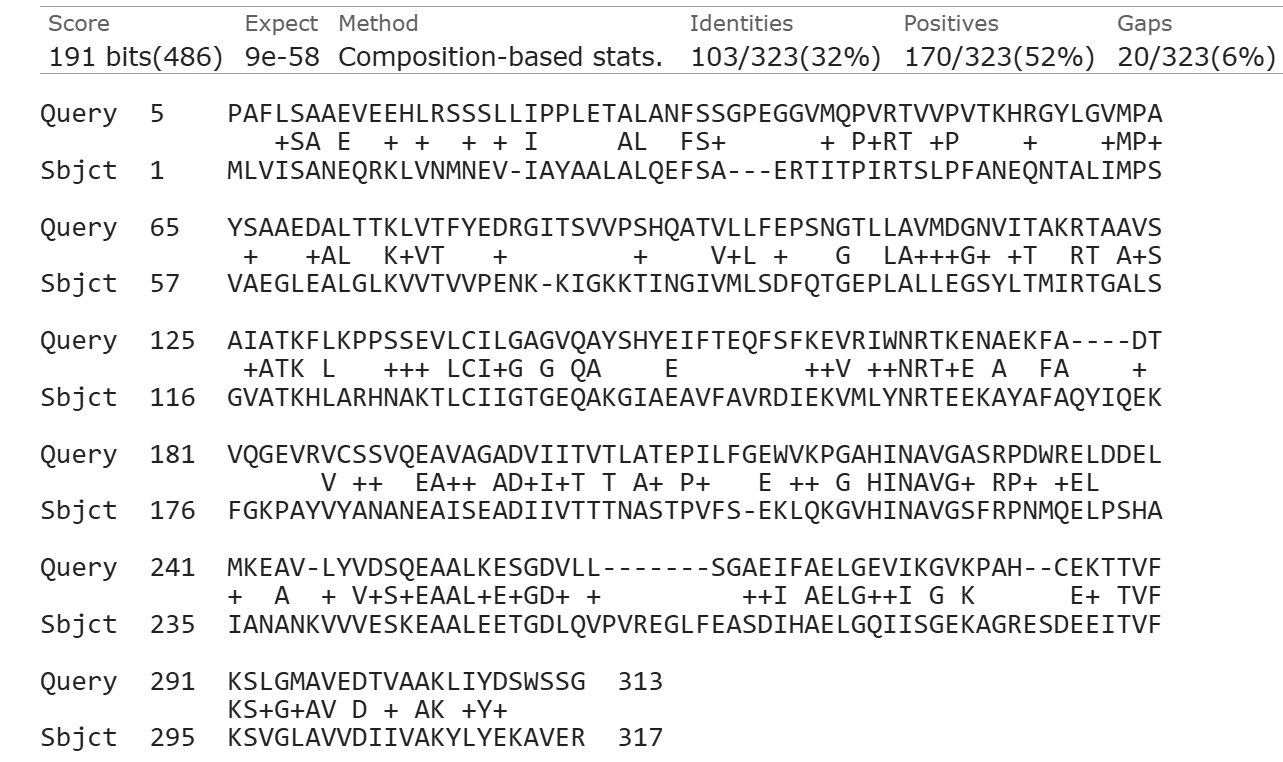
Итак, после пяти итераций подавляющее большинство находок составляют глутамил-тРНК редуктазы, также присутствуют μ-кристаллины нескольких млекопитающих, бактериальные орнитин циклодеаминазы и дельта-пирролин-2-карбоксилат редуктазы и некоторые другие редуктазы. Таким образом, среди находок оказались кетимин-редуктазы - дельта-пирролин-2-карбоксилат редуктазы (см. рис. 1). Это подтверждает предположение о том, что они могут являться древними предшественниками μ-кристаллина, возможно не только человека, но и всех млекопитающих (на то, что μ-кристалллины млекопитающих близки, указывает нахождение μ-кристалллинов нескольких млекопитающих с хорошим E-value уже на первой итерации psi-blast).
