Атлас контактов белка 4QKC
Оглавление
Вступление
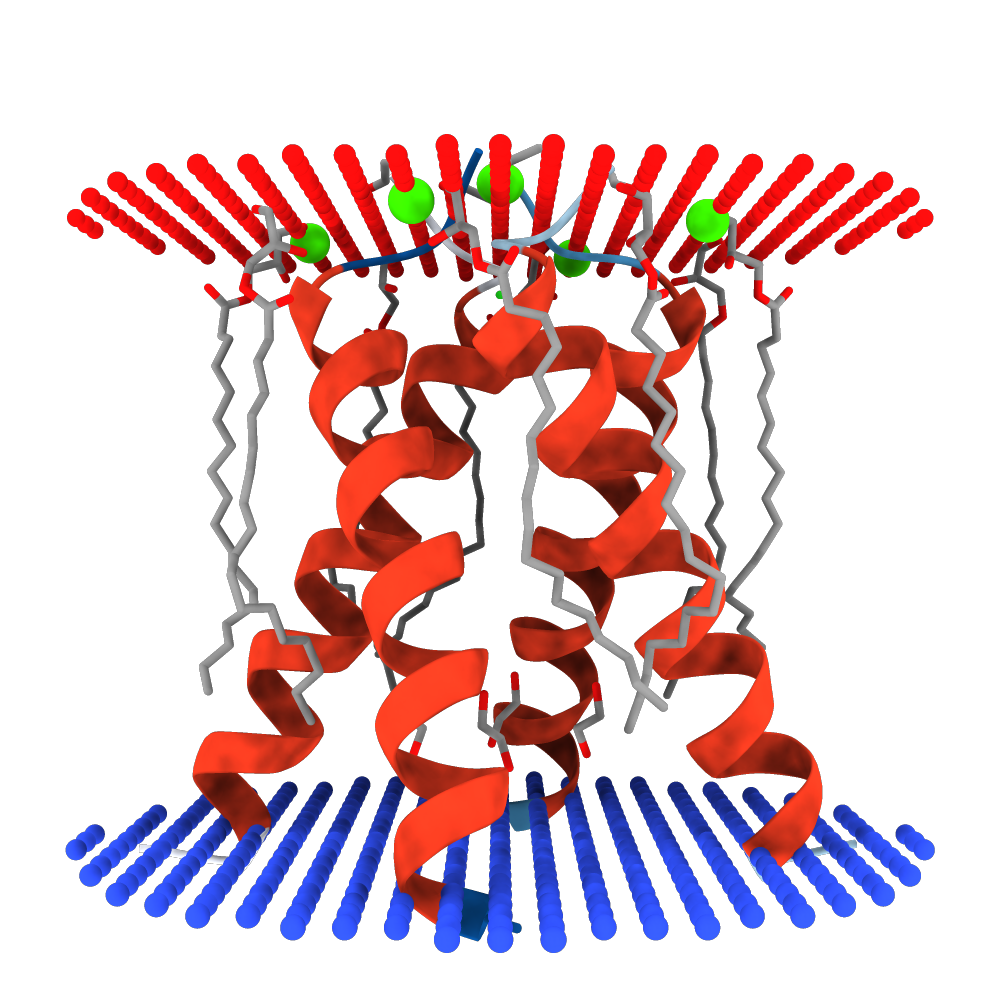
Матрица 2 (M2) белка из вируса гриппа А(Infulenza A virus H3N2) является протонным каналом, который использует остаток His37 в качестве селективного фильтра. То есть белок проводит протоны с одной стороны мембраны на другую. Протонный канал М2 вируса гриппа А является не только важным с медицинской точки зрения белком, но и простой, четко определенной системой для изучения переноса протонов через замкнутые пространства. Например, этот канал является мишенью противогриппозного препарата амантадин.2Некоторая общая информация о белке(по данным RSCB PDB3)
- Функциональная роль: протонный канал
- PDB id: 4QKC
- Общая масса структуры: 3645.10 Да
- Количество атомов: 407
- Количество остатков: 27
- Количество уникальных цепей: 1
Лиганды
C21H40O4| Cl-| Ca2+| C2H6O2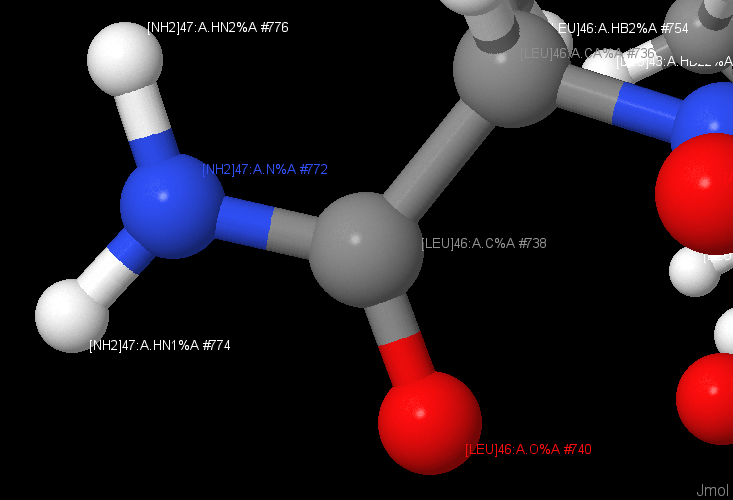
C21H40O4
Моноглицерид, или, если быть точнее, моноацилглицерин, представляет собой глицерид, состоящий из одной цепи жирной кислоты, ковалентно связанной с молекулой глицерина с образованием эфира. Действует как эмульгатор, помогая смешивать такие ингредиенты, как нефть и вода, которые в противном случае не смешивались бы.4 В данном случае входит в состав мембраны.
Данный глицерид фиксируется ионом кальция к боковой ветви аспарагина, 3 остатка белковой цепи, посредством ионных связей.
| Физико-химические свойства лиганда | ||
|---|---|---|
| Название | Значение | Упоминание |
| Молекулярная масса | 356.5 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Точная масса | 356.29266 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Топологическая площадь полярной поверхности | 66.8 Å2 | Cactvs 3.4.6.11 (PubChem release 2019.06.18) |
| Количество тяжелых атомов | 25 | PubChem |
Cl-
Ион хлорида - это анион хлора, который образует отрицательно заряженную часть некоторых солей, в том числе солей натрия и хлористого водорода, и является незаменимым электролитом, находящимся во всех жидкостях организма, отвечающим за поддержание кислотно-основного баланса, передачу нервных импульсов и регулирование жидкости в клетках и из них.6
| Физико-химические свойства лиганда | ||
|---|---|---|
| Название | Значение | Упоминание |
| Молекулярная масса | 35.45 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Точная масса | 34.968853 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Топологическая площадь полярной поверхности | 0 Å2 | Cactvs 3.4.6.11 (PubChem release 2019.06.18) |
| Количество тяжелых атомов | 1 | PubChem |
Ca2+
Кальций необходим живым организмам, особенно в клеточной физиологии, и является наиболее распространенным металлом у многих животных. Физиологически он существует как ион в организме. Кальций в сочетании с фосфором образует фосфат кальция в костях и зубах. Он необходим для нормального функционирования нервов и мышц и играет роль в свертывании крови (как фактор IV) и во многих ферментативных процессах.8
Так, демонстрируемый по нажатии кнопки ниже катион кальция связан ионной связью с кислородом бокового остатка аспарангина - 3 остатка в цепи. С другой стороны, еще одной ионной связью этот катион фиксирует положение глицерида.
| Физико-химические свойства лиганда | ||
|---|---|---|
| Название | Значение | Упоминание |
| Молекулярная масса | 40.08 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Точная масса | 39.962591 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Топологическая площадь полярной поверхности | 0 Å2 | Cactvs 3.4.6.11 (PubChem release 2019.06.18) |
| Количество тяжелых атомов | 1 | PubChem |
C2H6O2
Этиленгликоль - синтетическое жидкое вещество, поглощающее воду. Он не имеет запаха, но имеет сладкий вкус. Этиленгликоль используется для изготовления антифризов и антиобледенительных растворов для автомобилей, самолетов и лодок. Он также используется в гидравлических тормозных жидкостях и чернилах, используемых в колодках для печатей, шариковых ручках и типографиях.10
| Физико-химические свойства лиганда | ||
|---|---|---|
| Название | Значение | Упоминание |
| Молекулярная масса | 62.07 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Точная масса | 62.036779 г/моль | PubChem 2.1 (PubChem release 2019.06.18) |
| Топологическая площадь полярной поверхности | 40.5 Å2 | Cactvs 3.4.6.11 (PubChem release 2019.06.18) |
| Количество тяжелых атомов | 4 | PubChem |
Контакты с лигандами
Окружение лигандов показало взаимодействие лишь через ковалентные связи.
Водородные связи
| Параметры водородных связей между остовными атомами во вторичной структуре | |||
|---|---|---|---|
| # | Имена атомов | Длина связи(Å) | Угол N-O-H(°) |
| Альфа-спираль | |||
| 1 | N(038LEU)-O(034GLY) | 3.05 | 161.1 |
| 2 | N(041TRP)-O(037HIS) | 2.95 | 160.2 |
| 3 | N(042ILE)-O(038LEU) | 2.92 | 167.5 |
Водородные связи обеспечивают структуру альфа-спирали, можно заметить, что остатки связываются через каждые ≈4 аминокислоты, что соответствует "витку" спирали12. Все длины приведенных водородных связей <3.9Å, а все углы >90°, эти значения соответствуют типичным значениям параметров для таких химических связей13.
Помимо водородных связей в одной цепи при помощи симметрии Unitcell (включающей биологическую единицу) удалось воспроизвести водородные связи между цепями. Например между боковыми радикалами 26 серина в 4 цепях расстояние составляет 2.6 ангстрем, а угол - 95.5°. По данным статьи13, они соответсвуют нормам.
Солевые мостики
Солевые мостки образуются в результате реакции между противоположно заряженными боковыми радикалами аминокислот14. Однако в fasta последовательности данного белка обнаружены только 4 аминокислотных остатка, способные заряжатся при стандартных условиях: два аспартата, гистидин и аргинин. Все, за исключением последних аспартата и аргинина, удалены друг от друга более чем на 4 остатка и связь между ними невозможна. А если рассмотреть боковые радикалы расположенных рядом двух аминокислот, то несложно заметить, что между ними тоже нет никакой связи. В итоге белок не обладает никакими солевыми мостиками.
Гидрофобные контакты
В качестве гидрофобного ядра был выбран аланин (33) - не самая маленькая гидрофобная аминокислота. Как можно убедиться при воспроизведении предложенного ниже скрипта, этот остаток почти полностью покрывают окружающие атомы на расстоянии 2-3 ангстрем. Таким образом, к гидрофобному ядру не может проникнуть, например, молекула воды с примерным диаметром в 2.8 ангстрем.
Кроме того, при выполнении того же скрипта можно заметить, что характерное расстояние между не связанными атомами в белке - около двух ангстрем.
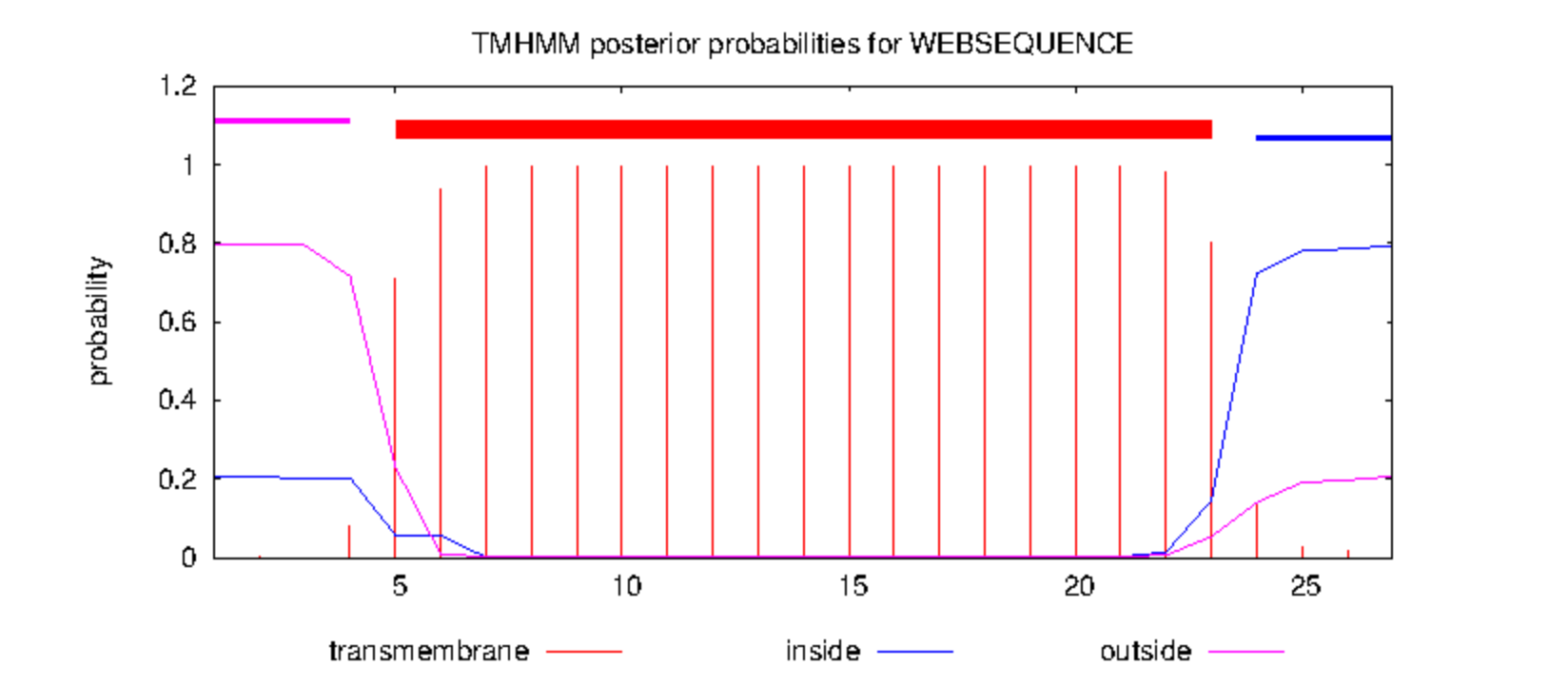
Положение в мембране
Проверка расположения белка в мембране осуществлена с помощью сервиса TMHMM15. Как видно из графика, снаружи от мембраны находятся аминокислотные остатки с первого по четвертый, в мембране - с 5 по 23, а внутри клетки - с 24 по 27.
Личный вклад
Вклад авторов: атлас контактов сделан совместными усилиями КМ и МИ. Текстовая верстка и дизайн страницы осуществлены МИ, в то время как КМ провел редакцию и проверку текста. Разделы "Гидрофобные контакты", "Положение в мембране" и подраздел модификаций концов белковой цепи созданы КМ, в том числе скрипты, иллюстрации и комментарии. Вступление, список литературы, вклады авторов, благодарности и разделы "Лиганды", "Водородные связи", "Солевые мостики" сделаны МИ, в том числе текст, оформление, иллюстрации и скрипты.
Благодарности
- Александру Злобину и Валентине Масловой за помощь в изучении синтаксиса HTML
- Артуру Залевскому за помощь в изучении команд JMol
- Всем читателям, заинтересовавшимся работой, и, возможно, прокомментировавшим ее
Литература
- 4QKC Transmembrane View
- High-resolution structures of the M2 channel from influenza A virus reveal dynamic pathways for proton stabilization and transduction Jessica L. Thomaston, Mercedes Alfonso-Prieto, View ORCID ProfileRahel A. Woldeyes, James S. Fraser, Michael L. Klein, Giacomo Fiorin, and William F. DeGrado
- Influenza A M2 wild type TM domain at low pH in the lipidic cubic phase under cryo diffraction conditions
- Human Metabolome Database (HMDB)
- National Center for Biotechnology Information. PubChem Database. CID=12178130
- NCI Thesaurus (NCIt)
- National Center for Biotechnology Information. PubChem Database. Chloride ion, CID=312
- Human Metabolome Database (HMDB)
- National Center for Biotechnology Information. PubChem Database. Calcium ion, CID=271
- CDC-ATSDR Toxic Substances Portal
- National Center for Biotechnology Information. PubChem Database. 1,2-Ethanediol, CID=174
- The discovery of the α-helix and β-sheet, the principal structural features of proteins. David Eisenberg
- Ivan Y. Torshin, Irene T. Weber, Robert W. Harrison, Geometric criteria of hydrogen bonds in proteins and identification of `bifurcated' hydrogen bonds, Protein Engineering, Design and Selection, Volume 15, Issue 5, May 2002, Pages 359–363, https://doi.org/10.1093/protein/15.5.359
- Jelezarov, Ilian & Karshikoff, Andrey. (2009). Defining the Role of Salt Bridges in Protein Stability. Methods in molecular biology (Clifton, N.J.). 490. 227-60. 10.1007/978-1-59745-367-7_10.
- TMHMM - 2.0 Prediction of transmembrane helices in proteins
Примечания
В каждом разделе вторая кнопка JMol связана с первой и является продолжением скрипта, поэтому нажатие первой клавише в одном разделе и второй в другом откроет продолжение скрипта первого раздела.