предсказание вторичной структуры трнк и анализ днк-белковых контактов
1. предсказание вторичной структуры трнк
мной была проанализирована трнк 1h4s (структура трнк по данным pdb). с помощью программ find_pair, einverted и viennarna (rnafold) была предсказана вторичная структура трнк на основе её нуклеотидной последовательности и построена сравнительная таблица результатов.
| участок структуры | позиции в структуре (по результатам find_pair) | результаты предсказания с помощью einverted | результаты предсказания по алгоритму зукера (viennarna) |
|---|---|---|---|
| акцепторный стебель | (4-7) - (69-66) | (1-7) - (73-67) | (1-7) - (73-67) |
| d-стебель | (10-13) - (25-22) | не найден | (11-14) - (24-21) |
| антикодоновый стебель | (38-44) - (32-26) | не найден | (25-31) - (41-35) |
| t-стебель | (49-53) - (65-61) | не найден | (37-41) - (51-47) |
| общее число пар | ≈20 | 7 | 23 |
из приведённой таблицы видно, что программа find_pair, работающая по экспериментально определённой pdb-структуре, даёт эталонное описание вторичной структуры трнк: корректно определены все четыре стебля и часть неканонических пар, поэтому общее число пар составляет около 20. программа einverted, основанная на поиске инвертированных повторов в линейной последовательности, уверенно находит только акцепторный стебель (7 пар), а остальные стебли (d-, антикодоновый и t-) не предсказывает вовсе, что существенно занижает количество пар и не позволяет восстановить полную вторичную структуру трнк.
алгоритм зукера, реализованный в пакете viennarna (rnafold), предсказал 23 пары и успешно восстановил все четыре стебля, однако границы стеблей (позиции пар нуклеотидов) заметно смещены относительно реальной структуры: в d-, антикодоновом и t-стеблях пары не совпадают с эталонными координатами, полученными с помощью find_pair. в целом rnafold существенно точнее воспроизводит реальную вторичную структуру трнк, чем einverted, но, по-видимому, не учитывает часть неканонических взаимодействий, присутствующих в pdb-структуре.
дополнительно с помощью viennarna был получен набор субоптимальных структур; среди 234 альтернатив одна из низкоэнергетических конфигураций визуально лучше остальных воспроизводит известную вторичную структуру трнк. это подчёркивает, что у трнк возможны несколько близких по энергии укладок, однако именно структура, соответствующая данным кристаллографии, остаётся наиболее биологически значимой и должна рассматриваться как референсная.
2. поиск днк-белковых контактов в структуре 1mhd
для анализа днк-белковых контактов была использована структура комплекса smad3 mh1-домена с днк (pdb id: 1mhd). с помощью скриптов в jmol были определены множества атомов днк, относящиеся к остаткам 2'-дезоксирибозы, фосфатной группы и азотистых оснований, после чего было рассчитано число полярных и неполярных контактов белка с каждым типом остатков.
| контакты атомов белка с | полярные | неполярные | всего |
|---|---|---|---|
| остатками 2'-дезоксирибозы | 7 | 13 | 20 |
| остатками фосфорной кислоты | 6 | 27 | 33 |
| остатками азотистых оснований (все основания) | 7 | 4 | 11 |
из таблицы видно, что в комплексе 1mhd большая часть контактов приходится на остатки фосфорной кислоты (33 контакта, преимущественно неполярные - 27), что указывает на важную роль фосфатного остова в связывании белка с днк. контакты с остатками 2'-дезоксирибозы (20 контактов, из них 13 неполярных) также вносят значительный вклад в стабилизацию комплекса. наименьшее число взаимодействий наблюдается с азотистыми основаниями (11 контактов), при этом полярные контакты (7) преобладают над неполярными (4). это согласуется с представлением о том, что узнавание специфической последовательности днк обеспечивается в основном за счёт полярных взаимодействий с азотистыми основаниями, тогда как неспецифическое закрепление белка на днк происходит через контакты с сахаро-фосфатным остовом.
для визуализации взаимодействий был использован пакет nucplot, работающий со старым форматом pdb-файлов. при попытке запустить nucplot для 1mhd_old.pdb программа выдавала ошибку segmentation fault, поэтому для дальнейшего анализа схемы контактов и индивидуальных взаимодействий был использован структурно сходный комплекс 1i3j, корректно обрабатываемый nucplot.

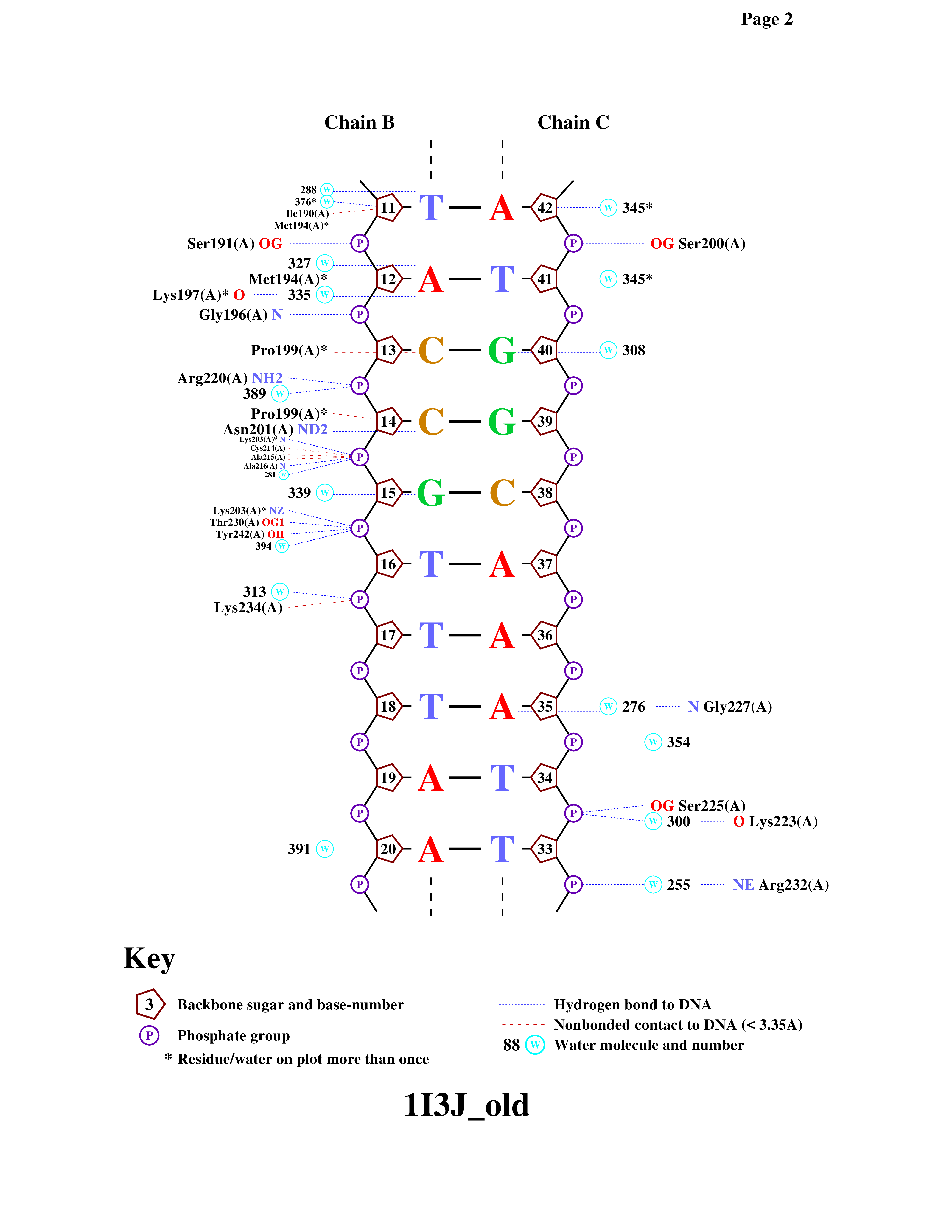
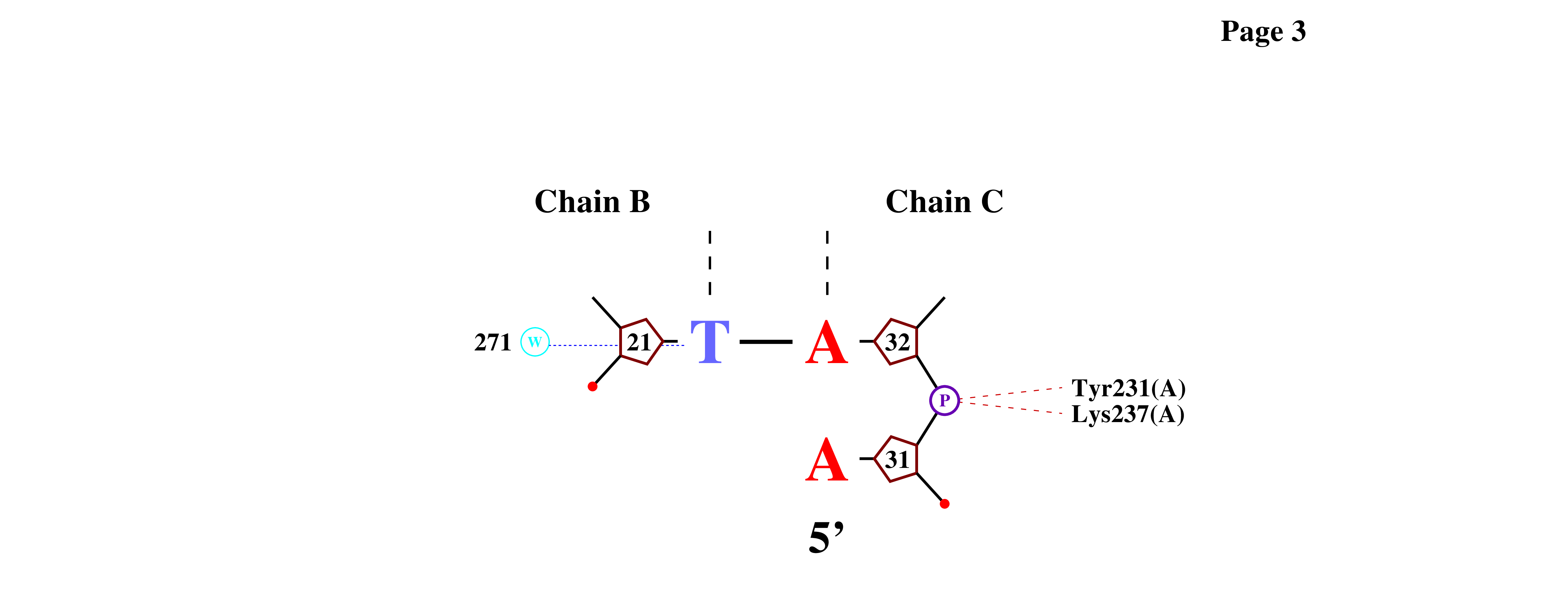
3. анализ контактов в комплексе 1i3j
для комплекса 1i3j были аналогичным образом подсчитаны контакты атомов белка с различными участками днк.
| контакты атомов белка с | полярные | неполярные | всего |
|---|---|---|---|
| остатками 2'-дезоксирибозы | 45 | 148 | 193 |
| остатками фосфорной кислоты | 59 | 27 | 86 |
| остатками азотистых оснований со стороны большой бороздки | 41 | 4 | 45 |
| остатками азотистых оснований со стороны малой бороздки | 9 | 0 | 9 |
| остатками азотистых оснований (неуточнённые по бороздке) | 0 | 18 | 18 |
из таблицы видно, что в комплексе 1i3j наибольшее число контактов приходится на остатки 2'-дезоксирибозы (193 контакта, из них 45 полярных и 148 неполярных), что указывает на важный вклад взаимодействий с сахарным остовом днк в стабилизацию комплекса. контактов с остатками фосфорной кислоты несколько меньше (86; 59 полярных и 27 неполярных), но они, как и в случае структуры 1mhd, отражают существенную роль электростатического связывания с фосфатным остовом. с азотистыми основаниями суммарно регистрируется 72 контакта (45 в большой бороздке, 9 в малой и 18 без уточнения бороздки), что подчёркивает важность оснований для специфического узнавания последовательности и позиционирования белка на днк.
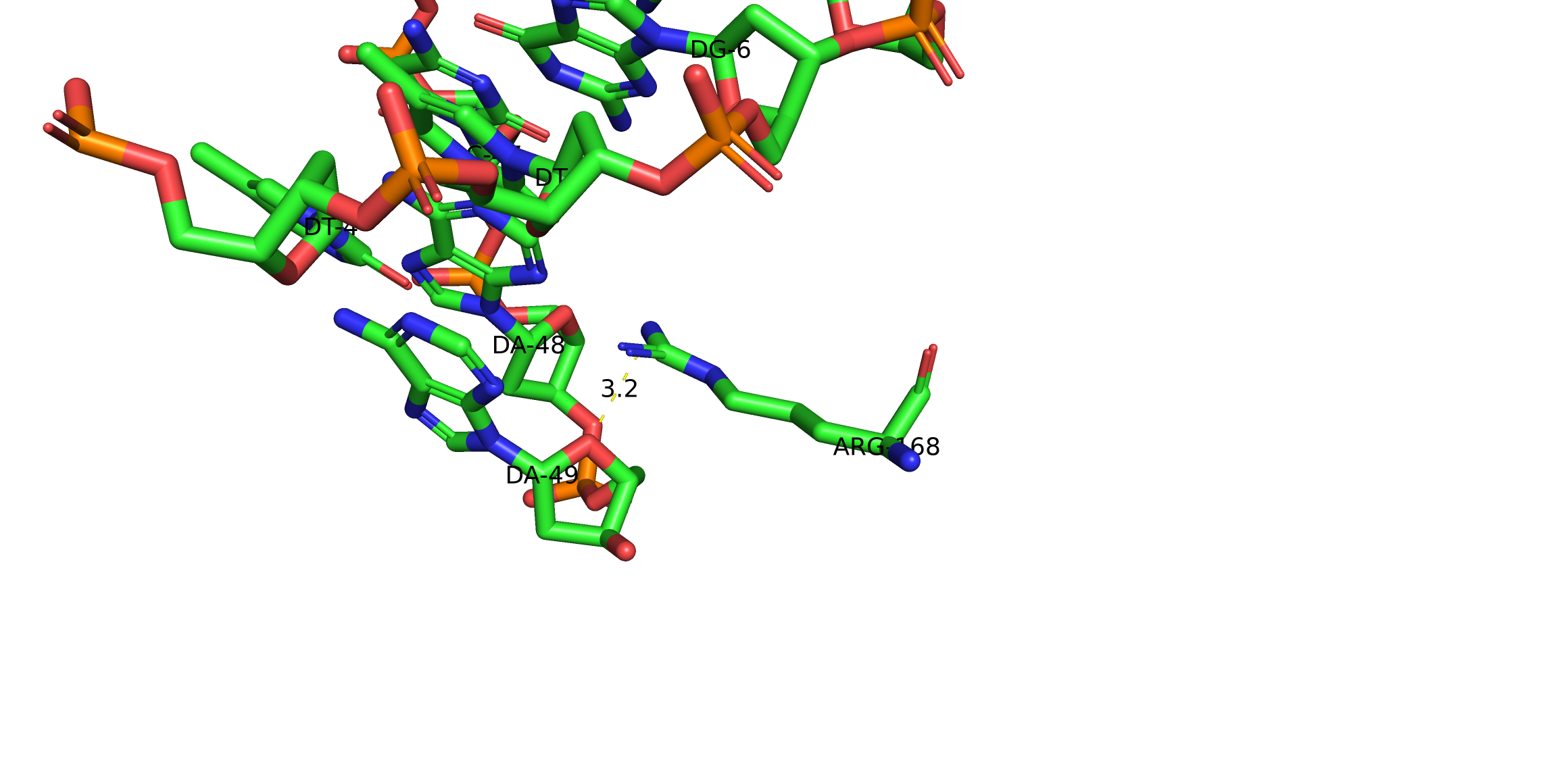
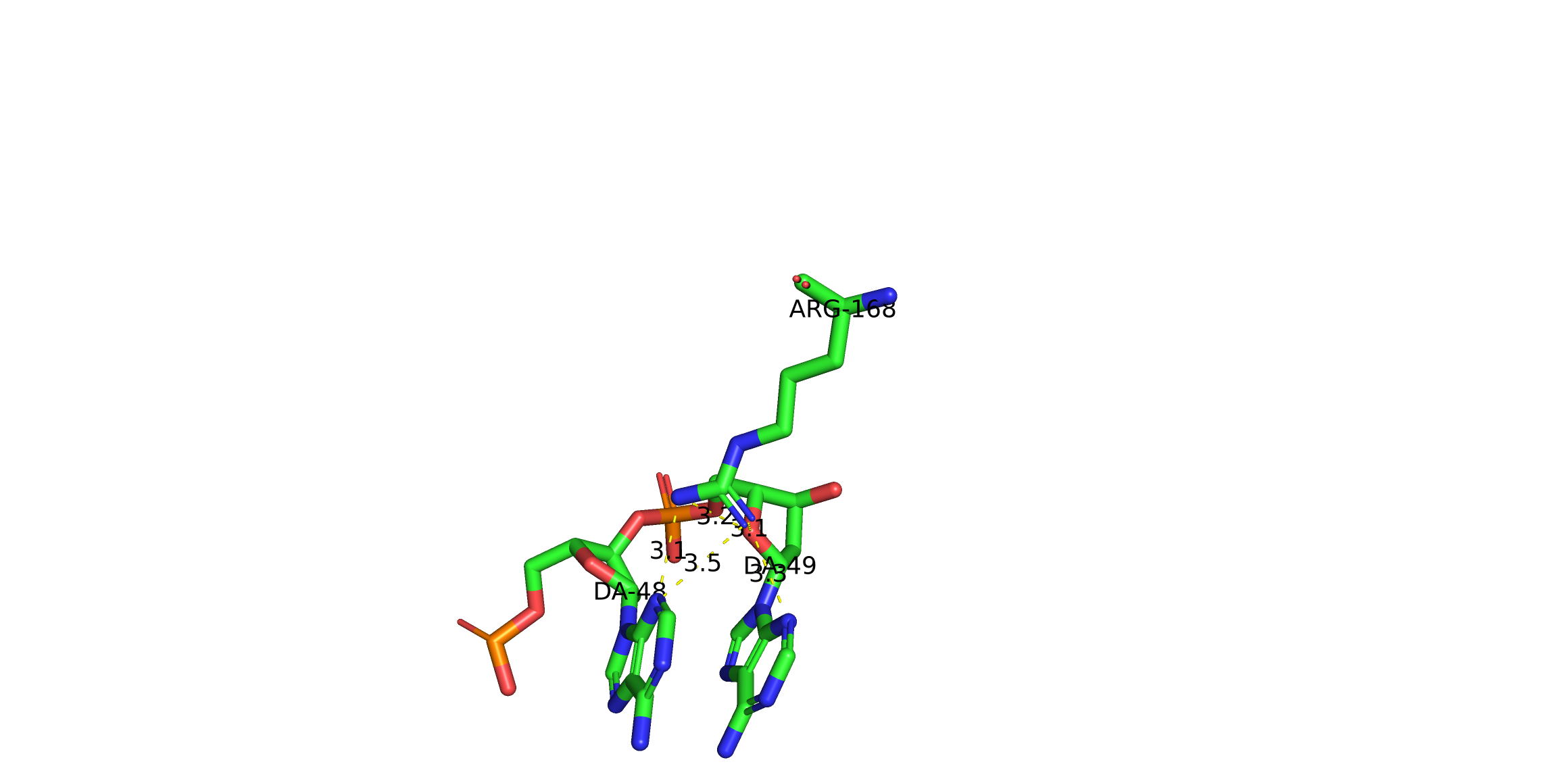
анализ индивидуальных контактов показал, что больше всего взаимодействий с днк образует остаток arg168. в частности, его боковая цепь формирует полярный контакт с атомом кислорода в остатке сахара аденина 49, а также взаимодействует сразу с двумя соседними аденинами: с da-49 через остаток сахара и с da-48 непосредственно через атомы азотистого основания. такое расположение arg168 позволяет ему одновременно стабилизировать сахарно-фосфатный остов и участвовать в специфическом распознавании последовательности, поэтому этот аргинин можно рассматривать как один из наиболее важных остатков, обеспечивающих связывание белка с днк в комплексе 1i3j.