Практикум 2. Альтернативные положения, B-фактор, кристалл
Задание 1. Альтернативные положения
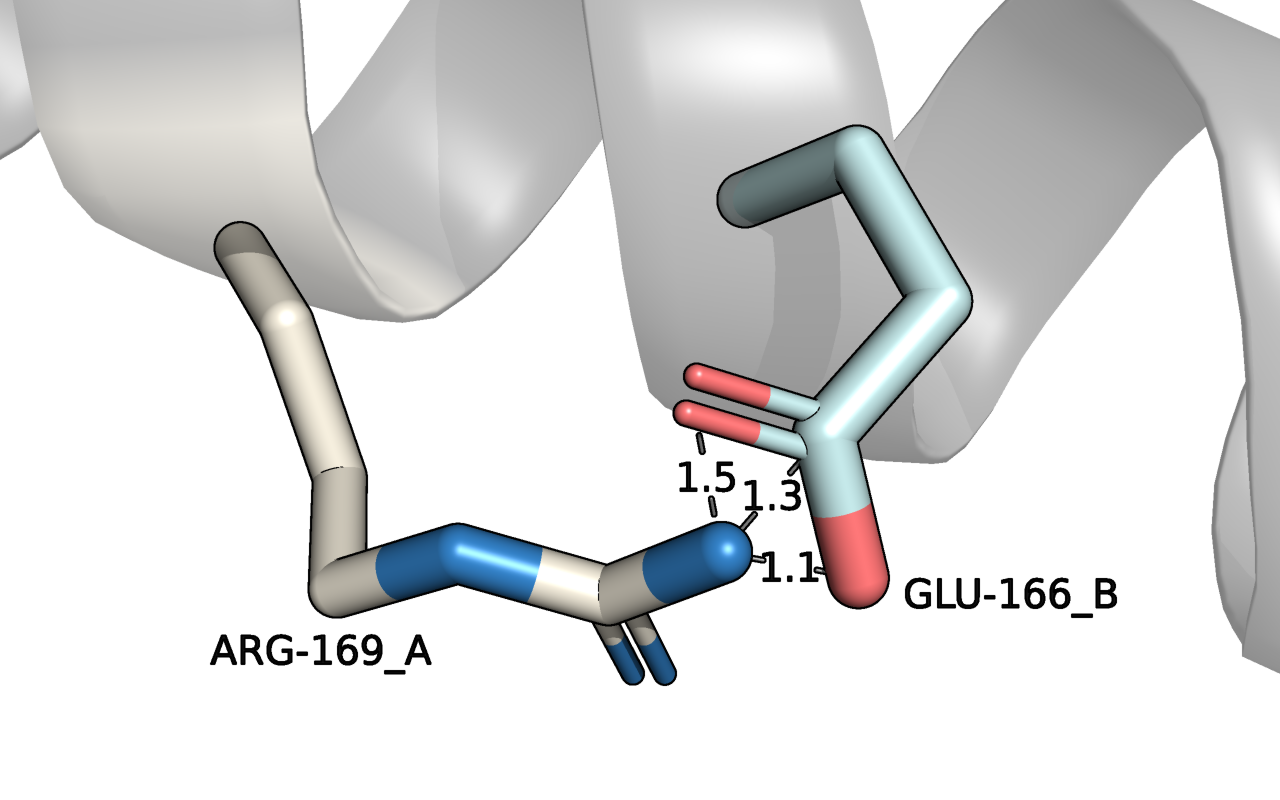
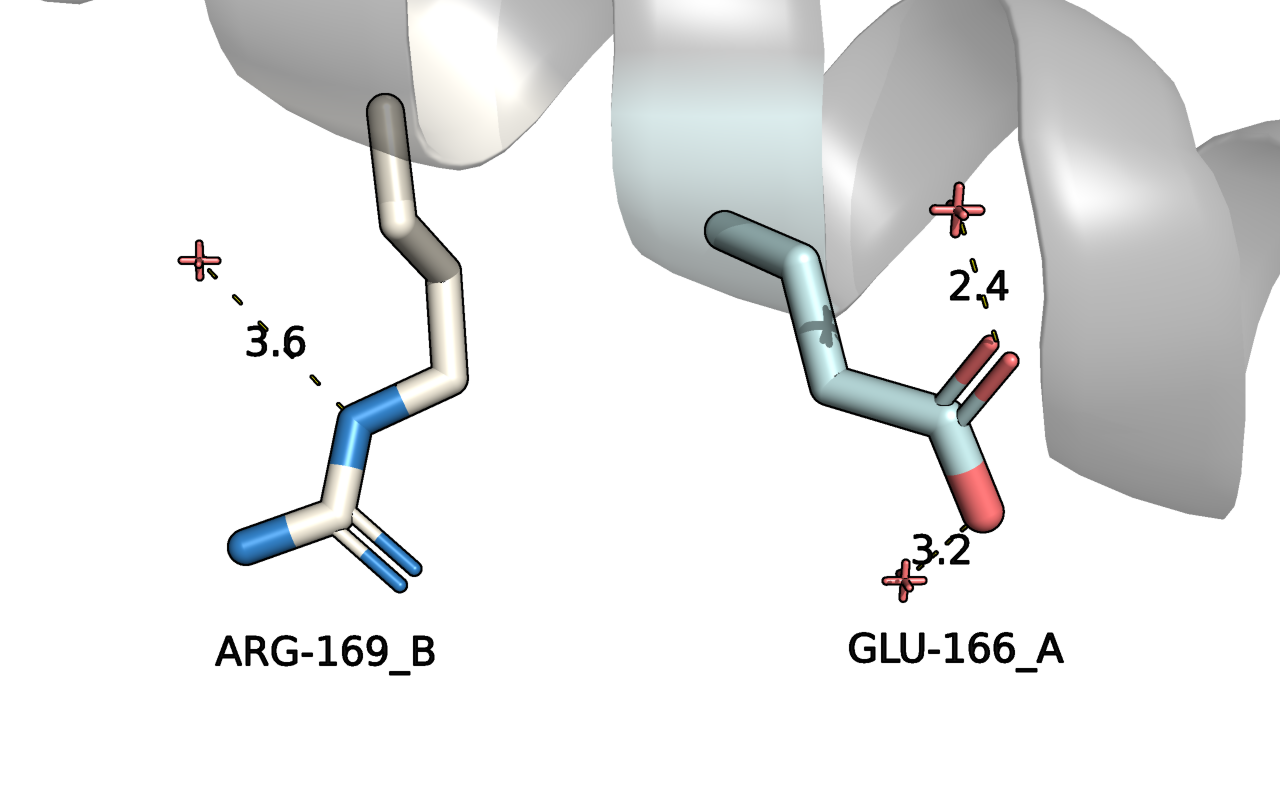
В данном задании рассматривали структуру с PDB: 3czf и два остатка цепи А: Glu-166 и Arg-169. У каждого по два альтернативных положения. Итого может быть 4 сочетания, но не все из них возможны в реальности. В частности невозможно одновременно сочетание альт-лока А Arg-169 и альт-лока B Glu-166, потому что расстояние между боковыми остатками не может быть 1.5 Å и меньше (Рис. 1). Это расстояние характерно для ковалентной связи, которой здесь нет.
Наиболее стабильным кажется сочетание альт-лока B Arg-169 и альт-лока А Glu-166 (Рис. 2). Альт-лок B Arg-169 возможно стабилизирован водородной связью с водой, чего не наблюдается для альтлока A Arg-169. Населённость у альт-локов одинаковая. Альт-лок А Glu-166 стабилизирован двумя водородными связями с водой, а ещё у данного альт-лока населённость больше, чем у альт-лока B (Табл. 1).
Аргинин - это положительно заряженная аминокислота, а глутамат - отрицательно заряжен, поэтому можем предположить, что мы будем наблюдать стабилизацию за счёт электростатических взаимодействий, но ни в одном сочетании такого не наблюдается - геометрия остатков для этого не подходит и большие расстояния.
| Название остатка | Альт-лок | Населенность (Occupancy) |
| Arg-169 | A | 0.5 |
| Arg-169 | B | 0.5 |
| Glu-166 | A | 0.6 |
| Glu-166 | B | 0.4 |
Задание 2. B-фактор
B-фактор позволяет оценить "размытие" ЭП от атома и является следствием неопределенности в его точном положении.
На уровне молекулы такая неопределенность может быть следствием большой термической подвижности.
B-фактор определяется, как:
Bi = 8π2Ui2, где Ui -
среднеквадратичное отклонение атома i. Т.е. чем более подвижен атом, тем больше "размазана" его электронная плотность и
тем выше B-фактор.
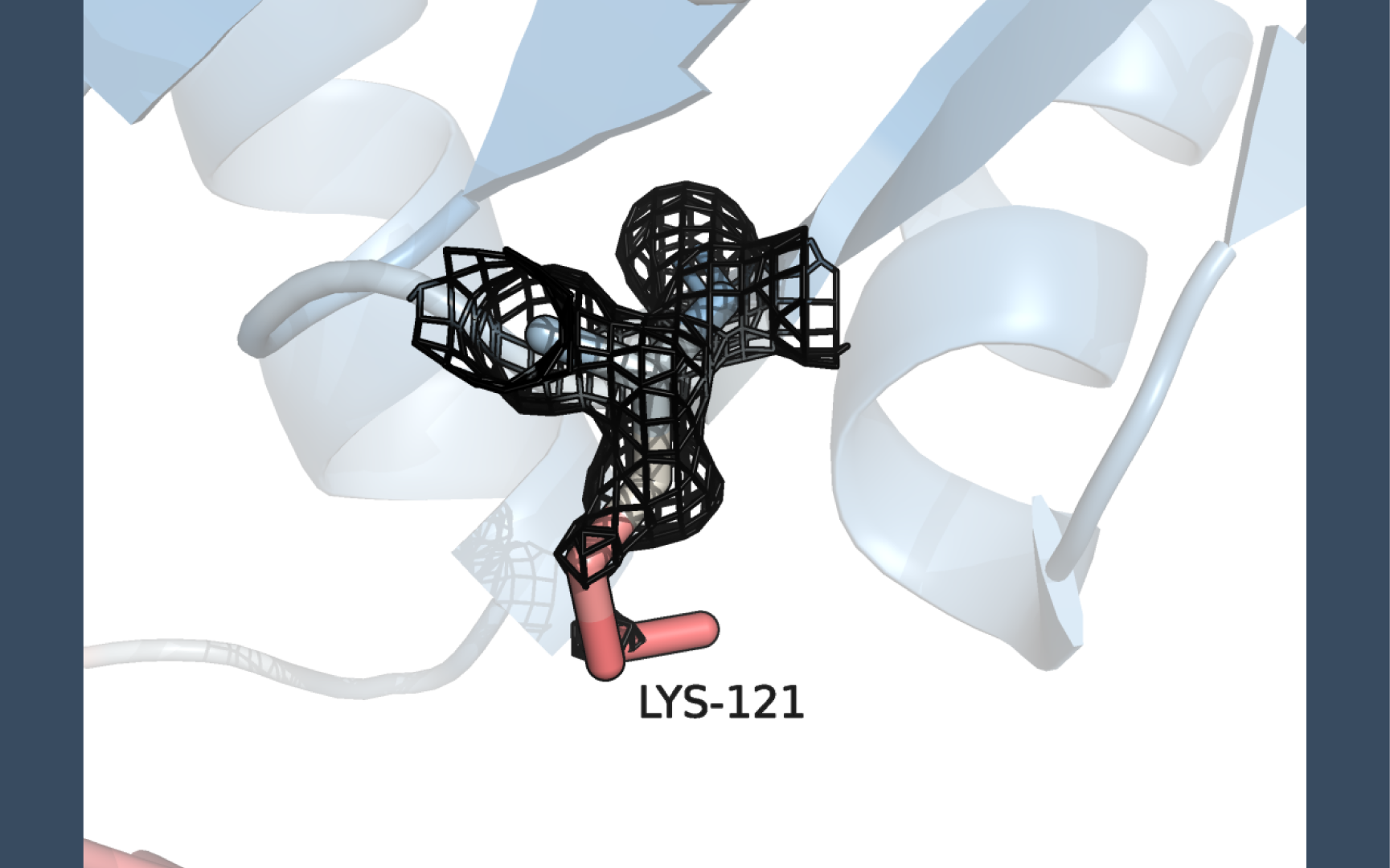
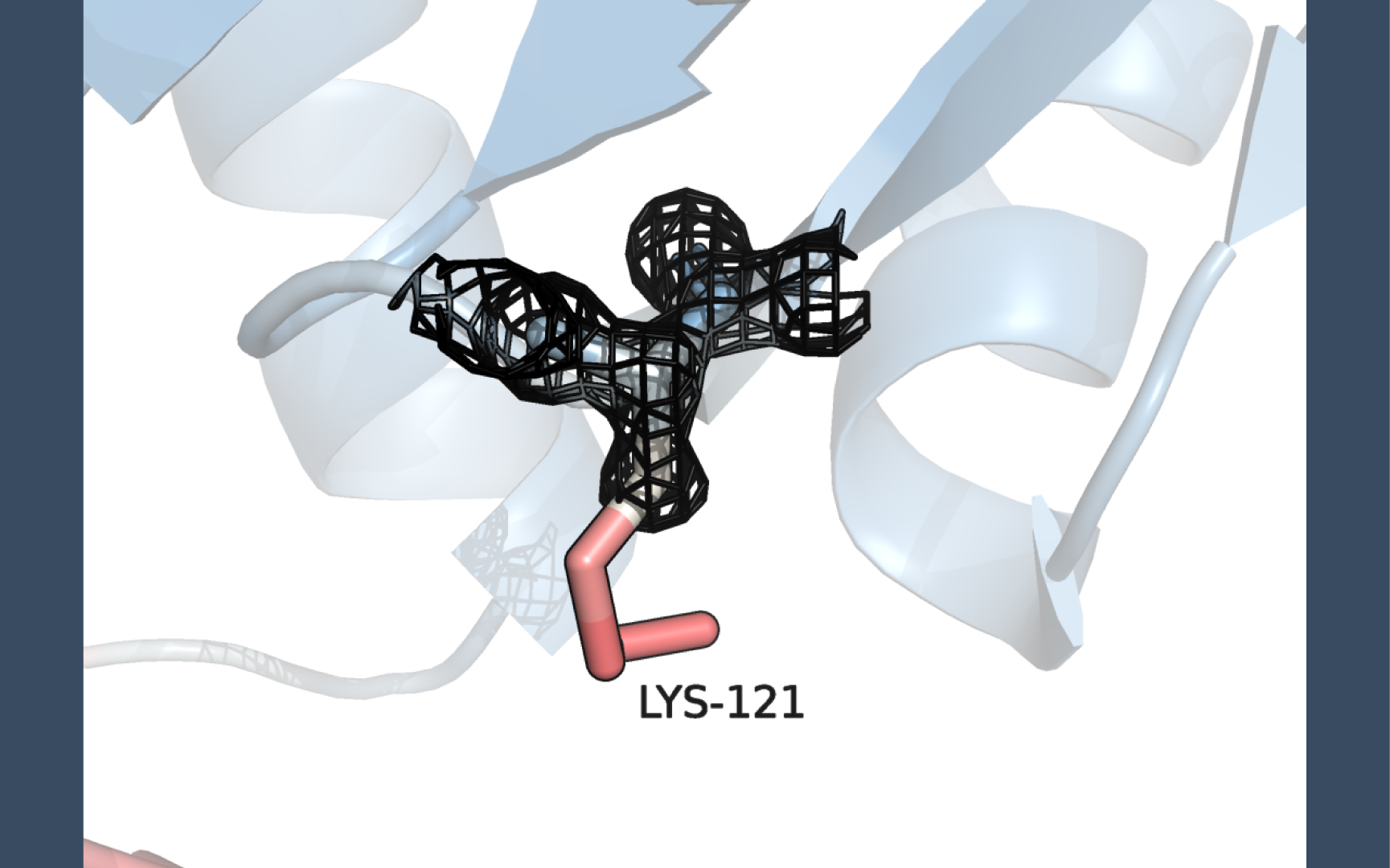
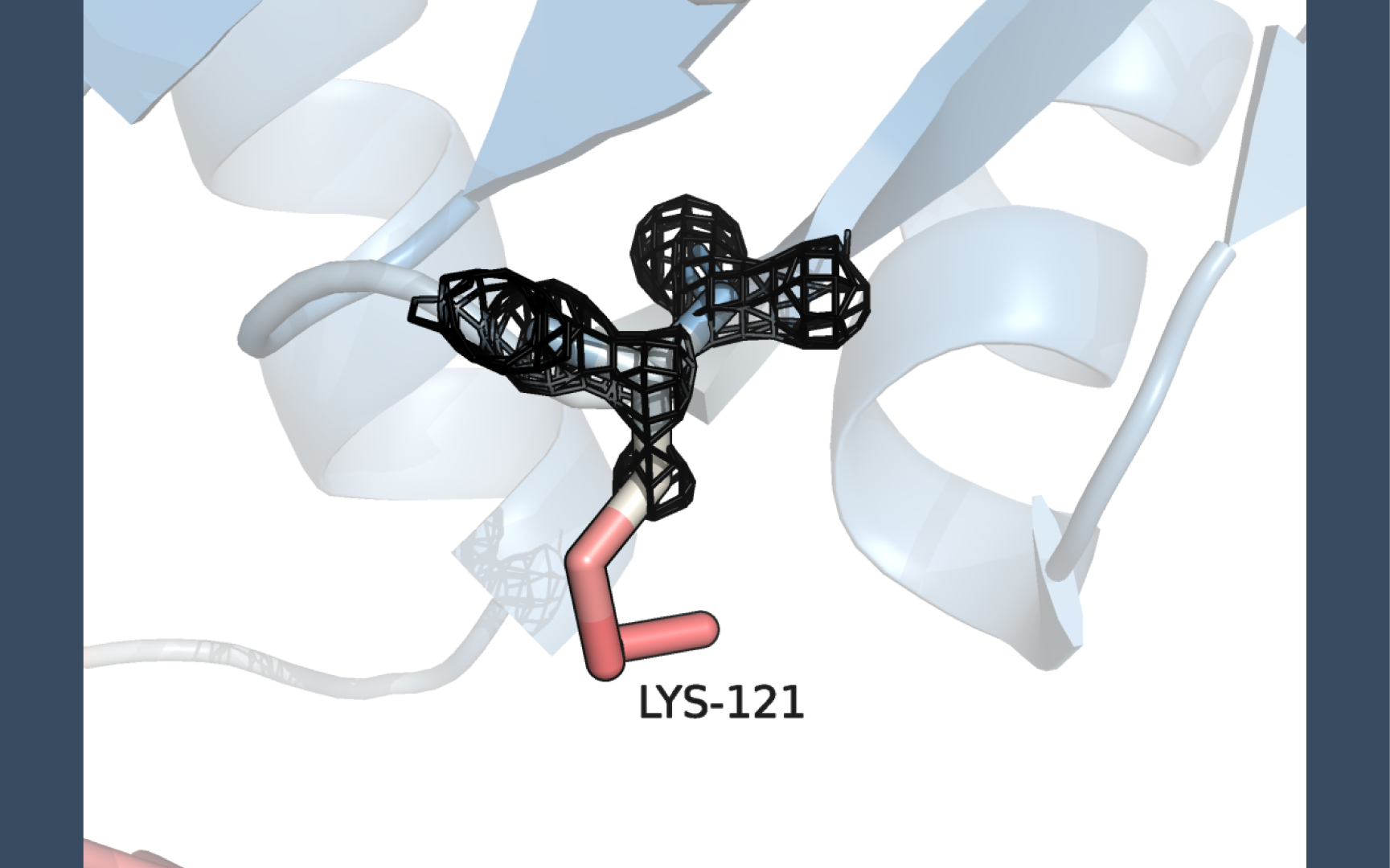
Для данного белка мы наблюдаем, что концы цепей и неструктурированные части более красные, т.е. имеют больший В-фактор, а значит, более подвижны. Внутренняя часть глобулы более синяя, т.е. имеет меньший В-фактор (Рис. 3).
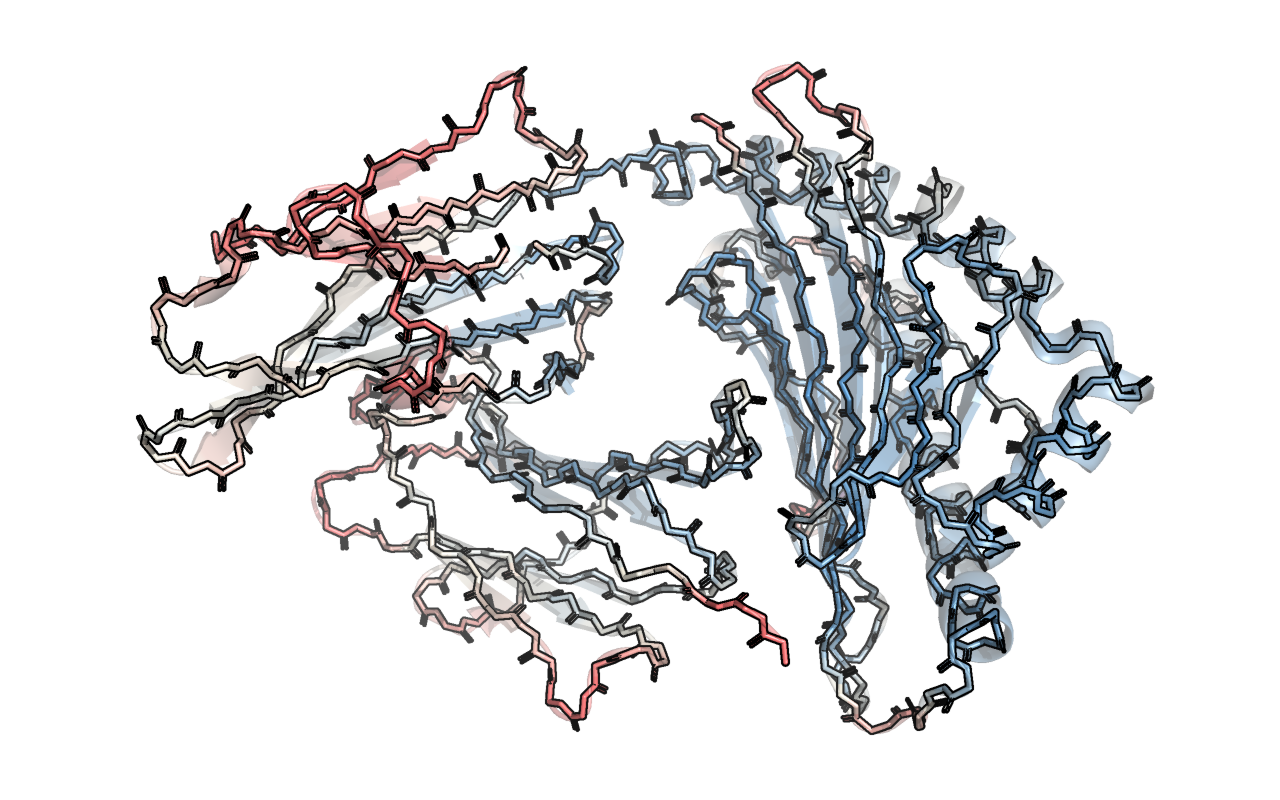
Остаток, который заметно краснеет к концу - Lys-121 A цепи белка, т.е. имеет высокий B-фактор. Это говорит о том, что боковой радикал этого аминокислотного остатка очень подвижен. Lys-121 расположен рядом с гидрофобным ядром, а сам является заряженным, т.е. гидрофильным, поэтому он смотрит наружу. Это можно объяснить тем, что термодинамически выгодно вступать во взаимодействие с водой, поскольку в таком случае энтропия системы увеличивается.
Электронная плотность на уже уровне подрезки 1 исчезает с участков с высоким B-фактором (показано красным). С низким B-фактором (показано синим) - наоборот, электронная плотность остаётся вплоть до уровне подрезки 3. Что логично, потому что чем больше В-фактор, тем больше "размазана" электронная плотность.
Задание 3. Соседи
Здесь мы восстанавливали кристалл структуры с PDB: 3czf с помощью GUI:
A > generate > symmetry mates > с отсечкой в 50 Å (Рис. 4).

Исходная структура соприкасается с 10-ю соседями (Рис. 5).
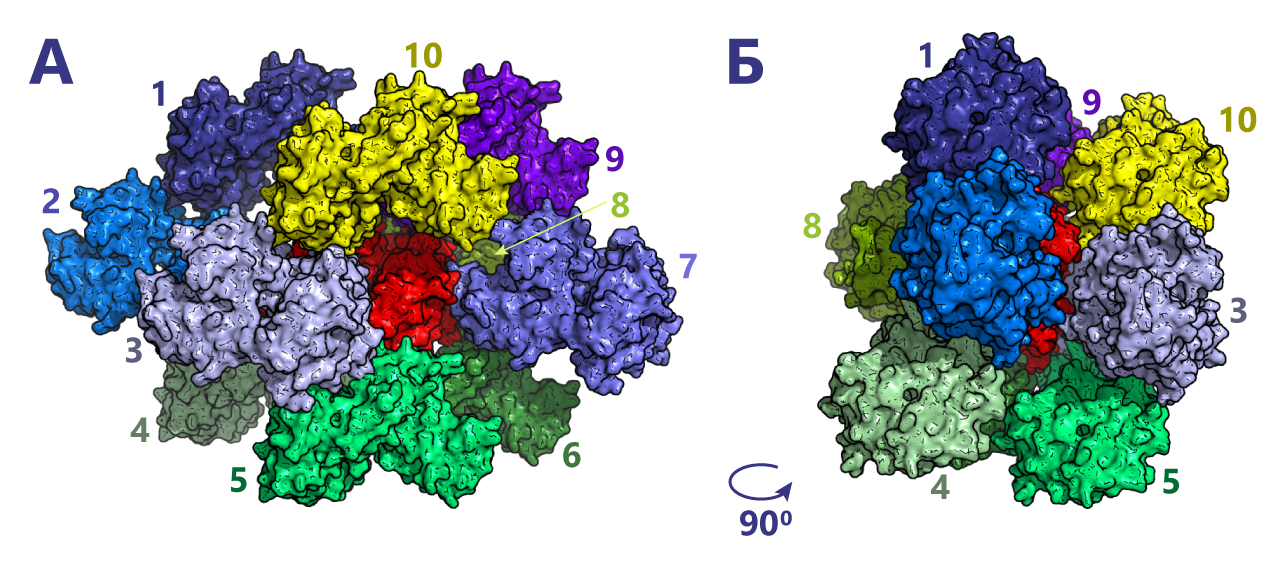
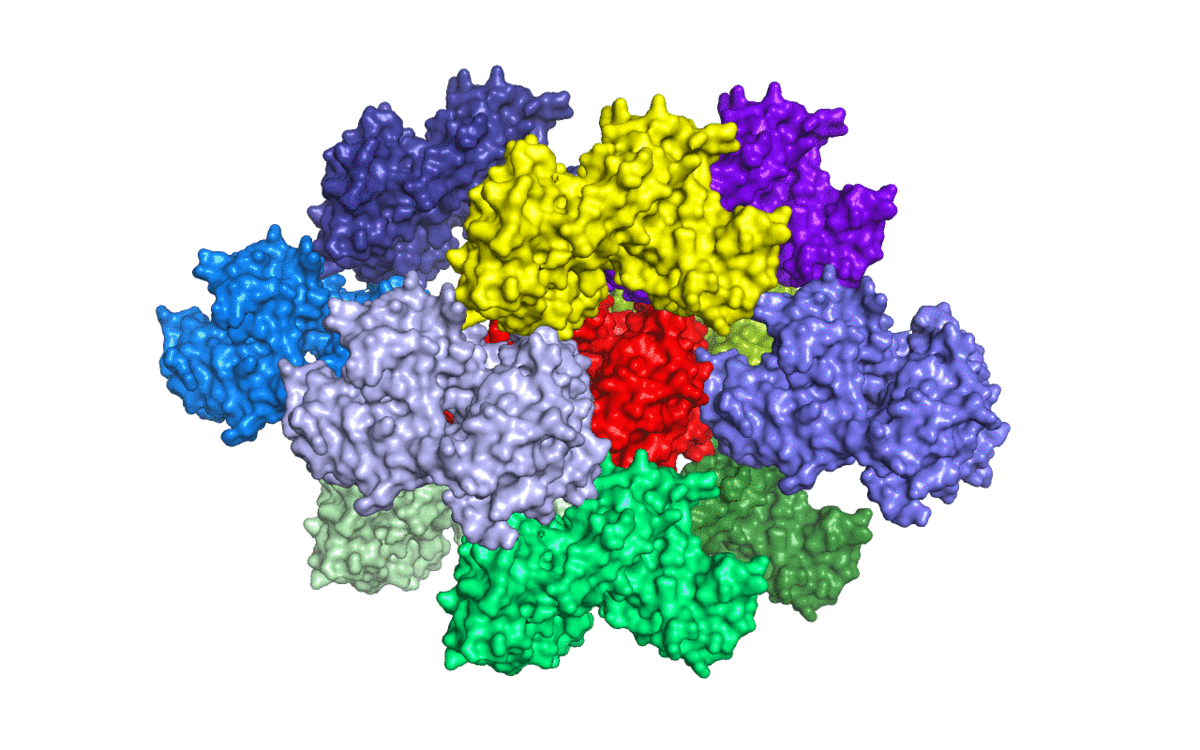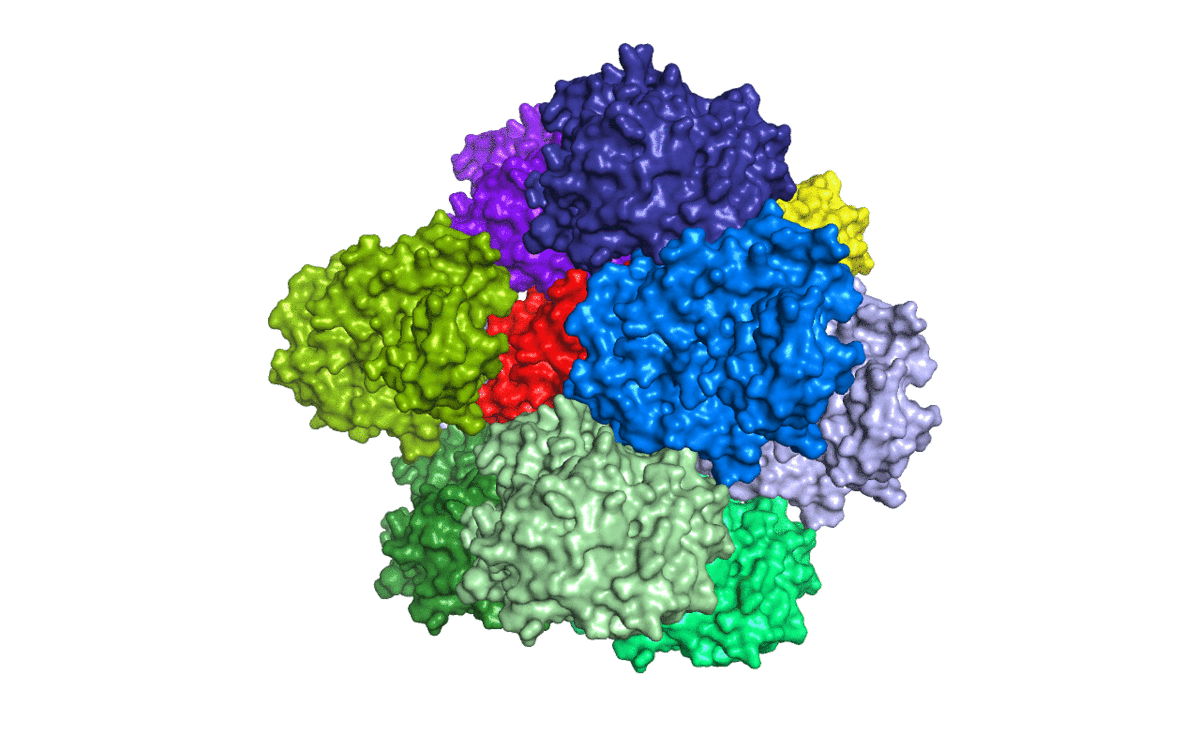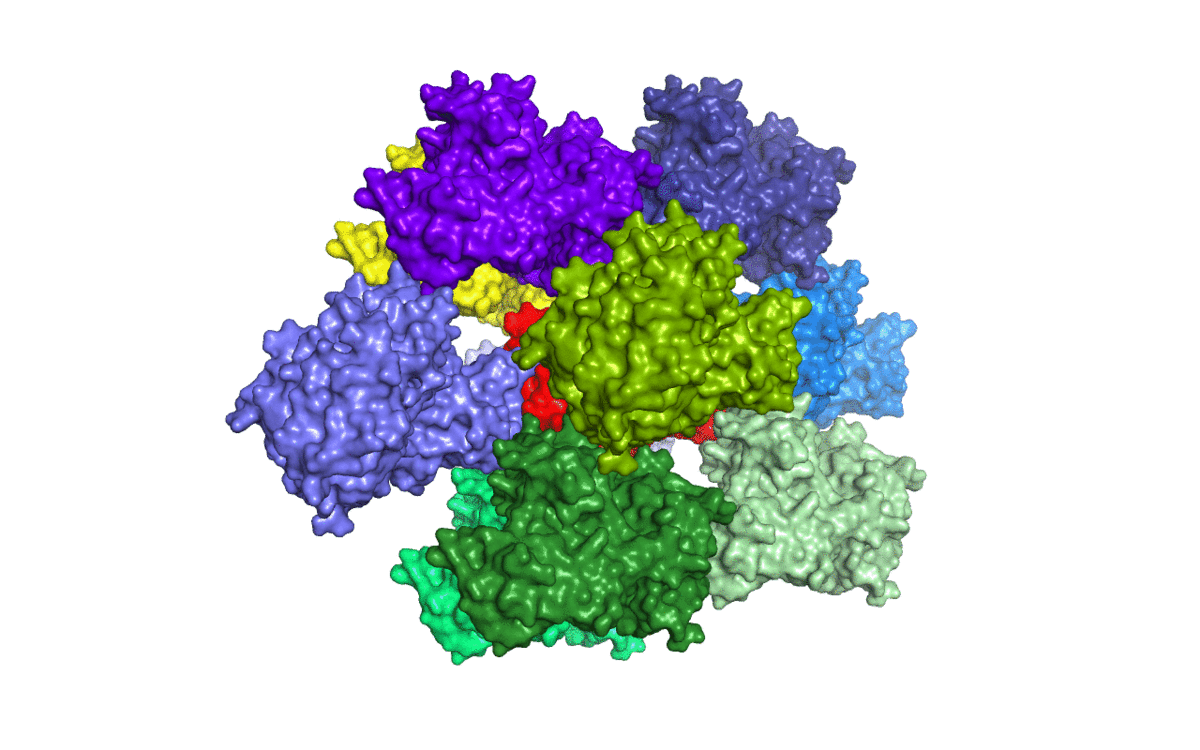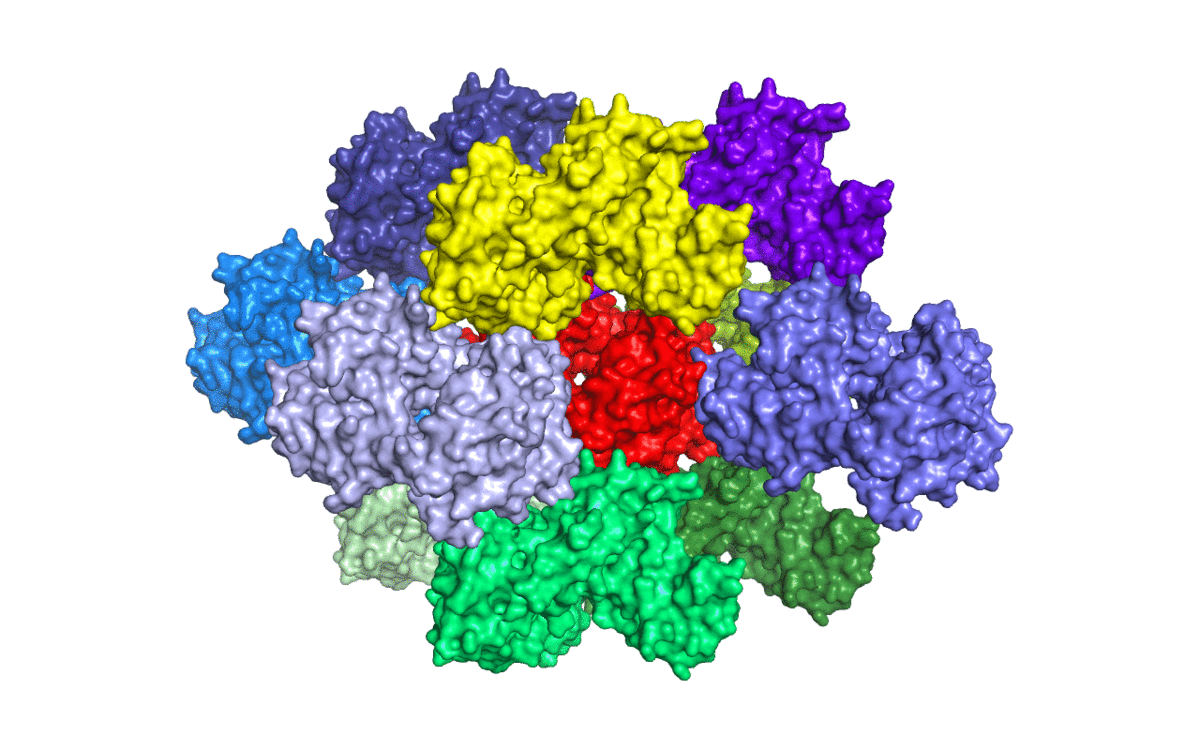
Список некоторых команд, чтобы я могла сориентироваться, как повторить сделанное.