Практикум 2
ЭП: хорошая и плохая расшифровки
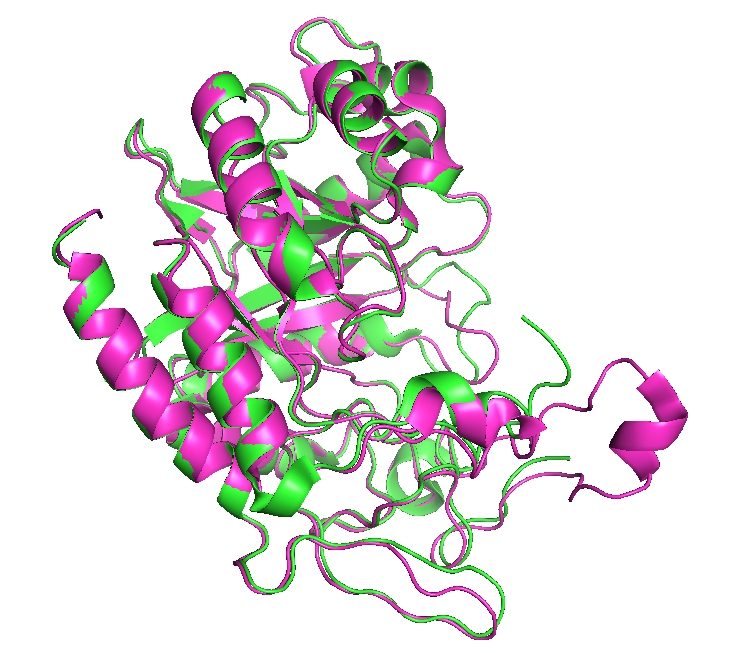
Мне было дано две кристаллографические расшифровки (PDB ID 6ZFQ и 6ZDF) одного и того же белка, имеющие разное качество. Cтруктура 6ZFQ - это бета-альфа бочонок. А структура 6ZDF представляет собой три таких же бочонка, поэтому я выбрала один из трёх бочонков 6ZDF (цепь А) и сравнивала только его со структурой 6ZFQ. Рассматриваемые структуры были выравнены (рис.1). В этом задании: розовым обозначается структура 6ZDF, а зелёным 6ZFQ. По этому выравниванию заметно отличие в структурах. В остове 6ZFQ есть ‘дырка’ (рис.2), в то время как у 6ZDF на этом месте есть короткая альфа-спираль.

Электронные плотности структур были изучены с помощью mesh. На рис.3 показаны визуализация mesh-ы структур с одинаковыми параметрами (carve=2, подрезка по Z-score =2). Поскольку у структуры 6ZFQ более ‘мелкая сетка’ (больше точек), то у неё разрешение должно быть выше. Данное предположение совпадает с действительностью. Разрешения структур, полученные из PDB, следующие: 6ZDF – 3 Å, 6ZFQ- 1.20 Å.

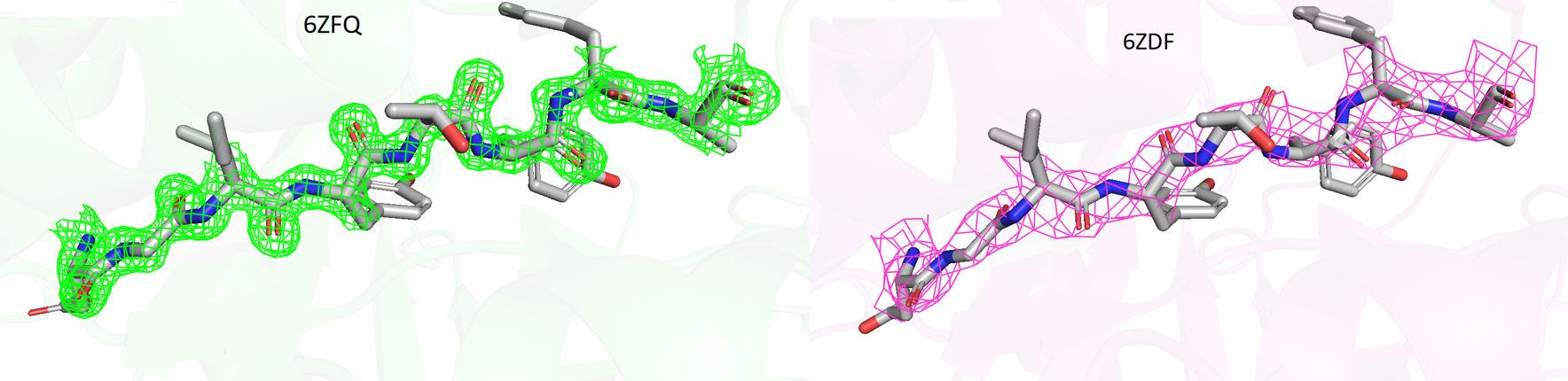
Далее был выбран фрагмент структуры с координатами 318-325 (позиции фрагментов совпадают в обеих структурах). На рис.4 показана ЭП выбранного фрагмента в обеих структурах с подрезкой по Z-score =2 и carve=2. Во фрагменте 6ZFQ плотность вполне однозначно соотносится с положением отдельных атомов, в то время как во фрагменте 6ZDF электронная плотность размазана и на рис.5 видно, что она плохо соотносится с положением отдельных атомов. Из этого следует, что структуры с более высоким разрешением позволяют более точно определить на основании ЭП положение отдельных атомов.
ЭП и положение в структуре
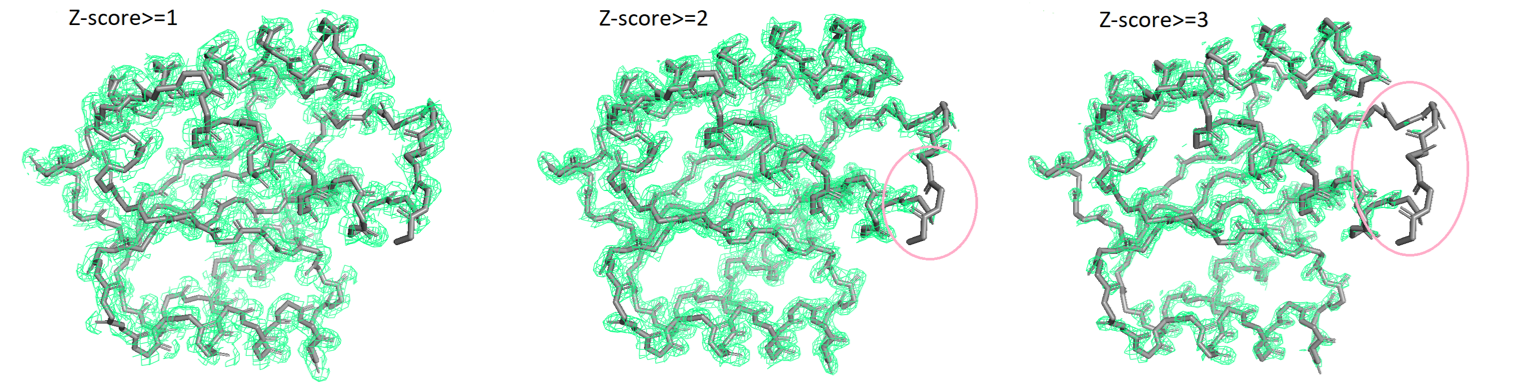
На рис. 5 приведена серия mesh-ей структуры PDB ID 7d7u с параметром carve=2 и подрезками по Z-score = 1, 2, 3. В первую очередь пропадает на C-конце. Судя по структуре эта часть белка довольна подвижна, возможно именно поэтому электронная плотность здесь такая размытая и пропадает при увеличении подрезки.
ЭП и типы атомов
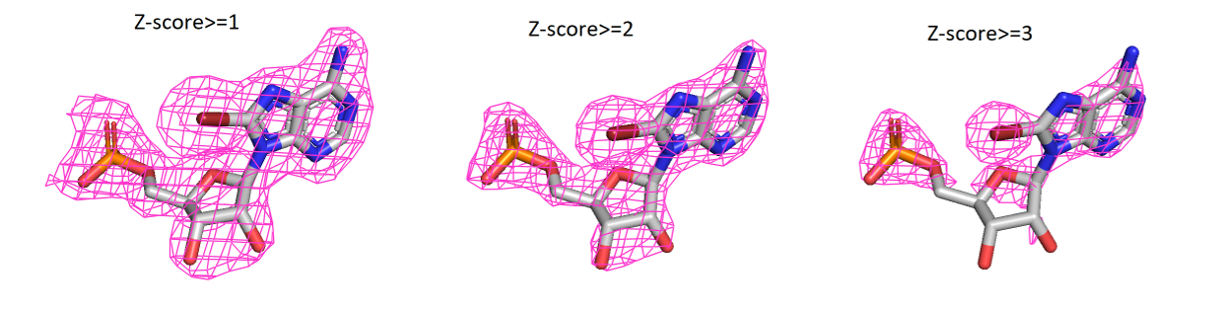
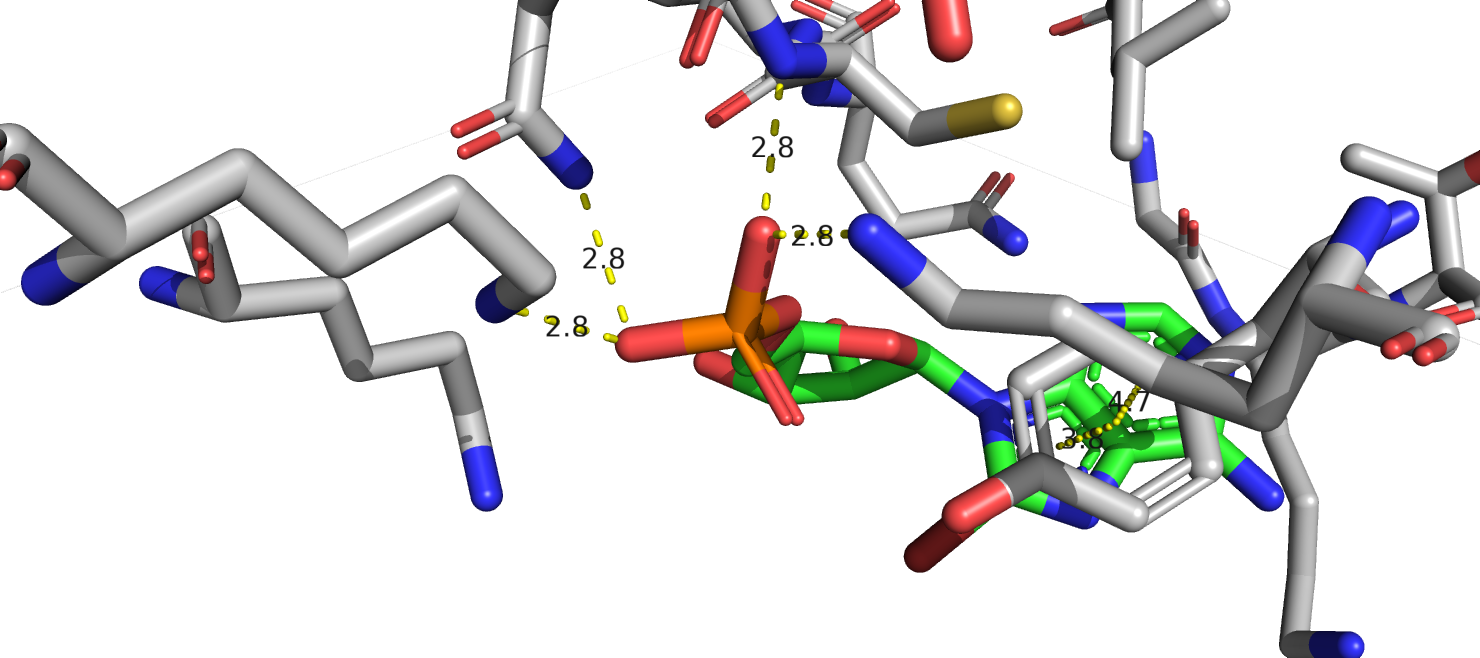
На рис.6 показана ЭП лиганда при разных уровнях подрезки (carve=1.8 везде). На уровне подрезки 1 все атомы покрыты плотностью. Но при увеличении уровня подрезки начинают ‘выпадать’ кислороды рибозы, а затем и азоты пуринового кольца (наверное бром стягивает на себя их электронную плотность и поэтому ЭП соответствующая азотам так плохо детектируется). С увеличением уровня подрезки плотность практически не меняется вокруг брома и она однозначно описывает положение атома. Думаю, сохранения ЭП связано с его высокой электроотрицательностью и неподвижностью. Также относительно неплохо сохраняется ЭП, которой соответствует остаток фосфорной кислоты. Вероятно, это происходит за счёт неподвижности этой группы, которая образует 4 водородные связи с остовом (1 связь) и боковыми радикалами а.к (3 связи) (рис. 7).