Оценка качества 3D структуры.
Странности в структурах PDB.
Модель 7GPB
Структура 7GPB - модель гомотетрамера гликогенфосфорилазы, полученная с разрешением 2.20 Å. Статья с расшифровкой структуры написана в 1991 году.
В данной структуре странными являются триптофаны цепи D. Пример такого ненормального триптофана показан на рисунке 1а. Для сравнения на рисунке 1б приведена структура нормального триптофана той же белковой цепи.

Рисунок 1. а) Trp67 цепи D. Отчетливо видно сильное нарушение планарности бокового радикала аминокислоты. б) Trp 825 цепи D.
На рисунке 2 представлена карта Рамачандрана для цепи D, полученная в базе PDBREPORT. Видно, что множество остатков лежит за пределами разрешенных областей, это говорит о том, что структура в целом разрешена плохо.
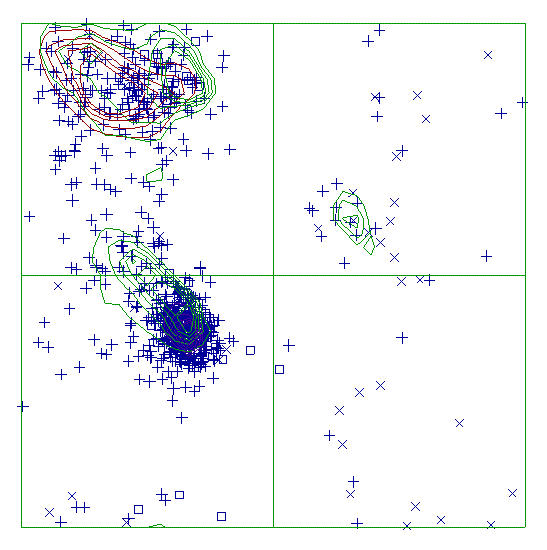
Рисунок 2. Карта Рамачандрана для цепи D структуры 7GBP.
Модель 5RXN
5RXN - модель рубредоксина, полученная с разрешением 1.20 Å.Структура была расшифрована в 1984 году. В структуре модели можно обнаружить два диастереомера треонина – (2S, 3S) и (2S, 3R). При этом первый диастереомер является нетипичным для белков.
На рисунке 3 показаны два стереоизомера треонина: Thr 5 и Thr 7.
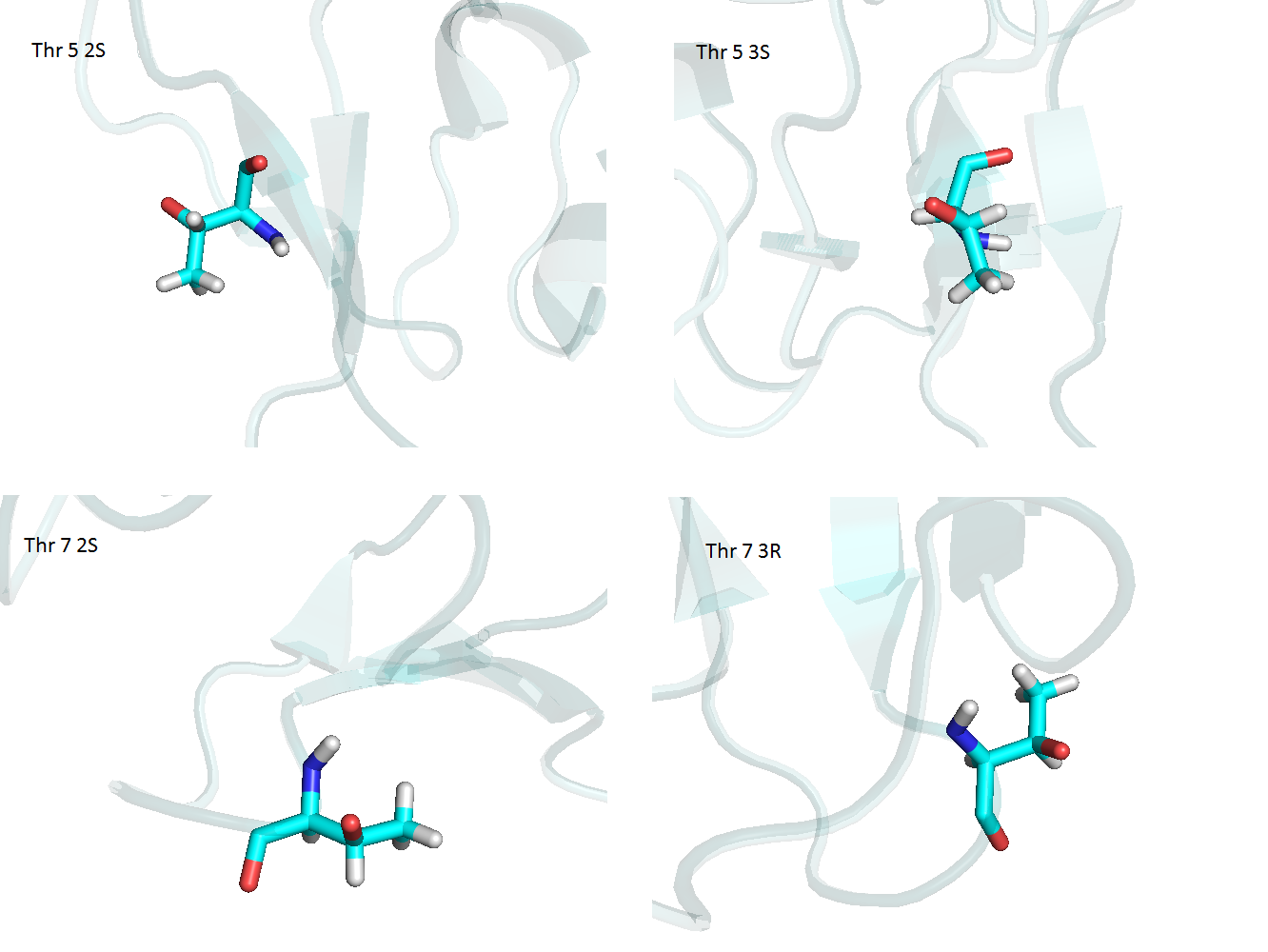
Рисунок 3. Два диастереомера треонина – (2S, 3S) и (2S, 3R).
Error: Threonine nomenclature problem The threonine residues listed in the table below have their O-gamma-1 and C-gamma-2 swapped. 5 THR ( 5-) AЭто говорит о том, что выбор стереоизомера (2S, 3S) Thr 5 ничем не обоснован. Кроме треонина из протеиногенных аминокислот хиральностью может обладать изолейцин.
Модель 1RC2
1RC2 - модель аквапорина Z полученная с разрешением 2.50 Å. Структура была получена в 2003 году. В файле .pdb присутствуют молекулы воды, находящиеся на расстоянии более 5 Å от белковой цепи, то есть не связанные с белком. На рисунке 4 показаны атомы кислорода этих молекул.
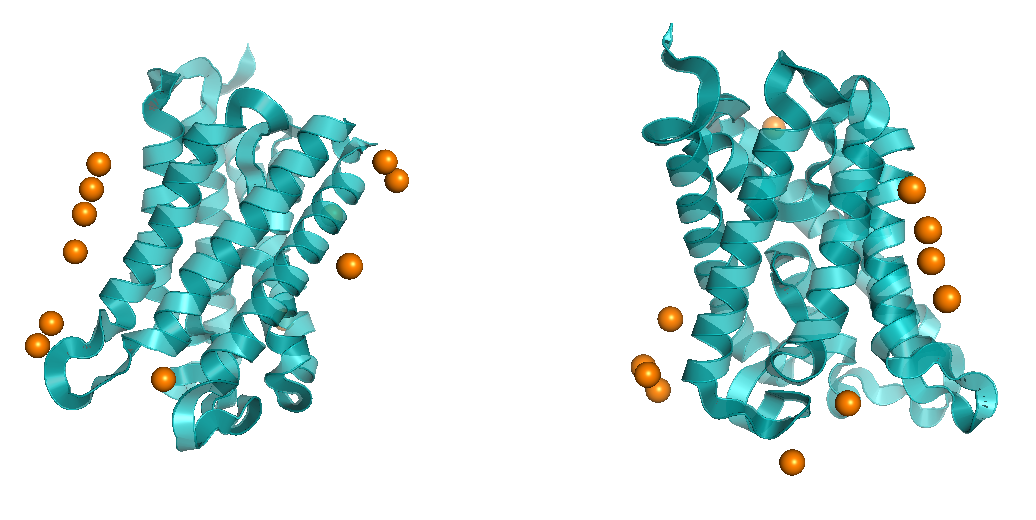
Рисунок 4. Цепи A и B аквапорина Z (расстояние между цепями уменьшено, по сравнению со структурой кристалла). Оранжевыми шариками показаны атомы кислорода молекул воды, не связанных с белковой цепью.
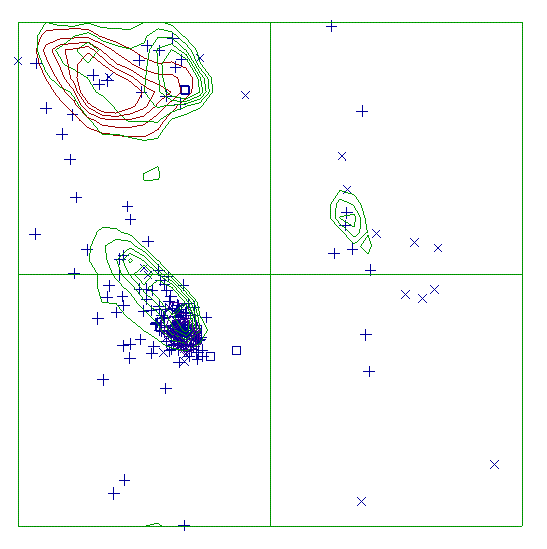
Рисунок 5. Карта Рамачандрана для цепи B аквапорина Z.
B-фактор и заполненность при разных разрешениях.
На сайте PDB c помощью Advanced search был произведен поиск структур с разрешением до 1 Å и от 2.0 Å до 2.5 Å (метод получения - X-Ray). Были выбраны структуры 3NIR с разрешением 0.48 Å (48 аминокислот) и 4U7Y с разрешением 2.5 Å (90 аминокислот).
На рисунке 6 представлены гистограммы для температурных факторов обеих структур. Они демонстрируют, что температурные факторы выше у структуры с меньшим разрешением (3NIR).
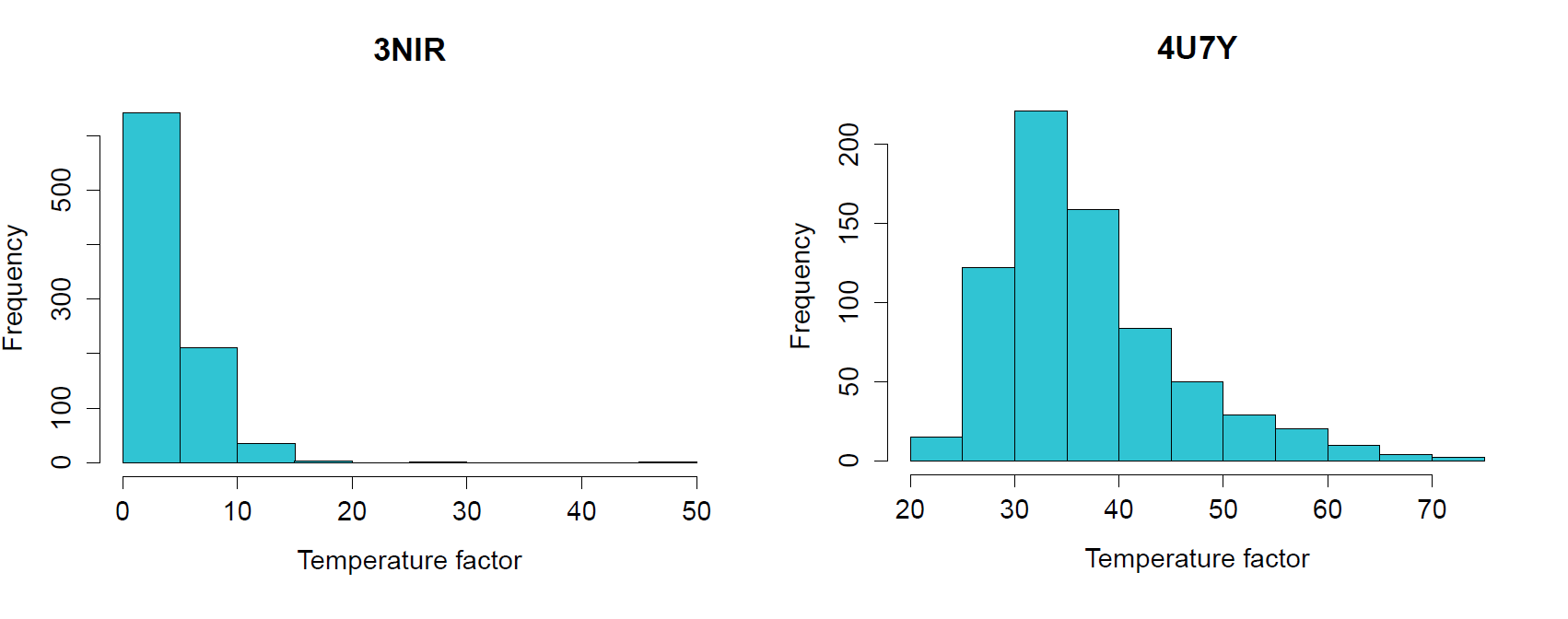
Рисунок 6. Распределение значений температурных факторов структур 3NIR и 4U7Y.
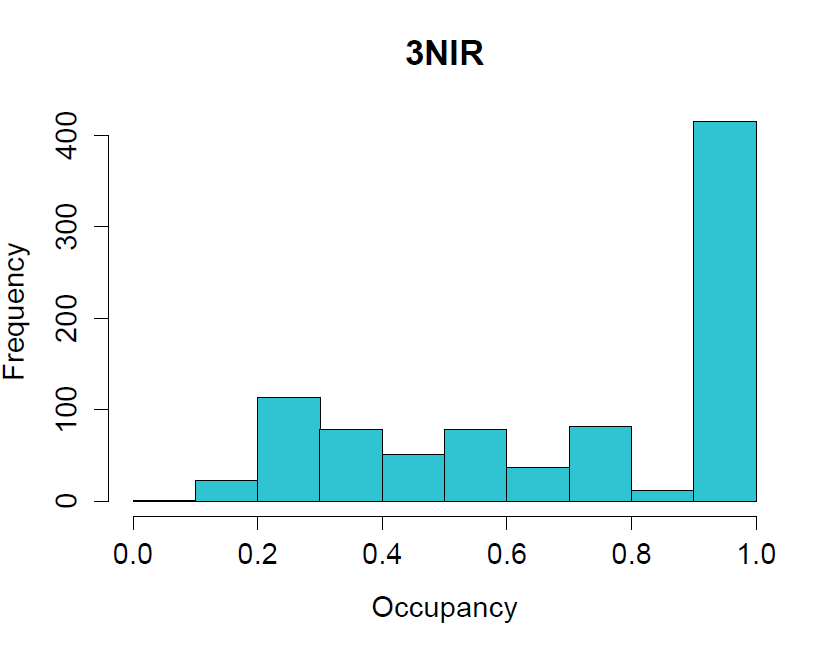
Рисунок 7. Распределение значений коэффициентов заполнения для атомов структуры 3NIR.
© Наталья Ланина
e-mail: n.lanina@fbb.msu.ru
последний раз обновлялось: 26.2.15