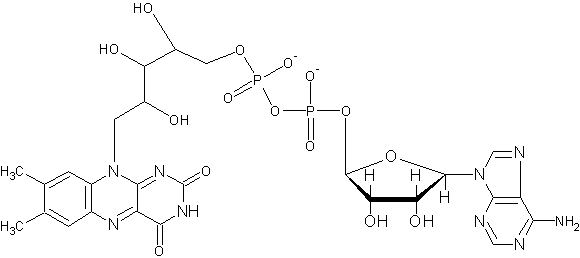
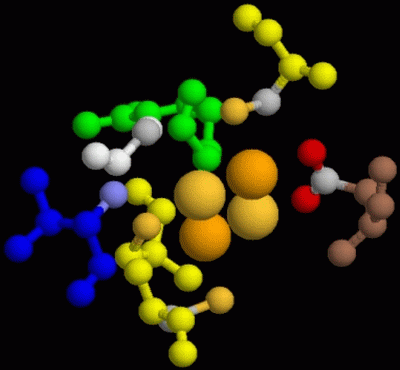
 Лиганд FeS выделен размером.
Лиганд FeS выделен размером.
Прилегающие аминокислотные остатки: атомы их, лежащие в радиусе 3.1Å от лиганда, окрашены в стандартные цвета (C,N,O,S); сами же АКО: Cys - 3 шт., Arg, Asp, Val, Gly - по одному.
Во-первых, сразу заметно, что здесь есть гидрофобная связь, потому что из 7 АКО, входящих в окружение лиганда, 5 являются гидрофобными (Gly, Val и 3 Cys), причем Cys все развернуты S-концами в сторону лиганда, а Gly и Val повернуты N-концами.
Во-вторых, имеются основания предполагать наличие водородных связей, из-за наличия в радиусе 3,1Å атомов кислорода от Asp и азота от Arg и Val. Я считаю, что водородные связи могут быть между S (относительно отрицательной) и NH из Arg, Val и Gly (причем у двух последних возможна и гидрофобность). Гидрофобны же наверняка связи FeS - Cys. Возможна также связь электростатической природы между Asp и Fe, так как аспарагин - кислота.